以发育滞后为首发表现的克罗恩病1例*
邱耀鹏 郑裕博 布小玲 王蓓蓓 戴世学& 沙卫红&
南方医科大学第二临床医学院1(510515)广东省人民医院(广东省医学科学院)消化内科 广东省老年医学研究所2
病例:患儿男性,14岁,因“反复发热1月半余”于2017-05-25收入广东省人民医院消化内科。患儿于2017年4月初出现发热,最高达39 ℃,伴畏寒、咽痛。当地医院考虑“急性呼吸道感染”,予抗感染治疗后症状一度缓解,但仍反复发热。患儿平素偶有轻度腹痛,进餐后加重,持续1~2 min后可缓解,偶有腹痛-便意-缓解规律,无黏液脓血便,无里急后重,粪质稀烂,约1~2次/d。无抽搐,无肌肉酸痛,无午后潮热、盗汗乏力,稍有咳嗽,无咳痰,无阵发性呼吸困难,无活动后气促,无头晕、头痛,无腹胀、腹泻,无关节肿痛、全身皮疹等。
入院查体:体温39.1 ℃,心率116次/min,呼吸20次/min,血压81/54 mm Hg(1 mm Hg=0.133 kPa),身高121 cm,体质量31 kg,体质指数(BMI)21.17 kg/m2;发育迟缓,营养中等,体型偏瘦;双侧扁桃体Ⅱ度肿大,表面有少许脓点,咽后壁轻度充血、滤泡增生;左右两侧腹股沟均可扪及数颗米粒大小的淋巴结,无触痛;心肺检查未见异常;腹软,全腹无压痛、反跳痛,未触及包块,肠鸣音4次/min,无气过水声;全身关节无肿胀、压痛。实验室检查:补体、免疫球蛋白、肾功能、肝功能、类风湿因子、抗链球菌溶血素O、血管炎指标五项、抗核抗体酶谱六项、尿常规均未见明显异常;粪隐血试验阳性,未发现虫卵;难辨梭菌毒素阴性;T-SPOT、结核分枝杆菌核酸检测阴性;伤寒杆菌抗原反应:伤寒O901 1∶80,伤寒H901 1∶160;外斐试验阴性;肺炎支原体IgM阴性。
入院后初步诊断为“化脓性扁桃体炎”,予抗感染等治疗,扁桃体脓点略减少,但仍反复发热。复习病史发现患儿近3年身高增长缓慢,2015年增高2 cm,2016年仅增高1 cm,2017年未增高,同时体质量亦增长缓慢,近2年仅增重1.5 kg。2015年8月出现肛门瘙痒、疼痛,当地医院考虑“肛裂”,行挂线治疗。考虑患儿有“肛裂”史、粪隐血试验阳性且平素粪质稀烂,遂行结肠镜检查,提示盲肠和升结肠变形,正常黏膜基本消失,见大量不规则溃疡,部分融合呈片状,并见大量息肉状隆起(图1)。活检病理:结肠黏膜溃疡形成,肉芽组织增生,局灶腺体扩张,间质较多淋巴细胞、浆细胞浸润;黏膜组织呈慢性炎,间质水肿,考虑炎症性肠病(IBD)(图2)。CT检查提示盆腔回肠、回盲部、升结肠肠壁改变,考虑炎性病变(图3)。
2017-06-04进行包括普外科、儿科、病理科、影像科、营养科等在内的多学科会诊(MDT),综合意见为:根据患儿临床、内镜、影像学、病理学等表现考虑克罗恩病(CD)诊断明确,蒙特利尔分型A1L3B2,目前暂无手术指征;CD活动指数(CDAI)为326分,且目前无活动性感染、无肿瘤征象,有使用生物制剂的指征。遂于2017-06-16起予英夫利西单抗(IFX)200 mg静脉注射,美沙拉嗪 1 000 mg qid 口服,辅以肠内营养治疗(安素®)。患儿精神、睡眠、食欲可,小便正常,大便成型,体质量半个月内增至33 kg。第2~6次IFX治疗均按期进行,期间无发热等不适,每日排便1~2次,均为成型便,无腹痛,无关节痛。

盲肠和升结肠变形,正常黏膜基本消失,见大量不规则溃疡,部分融合呈片状,并见大量息肉状隆起
图1 结肠镜下表现
第6次IFX治疗(2018-01-16)时患儿身高128 cm,体质量36 kg,BMI 22.0 kg/m2。次日复查结肠镜和活检病理,内镜下肠黏膜表现明显改善,鹅卵石征好转,无明显肠腔狭窄(图4);活检病理仅表现为轻度炎症(图5);CDAI降至89分。2018年1月下旬开始使用硫唑嘌呤(50 mg qd)维持缓解,期间未发生白细胞计数降低、呼吸道感染等。随访中患儿于2018年3月下旬出现双侧膝关节疼痛,追问有银屑病关节炎家族史,于外院行膝关节MRI扫描提示右侧膝关节滑膜增生(图6),考虑不能除外IBD并发关节炎可能。复查血常规白细胞 3.2×109/L,遂暂停硫唑嘌呤,以柳氮磺吡啶(SASP)替代美沙拉嗪进行维持治疗,同时进一步加强补充维生素D3[1]。使用SASP治疗4周后患儿膝关节疼痛症状消失,无腹痛、腹泻。随访至2018年11月,患儿未诉不适,一般情况良好。
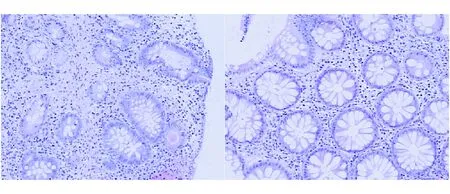
结肠黏膜溃疡形成,肉芽组织增生,局灶腺体扩张,间质较多淋巴细胞、浆细胞浸润;黏膜组织呈慢性炎,间质水肿
图2 结肠镜活检病理表现
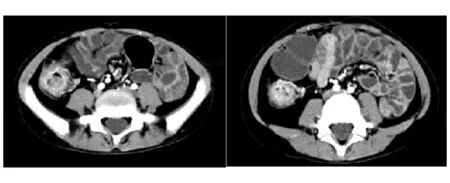
盆腔回肠、回盲部、升结肠肠壁改变
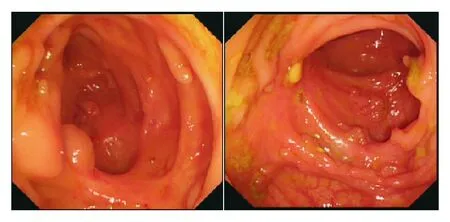
图4 第6次IFX治疗后结肠镜下呈现部分黏膜愈合
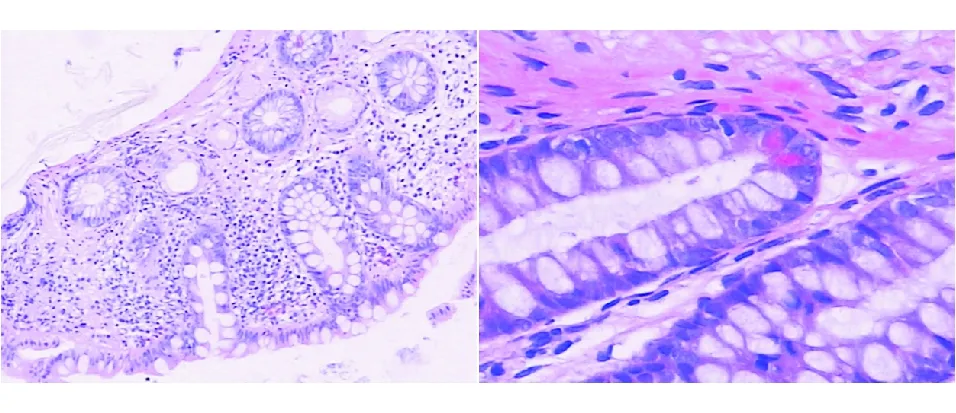
图5 第6次IFX治疗后结肠黏膜呈轻度慢性炎,隐窝结构和数量未见明显异常
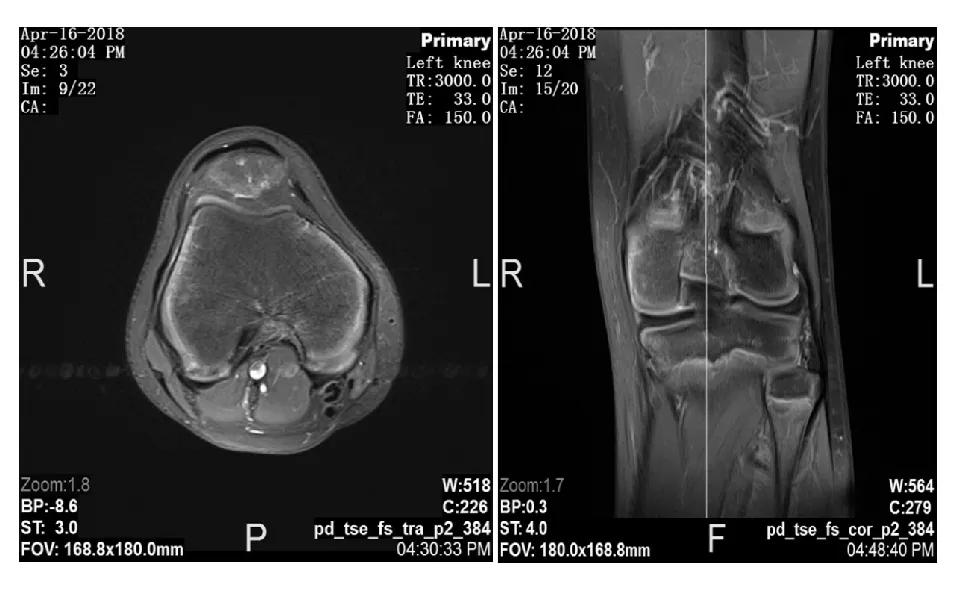
图6 膝关节MRI扫描提示右侧膝关节滑膜增生
讨论:发热是CD的常见肠外表现,约38%的CD患者可有发热症状,然而较少儿童CD患者以发热为主诉就诊[2]。有报道CD患儿发热可能比其他典型表现(如腹部不适、稀便)早数周甚至数月出现[3]。本例患儿尽管有消化道表现——发病前有轻度腹痛、“肛裂”史,但未能引起重视,是CD诊断延误的重要原因。
约50%的CD患儿出现发育滞后[4],病史复习显示发育滞后为本例患儿的首发表现。发育滞后可表现为身材矮小、肌肉含量偏低、青春期延迟、骨密度偏低等,《儿童炎症性肠病发育滞后处理指南》以及关于IBD患儿营养支持的临床报告建议所有IBD患儿定期测量体质量、身高和青春期状况,非活动期患儿建议每4个月测量一次,活动期或确诊有发育滞后者应增加测量频率,以便及时发现异常并进行干预[5-6]。引起儿童患者发育滞后的关键原因是IBD继发营养不良。维生素和微量元素缺乏往往是导致CD肠外表现的关键,如维生素D缺乏可诱发关节炎。在生长发育指标中,身高增长速度是最敏感的指标[6-7]。健康儿童95%生长速度超过4 cm/年,青春期男性可达6~12 cm/年,同龄女性为5~10 cm/年[8]。本例患儿在使用生物制剂、肠内营养以及长期补充维生素D36个月后身高增长7cm,体质量增加5 kg,表明患儿对治疗方案应答良好,也证明了营养干预对于儿童CD患者的重要性。
本例患儿在确诊CD近10个月后出现膝关节病变。关节病变是IBD最常见的肠外表现之一,16%~33%的IBD患者可能出现关节累及,从而导致畸形或功能障碍,因此其早期诊断非常关键[9]。在免疫性疾病领域,SASP是治疗关节病的一线口服缓解病情抗风湿药(DMARDs);在消化内科领域,SASP亦是溃疡性结肠炎(UC)维持治疗的主要制剂之一。《2018中国类风湿关节炎诊疗指南》指出,我国患者使用SASP治疗关节炎安全性良好且具有成本优势[10],初步提示了外周关节病变使用SASP治疗的合理性。然而,目前国内IBD诊治共识中并未提及儿童CD并发关节炎是否可选择SASP治疗[11]。针对本例患儿情况查阅其他相关指南或共识意见,发现2014年发布的关于IBD并发脊柱关节炎的处理的意大利专家共识指出,治疗IBD伴膝关节病变较安全的一线药物是糖皮质激素,其次为SASP[12]。由于糖皮质激素不可用于IBD的维持治疗,且SASP的适应证中包括外周关节病变,因此将该例患儿的维持治疗药物由美沙拉嗪更换为SASP。经SASP治疗4周,患儿关节症状明显改善,且截止至本文整理前末次随访,肠道和关节症状均持续缓解,亦证明SASP可同时用于CD并发关节病变与儿童CD本身的维持治疗。
尽管本例患儿以发热为主诉,但实际首发表现为发育滞后。由于后者隐匿性强,对儿童IBD患者需重视生长发育史的询问,并加强营养干预。对于已使用生物制剂诱导并维持缓解治疗但仍并发关节病变的IBD患者,及时调整抗炎制剂是使患者获得持续缓解的关键途径。

