右美托咪定行超声引导下臂丛神经阻滞时罗哌卡因的半数有效剂量研究
周 艳,凡丽华,张丽君,邓 瑜,卜 岚,刘 征
(海军军医大学长海医院麻醉学部,上海 200433)
随着微创外科的发展,肩关节镜手术日趋增多且逐渐走向技术成熟期,围手术期的创伤越来越小,尤其是手术时间明显缩短,多数外科医师可以将手术时间控制在4 h内,使患者有更多的机会在单纯神经阻滞下接受手术治疗。神经阻滞较全身麻醉的优点显著,如术后镇痛效果好,恶心、呕吐发生率低,但由于神经行走在身体深部,为了达到有效阻滞,麻醉医师往往通过增加局部麻醉药的剂量来降低麻醉失败率,但同时也增加了并发症,其中包括膈神经阻滞、膈肌活动受限,从而影响呼吸;霍纳(Horner)综合征、局部麻醉药中毒、血流动力学波动等严重问题[1]。超声引导下的神经阻滞,可减少局部麻醉药用量[2],使臂丛神经阻滞完成精准注射,显著提高了麻醉成功率,减少了并发症。
右美托咪定是α2肾上腺素能受体激动剂[3],由于其同时具有镇静和镇痛作用,可减少围手术期麻醉药的用量,因此广泛应用于临床。最近有研究表明,右美托咪定与神经阻滞剂联用,可提高神经阻滞疗效,延长作用时间,减少术后阿片类药物用量[4]。故本研究拟确定肩关节镜手术患者行超声引导下臂丛神经阻滞联合使用右美托咪定时0.375%罗哌卡因的半数有效剂量(ED50),为精准麻醉提供更多依据。
1 资料和方法
1.1 仪器和试药 X-Porte超声仪和线性超声扫描探头(美国Sonosite公司)。罗哌卡因(规格75 mg∶10 ml,瑞典AstraZeneca AB公司);右美托咪定(规格200 μg∶2 ml,江苏恒瑞医药股份有限公司)。
1.2 病例选择 选择海军军医大学长海医院麻醉学部2018年6-10月行肩关节镜手术的患者,性别不限,年龄<65岁,美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级Ⅰ或Ⅱ级,无穿刺部位感染、臂丛神经损伤或神经肌肉病变,中枢神经系统和凝血功能未见异常。手术种类仅限于肩关节镜手术。本试验方案获海军军医大学长海医院伦理委员会审查通过,所有患者及家属均签署知情同意书。
1.3 阻滞方法 患者入手术室后,开放外周静脉通路,常规监测心电图、无创动脉血压和脉搏氧饱和度,鼻导管吸氧2 L/min。给予右美托咪定0.5 μg·kg-1·h-1泵注,不给予负荷剂量[4]。患者取仰卧位,头偏向对侧,皮肤常规消毒、铺巾后,将无菌关节套包裹在超声探头,连线放置于无菌操作台,采用 50 mm、频率5~10 MHz的线性超声扫描探头,于超声引导下辨别臂丛的上、中、下干,平面内进针,穿过上干与中干之间至前斜角肌表面(见图1A),回抽无血后,注入0.375%罗哌卡因目标容量的一半,退穿刺针至中斜角肌表面,回抽无血后,注入0.375%罗哌卡因剩余容量(见图1B)。注射完成后局部麻醉药分布见图2。0.375%罗哌卡因由75 mg∶10 ml罗哌卡因与生理盐水按1∶1比例稀释配制而成。用于肌间沟臂丛神经阻滞的0.375%的罗哌卡因剂量由改良序贯法确定。首剂量为100 mg,即0.375%罗哌卡因溶液26.7 ml,相邻两个患者所用剂量之间的比值为1.2。即当前患者的罗哌卡因的剂量由上一例患者的阻滞情况决定,若上一例患者麻醉阻滞效果呈阳性,则当前患者使用的罗哌卡因剂量升1个阶梯;若呈阴性,则当前患者使用的罗哌卡因剂量降1个阶梯。当出现三个平衡点后将改变的幅度调整至一半。采用序贯法计算复合右美托咪定行超声引导下臂丛神经阻滞时罗哌卡因的ED50及95%可信区间。
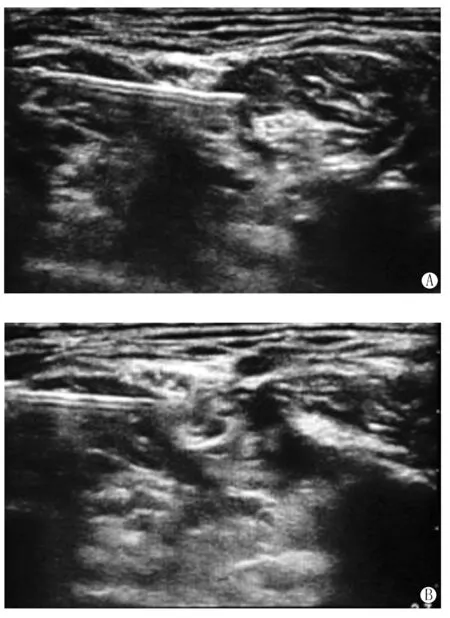
图1 超声引导下行臂丛神经阻滞的过程Figure 1 The process of ultrasound-guided interscalene brachial plexus blockA:穿刺针在前斜角肌表面;B:穿刺针退至中斜角肌表面
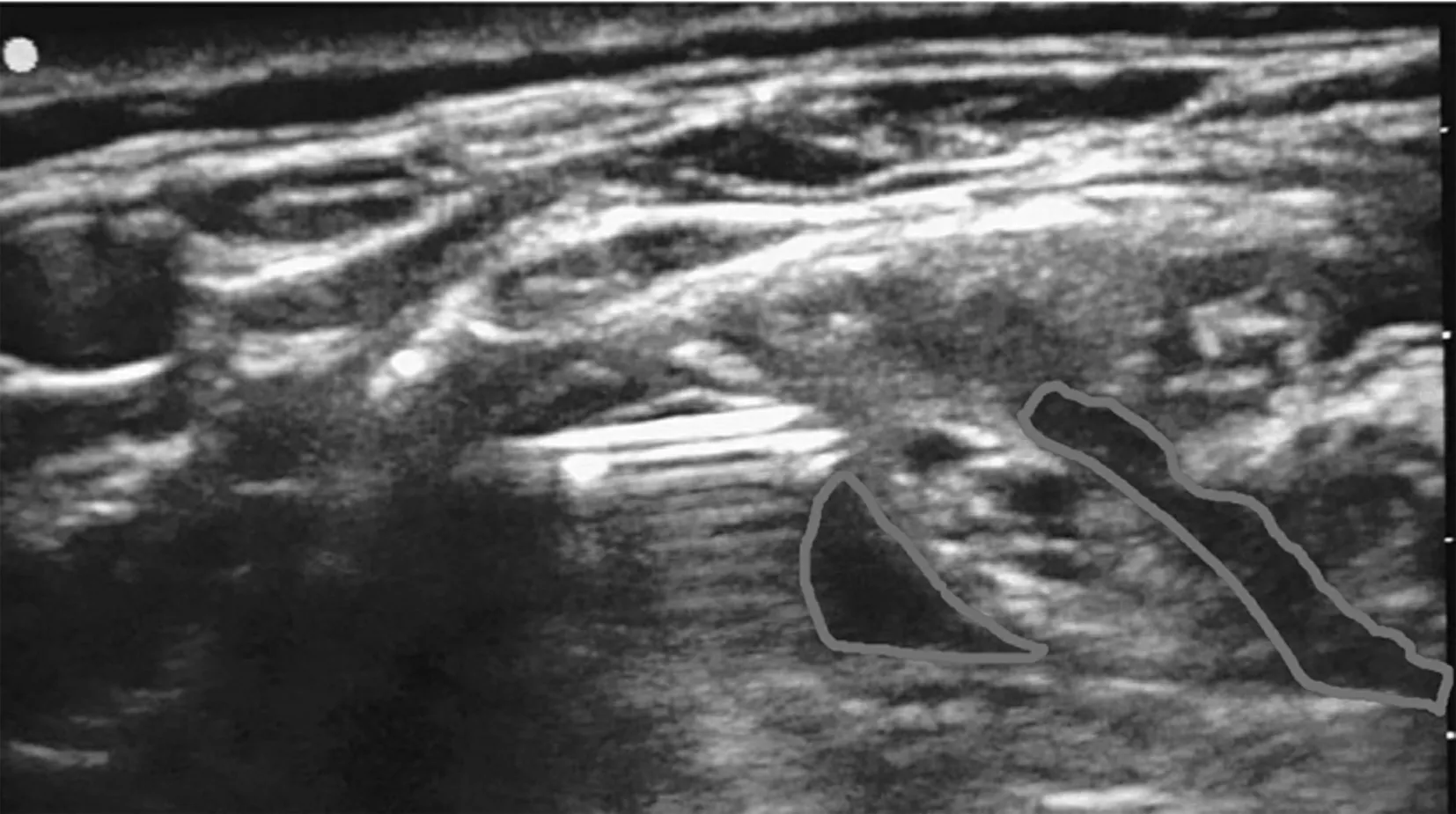
图2 肌间沟注入臂丛神经阻滞后的药物分布Figure 2 Drug distribution after brachial plexus block by intermuscular sulcus injection
1.4 神经阻滞和麻醉效果评价指标 采用单盲法给药,在注射罗哌卡因后30、35、40 min评价阻滞效果,即臂丛神经支配区域的感觉和运动阻滞情况。采用针刺法评价感觉神经(C5~T1)的阻滞情况:有针刺痛为1分,无针刺痛为0分。测试感觉神经阻滞的皮肤区域包括:三角肌下端(C5)、前臂下端桡侧(C6)、手背2~3指间(C7)、手背4~5指间(C8)、前臂内侧上端(T1)。感觉评分≥2,说明臂丛神经阻滞不全或失败,需更改麻醉方式为喉罩全身麻醉,同时剔除患者。以是否能握拳评估运动阻滞情况。麻醉效果评价:术中患者感到疼痛,无需或需辅助镇痛药(瑞芬太尼0.06~0.1 μg·kg-1·h-1)为阳性;术中患者未感到疼痛为阴性。
1.5 药品不良反应(ADRs)观察及满意度评价 记录Horner综合征、窦性心动过缓(心率<50次/min)、低血压[平均动脉压(MAP)<60 mm Hg或MAP<70 mm Hg且比正常情况下降>30 mm Hg]等ADRs发生情况。在术后4、6、8 h的随访中对患者的满意度进行了评估,分为非常满意、满意、不满意。
2 结 果
2.1 病例资料 试验共观察患者31例,1例患者因术前神经阻滞效果感觉评分≥2,复合了全身麻醉而剔除出试验。实际共纳入患者30例,其中男11例,女19例;年龄(58±8.9)岁,身高(167±5.9) cm,体重(65±13.9) kg,手术时间(118.9±21.6) min,麻醉时间(161.8±30.0) min;手术体位:沙滩椅位12例,侧卧位18例。
2.2 神经阻滞效果及用药剂量 所有患者均可耐受手术且顺利完成了手术。在超声引导下,应用不同剂量的罗哌卡因行肌间沟臂丛神经阻滞的患者用药量见图3。采用改良序贯法计算得复合右美托咪定用于超声引导下臂丛神经阻滞时0.375%罗哌卡因的ED50为19 ml,95%可信区间为17.5~21.5 ml。其中术中麻醉效果呈阳性患者16例,加用瑞芬太尼0.06~0.1 μg·kg-1·h-1;阴性患者14例。所有患者在阻滞45 min时和术后4 h的评估中均能完成握拳动作。

图3 患者在超声引导下行臂丛神经阻滞应用0.375%罗哌卡因的用药量分布Figure 3 Dosage distribution of 0.375% ropivacaine in ultrasound-guided interscalene brachial plexus block○:麻醉效果呈阳性;●:麻醉效果呈阴性
2.3 ADRs观察及满意度评价结果 1例患者术中出现了心动过缓,心率最低至35次/min,该患者使用0.375%罗哌卡因卡因26.7 ml。患者呈沙滩椅位复原平卧位,予阿托品0.5 mg,静脉推注+麻黄素6 mg,静脉推注后恢复正常,继续完成了手术。1例患者出现了Horner综合征,未予特殊处理,手术结束时恢复正常。所有患者术后8 h内均未使用辅助镇痛药,术后8 h的疼痛数字评分法(number rating scales,NRS)评分均≤3分。72%的患者满意度评价结果为非常满意,28%的患者满意。
3 讨 论
Vorobeichik等[8]对32项关于右美托咪定在区域阻滞方面的临床研究进行分析,对单独使用局部麻醉药(对照组)及局部麻醉药联合右美托咪定(右美托咪定组)的研究提示,右美托咪定联合局部麻醉药可以延长患者运动阻滞时长达58%,且明显缩短患者的感觉和运动阻滞起效时间,延长患者镇痛时间,显著减少术后镇痛药物的使用。本研究目的在于确定右美托咪定的使用是否可以减少局部麻醉药物的用量。在本研究中复合使用右美托咪定时,0.375%罗哌卡因的ED50为19 ml,即70 mg,与传统经验建议的100 mg相比,降低了30 mg,约减少8 ml的容量,因为容量的减少和浓度的降低,明显减少了臂丛神经阻滞麻醉的相关并发症,如Horner综合征、隔神经抑制所致的呼吸困难及围手术期显著的心动过缓发生率[9]。罗哌卡因作用时间为2~6 h[10]。本研究结果表明,复合右美托咪定术后镇痛时间明显延长,术后8 h所有患者臂丛神经支配的感觉区域刺痛为不痛,全部患者活动时的疼痛NRS评分≤3分,且术后所有患者均未使用辅助镇痛药。
罗哌卡因是用于神经阻滞的常用局部麻醉药之一,已有研究发现在应用低浓度罗哌卡因时可以实现感觉与运动分离[11-12]。本研究中臂丛神经阻滞后,患者均能完成握拳动作,有利于患者术后自主活动和康复。本研究中有1例患者术中出现了心动过缓、低血压事件。臂丛神经阻滞下行肩关节镜手术的心动过缓、低血压事件发生率高达28%[13]。该患者为本研究的第一位患者,手术体位为沙滩椅位,事件发生在手术开始后的30 min,实施麻醉后的80 min,与文献报道的低心率、低血压事件发生时间相似[13]。同时该患者也是本研究中罗哌卡因使用剂量最高的患者,可能是因为高容量局部麻醉药扩散至相关神经,影响了心脏的节律,从而导致低血压、低心率事件。该例低血压、心动过缓事件是否与联合使用的右美托咪定相关,尚需进一步的对照研究来确定。
本研究采用改良序贯法探索药物的ED50,该方法也称为上下法,是从“up and down” 或“Dixon-Massey”等英文原名翻译所得。与传统的药物有效剂量测定方法相比,改良序贯法的优势在于后面一个研究对象的药物使用剂量取决于前面一个研究对象的结果,并且以相同比例增加或减少剂量,大大减少了研究样本量,目前广泛应用于临床研究药物有效剂量的探索[7,14]。

