凝血因子Ⅹa抑制剂专利技术分析
赵冬梅,房长进,邱志霞
(1国家知识产权局专利局专利审查协作江苏中心,苏州 215163;2中国药科大学中药学院,南京 210009)
血栓能够引起血管腔狭窄与闭塞,导致组织缺血或坏死,从而引发各种心脑血管疾病。临床上用于治疗血栓疾病的药物主要包括溶血栓类药物、抗血小板聚集类药物以及抗凝血类药物。目前,抗凝血治疗是心脑血管疾病的主要预防和治疗措施[1]。
凝血因子Ⅹa是一种凝血酶形成过程中所必需的凝血因子,如图1所示,其占据了凝血瀑布反应中的中心位置,凝血因子Ⅹa通过与Va形成凝血酶原复合物,催化凝血酶原(Ⅱ)转化为凝血酶(Ⅱa),触发凝血级联反应的发生,从而导致血栓的形成[2]。正因为位于凝血途径中的关键环节,凝血因子Ⅹa已经逐渐成为抗凝药物研发中的极具吸引力的靶标。
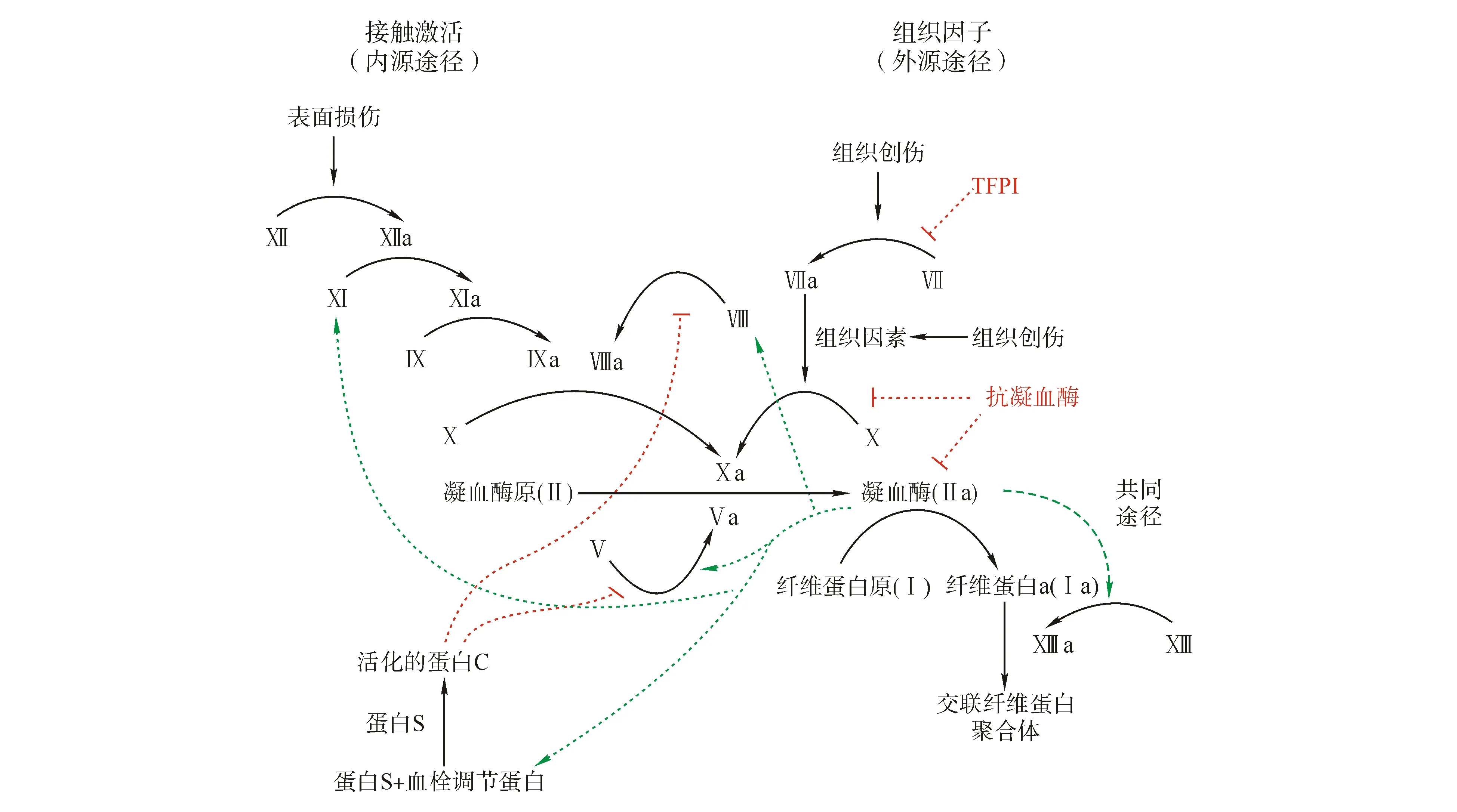
图1 Ⅹa复合物催化凝血酶原(Ⅱ)转化为凝血酶(Ⅱa)
抗凝血药物通过直接抑制凝血因子Ⅹa活性从而抑制凝血酶Ⅱa产生,包括肽类和合成的小分子化合物,其中合成的小分子化合物已经成为抗凝药物开发热点。本文从凝血因子Ⅹa抑制剂的专利技术入手,通过梳理重点企业专利申请中化合物的结构改造和修饰脉络,对相关化合物的技术发展和演进进行分析,总结凝血因子Ⅹa抑制剂可改造的结构位点和潜在修饰方向,以期能够为国内研发机构和相关企业对凝血因子Ⅹa的新药研发、专利保护以及知识产权布局提供有益的参考和建议。
1 相关专利申请趋势
笔者以“factor Xa s inhibitor?,factor X s inhibitor?,FXa s inhibitor?,+xaban+”为关键词在德温特世界专利索引数据库(DWPI)进行检索,截止2018年6月8日,涉及凝血因子Ⅹa抑制剂的发明专利申请共计1 721项(同一专利进入不同国家的同族申请被称为一“项”)。图2反映了凝血因子Ⅹa抑制剂相关发明专利申请总体趋势。
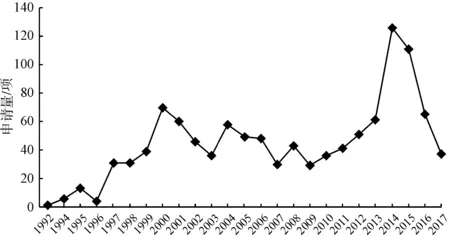
图2 凝血因子Ⅹa抑制剂相关发明专利申请的申请量趋势
由图2可见,凝血因子Ⅹa抑制剂的发明专利申请量总体呈上升趋势,从2011年起逐步上升,2013年至2015年更是快速发展,这也与热点抗凝血药物上市时间一致。例如,由百时美施贵宝公司与辉瑞公司合作开发的口服抗凝血药物阿哌沙班(Apixaban),其于2011年5月首先在欧盟上市,2012年12月获FDA批准在美国上市,2013年1月获CFDA批准进入中国,该药2017年的全球销售额为74亿美元,跻身当年全球畅销药物前10名。可见,从2011年开始,随着“重磅炸弹”式药物进入市场,针对基于抑制凝血因子Ⅹa的抗凝血药物的专利申请也日益增加,说明凝血因子Ⅹa逐渐引起人们极大的重视。此外,由于发明专利申请通常自申请日起满18个月才公布,2016-2017年所呈现的专利部分可能仍处于未公开状态,因此,不能代表相应时期的申请量趋势。
2 主要申请人分析
图3反映了凝血因子Ⅹa抑制剂化合物领域主要申请人的分布情况。百时美施贵宝63项、默沙东50项、赛诺菲安万特38项,位列前三甲;武田制药、拜耳、广东东阳光、罗氏、礼来、辉瑞、勃林格殷格翰申请量也很可观。
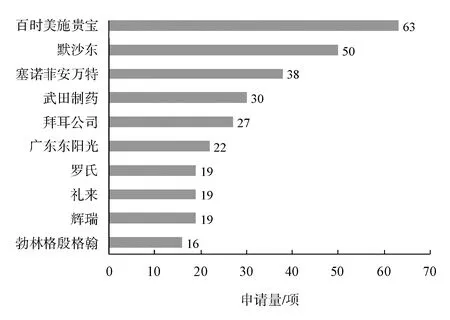
图3 凝血因子Ⅹa抑制剂化合物主要申请人分布
从图3可以看出,申请量前10位的所有申请人均为企业,没有高校或科研院所,且主要申请人集中在百时美施贵宝、默沙东、赛诺菲安万特、武田制药等国外大公司中,也反映出这一领域的研发创新是以企业为主体,以市场为驱动的。值得一提的是,国内企业广东东阳光药业有限公司,排名位列第6,可见从核心专利申请量的角度,国内申请人在该领域也有不俗的表现。
3 凝血因子Ⅹa抑制剂结构
阿哌沙班(apixaban)以及上市较早的利伐沙班(rivaroxaban)均是具有高选择性、强竞争性的口服直接凝血因子Ⅹa抑制剂的代表药物,两者虽然在化学结构上差异较大,但是与凝血因子Ⅹa却具有类似的结合模式,如图4和图5所示[3]:药物分子均以“L”形构象与凝血因子Ⅹa结合,两者与凝血因子Ⅹa蛋白结合的晶体复合物已经得到实验解析。
根据上述结合模式,可将凝血因子Ⅹa抑制剂结构分为如下3个部分(如图6),以阿哌沙班为例,P1、P4部分与蛋白S1、S4口袋相互作用,中心支架部分作为连接基团与S2、S3口袋相互作用。
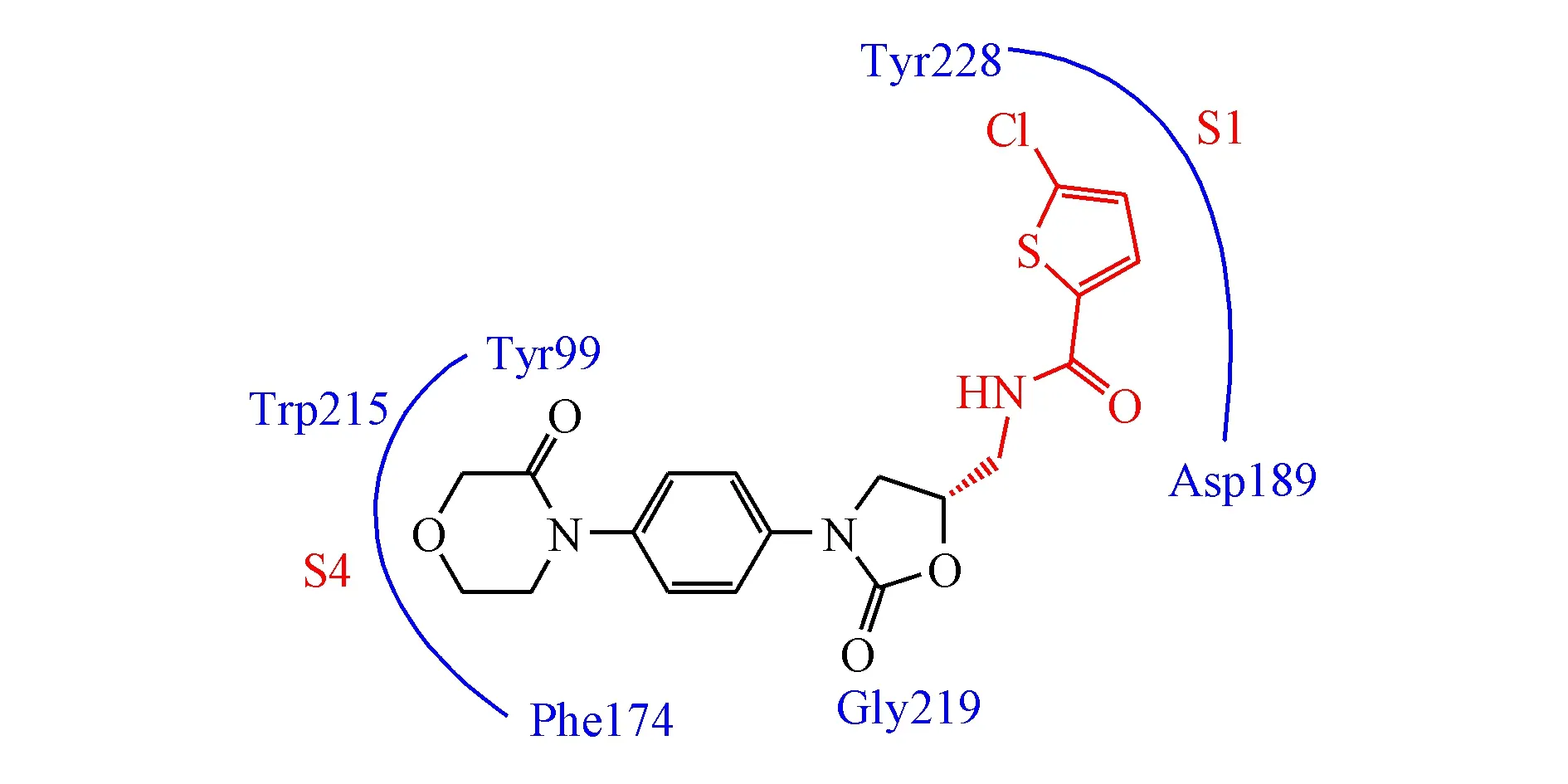
图4 利伐沙班与凝血因子Ⅹa结合模式图
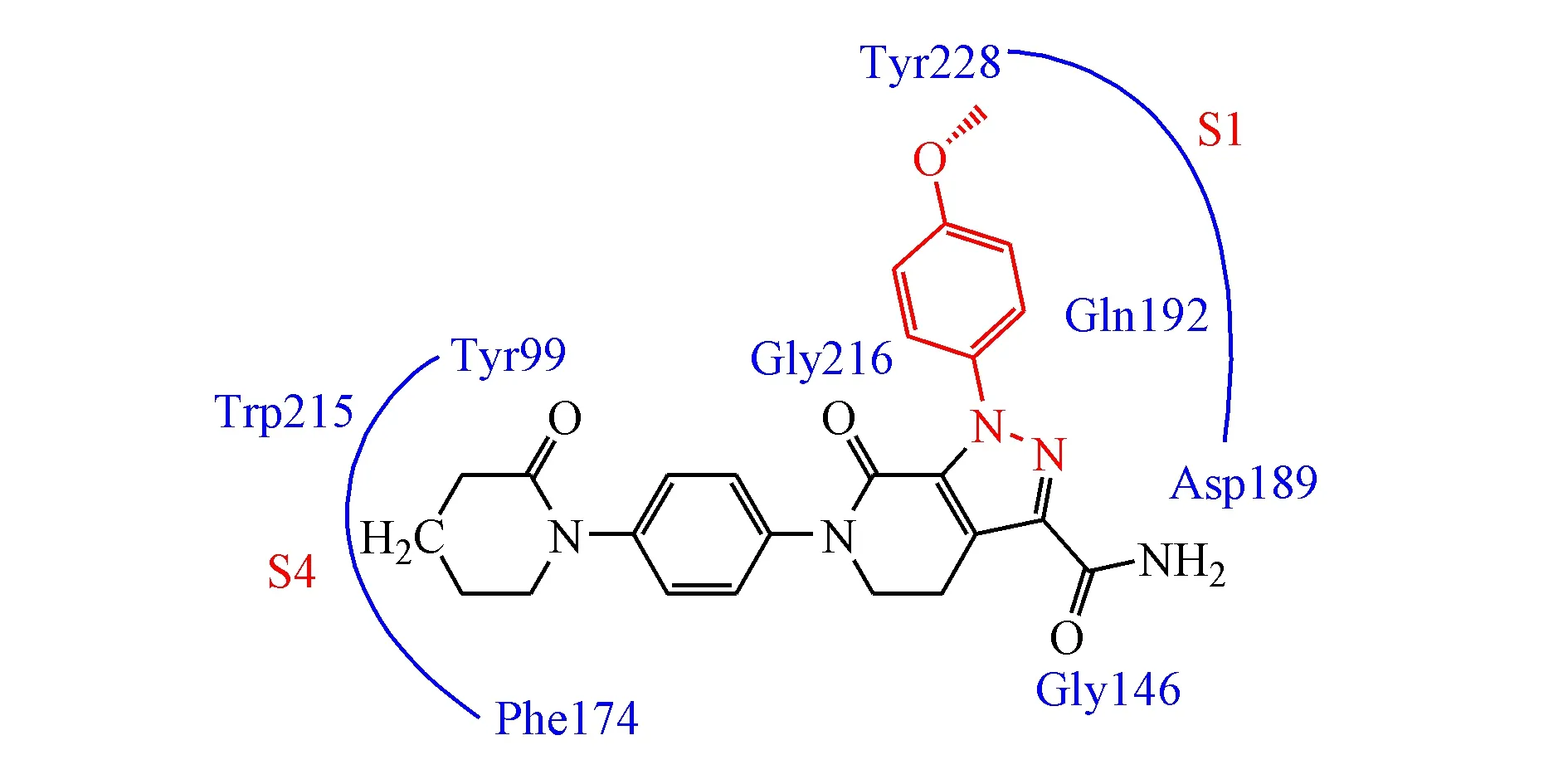
图5 阿哌沙班与凝血因子Ⅹa结合模式图
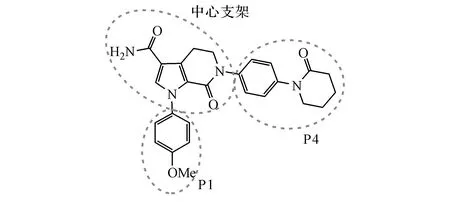
图6 凝血因子Ⅹa抑制剂3个部分划分示意图[4]
4 主要申请人的技术演进和发展
由于同一申请人的研发思路和专利布局通常比较清晰,结构修饰有据可依,构效关系有规律可循,因此笔者以该领域重点申请人为代表,以化合物结构改造为主线,梳理其专利布局的方向和脉络。
4.1 百时美施贵宝公司
百时美施贵宝公司为这一领域重要的申请人之一,心脑血管疾病是该公司的一条重要的研发管线,除阿哌沙班之外,多种药物已经上市或处于临床研究阶段。基于凝血因子Ⅹa抑制剂与底物的3部分结合位点,以下分3个方面详细介绍。
事情进展得很顺利,小虫得手了。玉敏摸着黑到了家,小虫就把玉敏拉进屋,关上门,从箱子里拿出了紫红色钻戒。玉敏捏着钻戒,左瞅右瞅,惊奇地说,和我卖给许沁的那款太像了,款型大小都一样,色泽也差不多。小虫竖起拇指,说那就好办了,你明天拿回店里,对雨落她们就说,许沁把钻戒还了。玉敏说她们会信么?小虫说,就这么说,信不信由她们。玉敏点点头。小虫吁了口气,说钻戒总算还了,我们再不用愁肠百结了。玉敏的眼泪突然迸发出来,趴在小虫肩上说,小虫,谢谢你。小虫抹去玉敏的泪,说谢什么,我不只是帮你,也是帮我自己嘛。我老婆去坐牢,我的日子多难熬。玉敏含着泪,说我们把钻戒还了,可姑妈呢?小虫说对于姑妈,这是九牛一毛。
4.1.1 中心支架(连接基团)部分 S2、S3口袋的主要残基为Gly219和Gly216,处于口袋中部,构成“凹槽”,可与药物分子中心支架部分形成氢键相互作用。该部分结构可分为饱和含氮杂环类、吡唑甲酸类、吡唑并哌啶酮类、(杂)芳基甲酰胺类、内酰胺类五个类别。
饱和含氮杂环类 1994年,百时美施贵宝公司提交了第一份凝血因子Ⅹa抑制剂相关专利申请US 19940323336,其中心支架部分为氨烷基酰胺基团取代的五元或六元饱和含氮杂环;1995年提交的专利申请US 19950555561中心支架不变;1996年提交的专利申请US 19960708292将氨烷基中的氨基进行修饰,即通式中的“Z”基团,除氨基外还可以为氧(图7)。
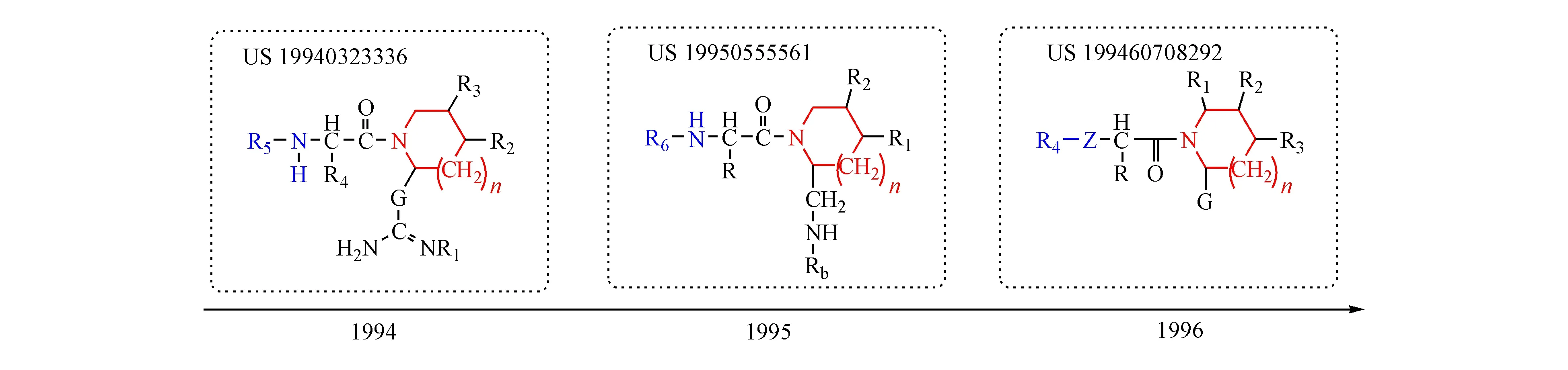
图7 饱和含氮杂环类凝血因子Ⅹa抑制剂相关专利申请
吡唑甲酸类 2000年提交的专利申请US 20000492708、同年提交的专利申请CN 00819731和2002年提交的专利申请US 20020033137将中心支架部分替换为五元芳香含氮杂环。如图8所示,其中吡唑甲酸类取得了突破性的研究进展,如化合物SN429即专利申请US 20000492708中的实施例化合物,其对凝血因子Ⅹa的抑制常数达到0.013 nmol/L,但由于分子中含有强碱性的脒基,不利于口服给药。将脒基替代为乙胺基或氨基唑后,得到口服有效的化合物DPC423和雷扎沙班(razaxaban)(图9),其对凝血因子Ⅹa的抑制常数均为0.15 nmol/L,目前化合物DPC423已经进入临床Ⅰ期,雷扎沙班进入临床Ⅱ期[5]。
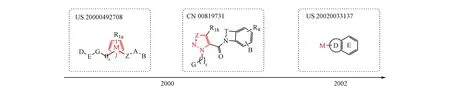
图8 吡唑甲酸类凝血因子Ⅹa抑制剂相关专利申请
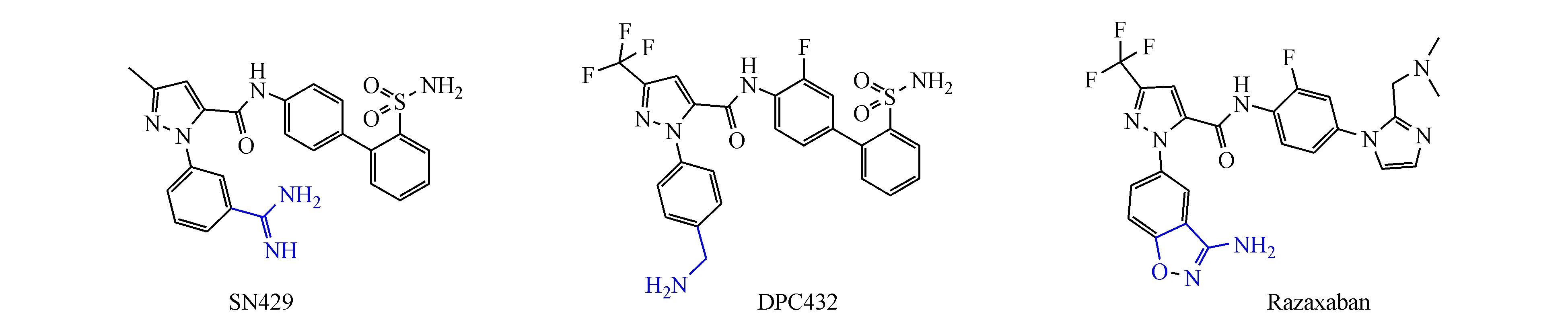
图9 吡唑甲酸类具有代表性的候选药物
内酰胺类 如图10所示,2000年提交的专利申请US 20000496571中心支架结构为内酰胺,优选为胍基取代的己内酰胺,2001年提交的专利申请US 20010874739增加了内酰胺上的取代基团数量,并将侧链胍基替换为脒基,2002年提交的专利申请US 20020118102尝试在内酰胺环上增加氮原子数量,并考察环上的饱和度带来的影响,将胍基、脒基进行刚性结构处理,将两个氮原子用亚烷基连接,形成含有两个氮原子的杂环结构,并进一步替换为其他的杂环。
吡唑并哌啶酮类 据文献报道[5],吡唑甲酸类化合物虽然对凝血因子Ⅹa有很好的抑制效能,但是由于含有吡唑甲酰胺结构,在生理条件下可能会释放出相应的羧酸及可致基因突变的苯胺,因此在后续的申请中,百时美施贵宝公司在吡唑中心支架上引入一个刚性的六元环哌啶结构即吡唑并哌啶酮,如图11所示:2001年提交的专利申请US 01811579即以此为优选的中心支架结构,并对两个环的结构进行了类似基团的替换,如五元环中的M1、M2均可以为碳或取代的氨基,右侧的哌啶酮还可以为七元环,其中的一个碳原子还可以替换为氮,当五元环为吡唑时,优选为三氟甲基取代;2002年提交的专利申请US 20020124383和US 20020124360将中心支架固定为吡唑并哌啶酮,Ra和R1优选为三氟甲基和氨甲酰基;同年提交的专利申请US 20020105477和US 20020153482继续考察中心支架的结构,将P从含氮五元杂环扩展为含氮、氧、硫的五元杂环,将M扩展为六元或七元含氮、氧的羰基取代的饱和、不饱和杂环,并对环上的取代基团P1~P3、M1~M3进行了选择和替换;2002年提交的专利申请CN 02821537也对中心支架基团进行了多种选择,并且在从属权利要求中将中心支架固定为吡唑并哌啶酮,相应授权专利保护了一系列具体化合物,其中即涵盖了阿哌沙班,该专利的申请日为2002年9月17日,专利到期日为2022年9月17日,随着专利到期日即将到来,已引起了国内众多企业的高度关注。
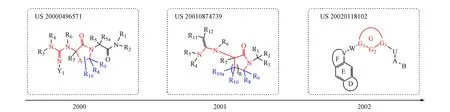
图10 内酰胺类凝血因子Ⅹa抑制剂相关专利申请
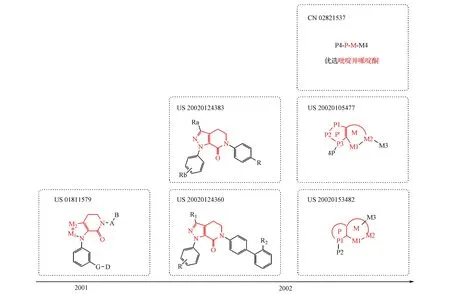
图11 吡唑并哌啶酮类凝血因子Ⅹa抑制剂相关专利申请
4.1.2 P1部分 S1是凝血因子Ⅹa的特异性结合口袋,也是决定底物特异性的主要因素之一,该口袋为一狭窄裂缝,主要由Tyr228和Asp189等构成的小的疏水口袋;凝血因子Ⅹa抑制剂与这一部分结合的结构称为P1部分,例如,利伐沙班的氯噻吩基团和阿哌沙班的甲氧苯基进入S1区域,两者均为取代(杂)芳基,插入该小的疏水口袋[6-7]。
百时美施贵宝公司早期专利中,P1部分多为强碱性的胍基或脒基(表1),US 5561146的P1部分固定为G连接的脒基,其中G可以为酰胺烷基或长链烷基取代的氨基、杂环基,当G为取代氨基时,P1部分与蛋白作用的取代基团即为胍基,胍基/脒基上的氨基还可以被氨基、羟基、氰基、烷氧基等基团取代;CN 1307560的P1部分为烷基胍;US 5583146公开的P1部分除上述基团外,还可以为酰胺烷基取代的杂环基、取代的胍、脒或氮甲基胺;US 6548512中的-D-E为4-脒基苯基;4(5)-卤素-3-脒基(氨基、酰胺基、甲氨基)苯基。
表1 凝血因子Ⅹa抑制剂P1部分结构修饰
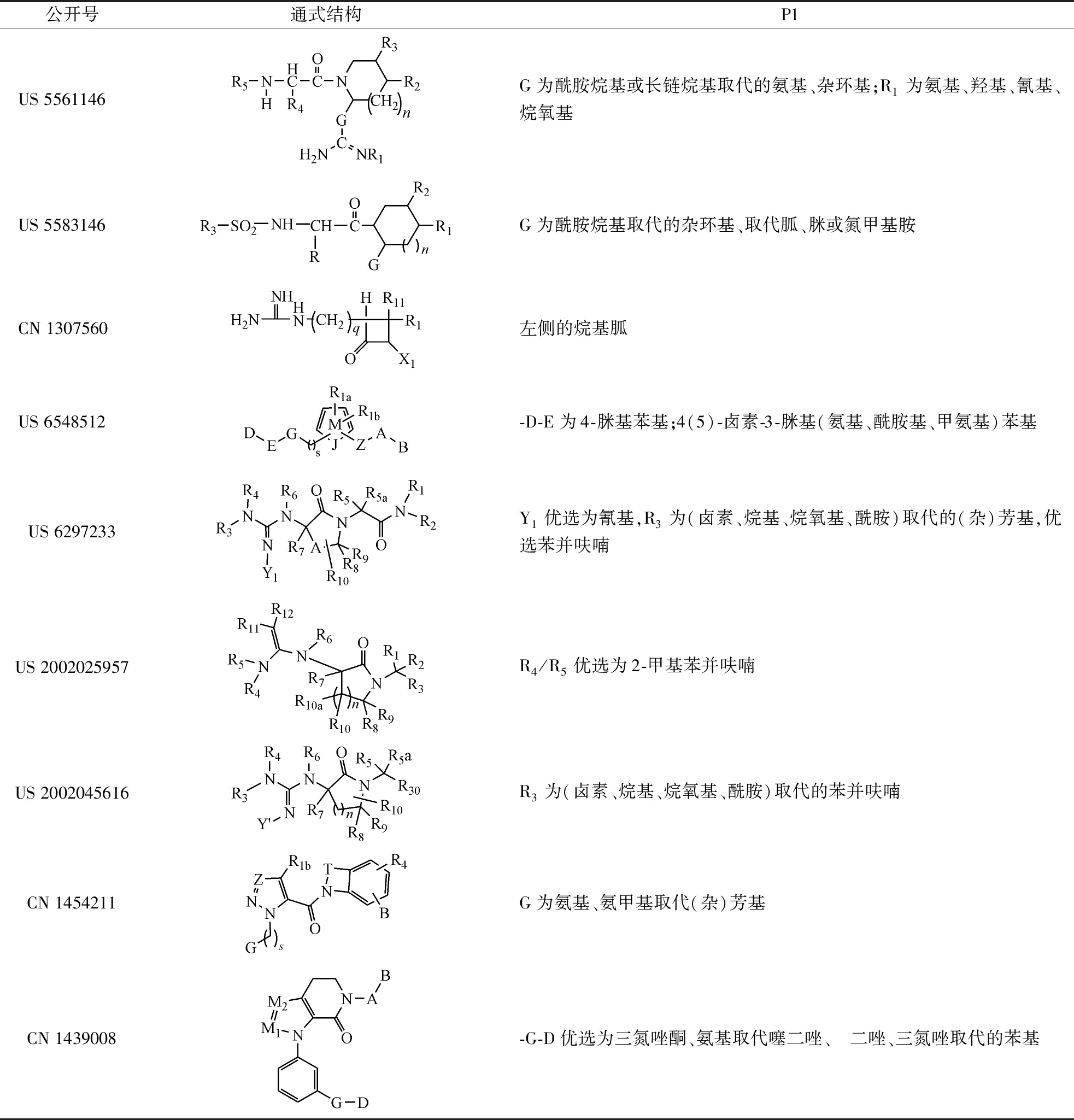
公开号通式结构P1US5561146G为酰胺烷基或长链烷基取代的氨基、杂环基;R1为氨基、羟基、氰基、烷氧基US5583146G为酰胺烷基取代的杂环基、取代胍、脒或氮甲基胺CN1307560左侧的烷基胍US6548512-D-E为4-脒基苯基;4(5)-卤素-3-脒基(氨基、酰胺基、甲氨基)苯基US6297233Y1优选为氰基,R3为(卤素、烷基、烷氧基、酰胺)取代的(杂)芳基,优选苯并呋喃US2002025957R4/R5优选为2-甲基苯并呋喃US2002045616R3为(卤素、烷基、烷氧基、酰胺)取代的苯并呋喃CN1454211G为氨基、氨甲基取代(杂)芳基CN1439008-G-D优选为三氮唑酮、氨基取代噻二唑、二唑、三氮唑取代的苯基
从上述早期专利申请中可以看出,正是由于S1口袋的Asp189为酸性残基天冬氨酸,能够与胍基或脒基等碱性残基产生直接的相互作用,但如上述化合物SN429,强碱性基团如脒基、胍基的存在不利于口服给药,因此研发人员尝试将其进行取代或用其他相对弱碱性基团进行替代。如表1所示,US 6297233中的Y1优选为氰基,R3为(卤素、烷基、烷氧基、酰胺)取代的(杂)芳基,优选为取代的苯并呋喃;US 2002025957中的R4/R5优选为2-甲基苯并呋喃;US 2002045616中的R3为(卤素、烷基、烷氧基、酰胺)取代的苯并呋喃;CN 1454211中的G为氨基、氨甲基取代(杂)芳基;CN 1439008中的-G-D优选为三氮唑酮、氨基取代噻二唑、二唑、三氮唑取代的苯基。
由于蛋白S1为特异性结合口袋,因此P1部分比较保守,且由于该口袋体积较小,含有天冬氨酸残基,P1多数为体积较小的呈强碱或弱碱性的取代基团,如脒基、胍基、氨基、酰胺基等。需要说明的是,该位置的取代基还优选为卤素和甲氧基,最具代表性的是利伐沙班和阿哌沙班,这两种基团显然不具备碱性,经过晶体结构分析,研究人员发现,该类取代基团与上述碱性取代基团的结合模式并不相同,氯或甲氧基在蛋白S1口袋底部与Tyr228的芳环通过相互作用形成特异性结合,两者中间的连接基团可以为杂芳基、芳基、杂环基、环烷基、烷基链等,这部分结构可以进行较大差异的替换和改造。
4.1.3 P4部分 蛋白S4是凝血因子Ⅹa的芳香性口袋,由残基Phe174、Tyr99和Trp215形成,凝血因子Ⅹa抑制剂与这一部分结合的区域称为P4部分,例如,利伐沙班的吗啉酮苯基和阿哌沙班的哌啶酮苯基即进入蛋白S4区域。
专利申请US 6548512、US 6500855、US 20030018023、US 2003087909、US 2003096804中P4部分均以-Z-A-B表示,Z为C(O)NH或C(O)CH2,A为取代的(杂)芳基,B为Y或-X-Y,X为亚甲基、羰基、取代的亚甲基氨基、取代的甲酰胺基、取代氨基、氧,Y为取代氨基或取代的(杂)环或(杂)芳基。CN 1454211将Z固定为甲酰基,A为苯并5元-7元含氮、氧杂(芳)环,B为氨基磺酰基、氨基烷基、磺酰基取代的(杂)芳基、四氢吡咯羰基、(苯并)咪唑基。
4.1.4 小 结 从以上对百时美施贵宝公司的相关化合物专利申请的分析可知,如图12所示,对于凝血因子Ⅹa抑制剂的中心支架、P1、P4 3个部分:中心支架部分起到支撑的作用,并且含有能够与氨基酸残基形成氢键的羰基或氨基,结构变化较多。P1部分又可分为G-E-D 3个砌块,D相对保守,可以为强碱性或弱碱性的脒基、胍基、氨基、酰胺基等基团,也可为卤素、甲氧基;E作为连接基团可以为杂芳基、芳基、杂环基、环烷基、烷基链等,可替换基团较多;G如果存在,可以为酰基、磺酰基等。P4同样可分为3个部分,Z、A区域较为保守,Z可不存在或与A共同选自(杂)芳基、长链烷基或环烷基;B变化较多,可采用杂芳基、芳基、酰胺、磺酰基、卤素、氰基、烷基、环烷基等基团替换。

图12 百时美施贵宝公司凝血因子Ⅹa抑制剂结构示意图
4.2 广东东阳光药业有限公司
广东东阳光药业有限公司(以下称为“东阳光”)是我国国内研发实力排名靠前的重点医药企业,专利申请量也名列前茅,如前述申请人分析可知,就申请量而言,东阳光是唯一一家跻身前十的中国药企。对于其申请的直接凝血因子Ⅹa抑制剂专利申请,共计25件,申请日为2014年9月的有13件,2014年12月的有11件,2015年1月1件,可见申请较为集中,根据中心支架可将结构划分为3组。
4.2.1 吡啶并哌啶酮类 在阿哌沙班的基础上,对凝血因子Ⅹa抑制剂进行结构改造。根据“4.1.4”项的结构划分原则,对阿哌沙班的结构进行划分,如图13所示,支架和P1部分的D、E基团基本未做修饰,改动主要在P4部分的B位置。位置B除了哌啶酮外,还可以为取代的哌啶酮、取代的氧杂环丁烷、N-吗啉甲酰基,以及甲基和如表2所示的其他杂环。位置A除苯基外还考察了哌啶并噻唑基、丁炔基。此外,还尝试对R1进行修饰,除氨甲酰基外,也可以为乙氧基羰基、氢。
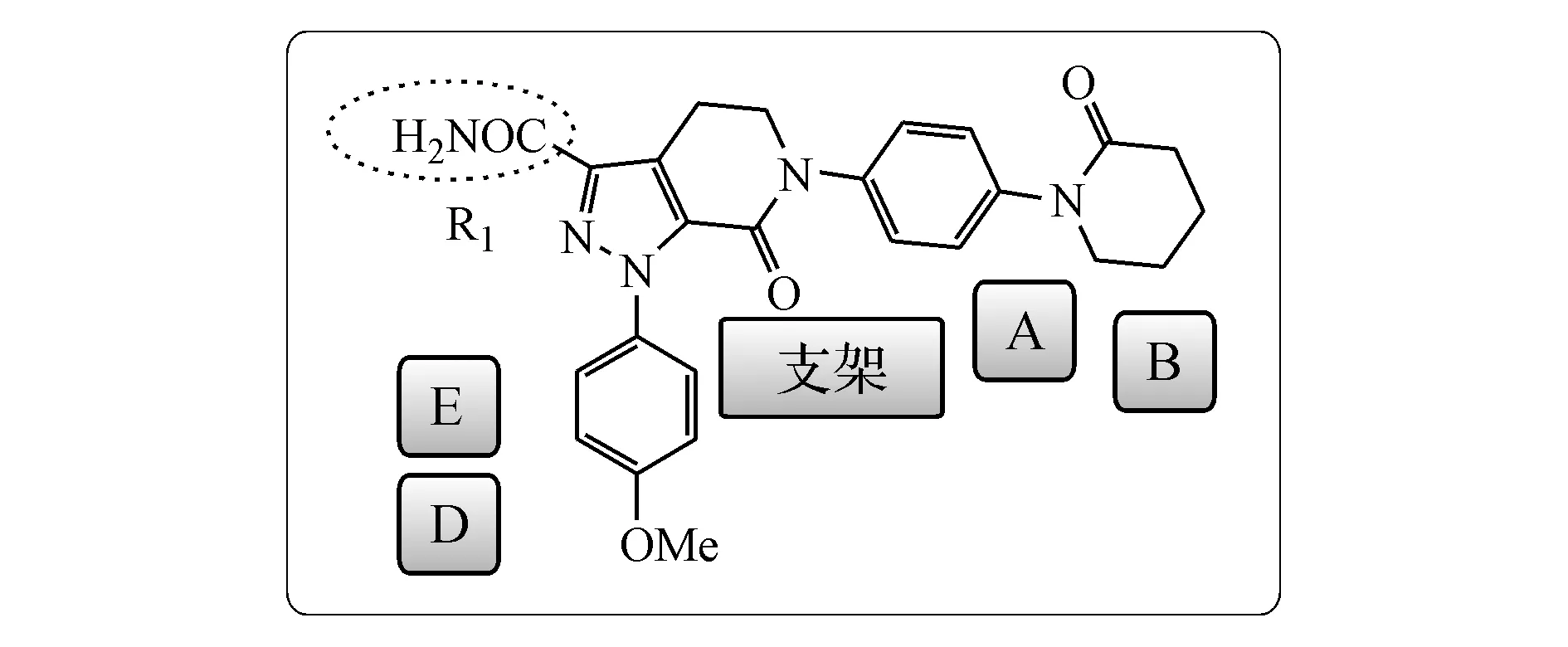
图13 阿哌沙班各部分示意图
表2 广东东阳光药业有限公司吡啶并哌啶酮类凝血因子Ⅹa抑制剂主要结构修饰
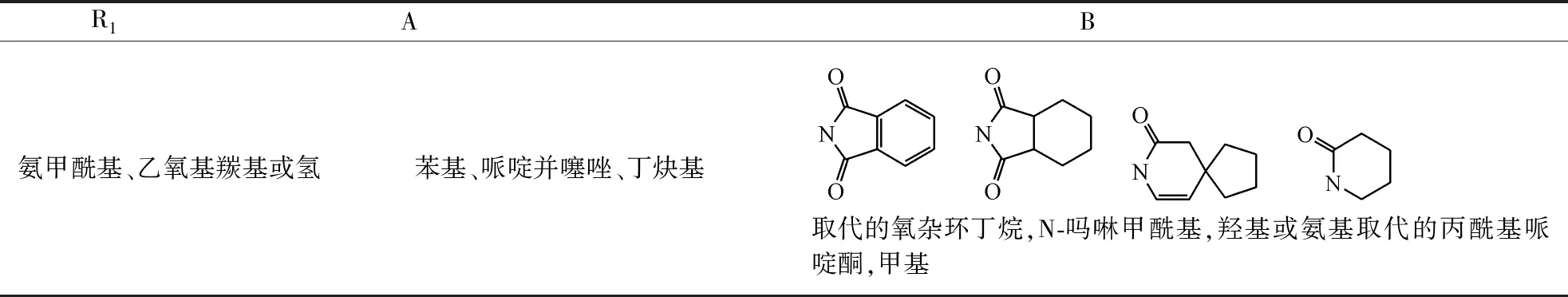
R1AB氨甲酰基、乙氧基羰基或氢苯基、哌啶并噻唑、丁炔基 取代的氧杂环丁烷,N-吗啉甲酰基,羟基或氨基取代的丙酰基哌啶酮,甲基
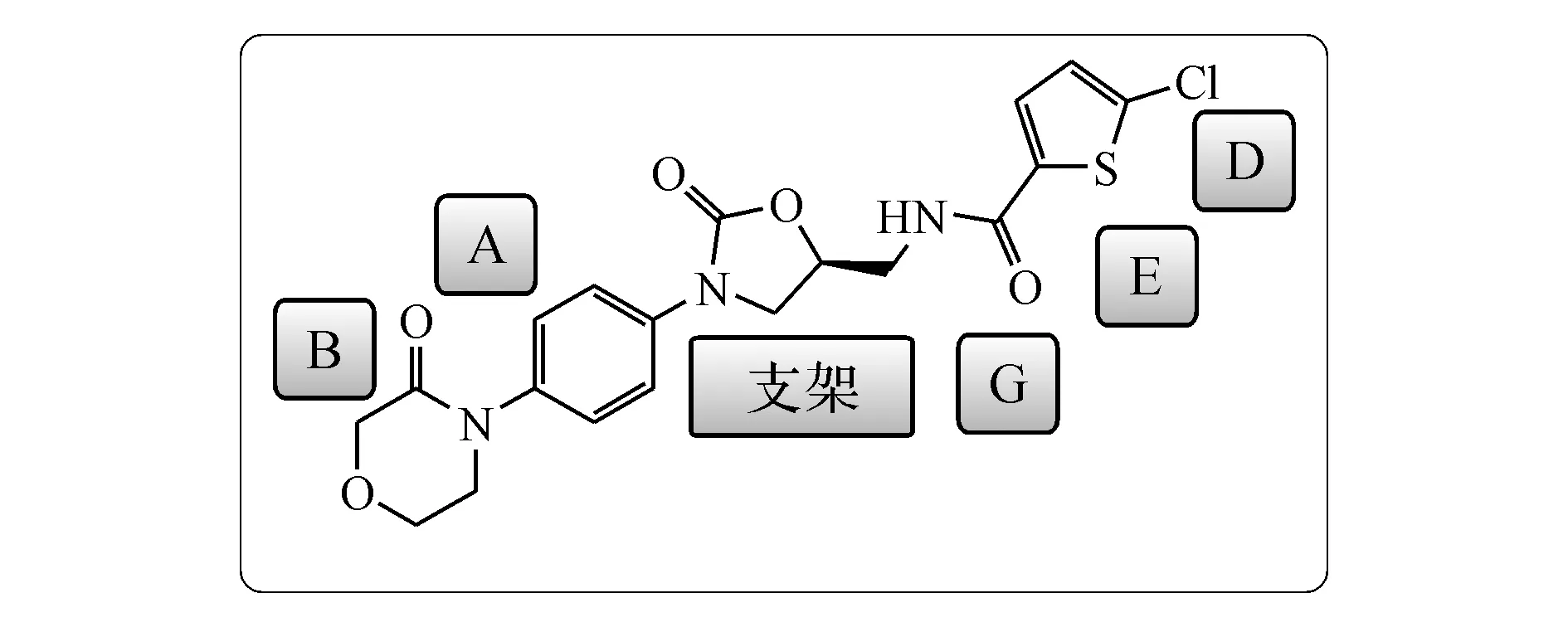
图14 利伐沙班各部分示意图
表3 广东东阳光药业有限公司唑烷酮类凝血因子Ⅹa抑制剂中心支架结构修饰
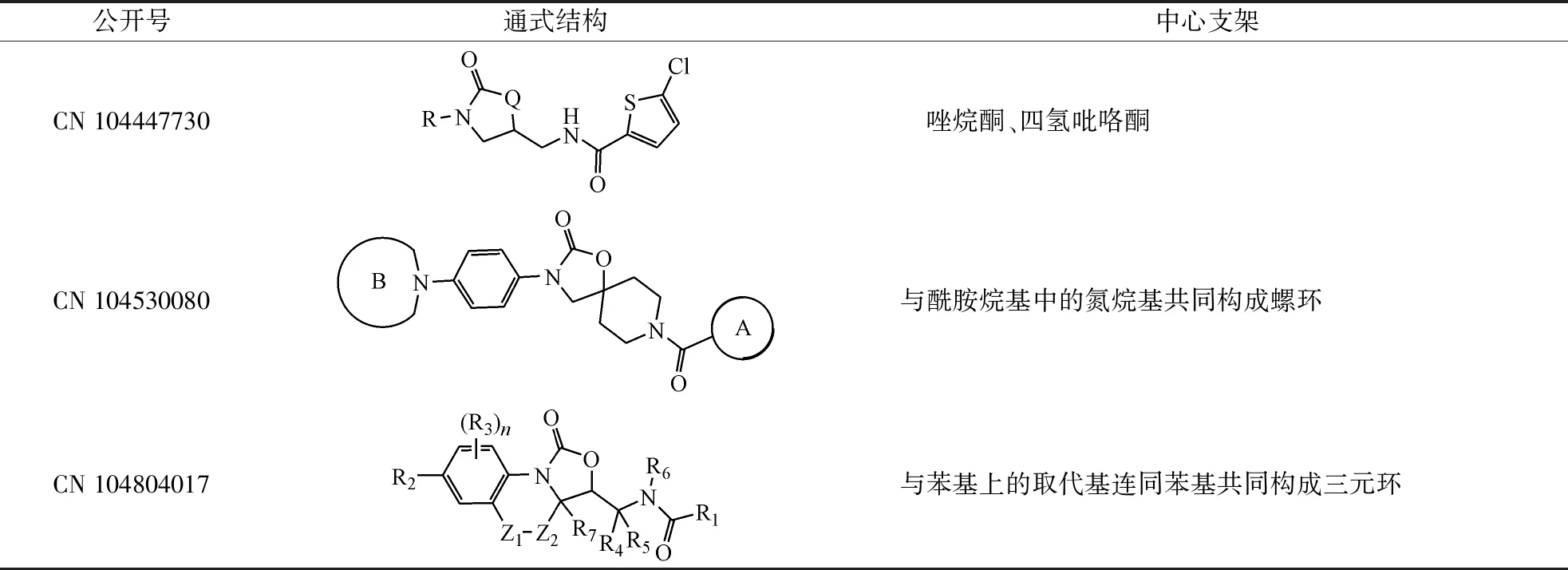
公开号通式结构中心支架CN104447730唑烷酮、四氢吡咯酮CN104530080与酰胺烷基中的氮烷基共同构成螺环CN104804017与苯基上的取代基连同苯基共同构成三元环
大部分专利申请中通式的P1部分与利伐沙班相同,个别有所改动(如表4所示),CN 104447729、CN 104530031将E由噻吩基扩展到吡啶基,CN 104530080的G为烷基酰胺与唑烷酮环合,CN 104804017将D从氯扩展到溴、甲基,同时将E扩展到吡咯、嘧啶。P4的A部分改动不大,除苯基外还可以为噻吩、噻唑、吡啶、嘧啶、吡嗪。B部分为主要修饰位点,CN 104478869、CN 104530080、CN 104804017公开了可以为哌啶酮或吗啉酮、吡啶酮、四氢吡咯酮等体积大小类似、性质相近的含有羰基的杂环基团;CN 104496978、CN 104530031将其修饰为磺酰基取代的苯基、N-甲基氨基、吗啉基取代的吡啶;CN 104447729、CN 104530030尝试增加这些基团与A部分的空间距离,即在上述基团和A基团之间增加一个亚甲基;CN 104447730的B基团更是增加了多种选择,CN 104478866也将其由环状改成了链状。
表4 广东东阳光药业有限公司唑烷酮类Ⅹa因子抑制剂P1、P4部分结构修饰

公开号P1P4CN104478866同利伐沙班A为噻吩、噻唑;B为甲基取代脒基、N-甲基取代氨甲基CN104478869同利伐沙班A为噻唑;B为哌啶酮、吗啉酮、吡啶酮CN104447730同利伐沙班A为苯基;B为吗啉酮、哌啶酮亚甲基、哌啶酮、环戊基取代的肟基、氧杂丙烷取代的甲氧甲基、苯并环戊砜基、氰基取代的吗啉基CN104447729E为噻吩、吡啶A为噻吩;B为哌啶酮亚甲基、四氢吡咯酮亚甲基CN104496978同利伐沙班A为吡啶、吡嗪、嘧啶;B为磺酰基取代的苯基CN104530031E为噻吩、吡啶A为苯基;B为N-甲基氨基、吗啉基取代的吡啶CN104530080G为烷基酰胺与唑;烷酮环合A为苯基;B为哌啶酮CN104530030同利伐沙班A为噻吩基;B为卤素、羧基或羟基取代的五元或六元含氮杂环亚甲基CN104804017D为氯、溴、甲基;E为噻吩、嘧啶、吡咯B为哌啶酮或四氢吡咯酮
4.2.3 其他结构 CN 104311541以吡唑甲酸为中心支架,前已述及,阿哌沙班的吡唑并哌啶结构即由此演变而来,如图15所示,将吡唑与酰胺采用烷基链合环即可得到,东阳光将吡唑甲酸保留,以DPC423为例,向酰胺键的右侧与苯基合环,使得P4的A部分成为苯并四氢吡咯基团,其他位置取代基团与阿哌沙班相同。

图15 广东东阳光药业有限公司CN 104311541通式结构演变过程示意图
CN 104530029A将中心支架替换为氧杂环丁烷,P1部分为氯取代的吡啶、噻吩酰胺基团,P4部分为吗啉酮基苯基;CN 104530046A中心支架为螺环,其余部分改动也比较明显(图16)。
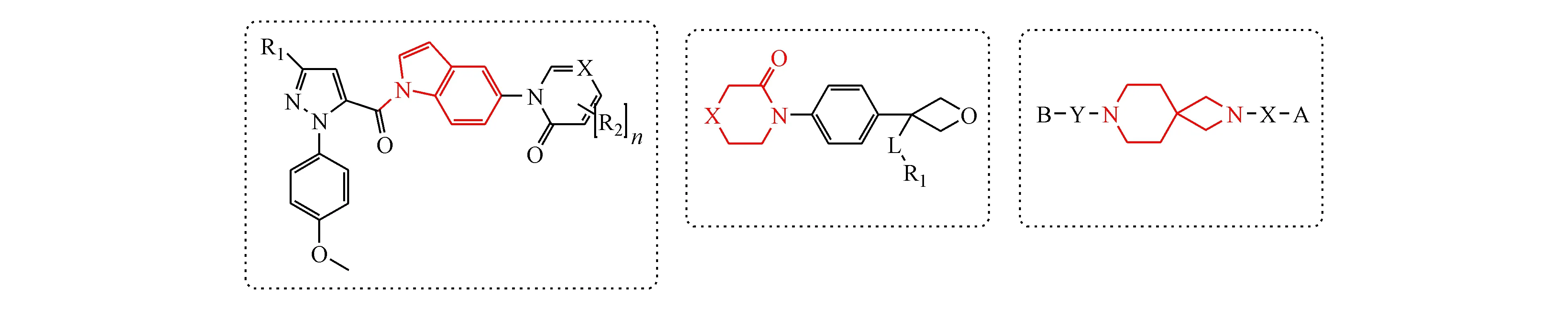
图16 广东东阳光药业有限公司其他类型Ⅹa因子抑制剂相关专利申请
4.2.4 小 结 通过上述分析,可见广东东阳光药业有限公司在凝血因子Ⅹa抑制剂领域投入了大量的研发力量,虽然多数专利申请仍然围绕利伐沙班和阿哌沙班进行结构修饰,但借鉴上市药物成功的经验是新药研发的有效途径之一,这也是目前我国研发自主创新药物的一条捷径。当然,纵观上述专利申请,也不乏全新支架结构的通式化合物,这更加体现了我国企业从“仿制”到“创制”的转型策略。
4.3 其他重点申请人
前面仅以全球范围内和我国的各一家公司为代表,通过各自专利申请中披露的通式化合物、优选的具体化合物阐释了凝血因子Ⅹa抑制剂的改造位点和重要修饰方向,当然,该领域还有很多的重点申请人,如利伐沙班的原研公司拜耳、依度沙班的原研公司第一三共株式会社、贝曲沙班的原研公司千年制药,以及申请量居第二位的默沙东。各大公司的专利申请中同样涉及多种结构类型,除上述提及的饱和内酰胺类、吡唑甲酸类、吡唑并哌啶酮类、唑烷酮类,还可以为环烷二胺和哌啶二胺类、吡咯氨酸类等。国内其他重点申请人如中国科学院上海药物研究所、天津药物研究院、山东大学、沈阳药科大学等也对凝血因子Ⅹa抑制剂的结构进行了修饰和改造。
5 总 结
本文通过专利申请量的分析确定了具有代表性的重点申请人百时美施贵宝,分析了该公司的相关化合物专利申请中凝血因子Xa抑制剂的中心支架、P1、P4三个部分的结构演变历程,初步总结了该类化合物的结构演变和活性的关系。从百时美施贵宝的专利分析可知,阿哌沙班这种"重磅炸弹"式的明星产品,是经历了长期的投入和不断的尝试,而正是由于新药研发投入高、风险大、周期长的特点,长期以来国内企业以仿制为主,但是,专利申请量的排名可知,广东东阳光却以排名第六的成绩跻身全球前十,对其重点专利进行分析也不难发现,在已有结构的基础上,东阳光也进行了大胆的创新,足以说明国内申请人无论是出于国际形势还是自身实力,也是走在由"仿"到"创"的路上,这也是提高自身竞争力的必经之路,这就要求国内企业在挖掘专利漏洞、绕开专利保护的基础上,加大研发投入、找准研究方向,要结合自身生产能力、研发实力,制定契合本企业自身实际情况的知识产权战略,做好全球药品知识产权检索分析,寻找专利突破口,有针对性的进行深入研究和专利布局,从而提高自身的行业竞争力。

