石墨烯功能修饰材料的电化学分析性能研究
郑德论 张锐龙 陈键侨

摘要:石墨烯(GR)是一种单原子碳纳米材料,具有独特的二维共轭平面结构,表现出优越的化学、力学、热学和电学性能。氧化石墨烯(GO)是制备石墨烯的前驱体,类似于石墨烯的二维结构,GO表面含大量的含氧官能团,具有良好的水溶分散性,GO通过化学还原方法可以得到导电性良好的GR材料。将GR材料与其他功能材料进行复合,可进一步改善复合物的物理和化学性能,如可分散性、可加工性和电催化活性等。综述了GR(包括GO)与碳纳米材料、金属纳米粒子、金属氧化物、非金属单质、聚合物或其他功能生物分子材料結合后,得到复合功能修饰材料用于构建高性能电化学生物传感器。探究了复合制备材料的纳米结构特征、功能结构作用对于提高传感器的电催化和电化学选择性能等方面的应用。
关键词:石墨烯(GR);氧化石墨烯(GO);功能修饰;电化学;分析性能
中图分类号:TH145.1+3 文献标识码:A
文章编号:0439-8114(2019)07-0005-06
Abstract: Graphene (GR), as a kind of monatomic carbon nanomaterial, which has a unique two-dimensional conjugate planar structure and shows excellent chemical, mechanical, thermal and electrical properties. Graphene oxide (GO) is a precursor of graphene, which similar to the two-dimensional structure of graphene. GO surface containing a large number of oxygen-containing functional groups,resulting has a good water-soluble dispersion. The good conductivity of GR materials can be obtained by the chemical reduction method of GO. The graphene materials compositing with other functional materials would further improve the complex physical and chemical properties, such as dispersibility, workability and electrocatalytic activity. The fabricated high performance electrochemical biosensors by combining graphene (including GO) with carbon nanomaterials, metallic nanoparticles, metal oxides, non-metallic, polymers or other functional biomolecule materials to form the composite functional modified materials were reviewed. The nanostructural features of the composite material were explored and the application of its functional structure for improving the electrocatalytic and electrochemical selectivity of the sensor was also discussed.
Key words: graphene(GR); graphene oxide(GO); functional modification; electrochemistry; analysis performance
石墨烯(GR)是一种无限延伸的二维(2D)碳晶体,碳原子的组装排列类似蜂窝状的六角边晶格结构[1,2]。目前,GR的概念已扩展到由一系列石墨材料组成,包括一个或多个石墨烯片层和大量的sp2杂化碳缺陷结构,并具有表面多孔的特点[3]。GR表现出各种优越的特殊属性,包括大的比表面积、高的透亮度、强的电场效应、良好的导热导电属性、优良的机械强度和延展性能等[4]。GR已广泛应用于电子触摸屏、超级电容器、燃料电池、 生物传感器、透明导电薄膜和相关电子元器件等领域[3,5,6]。
GR的制备一般以石墨为原料,主要方法有机械剥离法、化学合成法、电化学还原方法、化学气相沉积法(CVD)和SiC裂解法等[7-11]。在这些方法中,化学机械剥离法是制备GR的主要方法,可以产生大量适合进一步功能化的分子结构。氧化石墨烯(GO)作为制备GR的前驱体,拥有丰富的表面缺陷和大量的含氧官能团(如环氧基团、羧基和羟基等),这不仅可以作为电化学过程中的催化活性中心,还可以为共价或非共价功能化作用提供活性位点[12]。然而,这样破坏了石墨本体的sp2键网状结构,导致GO变为绝缘体材料。因此,需要对GO进行还原脱氧处理,如热学、化学或电化学还原方法等以恢复原始石墨烯的各种属性[13]。
功能性材料通常认为具有特定的本质属性及其特殊的功能作用。功能材料存在于所有类型的材料之中,包括金属单质、金属氧化物纳米粒子、聚合物分子、有机物和生物分子材料等。这些功能材料或功能生物分子常用于化学修饰电极的制备,可以提高传感界面的电学催活性或生物功能作用。GR材料尽管表现出多种优异的化学或物理性能,但单一组分的GR在实际应用中仍有一定的局限性[14]。GR与其他功能材料结合形成的复合物结构,可以很好地协调各组分之间的物理和化学性能,使复合物材料呈现多种功能性作用[15-19]。例如,GR的水溶剂性能够提高其分散性,有利于增强制备电极的成膜效应;修饰上聚电解质化合物可以大大提高带相反电荷物质的吸附能力;与金属纳米粒子结合(NPs)可以提高其对特定生物小分子的选择性催化性能;结合生物识别元素可以帮助捕获目标分析物并协助信号转换功能;与透明塑料的集成可制备成可穿戴的光敏电化学传感器等。
作为一种有前景的电极制备材料,石墨烯复合物在传感界面上表现出诸多优点,如良好的稳定性、低的过电位、宽的化学窗口和显著的催化活性,特别有利于设计高性能的电化学传感器或生物传感器[12,20,21]。电化学检测技术通常有循环伏安法(CV)、方波伏安法(SWV)、差分脉冲伏安法(DPV)、电化学阻抗谱法(EIS)、电流-时间测量法(IT)和电化学发光法(ECL)等,由于操作简单、成本低廉和环境污染少,被广泛用于提高传感界面的分析灵敏度[3,22-27]。本研究综述了GR与其他纳米材料、聚合物材料、生物分子材料等结合形成的复合功能性材料作为修饰界面,构筑出不同类型的电化学生物传感器,结合以上电化学检测方法实现对葡萄糖分子、H2O2分子、DNA生物分子、有机生物分子以及重金属Hg2+ 的高性能检测,并阐明了石墨烯复合修饰物的结构特征及其功能性作用在目标分析物中的重要应用途径。
1 GR和GO的分析性能及应用
1.1 对葡萄糖和H2O2的检测
Wang等[28]通过电流置换反应和热还原氧化石墨烯(rGO)方法制备出两种金属Ag/Pt纳米粒子与rGO杂化形成的复合材料。SEM、TEM、XRD、EDXS(能量色散X射线光谱)和FTIR(傅里叶红外光谱)表征方法用于对复合物的形貌表征和组分分析。图谱分析结果表明,热还原法能高效率制备出石墨烯膜层中稳定的空心型Ag/Pt纳米粒子结构,其中Pt、Ag原子的百分比分别为60%和40%。循环伏安法(CV)测量表明,rGO复合物修饰电极可以直接检测葡萄糖,并具有较高的电催化活性。葡萄糖在Ag/Pt-rGO上的理想测量电流响应灵敏度为129.32 A/mm·cm2, 信号响应时间少于3 s,获得较低的检出限为1.81 μmol/L。此外,该复合材料制备的非酶葡萄糖生物传感器也显示出良好的选择性、重现性和稳定性,因而可应用于实际样品中葡萄糖含量的快速、准确测定。
GR与金属半导体纳米复合材料的杂化共轭结构,具有大的比表面积和卓越的电气/电催特性,可以提高制备传感器的检测灵敏度。Krishna等[29]合成了一种还原氧化石墨烯和镍纳米颗粒(rGO-Ni NPs)的杂化共轭物,将该复合物进一步沉积在玻碳电极(GCE)上,作为壳聚糖和葡萄糖氧化酶的复合纳米膜层。SEM用于分析膜层的表面形态,CV和EIS电化学方法表征制备传感器的电流响应信号,结果表明,在低电位下,石墨烯复合物修饰界面对亚毫摩尔的葡萄糖浓度具有高的检测灵敏度(达到129 μA/cm2·mmol/L)和良好的线性检测范围。该项研究内容可应用于开发检测人体血液样本中的低血糖含量,以及无创测定某些体液如唾液或眼泪的血糖含量。
Ren等[30]通过采用多巴胺作为氮源和还原剂,将嵌段共聚物P123(聚乙烯-聚丙二醇)作为孔隙成膜剂,GO作为碳前驱体,制备出一种新型氮掺杂多孔石墨烯/Pt納米花材料(Pt/N-PGR)。TEM表征图谱显示,树枝状的Pt纳米花均匀分散在氮掺杂的多孔石墨烯上。XPS(X射线光电子能谱)分析结果表明,PGR复合制备材料表面存在C、O、N和Pt元素。电化学试验显示,Pt/N-PGR/GCE修饰电极提高了对H2O2还原和葡萄糖氧化的电催化活性,H2O2和葡萄糖的线性检测范围分别为0.5~40326 μmol/L和0.5~133.5 mmol/L,并获得较低的检测限达到0.2 μmol/L和0.05 mmol/L。抗干扰和选择性试验研究进一步表明,制备的PGR复合材料修饰界面可应用于构建高性能的葡萄糖生物传感器。
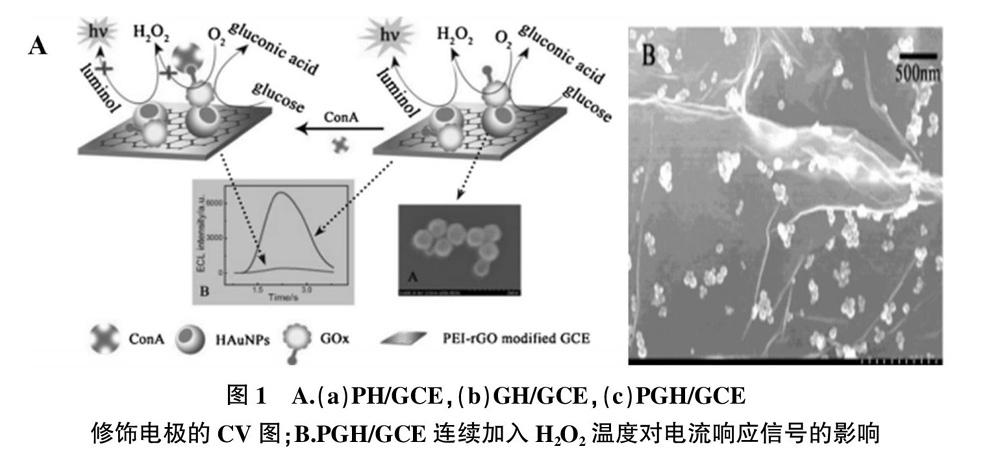
Zhou等[31]制备一种温度感应生物传感复合膜,该膜层由块状共聚物N-异丙基-b-丙烯酰胺基甲基苯甲酸酯(PNIPAM-b-PAAE),GO和血红蛋白(Hb)组成PGH,膜层优良的微环境可以促进Hb在GCE电极上发生电子转移。电化学CV法图谱(图1)表明,Hb在复合膜层(PGH)修饰GCE电极上有一对明显的氧化还原峰,显示出对H2O2内在的电催化活性。复合膜对H2O2可调控的催化活性可以通过温度变化来实现。当超过较低的临界溶解温度32 ℃时,GO复合膜修饰电极对H2O2的线性检测浓度范围为0.1~3.7 μmol/L;当温度低于30 ℃时,其浓度检测范围改变为0.2~3.7 μmol/L。这种现象可归因于PNIPAM-bPAAE的温度依赖性相变和与GO的协同作用。
Mani等[32]采用简单的溶液制备方法合成出还原氧化石墨烯、多壁碳纳米管、铂纳米颗粒和肌红蛋白的复合纳米材料(rGO-MWCNT-Pt/Mb),应用于对过氧化氢(H2O2)和亚硝酸盐(NO2-)的直接电化学传感分析。SEM 形貌表征可观察到rGO复合物的纳米多孔表面上覆盖有大量的Mb分子,显示出复合材料修饰界面大的表面积和良好的亲和力有利于Mb的固载或吸附。CV法图谱表明,Mb在rGO-MWCNT-Pt/Mb复合材料界面上有一对明显的氧化还原峰。对于检测H2O2,观察到两个线性浓度范围,分别为10 pmol/L~0.19 nmol/L和0.25 nmol/L~2.24 mmol/L。制备传感器还获得较低的检测限(LOD)为6 pmol/L,该数据是目前H2O2的最低检测限之一。对NO2检测,得到一种宽的线性范围浓度为1~12 mmol/L。上述试验数据表明,RGO复合物修饰材料构建的电化学传感界面具有高灵敏度的分析特征,是H2O2检测的可行性手段之一。
1.2 对DNA生物分子的检测
Yola等[33]开发一种2-氨基乙硫醇(AET)与Fe包覆Au纳米粒子进行功能化修饰的GO复合材料。TEM、XRD和X射线光电子能谱方法用于表征复合物的形貌结构和元素组成。图谱分析结果表明,通过利用2-AET上的硫基,GO被功能化修饰上壳核型Fe-Au双金属纳米颗粒,AuNPs对巯基官能团具有很高的结合亲和力。反射红外吸收光谱法(RAIRS)表征Au纳米颗粒与巯基之间的相互作用,证实了Fe@AuNps-AETGO复合物已经形成。将ss-DNA单链探被固定到GO复合纳米材料上面,以甲基蓝41(BB41)作为电化学指示剂,方波伏安法(SWV)检测DNA探针与互补链DNA的杂交形成过程,试验结果显示BB41峰电流与互补浓度的对数呈线性关系。与其他文献报道作比较,该DNA生物传感器还获得了较低的检测限为2.0×10-15 mol/L,表现出较高的检测灵敏度。将ssDNA-Fe@AuNPs-AETGO功能界面进一步应用于对单碱基、双碱基和三碱基错配DNA序列进行分析,GO复合修饰材料具有良好的选择性识别能力。
Huang等[34]将GR与Au纳米棒和聚硫堇的复合物(G/AuNR/PT)修饰到玻碳电极表面(GCE),制备出一种无酶和无标记超灵敏检测人乳头瘤病毒(HPV)的电化学DNA生物传感器。该项工作设计了两种辅助探针,用于远程自组装DNA纳米结构。EIS和DPV电化学测量试验结果表明,GR可以增加电极比表面积,协同提高G/Au NR/PT/GCE修饰界面的电子传递能力,结合DNA的自组装纳米结构功能,能够多重放大HPV DNA的电化学响应信号,从而大大增强了制备传感器的检测灵敏度,检测限值达到4.03×10-14 mol/L。采用不同方法对该试验过程进行优化后,也可以应用于对复杂人群血清样品中的HPV DNA检测。
Zhang等[35]设计出一种利用聚乙烯亚胺(PEI)还原氧化石墨烯(rGO)和空心金纳米粒子(HAuNPs)作为信号放大基质,萄糖氧化酶(GOx)作为识别元素构建的电化学发光(ECL)伴刀豆球蛋白A(ConA)生物传感器。SEM形貌表征明显观察到空心球型的AuNPs吸附在PEI-rGO表面。传感器的主要制备原理过程:首先,有丰富氨基官能团的rGO被固载到玻碳修饰电极上,用于吸附HAuNPs粒子增强ECL信号。接着,GOx通过Au与-NH2之间的相互作用力组装到修饰电极表面。当有葡萄糖(Glucose)存在时,GOx催化葡萄糖产生H2O2,ECL信号源得到联合加强。当ConA存在时,制备电极的响应信号降低,从而实现对ConA的检测。ConA的浓度对数与ECL信号强度呈线性关系,线性检测范围为1.0~20 ng/mL,并获得一个较低的检测限为0.31 ng/mL。此结果比之前报道ConA的低浓度检测限值提高了1 000倍,表明PEI/rGO复合修饰材料制备传感器具有极佳的检测灵敏度。
1.3 对有机生物分子的检测
Rani等[36]采用一种简单的化学合成方法,获得片层石墨烯与Fe3O4纳米粒子的复合物(Fe3O4/rGO),应用Fe3O4/rGO作为传感膜层界面电化学检测多巴胺(DA)。制备出的复合物形貌表征显示,Fe3O4的纳米结构类似绽放出6个对称分布的花瓣(图2),即便是在rGO存在的条件下,Fe3O4的立方反尖晶石结构形貌、大小及组分都没有发生改变。电化学试验研究表明,rGO修饰纳米结构复合物对DA具有显著的催化活性,DA的氧化测量电流响应时间为5 s,宽的线性检测浓度范围为0.010~0.270 mmol/L,并获得一个高的灵敏度检测单位为19.75 mA/mmol/L·cm2。选择性试验表明,即使有其他干扰物质如AP、UA、HA等存在條件下,制备传感器变亦能显示出对DA优越的识别能力。对人体尿液样本DA的精确度检测进一步说明制备的复合物纳米功能材料具有实际应用性能。
Sun等[37]利用氟磺酸(Nafion)良好的成膜性可以有效固载蛋白质分子,通过电共沉积方法将肌红蛋白(Mb),海藻酸钠(SA)和Fe3O4-graphene(Fe3O4-GR)的复合物修饰到碳离子液体电极(CILE)上,得到一种Mb-SA-Fe3O4-GR/CILE复合材料电化学传感界面。SEM表征图谱(图3)可以看到,Fe3O4-GR复合物纳米尺寸的粒子形貌,Mb-SA-Fe3O4-GR在CILE电极表面可得到均匀一致的复合膜层,这有利于增强制备传感器的稳定性能。红外光谱(FT-IR)和紫外可见吸收光谱(UV-vis)表征证实,Mb后可以保留原有结构被固定在SA-Fe3O4-GR复合膜层上。电化学循环伏安法(CV)图谱显示,修饰电极上有一双对称的氧化还原峰曲线,说明Mb在制备电极上实现了直接的电子转移,电子转移数(n),电荷转移系数(a)和电子转移速率常数(ks)分别为每秒0.982、0.357和0.234。这可归结为Fe3O4-GR复合物优异的电催化性能,SA良好的生物相容性以及SA和Fe3O4-GR结合的协同提高效应。该修饰材料制备电极对三氯乙酸(TCA)具有较宽的线性检测浓度范围(1.4~119.4 mmol/L)。
1.4 对重金属Hg2+的检测
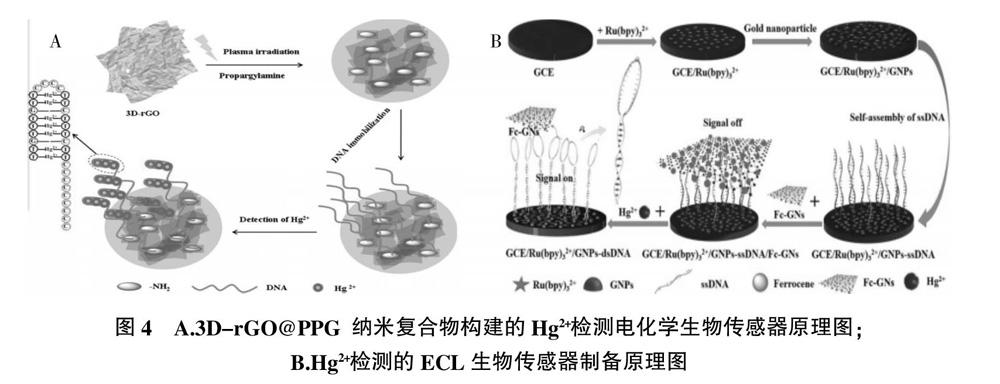
Peng等[38]合成一种三维还原氧化石墨烯(3D-rGO)与等离子聚丙胺基(PPG)的纳米复合材料,制备出高灵敏度的DNA生物传感器,用于检测重金属Hg2+离子。其制备原理为:①标记上Hg2+的DNA链及其含有的丰富T碱基(胸腺嘧啶),与3D-rGO@PPG纳米复合物上大量的氨基官能团通过强烈的静电相互作用,被固定于传感修饰界面上。②DNA与检测离子Hg2+形成T-Hg2+-T的化学结合作用,并转化为电化学响应信号,从而实现对Hg2+的传感分析。电化学测量结果表明,3D-rGO复合修饰膜层作为传感界面对Hg2+显示出高的灵敏度,线性检测范围为0.1~200 nmol/L,检测限值达到0.02 nmol/L,并具有较好的重现性和稳定性。选择性试验表明制备传感器可以消除其他金属离子对Hg2+检测的干扰。该复合材料可进一步应用于对水环境中重金属离子的检测。
Zhuo等[39]基于核苷酸与二茂铁-石墨烯(Fc-GN)纳米片层之间的π-π相互作用,制备出一种电化学发光方法(ECL)对Hg2+检测的生物传感界面。构建原理及主要过程见图4, 将单链DNA(ssDNA)探针组装到修饰上Ru(bpy)32+和金纳米粒子(GNPs)的玻碳电极(GCE)表面,由于GR与核苷酸之间强的作用,ssDNA探针能够强烈吸附GR,当存在Hg2+时,DNA构象的单链结构转变为双链结构,抑制了对GN的吸附。最后,以ssDNA作为探针指示剂、Fc-GN复合物作为Ru(bpy)32+的电化学发光淬灭装置,当Fc-GN离开Ru(bpy)32+时,淬灭效率发生转化,从而实现对Hg2+的检测。该传感制备界面对不同浓度的Hg2+具有高灵敏的响应信号,检测限达到18 pmol/L,应用于对自然水中的Hg2+检测,表现出优良的选择性能。
2 結论与展望
本研究综述了以GR复合物修饰材料作为传感界面,采用电化学或电化学发光方法检测多种生物分子如DNA、H2O2、葡萄糖、DA以及重金属离子Hg2+等的研究进展。研究表明,GR复合修饰材料具有以下功能性特点:纳米尺度的空间结构、丰富的表面缺陷、大量的含氧官能团、功能分子的目标选择、活性位点的催化效应和协同放大的电化学信号等。基于此,GR复合修饰界面提高了电化学检测的灵敏度和选择性识别能力, 拓宽了线性检测范围并降低了检测限,传感器的电化学稳定性也得到进一步增强。但是,GR功能修饰材料在电化学应用领域仍待深入研究以下问题[40-45]:①GR复合物的纳米尺寸、功能结构以及成分组成如何进行更加有效的调控和优化,以使其电化学检测性能得到最大程度的发挥;②GR复合物各组分之间的协同催化机理及其对目标检测物的影响与联系;③功能生物分子在GR复合材料界面上的组装模式与提高检测性能的最佳选择途径;④二维、三维GR材料复合其他纳米粒子或功能分子的微结构形成过程,包括比表面积、多孔构型等,对反应动力学和选择性的重要影响作用;⑤GR功能修饰材料制备电极的重现性、再生性和抗干扰能力与提高其电化学检测性能的有机统一等。随着对GR复合功能材料的深入研究,将赋予其更多丰富的功能化作用,构建协同发挥的电化学传感平台,从而能够实现对多种目标物的高性能分析与检测。
参考文献:
[1] XU J H,WANG Y Z,HU S S. Nanocomposites of graphene and graphene oxides:Synthesis,molecular functionalization and application in electrochemical sensors and biosensors[J].Microchim acta,2017,184:1-44.
[2] GEORGAKILAS V,TIWAR J N,CHRISTIAN KEMP K,et al. Noncovalent functionalization of graphene and graphene oxide for energy materials,biosensing,catalytic,and biomedical applications[J].Chem Rev,2016,116:5464-5519.
[3] AMBROSI A,CHUA C K,BONANNI A,et al. Electrochemistry of graphene and related materials[J].Chem Rev,2014,114(14):7150-7188.
[4] DREYER D R,TODD A D,BIELAWSKI C W. Harnessing the chemistry of graphene oxide[J].Chem Soc Rev,2014,43(15):5288-5301.
[5] BAI S,SHEN X. Graphene-inorganic nanocomposites[J].RSC Adv,2012,2(1):64-98.
[6] ZHAO B T,ZHENG Y,YE F,et al. ACS Appl. Multifunctional iron oxide nanoflake/graphene composites derived from mechanochemical synthesis for enhanced lithium storage and electrocatalysis[J].Mater Interfaces,2015,7:14446-14455.
[7] BUNCH J S,YAISH Y,BRINK M,et al. Coulomb oscillations and hall effect in Quasi-2D graphite quantum dots[J].Nano Lett,2005,5(2):287-290.
[8] REINA A,JIA X,HO J,et al. Large area,few-layer graphene films on arbitrary substrates by chemical vapor deposition[J].Nano Lett,2008,9(1):30-35.
[9] BERGER C,SONG Z,LI X,et al. Electronic confinement and coherence in patterned epitaxial graphene[J].Science,2006,312 (5777):1191-1196.
[10] GUO H L,WANG X F,QIAN Q Y,et al. A green approach to the synthesis of graphene nanosheets[J].ACS Nano,2009, 3(9):2653-2659.
[11] GIOVANNI M,BONANNI A,PUMERA M. Detection of DNA hybridization on chemically modified graphene platforms[J].Analyst,2012,137(3):580-583.
[12] CHEN D,FENG H,LI J. Graphene oxide:preparation,functionalization,and electrochemical applications[J].Chem Rev,2012,
112(11):6027-6053.
[13] PAREDES J I,VILLAR-RODIL S,FERNáNDEZ-MERINO M J,et al. Environmentally friend-ly approaches toward the mass production of processable graphene from graphite oxide[J].J Mater Chem,2011,21(2):298-306.
[14] SI Y C,SAMULSKI E T. Synthesis of water soluble graphene[J].Nano Lett,2008,8(6):1679-1682.
[15] SONG J,QIAO J,SHUANG S,et al. Synthesis of neutral red covalently functionalized graphene nanocomposite and the electrocatalytic properties toward uric acid[J].J Mater Chem,2012,22(2):602-608.
[16] LUO J H,LI B L,LI N B,et al. Sensitive detection of gallic acid based on polyethyleneimine-functionalized graphene modified glassy carbon electrode[J].Sensors actuators B chem,2013,186:84-89.
[17] GUO S,WEN D,ZHAI Y,et al. Platinum nanoparticle ensemble-on-graphene hybrid nanosheet one-pot rapid synthesis and used as new electrode material for electrochemical sensing[J].ACS Nano,2010,4(7):3959-3968.
[18] WANG Y,XIAO Y,MA X,et al. Label-free and sensitive thrombin sensing on a molecularly grafted aptamer on graphene[J].Chem Commun(Camb),2012,48(5):738-740.
[19] FAN Z,LIU B,LIU X,et al. A flexible and disposable hybrid electrode based on Cu nanowires modified graphene transparent electrode for non-enzymatic glu-cose sensor[J].Electrochim acta,2013,109:602-608.
[20] GEORGAKILAS V,OTYEPKA M,BOURLINOS A B,et al. Functionalization of graphene:covalent and non-covalent approaches,derivatives and applications[J].Chem Rev,2012,112(11):6156-6214.
[21] ZHU Y,JAMES D K,TOUR J M,et al. New routes to graphene,graphene oxide and their related applications[J].Adv Mater,2012,24(36):4924-4955.
[22] KOCHMANN S,HIRSCH T,WOLFBEIS O S,et al. Graphenes in chemical sensors and biosensors.TrAC[J].Trends Anal Chem,2012,39:87-113.
[23] FILIP J,KASáK P,TKAC J. Graphene as signal amplifier for preparation of ultrasensitive electrochemical biosensors[J].Chemical papers,2015,69(1):112-133.
[24] YANG F,HE D H,ZHENG B Z,et al. Self-assembled hybrids with xanthate functionalized carbon nanotubes and electro-exfoliating graphene sheets for electrochemical sensing of copper ions[J].J Electroanal Chem,2016,767:100-107.
[25] REN S Y,JI H F,ZHANG Z H. Fabrication of sensitive layers of the 3D graphene electrochemical biosensor for heavy metal ions detection[J].Journal of light industry,2016,31(3): 14-20.
[26] DALK1RAN B,ERDEN P E,K1L1?E. Electrochemical biosensing of galactose based on carbon materials:graphene versus multi-walled carbon nanotubes[J].Anal Bioanal Chem,2016,408:4329-4339.
[27] ZHAN F P,GAO F,WANG X,et al. Determination of lead(II) by adsorptive stripping voltammetry using a glassy carbon electrode modified with β-cyclodextrin and chemically reduced graphene oxide composite[J].Microchimica acta,2016,183(3):1169-1176.
[28] WANG C,SUN Y L,YU X H,et al. Ag-Pt hollow nanoparticles anchored reduced graphene oxidecomposites for non-enzymatic glucose biosensor[J].J Mater Sci:Mater Electron,2016,27(9):9370-9378.
[29] KRISHNA R,CAMPI?A J M,PAULA M V,et al. Reduced graphene oxide-nickel nanoparticles/biopolymer compositefilms for the sub-millimolar detection of glucose[J].Analyst,2016, 141:4151-4161.
[30] REN S,WANG H,ZHANG Y F,et al. Convenient and controllable preparation of anovel uniformly nitrogen doped porous graphene/Pt nanoflower material and its highly-efficient electrochemical biosensing[J].Analyst,2016,141:2741-2747.
[31] ZHOU Y Q,CAO J,ZHAO J,et al. Temperature-responsive amperometric H2O2 biosensor using a composite film consisting of poly(N-isopropylacrylamide)-b-poly(2-acrylamidoethyl benzoate),grapheneoxide and hemoglobin[J].Microchim Acta,2016,183:2501-2508.
[32] MANI V,DINESH B,CHEN S M,et al. Direct electrochemistry of myoglobin at reduced graphene oxide-multiwalled carbon nanotubes-platinum nanoparticles nanocomposite and biosensing towards hydrogen peroxide and nitrite[J].Biosensors bioelectronics,2014,53(15):420-427.
[33] YOLA M L,EREN T,ATAR N. A novel and sensitive electrochemical DNA biosensor based on Fe@Au nanoparticles decorated graphene oxide[J].Electrochim Acta,2014,125:38-47.
[34] HUANG H Y,BAI W Q,DONG C X,et al. An ultrasensitive electrochemical DNA biosensorbased on graphene/Au nanorod/polythionine for human papillomavirus DNA detection[J].Biosensors bioelectronics,2015,68(15):442-446.
[35] ZHANG J J,CHEN S H,RUO Y,et al. An ultrasensitive electrochemiluminescent biosensorfor the detection of concanavalin A based on poly(ethylenimine)reduced graphene oxide and hollow gold nanoparticles[J].Anal Bioanal Chem,2015,407:447-453.
[36] JENITA R G,BABU J K,KUMAR G G,et al. Watsonia meriana flower like Fe3O4/reduced graphene oxidenanocomposite for the highly sensitive and selective electrochemicalsensing of dopamine[J].J Alloys Compd,2016,688:500-512.
[37] CHEN X Q,YAN H Q,SHI Z F,et al. A novel biosensor based on electro-co-deposition of sodium alginate-Fe3O4-graphene compositeon the carbon ionic liquid electrode for the directelectrochemistry and electrocatalysis of myoglobin[J].Polym Bull,2017,74:75-90.
[38] PENG D L,JI H F,DONG X D,et al. Highly sensitive electrochemical bioassay for Hg(II) detection based on plasma-polymerized propargylamineand three-dimensional reduced graphene oxide nanocomposite[J].Plasma Chem Plasma Process,2016,36:1051-1065.
[39] ZHUO B G,LI Y Q, ZHANG A, et al. An electrochemiluminescence biosensor forsensitive and selective detection of Hg2+ based on interaction between nucleotides andferrocene-graphene nanosheets[J].J Mater Chem B,2014,2:3263-3270.
[40] LIU J Q,KONG N,LI A H,et al. Graphene bridged enzyme electrodes for glucose biosensing application[J].Analyst,2013, 138:2567-2575.
[41] LING Y Y,HUANG Q A,ZHU M S,et al. A facile one-step electrochemical fabrication of reduced graphene oxide-mutilwall carbon nanotubes-phospotungstic acid composite for dopamine sensing[J].Electroanal Chem,2013,693:9-15.
[42] DONG X C,WANG X W,WANG L H,et al. 3D Graphene foam as a monolithic and macroporous carbon electrode for electrochemical sensing[J].ACS Appl Mater Interfaces,2012,4(6):3129-3133.
[43] 于小雯,盛凱旋,陈 骥,等.基于石墨烯修饰电极的电化学生物传感[J].化学学报,2014,72(3):319-332.
[44] MELDE B J,JOHNSON B J. Mesoporous materials in sensing:morphology and functionality at the meso-interface[J].Anal. Bioanal Chem,2010,398:1565-1573.
[45] ZENG G H,XING Y B,GAO J,et al. Unconventional layer-by-layer assembly of graphene multilayer films for enzyme-based glucose and maltose biosensing[J].Langmuir,2010,26(18):15022-15026.

