玻璃体切除术联合雷珠单抗玻璃体注射治疗增殖性糖尿病视网膜病变的临床疗效观察
李俊岭 肖博文
玻璃体切除术(pars plana vitrectomy,PPV)为增殖性糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)常用治疗手段,但手术难度大、出血量多,难以有效控制,会延长手术时间、增加手术失败风险。采取有效措施优化治疗,降低手术风险是近年来的研究热点。雷珠单抗玻璃体注射治疗增殖性糖尿病视网膜病变可促进视网膜血管增生消退、减少出血、降低手术难度,提升手术效果[1]。PPV 联合雷珠单抗玻璃体注射治疗PDR 是否能够优化治疗效果尚存在争议。本研究将单纯PPV与PPV 联合雷珠单抗玻璃体注射进行对比,有助于明确联合治疗方案的应用价值,为今后PDR 治疗方案的制定提供科学指导。
1 材料与方法
1.1 一般资料选取2017年1月~2018年12月在我院眼科接受治疗的PDR 患者102例(109 眼),所有患者均符合《我国糖尿病视网膜病变临床诊疗指南(2014年)》[2]中PDR 诊断标准;随机分为对照组和研究组。对照组:51例,55 病眼,男27例,女24例;年龄40~79岁,平均(58.77±6.18)岁;糖尿病病程1~19年,平均(9.73±2.62)年。研究组:51例,54 病眼,男28例,女23例;年龄44~81岁,平均(59.62±6.08)岁;糖尿病病程1~21年,平均(10.05±2.41)年。两组上述基线资料比较差异无统计学意义(P>0.05)。本研究经医学伦理委员会批准通过。
1.2 纳入与排除标准纳入标准:①资料完整;②认知、理解、沟通能力正常;③了解本次研究,阅读、签署同意书后自愿参与。排除标准:①合并有重要脏器功能障碍疾病;②伴有精神疾病或认知障碍疾病;③有凝血功能障碍。
1.3 方法对照组:单纯接受PPV 治疗。常规消毒,全身麻醉,使用Evolution 超乳玻切一体机(威视健医疗设备公司提供),开展标准23G 巩膜三通道玻璃体切除术,首先切除中轴位置玻璃体,并清除积血;于巩膜外顶压下,彻底切除基底部位玻璃体,并切断牵引膜带,游离视网膜前膜;完全切除黄斑表面增殖膜,剥离干净后做气液交换处理,使视网膜平复;于视网膜清晰状态下,实施眼内激光光凝处理。对于牵拉性视网膜脱离者,以硅油或无菌气体做填充处理。
研究组:接受PPV 联合雷珠单抗玻璃体注射治疗。于PPV 前5~7d 应用雷珠单抗注射液(Novartis Pharma Schweiz AG,S20110085,10mg/ml)对玻璃体行注射治疗。取0.1ml 雷珠单抗注射液,注入玻璃体腔内;并使用红霉素眼膏(国药准字H20064342,浙江盛基药业有限公司,0.5%浓度)涂抹结膜囊。依据患者的实际情况,5~7d 后行PPV 治疗,PPV 方法与对照组相同。
1.4 观察指标观察两组患者手术相关指标,并分别于治疗前、治疗后3个月以标准视力表检查患者的视力水平,统计并发症发生情况,分别进行对比分析。手术相关指标包括手术时间、术中出血量、眼压、黄斑中心凹视网膜厚度。
1.5 统计学方法使用SPSS 23.0 统计学软件进行分析,计数资料以%表示,行χ2检验;计量资料以±s表示,行t检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 两组手术相关指标对比研究组手术时间、术中出血量低于对照组,差异有统计学意义(P<0.05);两组患者眼压、黄斑中心凹视网膜厚度相近,差异无统计学意义(P>0.05)。见表1。
表1 两组手术相关指标对比(±s)
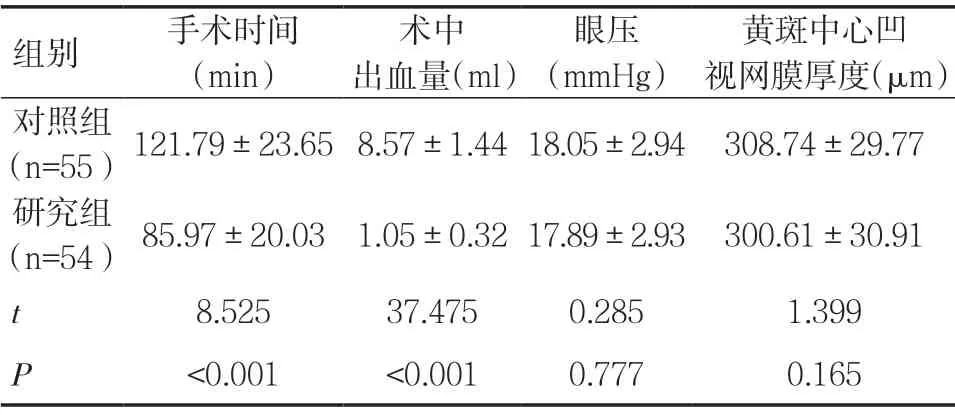
表1 两组手术相关指标对比(±s)
组别手术时间(min)术中出血量(ml)眼压(mmHg)黄斑中心凹视网膜厚度(µm)对照组(n=55)121.79±23.65 8.57±1.44 18.05±2.94 308.74±29.77研究组(n=54)85.97±20.03 1.05±0.32 17.89±2.93 300.61±30.91 t 8.52537.4750.2851.399 P<0.001<0.0010.7770.165
2.2 两组手术前后视力对比治疗前,对照组、研究组患者对数视力分别为(0.069±0.011)D、(0.068±0.013)D,视力水平相近,差异无统计学意义(t=0.434,P=0.665);治疗后3个月,两组均有所上升,分别为(0.436±0.027)D、(0.594±0.071)D,而研究组患者视力水平高于对照组,差异有统计学意义(t=15.409,P=0.001)。
2.3 两组并发症发生情况对比治疗后,对照组再出血、再增殖各项并发症发生率分别为14.55%(8/55)、7.27%(4/55);研究组各项并发症发生率分别为1.85%(1/54)、0(0/54)。对照组再出血、再增殖发生率均高于研究组,差异有统计学意义(t=5.796、4.077,P=0.016、0.043)。
3 讨论
PDR 是糖尿病常见并发症,其发生风险随糖尿病病程的延长而增加。相关流行病学数据显示:糖尿病病程<5年,PDR 发生率为38.90%;病程5~10年,PDR 发生率为50.00%~56.17%;病程>10年,PDR 发生率为70.00%~90.00%[1]。近年我国糖尿病发病率上升,PDR 发生率也随之升高,PDR 可直接损害患者的视功能,如不予以有效控制可使视网膜脱落,诱发失明[3]。PDR 是后天失明的主要病因[4]。探究科学有效的治疗方案是保证患者生命健康的关键。
PPV 以照明系统、观察系统为指导,于直视下实施手术操作。PPV 手术操作涉及范围包括:视网膜前、视网膜下、前房和玻璃体腔,而该手术空间范围内多有大量视网膜新生血管。手术期间新生血管破裂,引发出血、渗血,使术野模糊,对手术实施造成干扰,影响手术效果,导致术后视力改善有限;频繁切换手术器械与延长手术时间,会增加出血点及手术部位并发症的发生风险,影响手术安全 性[5]。因此,单用PPV 治疗PDR的手术难度较大。本次研究中对照组患者单纯接受PPV 治疗,患者的平均手术时间为(121.79±23.65)min,术中出血量(8.57±1.44)ml,术后3个月视力水平仍然偏低,仅为(0.436±0.027)D,再出血、再增殖发生率分别为14.55%、7.27%。证实单用PPV 手术时间长、出血多、视力改善不理想、并发症多。单纯PPV 治疗效果不佳的根本原因在于手术操作过程中会使新生血管破裂,出血和渗血干扰手术进行、影响手术效果[6]。由此判断有效控制术中出血对优化PPV 手术效果具有重要意义。
雷珠单抗属于全人源单克隆抗体,是一种血管内皮生长因子(vascular endothelial growth factor,VEGF)抑制剂,能够穿透视网膜,且具有很强的穿透力。雷珠单抗可直接与VEGF-A 中的所有亚型相结合,进而抑制VEGF 分泌,阻断VEGF 发挥作用,降低血管通透性,促进新生血管消退,减少新生血管,进而降低新生血管对手术产生的不良影响,减少PPV 术中出血和血液渗透[7]。在PPV 术前,应用雷珠单抗玻璃体注射,能够为手术创造良好的操作环境,优化术野,减少出血造成的干扰,保证术野的清晰度,能提升手术操作的精确度,快速准确的切除大增殖膜。因此PPV 联合雷珠单抗玻璃体注射能够缩短手术探索时间、止血操作时间,提升手术效率,优化手术效果,且降低了出血、渗血相关并发症的发生率[8]。本次研究中研究组患者采用雷珠单抗玻璃体注射联合PPV 治疗,患者的手术指标得到明显优化,手术时间缩短至(85.97±20.03)min,术中出血量降低至(1.05±0.32)ml,与对照组相比手术效率提升,出血量减少;且术后3个月,研究组患者的视力水平明显升高,达到(0.594±0.071)D,显著高于对照组。在并发症发生率方面,仅有1例患者发生再出血,予以对症处理后,未对手术效果产生影响,显著优于对照组。这一研究结果证实在PPV 术前联合应用雷珠单抗玻璃体注射更能优化PDR的手术效果。
综上,雷珠单抗玻璃体注射联合PPV 治疗PDR,可优化手术指标,改善视力水平,降低并发症发生率。因此,我们认为可以在PDR 临床治疗中推广使用此种治疗方式。

