银杏叶单组分双黄酮分离制备及抗氧化活性研究
张佳丽,李 玲,雷家珩,罗 珂
武汉理工大学化学化工与生命科学学院,武汉 430070
高浓度的双黄酮具有一定的细胞毒性[1],在银杏叶(GinkgoBilobaL.)提取物中,双黄酮一直被作为限量物质。但近年来,银杏双黄酮一些特殊药用价值,如抗流感病毒[2]、抗氧化[3]、治疗阿尔茨海默症[4]以及动脉粥硬化[5]等作用被陆续发现。
在双黄酮分析及其高纯单组分对照品研究方面,国内起始于2010年,孔繁晟[6]等首先采用硅胶柱色谱和重结晶方法得到98.5%的单组分金松双黄酮。2014年李冰等[7]通过硅胶色谱和半制备色谱,分离得到mg级纯度>95%的金松双黄酮、银杏黄素、异银杏黄素、白果素4种单组分双黄酮,但纯度没有达到>98%的对照品要求,特别是没有得到单组分阿曼托黄素。因此,国内双黄酮的定量分析一直落后于其药用研究,从而限制了其资源开发。
本工作以银杏叶粗提物为原料,反溶剂沉淀分离得到80.40%的多组分双黄酮粗品,再用半制备色谱分离制备得到>98%的高纯金松双黄酮、阿曼托黄素、白果素、银杏黄素异构体,系统研究了制备条件,并对银杏黄素异构体进行了分离,为单组分银杏双黄酮新药的研究与开发提供了重要的技术支持。
1 仪器与材料
半制备液相色谱仪 LC3000 北京创新恒通科技有限公司,Daisogel C18(50 mm×250 mm)色谱柱;高效液相色谱仪AgilentLC-1260,Elite Hypersil ODS2(200 mm×4.0 mm,5 μm)色谱柱;超导傅里叶核磁共振波谱仪 AscendTM 600 MHZ 瑞士Bruker 公司;二维液相色谱-离子阱质谱联用仪 Agilent 1100LC/MSD Trap;紫外分光光度计N4上海仪电电子股份有限公司;甲醇、乙腈为色谱纯;水为双蒸水;DPPH、ABTS、K2S2O8均购自阿拉丁;其他试剂均为分析纯;原料银杏叶采自本校南湖校区。
2 分离方法与结果
2.1 双黄酮粗品分离与提取
60%乙醇提取的银杏叶浸膏,用5倍水溶散后,加入等体积1∶1乙酸乙酯-正丁醇,搅拌提取3次。合并有机相,旋蒸浓缩,再用水分散,加入石油醚搅拌沉淀得到双黄酮粗提物。
取5 g双黄酮粗提物溶于40 mL乙酸乙酯,分3次加入80 mL石油醚,边加边搅拌,析出沉淀,离心分取,沉淀再溶于50 mL甲醇,加水再次沉淀。反复多次,得到含量为80.40%双黄酮粗品。图1为三次加水沉淀后的HPLC图谱。

图1 三次加水沉淀后双黄酮粗品HPLC谱图Fig.1 HPLC chromatograms of crude biflavonoids after three times of water precipitation注:化合物1~4分别为:阿曼托黄素、 白果素、银杏黄素异构体、金松双黄酮。Note:Compounds 1-4 :amentoflavone, bilobetin,ginkgetin,isomers,sciadopitysin.
2.2 单组分双黄酮色谱制备
称取1.00 g双黄酮粗品,用80%甲醇约100 mL至固体恰好溶解,离心分离,微孔滤膜过滤后进半制备色谱,洗脱分离,流速30 mL/min,柱温35 ℃,检测波长330 nm。
收集目标液,采用红外、核磁氢谱、质谱和分析型高效液相色谱对其结构及纯度进行检测。
2.2.1 洗脱梯度考察
考察流动相组成和多个洗脱梯度对分离效果影响。结果表明,制备条件为甲醇(A)-有机酸水溶液(B),0~2 min,76%A;2~45 min,76%~100%A;45~50 min,100%A,可完全分离阿曼托黄素、白果素、银杏黄素异构体和金松双黄酮(分别记为目标化合物1、2、3、4),其保留时间分别为14.1 min、18.5 min、28.2 min和41.1 min。此外,实验证明,流动相中加入0.005 mol/L三氟乙酸以及0.005 mol/L乙酸可规整峰型。
2.2.2 二次制备
将一次制备所得的阿曼托黄素(化合物1)和白果素(化合物2)用适量甲醇复溶,调节洗脱梯度为:甲醇(A)-有机酸水溶液(B),0~2 min,50%~80%A;2~45 min,80%~100%A;45~50 min,100%A。两次制备所得4种单组分双黄酮的HPLC谱图如图2。
4种单组分双黄酮阿曼托黄素、白果素、银杏黄素异构体、金松双黄酮产率(mg/kg)经计算分别为:22.5、23.8、192.5、71.8。

图2 4种高纯单组分双黄酮的HPLC谱图Fig.2 HPLC chromatograms of four high-purity one-component biflavonoids
3 定性及定量分析
3.1 结构鉴定
对得到的4个化合物进行了熔点、红外、紫外、质谱、1H NMR、13C NMR等检测,结果如下:
化合物1黄色粉末,mp.268~269 ℃,易溶于DMSO、甲醇、乙酸乙酯、丙酮。UV (MeOH) λMax266,337 nm;IR (KBr) νmax3 453 (OH),1 653 (共扼C = O),1 498 (芳C),1 240,827 cm-1;Positive ESI-MS:m/z539.1 [M+H]+(Calcd for C30H18O10);1H NMR (500 MHz,DMSO-d6) δ13.11 (s,1H,OH-5′′),12.98 (s,1H,OH-5),10.86 (s,2H,OH-7,7′′),10.31 (s,2H,OH-4′,4′′′),8.03 (d,J= 2.5 Hz,1H,H-2′),8.0 (dd,J= 8.8,2.5 Hz,1H,H-6′),7.58 (d,J= 8.5 Hz,2H,H-2′′′,6′′′),7.17 (d,J= 8.5 Hz,1H,H-5′),6.85 (s,1H,H-3),6.81 (s,1H,H-3′′),6.73 (d,J= 8.4 Hz,2H,H-3′′′,5′′′),6.48 (d,J= 2.1 Hz,1H,H-8),6.42 (s,1H,H-6′′),6.20 (d,J= 2.1 Hz,1H,H-6);13C NMR (150 MHz,DMSO-d6) δ182.1 (C-4,4′),166.4 (C-7),163.6 (C-2,2′),163.5 (C7′′),161.8 (C-5),160.7 (C-5′′),160.5 (C-2′),158.8 (C-9),157.7 (C-4′′′),156.3 (C-9′′),132.6 (C-4′),129.2 (C-2′′′,6′′′),128.1 (C-6′),123.4 (C-5′),122.9 (C-1′′′),120.8 (C-3′),117.6 (C-1′),115.8 (C-3′′′,5′′′),104.5 (C-3,3′),104.4 (C-10),104.1 (C-8′′),104.0 (C-10′′),98.8 (C-6′′),98.3 (C-6),94.0 (C-8)。以上数据与文献[9,10]基本一致,故确定化合物1为阿曼托黄素(amentoflavone)。
化合物2黄色晶体(CH2Cl2-CH3OH),mp.233~235 ℃,易溶于甲醇、乙酸乙酯、丙酮。UV (MeOH) λMax267,335 nm;IR (KBr) νmax3 498 (OH),1 654 (共扼C = O),1 496 (芳C),1 243,836 cm-1;Negative ESI-MS:m/z551.0 [M-H]-(Calcd for C31H20O10);1H NMR (500 MHz,DMSO-d6) δ13.11 (s,1H,OH-5′′),12.94 (s,1H,OH-5),10.85 (s,1H,OH-7′′),10.83 (s,1H,OH-7),10.29 (s,1H,OH-4′′′),8.20 (dd,J= 8.8,2.5 Hz,1H,H-6′),8.08 (d,J= 2.4 Hz,1H,H-2′),7.52 (d,J= 8.9 Hz,2H,H-2′′′,6′′′),7.36 (d,J= 8.9 Hz,1H,H-5′),6.95 (s,1H,H-3),6.82 (s,1H,H-3′′),6.72 (d,J= 8.9 Hz,2H,H-3′′′,5′′′),6.50 (d,J= 2.1 Hz,1H,H-8),6.41 (s,1H,H-6′′),6.21 (d,J= 2.1 Hz,1H,H-6),3.79 (s,3H,OCH3-4′);13C NMR (150 MHz,DMSO-d6),δ182.1 (C-4,4′′),166.4 (C-7),163.6 (C-2,2′′),163.5 (C-7′′),161.8 (C-5),161.7 (C-2′),160.7 (C-5′′),1588.8 (C-9),157.7 (C-4′′′),156.3 (C-9′′),132.2 (C-4′),129.2 (C-2′′′,6′′′),127.7 (C-6′),123.1 (C-5′),122.9 (C-1′′′),121.9 (C-3′),115.8 (C-3′′′,5′′′),111.0 (C-1′),104.5 (C-3,3′′),104.4 (C-10),104.1 (C-8′′),104.0 (C-10′′),98.8 (C-6′′),98.3 (C-6),94.0 (C-8),56.1 (OCH3-2′)。以上数据与文献[9,11]一致,故确定化合物2为白果素(bilobetin)。
化合物3黄色晶体(CH2Cl2-CH3OH),mp.24~246 ℃,易溶于乙酸乙酯、丙酮。UV (MeOH) λMax266,330 nm;IR (KBr) νmax3 434 (OH),1 658 (共扼C = O),1 500 (芳C),1 249,836 cm-1;Negative ESI-MS:m/z564.9 [M-H]-(Calcd for C32H22O10);由1H NMR谱图推出化合物3为银杏黄素(ginkgetin)与异银杏黄素(isoginkgetin)的混合物,将其进一步分离后得到银杏黄素1H NMR (500 MHz,DMSO-d6) δ13.10 (s,1H,OH-5′′),12.93 (s,1H,OH-5),10.83 (s,1H,OH-7′′),10.29 (s,1H,OH-4′′′),8.24 (d,J= 9.1 Hz,1H,H-1′),8.11 (d,J= 2.4 Hz,1H,H-5′),7.51 (d,J= 8.5 Hz,2H,H-2′′′,6′′′),7.38 (d,J= 8.8 Hz,1H,H-2′),7.03 (s,1H,H-8),6.83 (d,J= 2.8 Hz,2H,H-3,3′′),6.72 (d,J= 8.6 Hz,2H,H-3′′′,5′′′),6.43~6.36 (m,2H,H-6,6′′′),3.84 (s,3H,OCH3-7),3.80 (s,3H,OCH3-4′);13C NMR (150 MHz,DMSO-d6) δ182.1 (C-4,4′′),167.3 (C-7),163.6 (C-2,2′′),163.5 (C-7′′),161.7 (C-2′),161.4 (C-5),160.7 (C-5′′),158.4 (C-9),157.7 (C-4′′′),156.3 (C-9′′),132.2 (C-4′),129.2 (C-2′′′,6′′′),127.7 (C-6′),123.1 (C-5′),122.9 (C-1′′′),121.9 (C-3′),115.8 (C-3′′′,5′′′),111.0 (C-1′),104.5 (C-3,3′′),104.1 (C-10,8′′),104.0 (C-10′′′),98.8 (C-6′′),98.0 (C-6),92.8 (C-8),56.1 (OCH3-2′),55.8 (OCH3-7);异银杏黄素1H NMR (500 MHz,DMSO-d6) δ13.07 (s,1H,OH-5′′),12.94 (s,1H,OH-5),10.85 (d,J= 8.2 Hz,2H,OH-7,7′′),8.21 (dd,J= 8.8,2.4 Hz,1H,H-1′),8.07 (d,J= 2.3 Hz,1H,H-5′),7.63 (d,J= 8.8 Hz,2H,H-2′′′,5′′′),7.37 (d,J= 8.9 Hz,1H,H-2′),6.94 (dd,J= 9.3,4.9 Hz,4H,H-3,3′′,3′′′,5′′′),6.49 (d,J= 2.2 Hz,1H,H-6′′),6.42 (s,1H,H-8),6.20 (d,J= 2.1 Hz,1H,H-6),3.78 (d,J= 16.3 Hz,6H,OCH3-4′,4′′′);13C NMR (150 MHz,DMSO-d6) δ182.1 (C-4,4′′),166.4 (C-7),163.6 (C-2,2′′),163.5 (C-7′′),161.8 (C-5),161.7 (C-2′),160.7 (C-5′′),159.8 (C-4′′′),158.8 (C-9),156.3 (C-9′′),132.2 (C-4′),128.8 (C-2′′′,6′′′),127.7 (C-6′),123.1 (C-5′),122.6 (C-1′′′),121.9 (C-3′),114.2 (C-3′′′,5′′′),111.0 (C-1′),104.5 (C-3,3′′),104.4 (C-10),104.1 (C-8′′),104.0 (C-10′′′),98.8 (C-6′′),98.3 (C-6),94.0 (C-8),56.1 (OCH3-2′),55.8 (OCH3-4′′′)。以上数据与文献[9,12]基本一致,故确定化合物3为银杏黄素异构体(ginkgetin isomers)。
化合物4淡黄色晶体(CH2Cl2,CH3OH),mp.298~300 ℃,易溶于DMF、丙酮。UV (MeOH) λMax268,330 nm;IR (KBr) νmax3 423 (OH),1 652 (共扼C = O),1 504 (芳C),1 245,827 cm-1;Negative ESI-MS:m/z578.8 [M-H]-(Calcd for C33H24O10);1H NMR (500 MHz,DMSO-d6) δ13.07 (s,1H,OH-5′′),12.93 (s,1H,OH-5),10.86 (s,1H,OH-7′′),8.25 (dd,J= 8.8,2.5 Hz,1H,H-6′),8.10 (d,J = 2.4 Hz,1H,H-2′),7.62 (d,J= 9.0 Hz,2H,H-2′′′,6′′′),7.38 (d,J= 8.9 Hz,1H,H-5′),7.03 (s,1H,H-3),6.95 (d,J= 9.0 Hz,2H,H-3′′′,5′′′),6.93 (s,1H,H-3′′),6.82 (d,J= 2.3 Hz,1H,H-8),6.43 (s,1H,H-6′′),6.38 (d,J= 2.3 Hz,1H,H-6),3.91-3.70 (m,9H,OCH3-7,4′,4′′′);13C NMR (150 MHz,DMSO-d6) δ182.1 (C-4,4′′),167.3 (C-7),163.6 (C-2,2′′),163.5 (C-7′′),161.7 (C-2′),161.4 (C-5),160.7 (C-5′′),159.8 (C-4′′′),158.4 (C-9),156.3 (C-9′′),132.2 (C-4′),128.8 (C-2′′′,6′′′),127.7 (C-6′),123.1 (C-5′),122.6 (C-1′′′),121.9 (C-3′),114.2 (C-3′′′,5′′′),111.0 (C-1′),104.5 (C-3,3′′),104.1 (C-10,8′′),104.0 (C-10′′′),98.8 (C-6′′),98.0 (C-6),92.8 (C-8),56.1 (OCH3-2′),55.8 (OCH3-7,4′′′)。以上数据与文献[9,13]一致,故确定化合物4为金松双黄酮(sciadopitysin)。

图3 单组分双黄酮的红外光谱图Fig.3 Infrared spectra of one-component bioflavonoids注:阿曼托黄素、白果素、银杏黄素异构体、 金松双黄酮(A)银杏黄素及异银杏黄素(B)。Note:Amentoflavone,Bilobetin,Ginkgetin isomers, Sciadopitysin (A) Ginkgetin and Isoginkgetin(B).
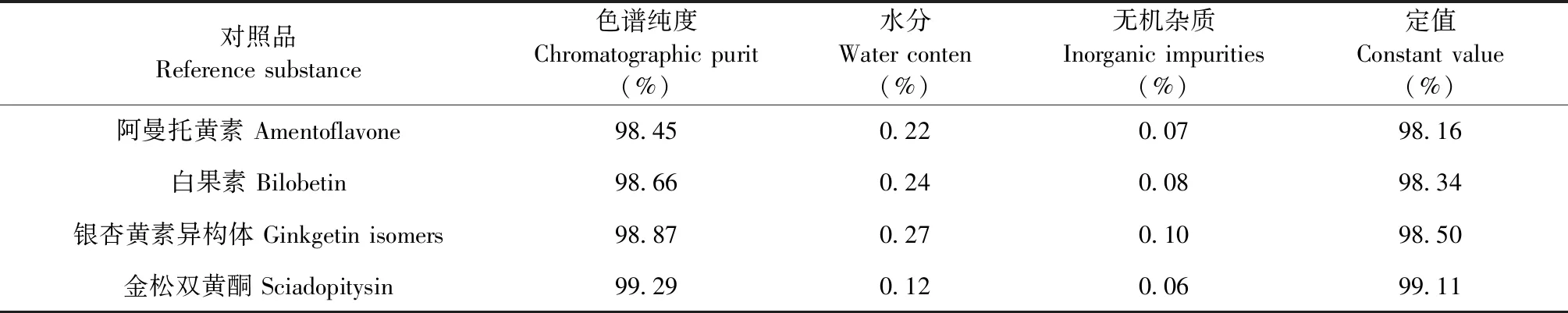
表1 两次色谱制备得到的单组分双黄酮纯度定值Table 1 Purity assessment of one-component biflavonoids after two chromatographic preparation
3.2 HPLC-DAD测定纯度
根据中国计量科学研究院关于国家标准物质纯度测定的要求[14],对双黄酮制备品以面积归一法计算纯度,测定4种双黄酮色谱纯度。
采用硅胶薄层色谱法对单组分双黄酮定性分析,观察发现4种单组分双黄酮均为单一黄绿色斑点。以质量平衡法测定单组分双黄酮纯度,结果如表1所示。
4 抗氧化活性和异构体分离
4.1 抗氧化活性测定
参照文献[8]测定桑椹根化学成分的抗氧化活性方法,分别在517 nm及734 nm处测定4种双黄酮样品清除DPPH、ABTS+自由基的清除率及半数抑制率IC50值。每份样品平行操作测定3次,取平均值,得到4种双黄酮的抗氧化活性结果见表2。结果显示4种双黄酮具有明显的抗氧化活性,与文献报道一致。
4.2 银杏黄素异构体进一步分离
关于银杏黄素异构体的进一步分离,我们尝试采用乙腈-水体系的方法[7],将甲醇-水分离体系得到的银杏黄素异构体(化合物3)用适量丙酮复溶,以60%乙腈和有机酸水溶液洗脱分离,所用有机酸为0.005 mol/L三氟乙酸-0.005 mol/L乙酸混合物,可实现银杏黄素和异银杏黄素的完全分离,其纯度定值分别为98.56%、95.70%,所得HPLC谱图如图4。

表2 待测化合物清除DPPH自由基和ABTS+自由基的IC50值Table 2 IC50 values of DPPH and ABTS+radical scavenging of the isolated compounds

图4 银杏黄素及异银杏黄素的HPLC谱图Fig.4 HPLC chromatograms of ginkgetin and isoginkgetin
5 结论
本实验以60%乙醇提取的银杏叶浸膏为原料,水-石油醚多次反溶剂沉淀分离得到纯度为80.40%的双黄酮粗品。再以甲醇-水为流动相,用制备色谱梯度洗脱分离得到4种符合中药化学对照品要求的单组分双黄酮,并采用60%乙腈和有机酸水溶液对银杏黄素异构体进行了完全分离,得到了5种纯度均大于95%的双黄酮,为双黄酮标样的生产提供思路,通过DPPH和ABTS+体外自由基清除实验,此次分离得到的五种双黄酮均具有一定抗氧化活性,也为双黄酮的开发利用提供了科学依据。

