盐酸埃克替尼联合全脑放疗治疗非小细胞肺癌脑转移的随机对照研究
纪蓉 王建芳 孙彩萍 刘建江 陈遐林

[摘要] 目的 探討全脑放疗联合盐酸埃克替尼治疗非小细胞肺癌(NSCLC)脑转移的疗效及安全性。 方法 选取2013年6月~2017年6月共44例脑转移的NSCLC患者,随机分为联合治疗组与单纯放疗组,比较两组间疗效及安全性。结果 中位随访18.5个月,联合治疗组及单纯放疗组的mPFS分别为9.3个月及6.6个月(log-rank P=0.006);联合治疗组EGFR突变者及野生型者的mPFS分别为12.2个月和6.5个月(log-rank P=0.002),单纯放疗组EGFR突变者及野生型者的mPFS分别为6.4个月和6.8个月(log-rank P=0.933)。联合治疗组及单纯放疗组的mOS分别为14.2个月及12.6个月(log-rank P=0.035);联合治疗组中EGFR突变者及野生型者的mOS分别为19.1个月和12.7个月(log-rank P=0.006),单纯放疗组EGFR突变者及野生型者的mOS分别为12.6个月和10.4个月(log-rank P=0.449)。两组间的ORR分别为78.3%及47.6%(log-rank P=0.035),DCR分别为91.3%及85.7%(χ2=0.341,P=0.560)。不良反应方面,联合组的皮疹发生率为56.5%,其中3例为3~4级;两组乏力、恶心呕吐、腹泻肝肾损伤、白细胞减少等不良反应均为1~2级,且两组比较差异无统计学意义。 结论 盐酸埃克替尼联合全脑放疗可提高非小细胞肺癌脑转移患者的客观缓解率,延长中位局部无进展生存期及中位总生存期,患者的不良反应耐受性良好。
[关键词] 盐酸埃克替尼;非小细胞肺癌;表皮生长因子受体;全脑放疗
[中图分类号] R979.1 [文献标识码] A [文章编号] 1673-9701(2019)10-0029-05
A randomized controlled trial of ectatinib hydrochloride combined with whole brain radiotherapy for brain metastasis of non-small cell lung cancer
JI Rong1 WANG Jianfang2 SUN Caiping2 LIU Jianjiang2 CHEN Xialin2
1.Department of Radiation Oncology, Shaoxing Second Hospital, Shaoxing 312000, China; 2.Department of Radiation Oncology, Shaoxing People's Hospital, Shaoxing 312000, China
[Abstract] Objective To investigate the efficacy and safety of whole brain radiotherapy combined with ectatinib hydrochloride in the treatment of non-small cell lung cancer(NSCLC) brain metastases. Methods A total of 44 patients with brain metastases from NSCLC from June 2013 to June 2017 were randomly divided into combination therapy group and radiotherapy group. The efficacy and safety between the two groups were compared. Results The median follow-up was 18.5 months. The mPFS of the combination therapy group and the radiotherapy group were 9.3 months and 6.6 months, respectively (log-rank P=0.006). The mPFS of the EGFR mutant and wild type in the combination group were 12.2 months and 6.5 months (log-rank P=0.002). The mPFS of EGFR mutants and wild-type patients in the radiotherapy group were 6.4 months and 6.8 months, respectively (log-rank P=0.933). The mOS in the combination therapy group and the radiotherapy group were 14.2 months and 12.6 months, respectively (log-rank P=0.035). The mOS of the EGFR mutant and wild type in the combination group were 19.1 months and 12.7 months, respectively(log-rank P=0.006). The mOS of EGFR mutants and wild-type patients in the radiotherapy group were 12.6 months and 10.4 months, respectively (log-rank P=0.449).The ORR of the two groups was 78.3% and 47.6%, respectively (log-rank P=0.035), and the DCR was 91.3% and 85.7%, respectively (χ2=0.341, P=0.560).In terms of adverse reactions,the incidence of rash in the combined group was 56.5%, of which 3 cases were grade 3-4. The adverse reactions such as fatigue, nausea and vomiting, diarrhea,liver and kidney damage, and leukopenia were all grade 1-2, and there was no statistically significant difference between the two groups. Conclusion Ectinib hydrochloride combined with whole brain radiotherapy can improve the objective response rate of patients with non-small cell lung cancer with brain metastases, prolong the median local progression-free survival and median overall survival, and the patient's adverse reaction tolerance is good.
[Key words] Ectinib hydrochloride; Non-small cell lung cancer; Epidermal growth factor receptor; Whole brain radiotherapy
肺癌是目前全世界发病率及病死率最高的恶性肿瘤,其中大约有80%为非小细胞肺癌(NSCLC),而约20%~40%的非小细胞肺癌患者在疾病的某一阶段会出现脑转移[1-2],未经治疗的脑转移患者多在1~3个月内死亡。目前,脑转移的标准治疗包括全脑放疗、立体定向放疗、外科手术等常规治疗方法,但效果均不理想[3-4]。随着靶向治疗药物表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)在临床的广泛使用,晚期肺癌患者的生存期已有大幅度提高[5-7]。Park SJ等[8]进行的一项Ⅱ期研究证实,利用EGFR-TKIs治疗存在EGFR突变的伴有脑转移的肺腺癌患者,部分缓解率达83%,中位无进展生存期及中位总生存时间分别为6.6个月、15.9个月。基础研究发现EGFR信号通路与肿瘤细胞放射抗拒密切相关,而运用EGFR抑制剂可以增强肿瘤细胞的放射敏感性[9-10]。因此,本研究将对全脑放療联合或不联合EGFR-TKI治疗非小细胞肺癌脑转移患者做随机研究,探讨两组间的疗效及不良反应。
1 资料与方法
1.1 一般资料
选取2013年6月~2017年6月存在脑转移的NSCLC患者共44例。其中男19例,女25例;脑转移数目≤3个18例(患者不适合行外科手术或立体定向放射外科(SRS)治疗),>3个26例;中位年龄59岁(49~74岁)。采用随机数字表法分成两组(盐酸埃克替尼联合全脑放疗组、单纯全脑放疗组),联合治疗组:男10例、女13例,腺癌22例、鳞癌1例,EGFR野生型10例、EGFR突变型13例,中位年龄58.7岁;单纯放疗组:男9例、女12例,腺癌20例、鳞癌1例,EGFR野生型9例、EGFR突变型12例,中位年龄60.1岁。见表1。本研究经绍兴市人民医院伦理委员会审批同意(2015伦理第010号),所有患者在治疗前均签署治疗知情同意书。
1.2 纳入与排除标准[11]
纳入标准:(1)经病理组织学和(或)细胞学检查确诊并经CT或MRI证实存在脑转移;(2)KPS评分>70分;(3)预计生存期>3个月。排除标准:(1)合并心、肺、肾、脑血管等脏器严重疾病;(2)白细胞、血小板、血红蛋白异常;(3)合并其他肿瘤病史者。
1.3 治疗方法
单纯放疗组:采用常规全脑放疗。全脑放疗的方法:全脑两侧野对穿照射,剂量(30~35)Gy/(2~3)周,如转移灶数目为1~3个,行全脑放疗同时对转移病灶局部推量5~12 Gy。联合治疗组:在放疗开始前1周口服盐酸埃克替尼(浙江贝达药业有限公司,国药准字H20110061,125 mg/片),125 mg/次,一天3次,4周为一个疗程。放疗结束后继续予盐酸埃克替尼治疗,直至出现不可耐受反应或疾病进展。
1.4 疗效评价及不良反应评估
按照实体瘤的疗效评价标准(RECIST1.1)[12],完全缓解(CR):所有目标病灶消失,且病理性淋巴结短轴<10 mm;部分缓解(PR):所有目标病灶直径总和减少>30%;疾病进展(PD):所有目标病灶直径总和增加>20%且增加值>5 mm或出现新病灶;稳定(SD):介于PR与PD之间。所有患者在放疗结束后4周及每隔3个月直到死亡或失访都进行全面评估,包括血常规、生化指标、肿瘤指标、胸腹部CT、头颅MRI。于放疗结束后4周评定近期疗效,客观有效率为(CR+PR)/(CR+PR+SD+PD)×100%,疾病控制率为(CR+PR+SD)/(CR+PR+SD+PD)×100%。中位局部无进展生存期指治疗开始时至颅内病灶进展或颅内出现新发病灶的时间。不良反应评估按照美国癌症研究所常见毒性判定标准NCI-CTCAE 3.0版抗癌药物毒性评价标准[13]及RTOG/EORTC急性放射不良反应评价标准[14]进行评价。
1.5 统计学方法
采用SPSS20.0统计软件进行分析,计量资料用(x±s)表示,进行t检验;计数资料用[n(%)]表示,采用χ2检验;采用Kaplan-Meier法进行无进展生存期(progression free survival,PFS)及总生存期(overall survival,OS)生存曲线分析,并应用对数秩检验(log-rank test)计算生存曲线间的统计学差异;双侧P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
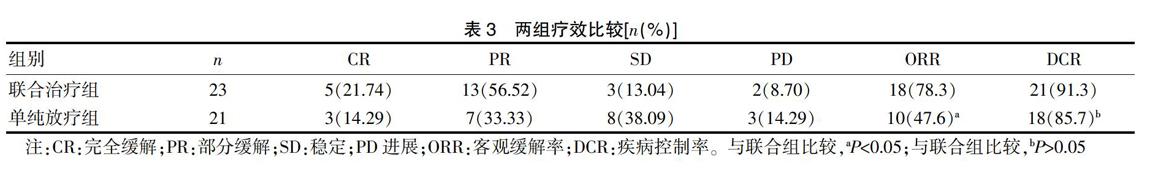
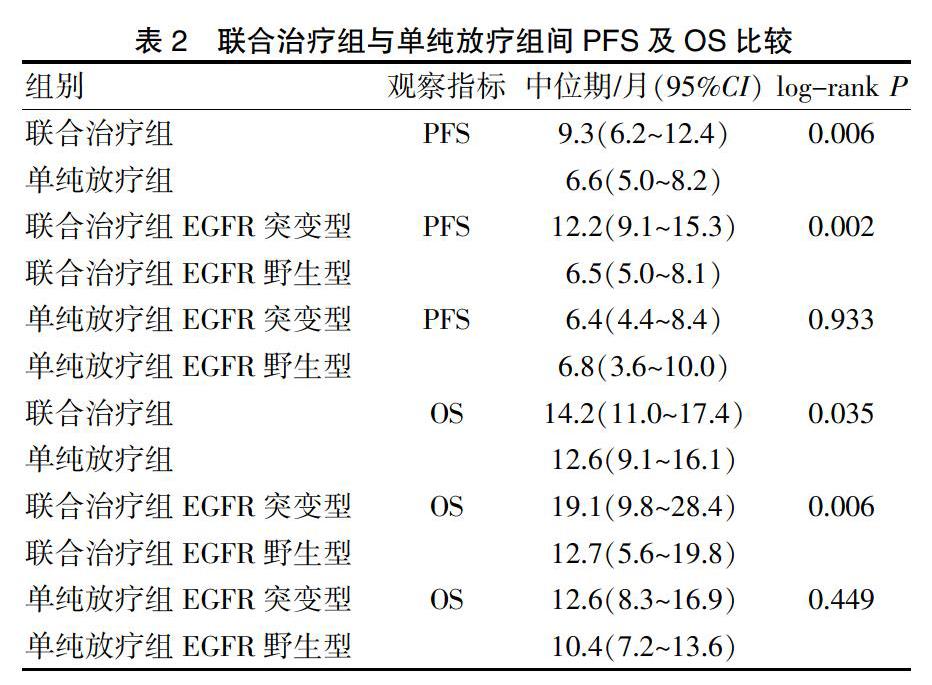
至末次随访时间2017年6月31日,所有患者均未失访,中位随访时间为18.5个月。联合治疗组的中位无进展生存期(median progression free survival,mPFS)为9.3个月(95%CI:6.2~12.4个月),单纯放疗组的mPFS为6.6个月(95%CI:5.0~8.2个月),差异有统计学意义(log-rank P=0.006),见图1。联合治疗组中EGFR突变患者mPFS为12.2个月(95%CI:9.1~15.3个月),野生型患者mPFS为6.5个月(95%CI:5.0~8.1个月),差异具有统计学意义(log-rank P=0.002),见图2A;而在单纯放疗组中EGFR突变患者mPFS为6.4个月(95%CI:4.4~8.4个月),野生型患者mPFS为6.8个月(95%CI:3.6~10.0个月),未见明显差别(log-rank P=0.933),见图2B。联合治疗组的中位总生存期(median overall survival,mOS)为14.2个月(95%CI:11.0~17.4个月),单纯放疗组的mOS为12.6个月(95%CI:9.1~16.1个月),差异有统计学意义(log-rank P=0.035),见图3。联合治疗组中EGFR突变患者mOS为19.1个月(95%CI:9.8~28.4个月),野生型患者mOS为12.7个月(95%CI:5.6~19.8个月),差异具有统计学意义(log-rank P=0.006),见图4A;而在单纯放疗组中EGFR突变患者mOS为12.6个月(95%CI:8.3~16.9个月),野生型患者mOS为10.4个月(95%CI:7.2~13.6个月),未见明显差别(log-rank P=0.449),见图4B和表2。两组患者的ORR分别为78.3%及47.6%(χ2=4.454,P=0.035),DCR分别为91.3%及85.7%(χ2=0.341,P=0.560),见表3。
2.2 两组不良反应发生情况
联合治疗组的主要不良反应为皮疹,其中有3例患者为3~4级,经对症处理后均能耐受继续口服靶向药物。其余乏力、恶心呕吐、腹泻、肝肾损伤、白细胞减少等不良反应均为1~2级,且两组比较差异无统计学意义(P>0.05)。见表4。
3 讨论
脑转移是常见的肺癌远处转移部位,目前虽可通过外科手术切除、化疗、放疗等治疗达到部分缓解,但远期效果均不够理想。表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)作为一种小分子靶向药物,能透过血脑屏障进入颅内起作用[15-16],而放疗本身可进一步破坏血脑屏障的完整性,更有利于EGFR-TKI进入脑组织发挥作用。褚建华等[17]报道全脑放疗序贯吉非替尼治疗颅内病灶RR为43.3%,DCR为80%,中位生存时间为12.8个月。Welsh等[18]应用特罗凯同步全脑放疗治疗40例非小细胞肺癌脑转移患者,总客观反应率达到86%,神经毒性未见增加,MST为11.8个月,其中EGFR野生型MST时间为9.3个月,EGFR突变型MST为19.1个月。Zhuang等[19]进行的一项Ⅱ期研究对比厄洛替尼联合全脑放疗治疗与单纯全脑放疗治疗非小细胞肺癌脑转移的临床疗效,结果提示联合治疗组的ORR、mPFS、中位OS分别为95.65%、6.8个月、10.7个月,明显高于单纯放疗组的54.84%、5.2个月、8.9个月。
盐酸埃克替尼是我国自行研制的小分子靶向抗肿瘤药,以表皮生长因子受体(EGFR)为靶标,是一种强效、高选择性的口服酪氨酸激酶抑制剂。ICOGEN研究结果显示,盐酸埃克替尼总体疗效不逊于吉非替尼,无进展生存期4.6个月对3.4个月(P=0.13),且盐酸埃克替尼组的药物相关不良事件发生率明显低于吉非替尼(61% vs 70%,P=0.046)[20]。Gong等[21]回顾性分析盐酸埃克替尼治疗21例EGFR突变型的NSCLC软脑膜转移患者,中位总生存时间达10.1个月。本研究对比盐酸埃克替尼联合放疗与单纯放疗的疗效,结果显示,联合治疗组对非小细胞肺癌脑转移的mPFS(9.3个月 vs 6.6个月,P=0.006)及中位总生存期(14.2个月 vs 12.6个月,P=0.035)更长,同步治疗组的客观缓解率明显升高(78.3% vs 47.6%,P=0.035)。亚组分析提示,联合治疗组中EGFR突变患者mPFS及中位总生存期均明显高于野生型患者(12.2个月 vs 6.5个月,P=0.002)、(14.2个月 vs 12.6个月,P=0.035),而在单纯放疗组中不同EGFR表达之间mPFS及中位总生存期均未见明显差别(6.4个月 vs 6.8个月,P=0.933)、(12.6个月 vs 10.4个月,P=0.449)。埃克替尼与放疗联合增强疗效机制除了血脑屏障透过率增加以外,还可能和埃克替尼的放疗协同增敏作用有关:(1)埃克替尼可使癌细胞阻滞于G1期,使得对射线敏感性差的S期癌细胞数量下降,提高癌细胞的整体放射敏感性;(2)固化放射效应,抑制放射后损伤的修复;(3)抑制放射诱导的EGFR磷酸化,减少癌细胞增殖;(4)抑制PI3K-Akt信号通路,增强放疗后癌细胞凋亡[22]。不良反应方面,联合治疗组中有56.5%的患者发生皮疹反应,其中3例患者皮疹达3~4级,但经对症处理后能耐受继续口服靶向藥物;其他不良反应,如乏力、恶心呕吐、腹泻、肝肾损伤、白细胞减少等均为1~2级。本研究结果与文献[23]报道的小样本回顾性研究结果基本吻合,表明盐酸埃克替尼联合放疗能提高非小细胞肺癌脑转移治疗的近期疗效,改善生存质量,毒副反应可以耐受。
从该临床研究中可以看出,盐酸埃克替尼联合全脑放疗主要在EGFR突变患者中起作用,但由于本研究开始时部分患者尚未行EGFR基因检测,在治疗结束后才补行基因检测,因此未按照EGFR突变状态来进行分组研究,而且本次研究入组病例较少,不能进行分层分析各种因素对治疗效果的影响,最终结论有待扩大样本及延长随访时间来验证。
[参考文献]
[1] Mujoomdar Amol Austin,John HM,Malhotra Rohin,et al. Clinical predictors of metastatic disease to the brain from non-small cell lung carcinoma:Primary tumor size,cell type,and lymph node metastases[J]. Radiology,2007,242(3):882-888.
[2] Barnholtz-Sloan Jill S,Sloan Andrew E,Davis Faith G,et al. Incidence proportions of brain metastases in patients diagnosed(1973 to 2001) in the Metropolitan Detroit Cancer Surveillance System[J]. J Clin Oncol,2004, 22(14):2865-2872.
[3] 冯宇,胡兴胜.非小细胞肺癌脑转移治疗的研究进展[J].中国肿瘤临床,2018,45(7):331-338.
[4] Mulvenna P,Nankivell M,Barton R,et al. Dexamethasone and supportive care with or without whole brain radiotherapy in treatingpatients with non-small cell lung cancer with brain metastases unsuitable for resection or stereotactic radiotherapy(QUARTZ):Results from a phase 3,non-inferiority,randomized trial[J]. Lancet,2016,388(10055):2004-2014.
[5] 郭芷汛,刘欢,李艳,等.表皮生长因子受体-酪氨酸激酶抑制剂在治疗非小细胞肺癌方面的研究进展[J].实用医院临床杂志,2018,15(1):208-210.
[6] 郭丽丽,李明智,唐俊舫,等.厄洛替尼治疗EGFR突变的晚期非小细胞肺癌临床疗效分析[J].医学研究杂志,2017,46(3):138-140.
[7] 王银叶,朱波,贾美莹.吉非替尼与多西他赛治疗晚期非小细胞肺癌的临床效果比较[J].实用癌症杂志,2017,32(12):1978-1980.
[8] Park SJ,Kim HT,Lee DH,et al. Efficacy of epidermal growth factor receptor tyrosine kinase inhibitors for brain metastasis in non-small cell lung cancer patients harboring either exon 19 or 21 mutation[J].Lung Cancer,2012,77(3):556-560.
[9] Chinnaiyan Prakash,Huang Shyhmin,Vallabhaneni Geetha,et al. Mechanisms of enhanced radiation response following epidermal growth factor receptor signaling inhibition by erlotinib(Tarceva)[J]. Cancer Res,2005,65(8):3328-3335.
[10] Tanaka Toshimitsu,Munshi Anupama,Brooks Colin,et al.Gefitinib radiosensitizes non-small cell lung cancer cells by suppressing cellular DNA repair capacity[J]. Clin Cancer Res,2008,14(4):1266-1273.
[11] 杨妤,杨新辉,苏加利.替莫唑胺联合全脑放疗治疗非小细胞肺癌脑转移瘤的疗效[J].广东医学,2013,34(7):1115-1117.
[12] Eisenhauer EA,Therasse P,Bogaerts J,et al. New response evaluation criteria in solid tumours:Revised RECIST guideline(version 1.1)[J]. Eur J Cancer,2009,45(2):228-247.
[13] Common Terminology Criteria for Adverse Events, Version 3.0. http://ctep.cancer.gov/protocoldevelopment/electronic_applications/docs/ctcaev3.pdf.
[14] Cux JD,Stetz J,Pajak TF. Toxcicity criteria of the radiation therapy oncology group(RTOG) and the european organization for research and treatment of cancer(EORTC)[J].Int J Radiat Oncol Biol Phys,1995,31(5):1341-1346.
[15] Yosuke Togashi,Katsuhiro Masago,Masahide Fukudo,et al. Cerebrospinal fluid concentration oferlotinib and its active metabolite OSI-420 in patients with central nervous systemmetastases of non-small cell lung cancer[J].J Thorac Oncol,2010,5(7):950-955.
[16] Weber Britta,Winterdahl Michael,Memon Ashfaque,et al. Erlotinib accumulation in brain metastases from non-small cell lung cancer:Visualization by positron emission tomography in a patient harboring a mutation in the epidermal growth factor receptor[J].J Thorac Oncol,2011,6(7):1287-1289.
[17] 儲建华,徐杰,沈预程.全脑放疗序贯吉非替尼治疗老年非小细胞肺癌伴脑转移的临床观察[J].临床肿瘤学杂志,2013,18(7):656-658.
[18] Welsh James W,Komaki Ritsuko,Amini Arya,et al. Phase II trial of erlotinib plus concurrent whole-brain radiation therapy for patients with brain metastases from non-small-cell lung cancer[J]. J Clin Oncol,2013,31(7):895-902.
[19] Zhuang Hongqing,Yuan Zhiyong,Wang Jun,et al. Phase II study of whole brain radiotherapy with or without erlotinib in patients with multiple brain metastases from lung adenocarcinoma[J].Drug Des Devel Ther,2013,7:1179-1186.
[20] Shi Yuankai,Zhang Li Liu,Xiaoqing,et al. Icotinib versus gefitinib in previously treated advanced non-small-cell lung cancer(ICOGEN):A randomised, double-blind phase 3 non-inferiority trial[J]. Lancet Oncol,2013,14(10):953-961.
[21] Gong Lei,Xiong Ming,Huang Zhiyu,et al. Icotinib might be effective for the treatment of leptomeningeal carcinomatosis in non-small cell lung cancer with sensitive EGFR mutations[J]. Lung Cancer,2015,89(3):268-273.
[22] 郭红云,贾亚森.埃克替尼联合放疗治疗晚期非小细胞肺癌的研究进展[J].中国临床新医学,2017,10(5):491-494.
[23] Li Jin-Rui,Zhang Ye,Zheng Jia-Lian.Icotinib combined whole brain radiotherapy for patients with brain metastasis from lung adenocarcinoma harboring epidermal growth factor receptor mutation[J].J Thorac Dis,2016,8(7):1504-1512.

