基于UPLC-Q-TOF/MS法分析不同产地前胡药材质量
李颖硕,周 秀,李瑞芳,徐增莱,盖亚男∗
(1.江苏省中国科学院植物研究所,江苏 南京 210014;2.深圳市和顺本草药业有限公司,广州 深圳 518027)
前胡为伞形科植物白花前胡Peucedanum PraeruptorumDunn 的干燥根,始载于 《名医别录》,被列为中品,性微寒,味苦、辛。具有宣散风热、降气化痰的功效。临床主要用于风热头痛、痰多咳喘、上呼吸道感染等症[1-2]。前胡产地众多,浙江、安徽、江西、湖北、贵州、湖南、重庆等地为道地产区。近年来,在安徽、四川等地也有大范围种植。香豆素类是前胡质量评价的重要指标,以角型吡喃香豆素、呋喃香豆素为主[3-4]。
前胡质量受到产地、气候、采收时间等因素影响,2015版 《中国药典》 以白花前胡甲素、白花前胡乙素为含有量测定指项标。现有前胡指纹图谱研究使用 HPLC 法建立6 个共有峰[5],缺少对其化学成分的综合评价及多指标含有量测定的研究方法。近年来由于超高效液相色谱-飞行时间质谱(UPLC-Q-TOF/MS)具有高分离能力和高分辨质谱的鉴定能力,而广泛用于中药成分分析与鉴定[6-7]。本实验收集传统药材产区和新兴药材产区的前胡药材,进行指纹图谱研究和多共有成分含有量测定,为前胡的质量评价提供更全面、科学的依据。
1 仪器与材料
岛津LC-2010AHT 高效液相色谱仪(日本岛津公司);TP040S 超声波清洗设备(深圳洁梦清洗设备有限公司);AB204 电子天平(瑞士梅特勒托利多公司);Agilent 1260 UPLC-6530Q-TOF/MS仪,配置电喷雾离子源、MassHunter 5.0 工作站、PCDL B.03.01 数据库(美国 Agilent 公司)。甲醇(美国Tedia 公司);纯净水(杭州娃哈哈集团有限公司)。白花前胡甲素(ps0422-0020-ps000114,含有量≥98.5%)、白花前胡乙素(ps0422-0020-ps000116,含有量 ≥ 98.5%)、白花前胡E素(ps0423-0020-ps001175,含有量≥98.5%)对照品购于成都普思生物有限公司。
前胡药材均为 1年生,2017年采集,由广州深圳市和顺堂医药有限公司等提供,23 批药材经江苏省中科院植物研究所徐增莱研究员鉴定为正品。信息见表1。
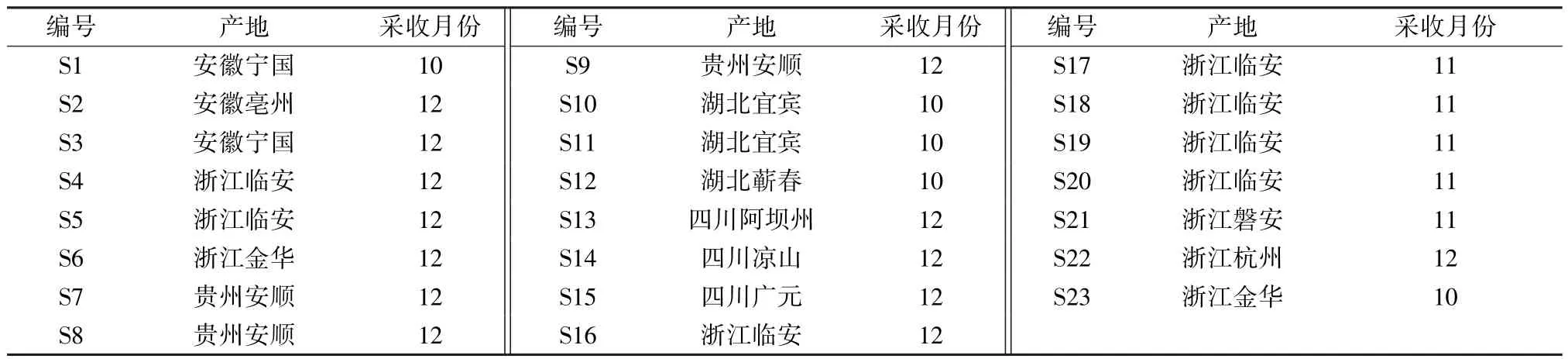
表1 样品信息Tab.1 Information of samples
2 方法与结果
2.1 色谱条件
2.1.1 UPLC-Q-TOF/MS 定性 分析 ZORBAX Eclipse plus C18色谱柱(250 mm×4.6 mm,5 μm);流动相甲醇(A)-水(B),梯度洗脱(0~15 min,40%A;15~16 min,40%~60% A;16~36 min,60%A;36~56 min,60%~100% A;56~60 min,100%A);柱温 30 ℃;体积流量 1 mL/min;检测波长270 nm。电喷雾离子源(ESI),正离子模式;扫描范围m/z100~1 500;毛细管电压3 500 V;碎裂电压 170 V;干燥气(N2)体积流量 10 L/min;干燥气温度350 ℃;雾化气压力344.75 kPa;碰撞诱导解离(CID)能量 35 eV;碰撞气 N2。实验数据采用 Masshunter Qualitative Analysis(B.05.00)分析软件和 PCDL Manager(B.03.0l)处理。
2.1.2 HPLC-DAD 定量分析 0~10 min,10%~20%A;10~36 min,20%~70% A;36~46 min,75%A;柱温 30 ℃;体积流量 1 mL/min;检测波长320 nm。
2.2 溶液制备
2.2.1 对照品溶液制备 分别精密称取白花前胡甲素、白花前胡乙素、白花前胡 E 素 0.525、0.250、0.350 mg,置于 1 mL 量瓶,用 100% 甲醇溶解,定容,摇匀,即得混合对照品溶液。
2.2.2 供试品溶液制备 白花前胡干燥根打粉,取粉末(过3 号筛)约1.0 g,精密称定,置具塞锥形瓶中,精密加入100%甲醇10 mL,超声(功率 250 W,频率40 kHz)处理10 min,补足减失质量,过 0.45 μm 微孔滤膜,即得。
2.3 方法学考察
2.3.1 精密度试验 精密吸取同一供试品(S1)溶液,在 “2.1”项条件下分别在相同的仪器上重现6 次,各主要色谱峰相对保留时间的RSD 均小于0.3%,相对峰面积的RSD 均小于2.0%,表明该仪器精密度良好。
2.3.2 稳定性试验 取同一供试品(S1)溶液,在 “2.1”项色谱条件下,于制备后 0、2、4、8、12、24 h 进样测定,各主要色谱峰相对保留时间的RSD 均小于1.0%,相对峰面积的RSD 均小于2.0%,表明该方法稳定性良好。
2.3.3 重复性试验 取同一批药材(S1)6 份,按 “2.3”项下方法制备供试品溶液,在 “2.1”条件下平行进样6 次,各主要色谱峰相对保留时间的RSD 均小于1.0%,相对峰面积的RSD 均小于2.0%,表明该方法重复性良好。
2.3.4 线性关系考察 将混合对照品溶液按照2倍稀释法,共稀释4 次,得到不同质量浓度的混合对照品溶液,在 “2.1.2”项条件下,以对照品溶液的质量浓度为横坐标(X),峰面积积分值为纵坐标(Y)进行回归,结果见表2。
2.3.5 加样回收率试验 精密称取已测定含有量的同一批药材(S1)6 份,每份 0.5 g,分别加入相当于0.5 g 药材含有量的对照品,按 “2.2.2”项下方法制备供试品溶液,在 “2.1”项色谱条件下进样,计算回收率。测得白花前胡甲素、白花前胡乙素、白花前胡 E 素的平均回收率分别为101.2%、99.7%、96.8%,RSD 分 别 为 1.3%、1.4%、1.7%。
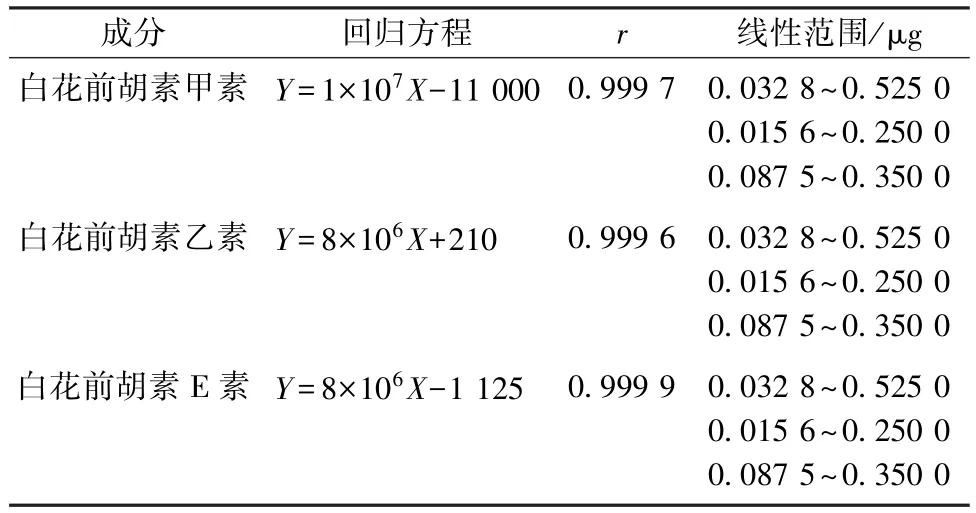
表2 各成分线性关系Tab.2 Linear relationships of various constituents
2.4 指纹图谱建立
2.4.1 色谱峰归属 白花前胡 23 批药材按“2.3”项下方法制备试品溶液,在 “2.1”项色谱条件下进样,记录UPLC 图,用 “中药色谱指纹图谱相似度评价系统”(2004A版)进行分析,得到白花前胡的UPLC 对照指纹图谱见图1,其中共有峰23 个。
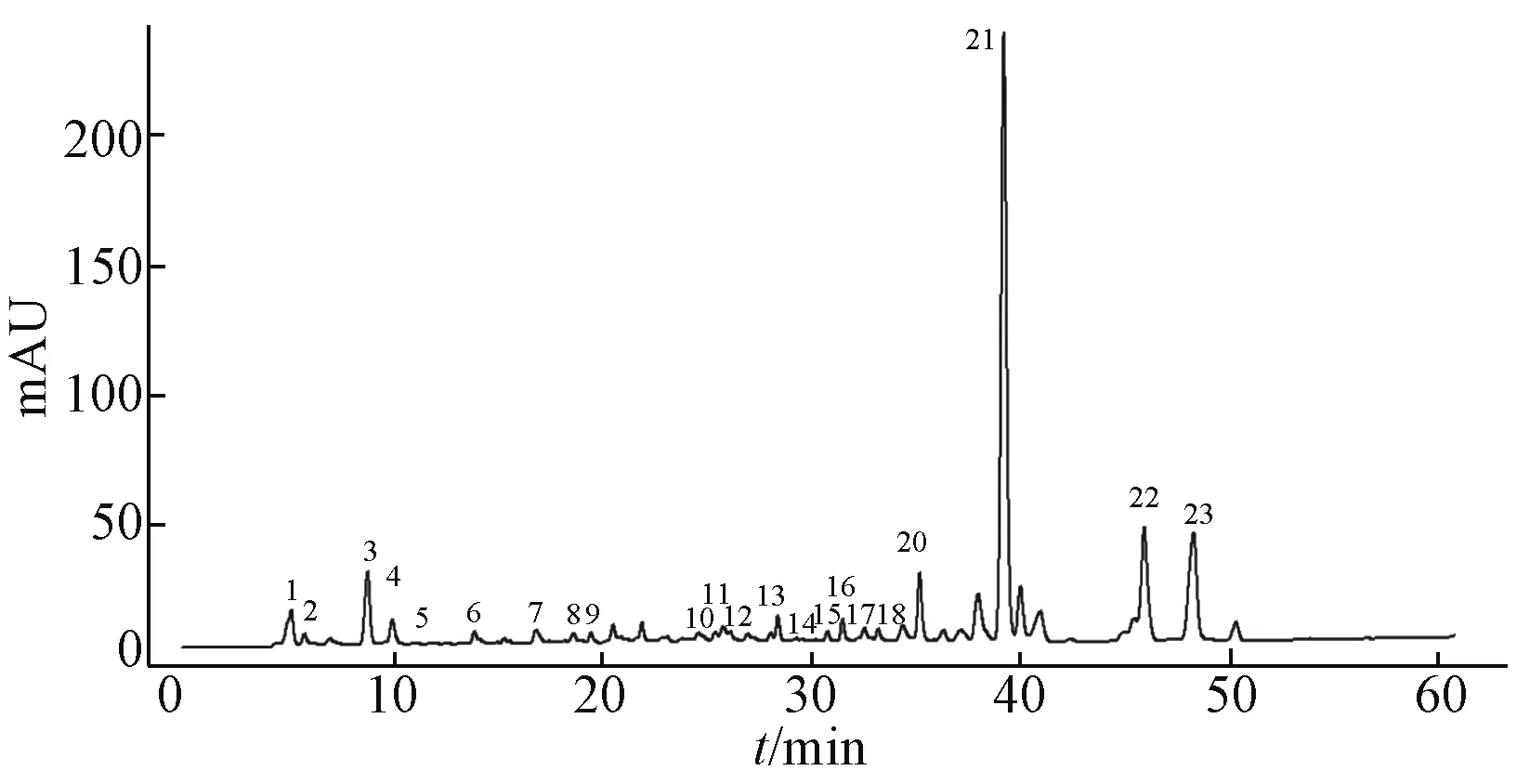
图1 白花前胡对照指纹图谱Fig.1 HPLC reference spectrum of P.Praeruptorum
2.4.2 相似度分析 按照2015版 《中国药典》中前胡含有量测定的方法对S1 样品进行测量,结果显示白花前胡甲素、白花前胡乙素含有量均高于药典规定的最低数值,故以S1 为参照图谱,统计23 批样品图谱的相似度,见图2。23 批药材图谱与参照图谱的平均相似度依次为0.958、0.958、0.970、0.986、0.960、0.987、0.959、0.991、0.965、0.963、0.946、0.960、0.139、0.911、0.963、0.911、0.972、0.953、0.977、0.966、0.956、0.958,结果相似度大多都在 0.9,且只有1 个低于0.9,表明23 批药材相似度良好。
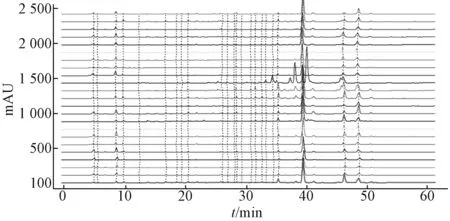
图2 23 批白花前胡HPLC 指纹图谱Fig.2 HPLC fingerprints of twenty-three batches of P.Praeruptorum
2.4.3 前胡共有峰鉴定 在 “2.1”项条件下进样检测,通过各化合物的准分子离子峰确定其分子式,进一步通过质谱碎片,结合文献报道[8-16]和对照品对前胡成分进行结构推测和验证,从前胡共有峰中鉴定出20 个化合物,结果见图3、表3。

图3 前胡饮片基峰图Fig.3 Base peak ion chromatogram of P.Praeruptorum decoction pieces
2.5 比较不同产地前胡质量统计23 批白花前胡药材的指纹图谱共有峰的峰面积,见图4。将23 批药材 按 “2.3”项下方法制备试品溶液,在“2.1.2”项色谱条件下进样,结果见表4。显示不同产地的白花前胡中的白花前胡甲素、白花前胡乙素、白花前胡E 素含有量有明显差异。

图4 23 批样品共有峰峰面积三维条形图Fig.4 3-D bar chart of the peak area of common peaks of twenty-three batches of samples
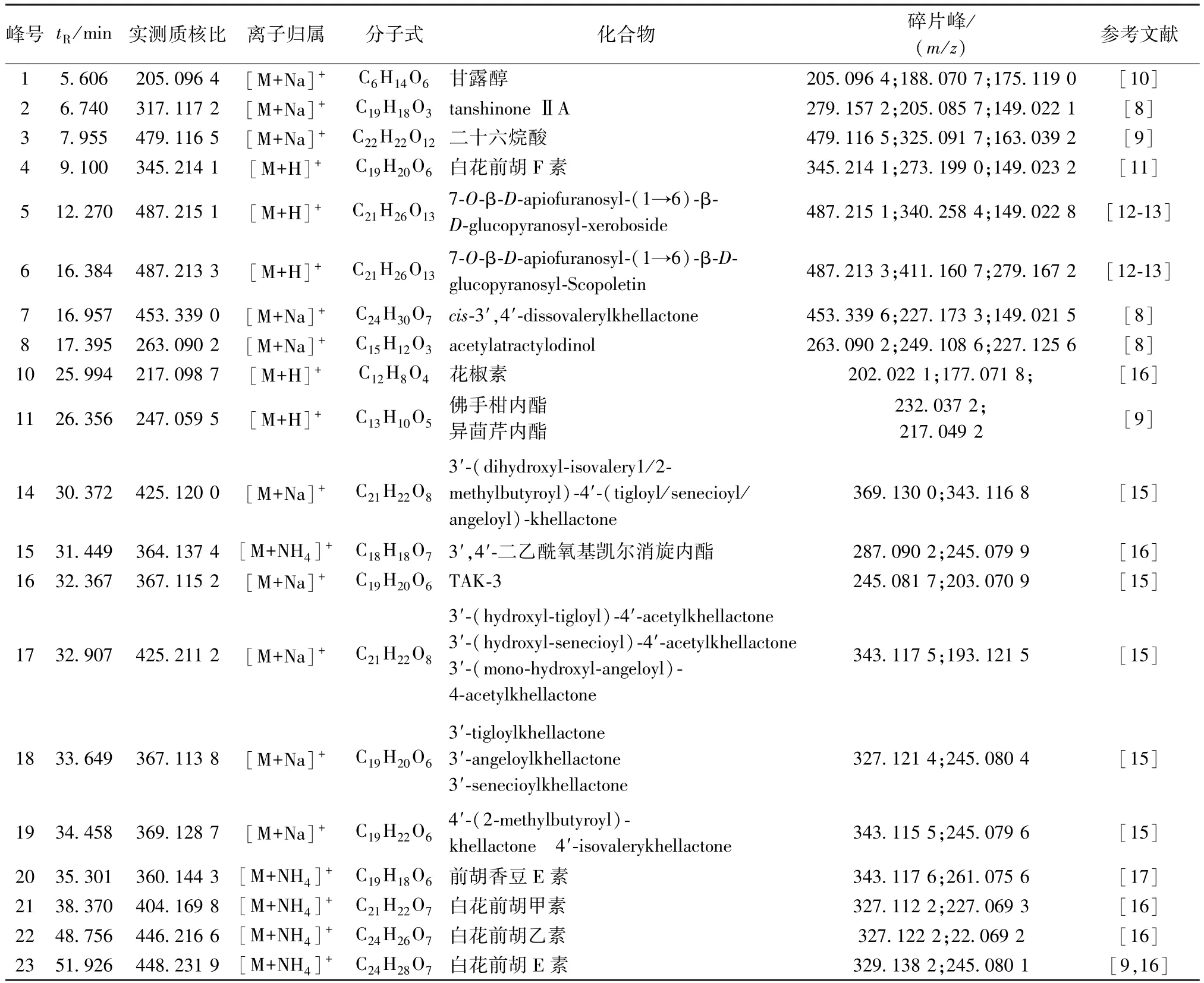
表3 前胡化学成分鉴定Tab.3 Identification of chemical constituents from P.Praeruptorum
对不同产地的前胡药材进行收集和含有量测定,23 批样品所含的白花前胡甲素、白花前胡乙素、白花前胡 E 素含有量的 RSD 值分别为47.527%、134.056%、46.814%,表明不同产地的白花前胡药材所含3种香豆素类化合物的含有量存在显著差异。除S15 样品的前胡外,其他地区的药材白花前胡甲素大于白花前胡乙素的含有量。
图4、表4显示,11月份采收品 S16、S17、S19、S21 白花前胡乙素含有量低于白花前胡E 素,S18、S20 中相反;12月份采收品 S2-S9、S13-S16、S22 中白花前胡乙素含有量小于白花前胡E 素的含有量。
产地为湖北的前胡药材(S10-S12)的3种香豆素类化合物的含有量相差不大,但其3种香豆素类化合物的含有量偏少,而产地为贵州的前胡药材(S7-S9)的3种香豆素类化合物的含有量相差不大且其含有量均高于湖北的前胡药材(S10-S12)。
3 讨论
3.1 提取条件考察 研究中分别采用甲醇、三氯甲烷、乙醇、50%乙醇、水超声提取,采用甲醇溶液溶解,并采用超声仪超声10 min,色谱峰量多,峰面积大,且该方法提取方便,操作简单,重复性好。
3.2 波长选择 本实验比较 220、270、322、350 nm处的色谱图,结果表明270 nm 处前胡药材色谱峰信息最全,特征性最强,故选择270 nm 波长为指纹图谱检测波长。在320 nm 处3种待测香豆素成分的紫外吸收度最强,故选择320 nm 波长进行含有量测定。
3.3 结果分析 本实验采用甲醇超声提取,反相色谱柱分离,主要针对中等及大极性成分进行定性、定量分析,对前胡药材的质量研究也偏向于极性化合物,后续研究将建立对前胡脂溶性成分的分析方法,更全面地对前胡药材质量进行研究。同时,本实验对前胡药材3种香豆类成分的含有量测定发现,贵州产的前胡药材质量稳定且3种香豆素类化合物的含有量高。另外,指纹图谱相似度显示,除S14 药材外其他前胡药材相似度达到0.9 以上,且在叠加指纹图谱中发现S14 药材的指纹图谱与其他药材的存在明显差异,可能与种植地的栽培方法、土壤环境、地势等有关系,后续将对四川凉山地区不同环境下生产前胡的化学成分进行进一步研究。同时对23 个共有峰进行进行结构推测,而针对其中3种共有成分白花前胡甲素、白花前胡乙素、白花前胡E 素的含有量测定结果显示,不同产地药材存在显著差异。为进一步全面反映药材质量,后续研究还应增加共有成分的定量指标,为全面评价中药质量提供了可行的方法。

表4 各成分含有量测定结果(%)Tab.4 Results of content determination of various constituents(%)
致谢感谢药材提供单位深圳市和顺本草药业有限公司、浙江省药检院、江苏华宏药业有限公司、南京食品药品监督院、徐州食品药品监督中心、南京中医药大学附属医院。

