骨髓间充质干细胞与软骨细胞体外构建软骨的比较研究
何爱娟 张天宇
(复旦大学附属眼耳鼻喉科医院眼耳鼻整形外科 上海 200031)
软骨细胞是软骨组织工程最成熟的种子细胞[1-2],但来源不足、供区软骨缺损、去分化[3-5]等问题,限制了其临床应用范围。与软骨细胞不同的是,骨髓间充质干细胞(bone marrow mesenchymal stem cells, BMSCs)具有来源丰富、可大量扩增、成软骨能力强等优势[6-8],因此是软骨组织工程的理想种子细胞。
前期研究已证实:在关节微环境中,应用自体BMSCs复合聚羟基乙酸/聚乳酸(polyglycolic acid/polylactic acid,PGA/PLA)可成功修复大动物关节软骨与骨复合缺损[8-9];而在皮下微环境中,BMSCs极易发生血管化、骨化[10-11],难以获得理想的软骨再生效果。进一步研究发现,通过充分的体外软骨定向诱导可以有效解决这一问题。由此可见,体外软骨构建对BMSCs的软骨再生稳定性十分重要(皮下环境)。然而,BMSCs体外构建的软骨组织在形态、结构和生化组成上能否达到软骨细胞体外构建软骨水平?其与软骨细胞的体外软骨形成规律是否有差异?这些与临床转化密切相关的问题目前尚未明确。而阐明这些对BMSCs的临床应用十分重要,因为明确软骨形成规律是把握体外诱导时间及体内回植时机的关键;明确软骨形成质量是决定BMSCs能否应用于临床的前提。
为了阐明上述问题,本研究分别将猪的BMSCs及软骨细胞复合PGA/PLA支架后进行体外软骨构建,前者为实验组,后者为对照组。体外构建2、4及8周后,取材检测各组的大体、组织学、组织化学及细胞外基质含量,评估各组的软骨形成规律和形成质量,明确BMSCs与软骨细胞体外构建软骨的异同,为BMSCs的临床应用提供理论依据。
1 材料与方法
1.1 主要试剂 高糖DMEM培养液、低糖DMEM培养液、胎牛血清(fetal bovine serum,FBS)、胰酶、三抗(Hyclone公司,美国)、地塞米松、胰岛素、牛血清白蛋白、L-谷氨酰胺、维生素C、番红O染料(Sigma公司,美国)、转化生长因子-β1(transforming growth factor-β1,TGF-β1)、胰岛素样生长因子(insulin-like growth factor-1,IGF-1)、碱性成纤维细胞生长因子(basic fibroblast growth factor, b-FGF)、胰岛素转铁蛋白亚硒酸(insulin-transferrin-sodium,ITS;R&D公司,美国)、聚羟基乙酸(project of global access,PGA;国睿生命科技有限公司,中国)。
1.2 实验方法
1.2.1 实验动物 5月龄巴马香猪3只,体重20 kg,雌雄不限(上海甲干生物科技有限公司)。
1.2.2 猪BMSCs的分离培养 每只实验动物抽取10 mL骨髓,参照全骨髓培养法进行BMSCs的分离培养[12]。以含10%FBS、10 ng/mL b-FGF的DMEM低糖培养液培养,5 d后首次换液,待细胞生长近70%~80%汇合时按1×104个/ cm2传代培养,收集第2代细胞用于后续实验。
1.2.3 软骨细胞的分离培养 无菌获取相同个体猪的部分耳郭软骨,随后按照前期建立的软骨细胞分离培养方法[13],分离获取软骨细胞,以含10%FBS、10 ng/mL b-FGF的DMEM高糖培养液(普通培养液)培养。待细胞生长近80%~90%汇合时可行传代培养,收集第2代细胞备后续实验用。
1.2.4 PGA/PLA支架材料制备 无纺的15 mg PGA均匀放入直径10 mm的模具中压制成圆柱状,加入0.5%PLA定型,制备成直径10 mm、厚度1.5 mm的圆柱体支架材料[13],灭菌后备接种细胞用(图1A)。
1.2.5 细胞接种及成软骨诱导培养 细胞体外扩增到第2代时,用倒置相差显微镜下观察其细胞状态,初步评估细胞功能。随后分别收集第2代BMSCs及软骨细胞,以普通培养液将细胞重悬成100×106个细胞/mL的细胞悬液,将后者接种于PGA/PLA支架材料上(图1B),孵育4 h后,以成软骨诱导液培养(含0.3 g/LL-谷氨酰胺、0.05 g/L抗坏血酸、3.7 g/L碳酸氢钠、10万U/L青霉素钾、0.1 g/L硫酸链霉素、10 ng/mL TGF-β1、100 ng/mL IGF-I、1%ITS、40 ng/mL地塞米松的高糖DMEM培养液)。软骨细胞-PGA/PLA组为对照组,BMSCs/PGA组为实验组。实验组及对照组均经体外培养2、4、8周后取样行相关检测。
1.2.6 细胞在材料上的基质分泌情况检测 细胞材料复合物体外培养2、4周时,每组各取3个样本于倒置相差显微镜下观察细胞在材料上的黏附及基质分泌情况。
1.2.7 构建软骨的大体观察、组织学检测 细胞材料复合物体外培养4、8周时,每组各取3个样本进行大体观察和组织学检测。苏木素-伊红染色观察组织细胞形态;番红O染色观察细胞外基质中GAG的合成和分泌情况;Ⅱ型胶原免疫组化观察细胞Ⅱ胶原蛋白的合成和分泌情况,具体实验方法参见前期建立的检测体系[14-15]。
1.2.8 构建软骨的定量检测 细胞材料复合物体外培养4、8周时,每组各取5个样本进行湿重、GAG、Ⅱ型胶原等定量测定。阿利辛兰法测定样本的GAG含量;ELISA法测定样本的Ⅱ型胶原含量,具体实验方法参见前期建立的检测体系[14-15]。
1.3 统计学处理 应用SPSS 11.5软件分析数据。行t检验分析定量数据的组间差异,结果用均数±标准差表示,以P<0.05 为差异有统计学意义。
2 结果
2.1 细胞形态及功能 细胞形态是细胞功能的重要体现。从图1C、D上可见,扩增到第2代的软骨细胞呈多角形或长梭形,未见明显老化现象,间接说明其细胞功能保持尚可;而扩增到第2代的BMSCs则以多角形细胞为主,细胞有较多角状突起,增殖也较快,说明细胞活性好。
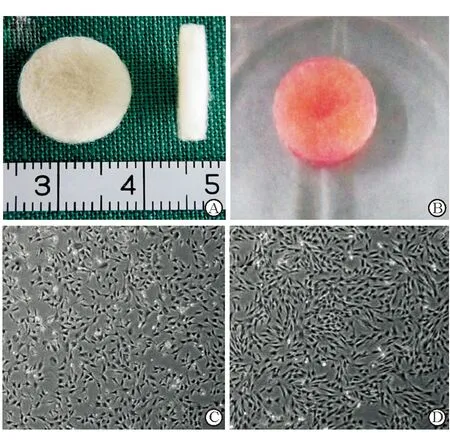
图1. 细胞及支架材料 A.扩增到第2代的BMSCs;B.同一个体的耳软骨细胞(第2代细胞);C.PGA/PLA支架材料;D.细胞/材料复合物
2.2 细胞在直接材料上的基质分泌情况 体外培养2周时,BMSCs在支架材料上的基质分泌厚度显著低于软骨细胞组,但诱导到4周时,BMSCs的基质厚度及材料的基质包裹情况与软骨细胞组十分接近(图2)。这些结果说明,BMSCs在体外成软骨诱导的早期,基质分泌能力明显低于软骨细胞,但随着诱导时间的延长,基质分泌能力明显提高,4周时BMSCs的基质分泌能力基本能达到软骨细胞水平。
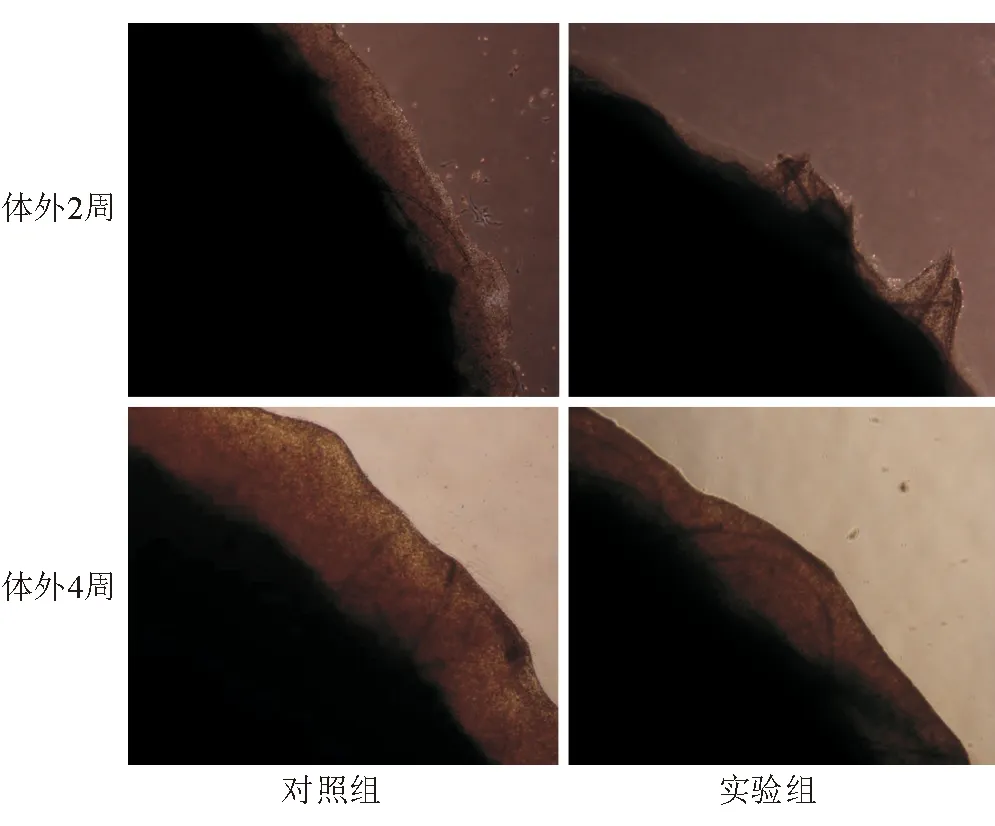
图2. 细胞在PGA/PLA支架材料上的基质分泌情况 体外构建2周时,实验组的细胞外基质厚度及其包裹材料程度低于对照组;4周时实验组的细胞外基质厚度及其包裹材料程度与对照组未见明显差异
2.3 体外软骨形成大体观及湿重检测 体外软骨构建4周时,实验组和对照组均形成了瓷白色的软骨样组织,但大体观上可见实验组的厚度及致密程度较对照组低(图3),湿重检测进一步说明了这一点(图4A),诱导到8周时,2组均形成了表面光滑、瓷白色的软骨样组织(图3),且湿重已无明显差别(图4A)。这些结果说明随着诱导时间的延长,BMSCs的软骨形成逐渐趋于成熟。
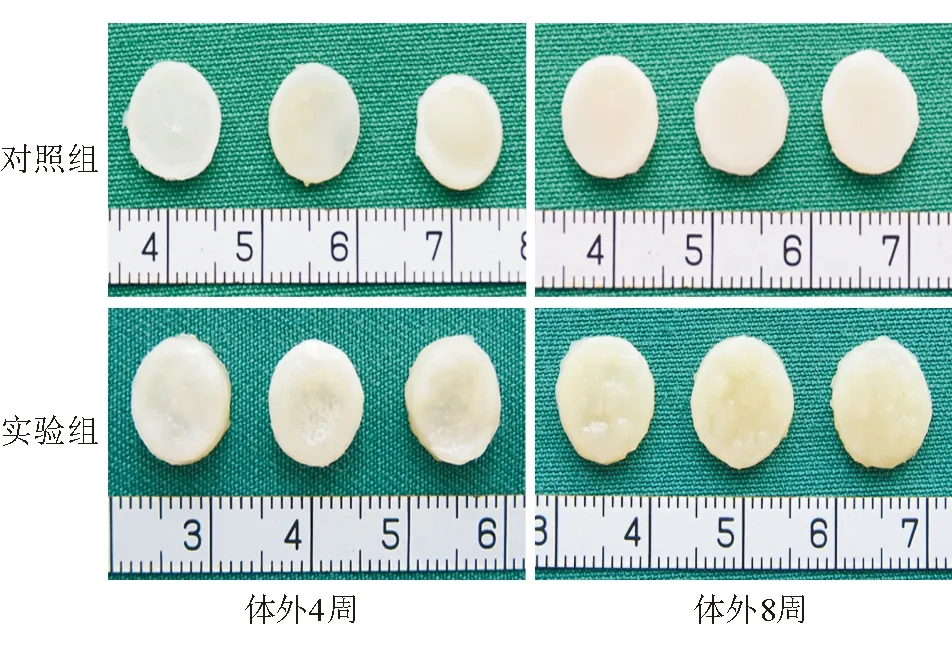
图3. 体外软骨形成大体观 体外构建4周时,实验组和对照组均形成了瓷白色的软骨样组织,外观上看,前者的厚实度略低于后者;体外8周时,两者均形成了厚实、均质的软骨样组织,二者在大体观上未见明显差异

图4. 体外软骨形成的相关定量检测 体外4周时实验组的湿重、GAG及Ⅱ胶原含量均低于对照组;而体外培养到8周时,BMSCs体外构建的软骨湿重、GAG及Ⅱ胶原含量基本上达到了软骨细胞组的水平。有相同字母的柱状图表示差异无统计学意义,无相同字母的表示差异有统计学意义
2.4 体外软骨形成组织学及定量检测 诱导4周后,2组苏木素-伊红染色均观察到明显的软骨陷窝结构,陷窝周围均有蓝染的细胞外基质沉积,番红O染色及Ⅱ型胶原染色均呈阳性。但实验组的软骨陷窝数量较软骨组少,细胞外基质的蓝染程度、番红O和Ⅱ胶原的着色程度也明显浅于对照组(图5)。这些结果说明体外诱导4周后,BMSCs已初步形成软骨样组织,但其成熟度明显低于对照组。诱导8周,实验组的软骨陷窝数量明显增多,陷窝周围基质的蓝染程度、番红O和Ⅱ型胶原的着色程度均较4周时加深,且与对照组未观察到明显差异(图5)。Ⅱ型胶原及GAG定量检测进一步验证了组织学的检测结果(图4B、C)。所有这些结果说明,体外软骨定向诱导8周后BMSCs基本上形成了成熟的软骨组织,同时也说明通过延长体外诱导时间可显著缩小BMSCs构建软骨与软骨细胞构建软骨在组织结构及生化组成上的差异。
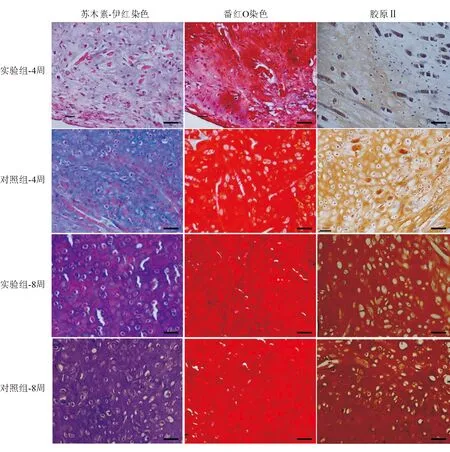
图5. 体外软骨形成的相关组织学检测 体外4周时实验组和对照组均有软骨陷窝形成,番红O染色及Ⅱ型胶原免疫组化染色均呈阳性,但实验组的陷窝数量较软骨组少,细胞外基质的蓝染程度、番红O和Ⅱ型胶原的着色程度也浅于对照组。诱导8周后,实验组的软骨陷窝数量及陷窝周围基质的蓝染程度、番红O和Ⅱ型胶原的着色程度明显增高,且与对照组十分接近
3 讨论
BMSCs是软骨组织工程最有应用前景的种子细胞之一[6, 8]。尽管基于BMSCs的软骨组织工程修复技术已在动物体内取得较大成功[8-9],但其临床转化尚未获得重要突破[16]。主要原因在于与临床转化密切相关的一些问题尚未明确。如:BMSCs的体外软骨形成规律如何?其软骨形成规律与目前最成熟稳定的软骨再生模式——软骨细胞体外构建软骨是否有差异?如果存在差异,那么这些差异能否通过延长体外诱导时间、优化诱导条件等缩小?BMSCs体外构建的软骨最终能否达到软骨细胞体外构建软骨的水平?本实验结果提示,BMSCs体外构建软骨在4周时软骨初步形成,8周时软骨基本成熟;BMSCs的体外三维软骨形成规律与软骨细胞的软骨形成确实存在差异,但随着诱导时间的延长,这种差异逐渐减少直至消失。
然而是什么原因导致上述差异从有到无的变化过程?本研究结果表明,在软骨形成早期即体外软骨定向诱导2周左右时,倒置显微镜下观察到软骨细胞的细胞外基质分泌较BMSCs的基质分泌明显旺盛,但随着诱导时间的延长,基质分泌差异逐渐减小。诱导满4周后二者的基质分泌在倒置显微镜下已无明显差别。虽然镜下基质分泌情况差异不明显,但组织学上仍可观察到BMSCs组形成的软骨陷窝数量明显少于软骨细胞组;软骨特异性细胞外基质GAG和Ⅱ型胶原的定性、定量检测更是提示了BMSC组的细胞外基质含量明显低于软骨细胞组。这说明在诱导早期,BMSCs构建的软骨成熟度显著低于软骨细胞组。这种差异可能是由于诱导早期BMSCs尚未转化成为软骨样细胞,因此细胞外基质的分泌能力仍较低;而软骨细胞是成熟的终末分化细胞,无需经诱导分化就具有分泌软骨特异蛋白多糖和Ⅱ型胶原蛋白的能力。诱导到8周时,实验组和对照组均形成了瓷白色的软骨样组织,组织学、免疫组织化学及特异性细胞外基质的定量测定结果显示,此2种细胞所构建的组织工程软骨在形态、结构及生化组成上已无明显差别。这可能是由于这时候的BMSCs已经完全转化成为较为成熟的软骨样细胞,可大量分泌软骨特异细胞外基质,从而使二者的差异显著缩小,甚至消失。
尽管在诱导早期,BMSCs的软骨形成较软骨细胞慢,但通过延长诱导时间二者的差异显著缩小,诱导超过8周时,BMSCs构建的软骨与软骨细胞构建的软骨并无显著差异。这些结果为BMSC的临床应用转化提供了有利的理论依据。此外,课题组前期研究表明:应用未经体外软骨定向诱导的BMSC-PGA/PLA复合物虽可实现大动物体内关节软骨缺损修复,但其成功率低[16]。Angele等[17]将未经体外成软骨诱导的兔BMSCs与人工材料复合后植入裸鼠的皮下和背部肌肉内,3周后植入物出现了骨样组织形成(软骨再生失败)。这些结果说明,对BMSCs而言,单纯依靠体内微环境构建软骨的结果极不稳定。而课题组另一研究表明,将BMSCs复合支架材料体外成软骨诱导8~12周后再植入裸鼠皮下,则可获得稳定的软骨再生效果[10]。这些结果提示,要应用BMSCs修复整形外科中常见的软骨缺损,进行充分的体外软骨定向诱导和构建十分重要而且必要。
总之,本研究证明BMSCs体外构建软骨随诱导时间的延长逐渐趋于成熟,其体外构建软骨在组织结构和生化组成上能达到软骨细胞体外构建软骨的水平。这为BMSC的临床应用提供了有利的实验依据。但关于BMSC体外构建组织工程软骨的体内长期转归、体内应用稳定性等相关问题尚需进一步研究。

