应用荧光成像技术研究磷酸铝凝胶在小鼠胃肠道中的分布
苏日娜,樊万君,姚 静
中国药科大学 药学院,南京 210009
磷酸铝凝胶是一种抗酸剂,能中和胃酸,使胃内pH升高,从而缓解胃酸过多引起的反酸、十二指肠溃疡等症状。凝胶剂中的磷酸铝能形成胶体保护性薄膜,从而隔离并保护损伤组织。有报道称,选择胶体次枸橼酸铋为对照品、128名患者的临床治疗研究显示,磷酸铝凝胶能提高胃内pH值至3,胃肠道副作用少,成功缓解胃痛、反酸、烧心的案例所占比分别为90.7%、94.2%和89.7%,有效缓解各症状总比率为85%[1]。然而,目前国内对于其在胃肠道中的分布研究未见报道。
小动物活体荧光成像技术可以实时、无损、动态地监测标记物在活体小动物体内的分布等[2,3]。相比其他检测药物浓度、组织切片等考察药物分布的方法,荧光成像法更加直观且方便。本实验采用荧光成像技术研究磷酸铝凝胶(洁维乐®)在禁食小鼠的离体胃肠道中的分布情况,为胃肠道分布研究提供新思路。
1 材料与方法
1.1 材料与仪器
磷酸铝凝胶(洁维乐®)购自韩国保宁制药株式会社;深红色碘化物荧光探针DiR购自北京富百科生物技术有限公司;荧光探针菁染料琥珀酰亚胺酯Cy5购自西安瑞禧生物科技有限公司;水合氯醛购自永华化学科技(江苏)有限公司。
VISQUE In Vivo Elite小动物活体成像系统(Korea)用于荧光成像;分析软件为CleVue。
1.2 实验动物
SPF级ICR小白鼠,雄性,体重为25~32 g,由南京市江宁区青龙山动物繁殖场提供,许可证号SCXK(苏)2017-0001。实验前小鼠禁食 15 h(自由饮水)。实验过程中对小鼠的处置按照《实验动物管理条例》的相关规定进行,符合动物伦理学。
1.3 洁维乐标记物制备
根据洁维乐说明书,口服用量为一次20~40g凝胶,换算成小鼠灌胃等效剂量为2.5999~5.1997g·kg-1。
根据小鼠体重,精密称取5.1997g·kg-1洁维乐至1mL注射器中,在避光条件下精密加入300 μg·kg-1Cy5(2 mg·mL-1的 DMSO 溶液)或 DiR(10 mg·mL-1的DMSO溶液),与洁维乐混匀即得洁维乐标记物。
1.4 荧光探针的筛选
取禁食小鼠4只,称重,随机分为2组(n=2),分别灌胃给予洁维乐DiR标记物和洁维乐Cy5标记物,计时。在灌胃后24 h麻醉小鼠,分别进行小鼠在体荧光成像;随后立即处死,分别打开腹腔后、取出胃肠道进行荧光成像。荧光成像参数为:DiR组激发波长为740~790带通,发射波长为810~860 nm长通,曝光时间1 s;Cy5组激发波长为630~680带通,发射波长为690~740nm长通,曝光时间1s。
1.5 考察洁维乐Cy5标记物在小鼠离体胃肠道中的荧光成像情况
取禁食小鼠30只,称重,随机分为6组(n=5),灌胃给予洁维乐Cy5标记物,计时。以非标记给药组为平行对照, 在灌胃后于 0.5、2、4、8、12、24 h 处死小鼠,取出胃肠道,采用小动物活体成像系统进行荧光成像,荧光成像参数同“1.4”项Cy5组。
1.6 考察洁维乐Cy5标记物在小鼠其他器官(心脾肝肾肺)中的分布情况
禁食小鼠灌胃给予洁维乐Cy5标记物在各个时间点进行胃肠道荧光成像后,同时取出小鼠的其他器官(心脾肝肾肺),采用小动物活体成像系统在相同条件下进行荧光成像。
2 实验结果
2.1 荧光探针的筛选
分别灌胃给予洁维乐DiR标记物和洁维乐Cy5标记物的两组小鼠,在24 h时观察在体、开腹腔和离体胃肠道荧光成像情况,见图1。
实验结果显示,由于成像深度有限[4],在考察限度下,两组均未观察到小鼠在体荧光成像情况;而洁维乐Cy5标记物组可更明显观察到小鼠开腹腔及离体胃肠道中的荧光成像,故选择Cy5作为荧光探针。
2.2 考察洁维乐Cy5标记物在小鼠离体胃肠道中的荧光成像情况

图1 DiR和Cy5洁维乐标记物分别灌胃给药小鼠在24h时的荧光成像图
灌胃洁维乐Cy5标记物和平行对照组的小鼠在不同时间点的离体胃肠道荧光成像情况,见图2。

图2 灌胃Cy5洁维乐标记物的小鼠在不同时间点的离体胃肠道荧光成像图(n=5)
荧光标尺从蓝色至红色代表荧光信号由弱至强。实验结果显示,0.5h时洁维乐Cy5标记物已进入肠道内,2h开始进入盲肠和结肠,表明洁维乐在2 h可分布至胃肠道各部位,此后胃、小肠红色荧光信号开始变弱,4 h开始盲肠和结肠呈现强烈红色荧光信号,8 h后盲肠和结肠红色荧光信号减弱,24 h时各部位荧光信号均降至最弱。胃内荧光信号随时间的延长呈减弱趋势,在0.5 h呈强烈红色荧光信号,24 h呈蓝色弱信号或基本无信号;盲肠及结肠内荧光在0.5 h几乎没有荧光信号,随后呈现先增强为红色强烈荧光信号、而后减弱。
将小鼠离体胃肠道荧光成像图作进一步分析,采用分析软件Clevue计算各部位平均荧光强度,绘制胃肠道各部位(胃、小肠、盲肠、结肠)的荧光强度-时间曲线图(见图3)及堆积百分图(见图4)。

图3 灌胃Cy5洁维乐标记物的小鼠胃肠道(胃、小肠、盲肠、结肠)内荧光强度-时间曲线图*P<0.05,**P<0.01
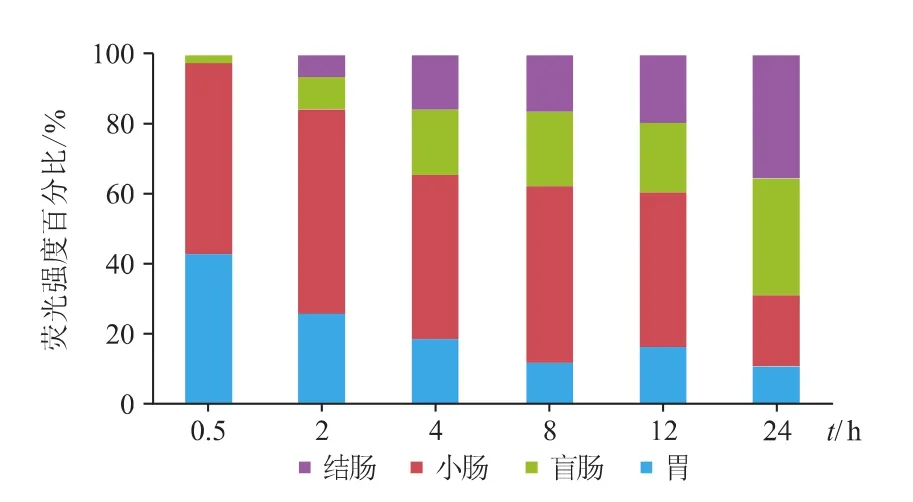
图4 灌胃Cy5洁维乐标记物的小鼠胃肠道(胃、小肠、盲肠、结肠)内荧光强度堆积百分比-时间图
从图3可知,洁维乐Cy5标记物的小鼠胃内荧光强度曲线显示,随着时间的延长而呈减弱的趋势,这是由于洁维乐Cy5标记物灌胃后达到最大量并逐渐进入肠道,因而呈减弱趋势;小肠内荧光强度曲线则是0.5h即显示较大荧光强度,且在0.5~2h点持续增强,而2 h后开始逐渐减弱,可以表明洁维乐Cy5标记物在0.5 h已经开始进入肠道,且前2 h持续推进至肠道内分布,而2 h后逐渐进入盲肠和结肠处,从而呈减弱趋势;盲肠和结肠内荧光强度在0.5h时几乎忽略不计,而随着时间的延长呈先增强后减弱,可说明洁维乐Cy5标记物0.5 h还未到达盲肠和结肠,随后持续进入盲肠和结肠而增强,再逐渐排出体外而呈减弱趋势。
图4结果显示,洁维乐Cy5标记物在2 h时基本分布至小鼠胃肠道各部位;0.5 h时,胃及小肠所占分布比率最大,随着时间的延长呈现降低趋势,而盲肠及结肠部位分布比率持续上升,至24 h时主要分布在盲肠及结肠部位然而,在24 h胃肠道各部位仍有不同程度的洁维乐分布。
2.3 考察洁维乐标记物在小鼠其他器官(心脾肝肾肺)中的分布情况
灌胃用Cy5标记的洁维乐小鼠在各个时间点进行荧光成像后,取出小鼠的其他器官(心脾肝肾肺)进行荧光成像。结果显示,灌胃洁维乐Cy5标记物的小鼠其他上述器官内均未见荧光显示,见图5。
3 讨 论
近年来,荧光成像技术在监测肿瘤细胞生长和转移[5]、生物体内特定基因的表达[6]、靶向药物治疗效果评价[7]等方面,具有广泛的应用前景。在口服药物胃肠道分布研究中,小动物活体荧光成像会有生物组织深度限制和各个小鼠胃肠道在腹腔的位置偏差,而对分布研究有所干扰,因此,选择离体胃肠道荧光成像,以避免生物组织深度限制,同时达到直观、实时地观察药物在体内的分布及停留情况。
本研究基于小鼠体重范围在30 g左右而导致洁维乐给药量基本不大于0.2 g,加之灌胃操作时的平行残留量不可避免,最终选择较大的灌胃给药量5.1997g·kg-1,以减小给药偏差。洁维乐为黄白色凝胶,与水及其他溶剂混合变成混悬液,并缓慢沉淀。因此,制备标记物时,先将荧光染料溶于二甲基亚砜配制成高浓度荧光染料母液,再根据小鼠体重精密移取300 μg·kg-1荧光染料母液,并与洁维乐混合,以减小溶剂对凝胶性质的影响,保证洁维乐呈凝胶状态。
本研究应用小动物在体荧光成像系统和荧光染料Cy5成功对磷酸铝凝胶(洁维乐®)在禁食小鼠的胃肠道中的分布进行了可视化示踪,可为考察洁维乐胃肠道分布中提供参考。

图5 灌胃Cy5洁维乐标记物小鼠的其他器官(心脾肝肾肺)在不同时间点的荧光成像图(n=5)

