一种新型氢键与静电力共存的二元高分子复合体系
许小伟,杨曙光
(东华大学 材料科学与工程学院,上海 201620)
通常,高分子复合物形成的驱动力包括氢键作用、静电作用、配位作用、疏水相互作用、电荷转移作用和范特华尔兹作用等[1]。这些高分子复合物体系,提供了一种简单而经济的开发用于合成工业,生态学,生物和医药试剂和材料的途径[2-4]。Lichkus[5]和Chen[6]等报道了PEtOx与PMAA或PAA分子间由于氢键作用形成复合物,且复合体系的玻璃化转变温度随着复合条件不同而发生一定的变化。Matsuda[7]的研究发现当复合体系中PEtOx和PMAA溶液的浓度比改变时,所得的氢键复合物体系存在不同的结构、组成及尺寸。Jamieson[8]等使用动态光散射和黏度测定,研究了羟丙基纤维素和十六烷基三甲基溴化铵在不同配比下的特征黏度变化规律及其与溶液体系中的动力学半径的对应关系。Hu[9]等以紫外光谱和荧光分子探针技术为基础探索了聚甲基丙烯酸与聚(N,N-二乙基丙烯酰胺)在较低pH值下络合体系中的分子链在不同pH值下的构象变化,并据相关数据分析了其络合结构与梯状模型的符合度。Audebert[10]等将荧光分子探针技术与流变仪结合,探索了宏观的流变学特征与微观分子结构之间的对应关系。
我们采用常用的FTIR手段来检测不同酸度值下,PEtOx-EI/PAA复合物体系中官能团的变化情况,及不同基团之间相互作用力。采用静态剪切流变仪来观测不同剪切速率下,均质溶液体系的黏度变化情况。来初步判断不同酸度值下,复合物体系中的作用力及为后续的加工应用提供一定的理论基础。
1 实验
1.1 实验原料

表1 主要药品
1.2 水解过程
由于PEtOx的LCST为60 ℃[11],对其进行水解操作前,需先将其在常温下充分搅拌进行预溶解,以使水解过程中,PEtOx更快处于均质状态。实验采用盐酸溶液加热水解的方法进行PEtOx的水解,称取PEtOx粉末状颗粒2.5 g,置于三口烧瓶中。室温下,加入去离子水23 g,充分搅拌至溶解均匀。
将充分溶解的PEtOx溶液移至温度稳定为100℃的油浴锅中,加入HCl浓溶液(37 %)27 g,并开始计时。控制加热时长分别为1,3,5和6h。当水解时长为设定时长时,停止加热并将烧瓶移出油浴锅。水解过程中,PEtOx的化学变化过程如图1所示。水解后配制NaOH(3M),并使用分液漏斗逐步滴加,直至水解高分子溶液呈中性。

图1 PEtOx水解过程化学变化过程
将上诉水解溶液置于透析袋中,使用去离子水进行透析直至其电导率与去离子水电导率值相近,且6h维持不变。所得纯化的水解产物使用旋转蒸发仪进行浓缩后于冻干机中冷冻干燥后取出,密封并存储于干燥器中,待进一步测试及使用。
1.3 复合体系制备
分别配制PEtOx-EI与PAA的水溶液,控制PEtOx-EI与PAA的浓度为1.0 %,且PEtOx-EI与PAA的物质量比为1∶1([EtOx] + [EI]=[AA])。在配制两组溶液过程时称取NaOH其摩尔量与PAA相比,满足[NaOH]/[AA]=0~1.0,由此溶液配制的混合物被标记为PC-X,如[NaOH〗/[AA]=0.1,则混合物标记为PC-10。分别使用以上方法配制的水溶液进行PEtOx-EI与PAA溶液的配制,将PEtOx-EI逐滴滴加到PAA溶液中,直至两者完全共混。若共混体系出现络合沉淀,则经过静置沉淀,待后续分析检测;若所得共混物为均质溶液体系,则继续搅拌,至体系完全均匀。
2 结果与讨论
2.1 PEtOx水解产物
使用1H NMR(Bruker 600 MHz光谱仪)对产物的HD进行测试,其核磁谱图如图4 (a)所示。对水解度进行计算时,使用公式为:
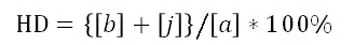

(a:水解时长为3小时时,水解产物的核磁谱图;b:HD与水解时长的对应关系)
图2 水解产物1H NMR谱图及不同水解时长对应的HD变化图
2.2 PEtOx-EI/PAA复合体系
PEtOx-EI分子链上同时存在EtOx与EI链段,EtOx侧链上含有的-C=O基团可作为氢键受体,而EI链段上的-NH基团上的N可作为质子受体。因而在合适的pH值条件下,PEtOx-EI与PAA既可形成氢键,又可形成离子键。不同键的键能不同,则分子间的络合作用力的类型和强度可实现一定调控。为研究这一氢键与静电作用力共存体系中可能存在的作用力类型,本文选用水解时长为3 h的产物为基础,进行复合体系的研究,为便于标记,亦简称PEtOx-EI。
PAA或PMAA与PEtOx及PEI的络合过程具有pH响应性[7,12-13],而作为其无规共聚物的PEtOx也有类似的性质。通常,在PEtOx/PAA共混体系中,当PAA的离子化程度超过10 %时,PEtOx与PAA溶液共混时,两者之间无法形成基于氢键的络合沉淀[14]。而在PEtOx-EI/PAA共混体系中,当PAA的离子化程度达到30 %时,仍可观察到络合沉淀,这意味着分子体系中存在这氢键之外的静电作用力[15]。由不同离子化程度的PAA对应的络合物体系的可见光照片图3可见,当[NaOH]/[AA]=0~0.3时,体系中出现络合沉淀,溶液不均匀。而当体系中[NaOH〗/[AA]=0.4~1.0时,体系为均质透明液体,且具有一定黏度。分析可得,当PAA离子化程度较低时,分子自团聚,分子内形成以-COOH中H为氢键供体,-C=O上的O作为氢键受体的氢键。同时由于体系中含有较多的-COOH,作为氢键供体,可与呈伸展状态的EtOx侧基上的-C=O形成氢键,因此形成络合沉淀。而当体系中PAA的离子化程度较高时,分子链伸展,即使理论上部分-COOH仍可与PEtOx-EI中的-C=O之间形成氢键,但-COOH总量减少,分子间作用力减弱,无络合沉淀生成。随NaOH含量进一步增加,-COOH需部分参与到PEtOx-EI中-NH的质子化过程中,存留的静电作用位点极少,相互作用力进一步减弱,络合物沉淀形成难度进一步增加。
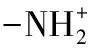

(PEtOx-EI/PAA复合体系配制条件满足[NaOH]/[AA]=0~1.0,并分别标记为PC-X,如[NaOH]/[AA]=0.2的共混体系,标记为PC-20)
图3 (A) PEtOx-EI/PAA复合体系对比图; (B) PAA,PEtOx-EI与P-00,PC-20沉淀及载玻片上沉积的PC-40,PC-60,PC-80和P-100膜的红外光谱图 (2000-1400 cm-1); (C) 不同[NaOH]/[AA]比值的共混溶液黏度随剪切速率的变化规律图
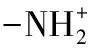

由此分析,红外光谱分析结果与可见光照片所反映的情况相符,当PEtOx-EI与PAA共混体系在较低中和度,如[NaOH]/[AA]=0~0.3时,分子间作用力以氢键络合为主,分子间形成络合沉淀。而当[NaOH]/[AA]= 0.4~1.0时分子间作用力以离子键为主,且离子键强度先逐渐增强。
2.3 PEtOx-EI/PAA复合体系的稳态剪切行为的研究
利用平板流变仪(哈克旋转流变仪,Haake Mars 60)将所得的溶液利用流变仪进行不同剪切速率下溶液黏度变化测试,测试结果如图所示。由图4 (C)可明显看出,在[NaOH]/[AA]=0.4~0.7时,溶液的零剪切黏度逐渐增大。但随着剪切速率增大,该四组组分溶液黏度均有明显降低,表现为明显的非牛顿流体特性[20]。由于较低pH值下PAA分子链均呈现卷曲状态,伸直状态的PEtOx-EI分子链包裹[19]。随着pH的增加,PAA分子链的卷曲状态相对伸展,其动力学半径增加,体系黏度相对增加。而在这一过程中,由于分子间具有明显的氢键和静电作用力的存在,分子间作用力较强。共混溶液表现为明显的剪切变稀流体的流变学特征。

3 结语
水解所得的PEtOx-EI分子链段为EtOx与EI链段无规共聚物,该体系中同时含有氢键受体(EtOx链段上的羰基)和可质子化位点(EI链段上的-NH)。通过控制[NaOH]/[AA]比值,精确的进行了PEtOx-EI/PAA体系的共混条件的控制。在较低[NaOH]/[AA]比值下,PEtOx-EI/PAA之间存在极强的氢键作用力,会直接生成络合沉淀。而当[NaOH]/[AA]比值增加到0.4及以上时,分子间作用力逐渐转变为氢键与静电作用力共存状态。且在静电力作用力逐渐增强的过程中,体系中表现出零剪切黏度逐步增强,静态剪切黏度表现为明显的剪切变稀的非牛顿流体特性。在[NaOH]/[AA]比值大于0.7后,体系中氢键作用力急剧减弱,静电作用力不在增强,黏度转而逐步下降。

