肾下盏解剖结构在输尿管软镜治疗肾下盏结石中的研究进展
谭 军 综述,杨国胜 审校
(1.南方医科大学第二临床医学院,广东 广州 510515;2.广东省第二人民医院泌尿外科,广东 广州 510317)
近年来,由于软性输尿管肾镜治疗肾脏结石具有安全性高、创伤小、结石清除率高、恢复快的特点,目前已成为肾脏2 cm以下结石的首选治疗方式之一。肾下盏是肾结石最常见的好发部位,肾下盏结石在输尿管软镜治疗后的疗效与其他肾盏结石相比较欠佳[1]。国内外临床研究提示,肾下盏结石软镜术前预测、术后疗效与肾下盏的解剖结构有着密不可分的关系。为此,本文旨在回顾近年来国内外相关文献,探讨肾下盏解剖结构对输尿管软镜治疗≤2 cm肾下盏结石疗效的研究进展。
1 肾下盏解剖结构及测量方法
对于肾下盏解剖结构详细而标准的分类,有待进一步研究,在临床工作中,泌尿外科医师常通过肾下盏解剖形态的差异划分为两种类型:单型肾下盏与复杂型肾下盏,前者为肾小盏于肾大盏远端处汇入,与肾盂直接连通;后者则由数个肾小盏融合形成分枝状开口于肾大盏或者多个肾小盏各自直接开口于肾盂。
随着影像学的发展,肾下盏解剖结构的测量方法有三维彩超、静脉肾盂造影、三维重建CT等,但大多数学者及临床医师仍以静脉肾盂造影为主[2],下面将介绍4个相关的肾下盏解剖参数(测量详见图1)。
肾盂肾下盏夹角(infundibulopelvi angle,IPA)是反映肾下盏汇入肾盂的转角,是国内外学者公认对肾下盏结石排空影响最重要的解剖参数。关于IPA的测量,不同学者对IPA的测量方法并不完全一致。SAMPAIO等[3]考虑到肾下盏结石有简单型与复杂型之分,如果存在复杂型肾下盏的结石在肾小盏而不在肾大盏的情况,那么IPA就应为结石所在肾小盏的轴线即线4与上段输尿管中轴线即线2之间的夹角(角A)。ELBAHNASY等[4]认为SAMPAIO所提及的肾小盏轴线并不能较好反映该角度,他们考虑更多的是输尿管软镜进入肾下盏时所需下弯的角度,故他们将IPA定为肾下盏中轴线即线1与上段输尿管中轴线即线2相交而成的夹角(角B)。SABNIS等[5]对IPA的定义为肾下盏方向线即线4与肾盂方向线即线5之间的夹角(角C),但由于该作者测量IPA并未在片子上作出准确的标记,偏差可能较大。我国学者夏明义等[6]认为肾下盏结石能否排入肾盂与上段输尿管轴线无关,而与肾盂轴线关系密切,故他们采取了与SABNIS的测量方法,该方法简便可行,但与SABNIS测量不同的是,他们在其基础上对各条轴线作出详细的测量方法,IPA为肾盂的中轴线即线3与结石所在肾下盏的中轴线即线1相交所构成的夹角(角D),肾盂中轴线为肾上下极内侧缘连线经过肾窦部肾盂的中点与肾盂上下唇中点的连线。尽管国内外学者对IPA角度测量方法各有各的看法,但大体上均反映了肾下盏结石排出所需要克服的转角。
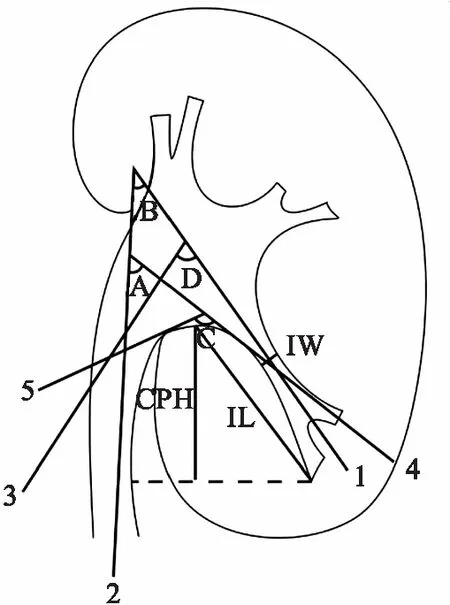
图1 IPA常见的几种测量方法及IW、IL、CPH的测量示意图
IPA:肾盂肾下盏夹角;IW:肾下盏漏斗部宽度;IL:肾下盏漏斗部长度;CPH:肾盂肾盏高度;角A为线2和线4的夹角;角B为线2和线1的夹角;角C为线5和线4的夹角;角D为线3和线1的夹角。
肾下盏漏斗部宽度(infundibular width,IW)和肾下盏漏斗部长度(infundibular length,IL)也是影响肾下盏结石排空的重要解剖参数。目前这两个参数的测量方法争议较少,IW为沿肾下盏中轴线最狭窄处的宽度;IL则为结石所在肾小盏最远端至肾盂下唇中点连线的长度。
其他影响输尿管软镜治疗下盏结石的可疑肾下盏解剖参数如肾盂肾盏高度(the caliceal pelvic height,CPH),其定义为结石所在的肾下盏最低点到肾盂下唇最高点的高度。TUCKEY等[7]认为测量IPA过于复杂,于是提出CPH代替IPA,发现CPH<15 mm时,ESWL治疗肾下盏结石清除率高达92%;但国外关于CPH对软镜治疗肾下盏结石疗效影响的研究尚少,RESORLU[8]首次进行了CPH与软镜治疗肾下盏结石疗效的相关性研究,发现CPH<25 mm时,结石清除率为74.1%,虽然CPH无统计学差异,在结石残余组中CPH值是偏高的;最近的一篇报道,SARI等[9]发现CPH是一个术前预测的指标,CPH≤20.2 mm时手术成功率高。目前国内外研究对于CPH与软镜治疗肾下盏结石疗效影响的结论不一致,但在现有研究中,CPH还是一个比较有前景的预测指标,至于其预测价值有待进一步评估。
2 肾下盏解剖结构在肾下盏结石形成中的作用
泌尿系结石最常见的好发部位是肾脏,约占40%~50%;其中下盏结石据统计约占全部肾脏结石的36%,下盏是最低位,在重力因素的引导下,肾下盏成为了肾脏集合系统中尿液毒素、晶体等物质的聚集地,尤其复杂型的肾下盏,位置低而不易排出,周而复始沉积于此便形成了结石;此外,在GOKALP等[10]的对比研究发现,当具备不利的肾下盏解剖因素时,如肾盂肾下盏夹角过小[11]、肾下盏漏斗部长度过长会促进肾下盏结石的形成。同时,不利的肾下盏解剖因素也增加ESWL术后下盏结石的复发率,谢立平等[12]对纳入的145例肾下盏结石患者行体外冲击波碎石术(extracorporeal shock wave lithotripsy,ESWL)治疗,发现IPA<90°、IL30 mm、IW≤4 mm和复杂型肾下盏不利于ESWL术后结石的排出而导致肾下盏结石复发,反之结石易于排空。
目前肾下盏结石治疗的成功率较为一般,经验丰富的临床医师在术前会通过评估肾盂肾下盏夹角、盏颈宽度、长度等解剖结构及结石大小去选择手术方式及预测术后成功率[4,8,13]。
3 肾下盏解剖结构对肾下盏结石治疗选择的考量
对于直径≤2 cm大小的肾下盏结石,目前已有多种可选的治疗方法包括ESWL、经皮肾镜碎石取石术(percutaneous nephrolithotomy,PNL)以及软性输尿管肾镜碎石术(retrograde intrarenal surgery,RIRS)等。相关研究表明ESWL治疗1~2 cm肾下盏结石的术后排石率约52%~67.7%[14-15],而在ALBALA[14]的随机对比研究中,对成功纳入68例符合标准的肾脏下盏结石患者实施ESWL术,术后当日排石率低至37%,而大于1 cm的肾下盏结石术后的排石率仅为33%。对治疗1~2 cm的肾下盏结石尤其是过度肥胖患者,ESWL的治疗效果不佳,远低于临床诊疗需求。PNL在过去常用于治疗肾下盏结石,其结石清除率高达95%,PNL是通过在B超定位下建立经皮肾通道碎石,有相对高的有创性,虽碎石高效,但与之伴随的各类并发症如术中术后出血、感染等风险高达50%[16-17]。20世纪70年代,外国学者MARSHALL等[18]首次报道输尿管软镜应用于临床,经过半个世纪发展,输尿管软镜及相关设备的快速发展,临床医生也倾向使用软镜治疗各种位置的肾结石,尤其是肾下盏结石为多。 由于软性输尿管肾镜治疗肾脏结石具有创伤小、结石清除率高、恢复快的特点,近年已成为难治性肾下盏结石微创治疗的有效手段[19-21]。欧洲泌尿外科结石疾病诊疗指南从2012年开始建议:1.5 cm以下肾脏结石以及2 cm以下的肾下盏结石,软性输尿管肾镜手术均可作为一线治疗方式,相比PNL的手术创伤大、风险高,RIRS通过人体自然通道进入肾盂、肾盏,更接近于“无创”,患者也更容易接受。2017年欧洲泌尿外科指南已将软性输尿管肾镜作为下组肾盏结石的一线治疗方式[16]。
新一代软性输尿管肾镜主动弯曲可达280°,末端6.7~7.2 cm镜头部分能进行二次偏移,对于95%以上的肾脏集合系统区域软镜均能无“死角”碎石或探查[22],但目前软镜在肾脏结石治疗中仍存在一些局限性,其中最为主要的难点在于处理肾下盏结石。当需要处理肾下盏结石时,软性输尿管肾镜往往需要在大角度主动弯曲的基础上,结合镜身的被动弯曲功能才能进入下盏空间。目前认为影响输尿管软镜治疗肾下盏结石可能相关的解剖因素包括:肾盂肾下盏夹角、肾下盏漏斗部长度、及肾下盏漏斗部宽度等。
4 肾下盏解剖结构对软镜治疗肾下盏结石的影响
肾下盏解剖结构对肾下盏结石的影响很早就受到重视,特别是ESWL治疗肾下盏结石的研究中,但是肾下盏解剖结构尤其是CPH对软镜治疗肾下盏结石疗效影响的国内外研究并不多。
4.1 IPA对软镜治疗肾下盏结石的影响1999年,GRASSO等[23]报道,采用纤维软性输尿管镜治疗下盏结石,发现IPA(测量方法不详)在治疗肾下盏结石中并无意义;相似的研究还有KILICARSLAN等[24],认为IPA(采取ELBAHNASY的测量方法)并不会影响软镜治疗肾下盏结石的疗效。但随后的研究均表明IPA也是软镜治疗的重要解剖参数。2008年GEAVLETE等[13]报道:IPA(测量方法不详)角越大,输尿管软镜进入肾下盏成功率越高,碎石成功率越高;而当IPA<30°时,软镜则几乎无法处理下盏结石。2012年,RESORLU等[8]用了新型的软性输尿管镜治疗肾下盏结石,评估了67列肾下盏结石患者并进行了回顾性分析,发现结石排空组与结石残留组的IPA(采取ELBAHNASY的测量方法)分界点分别为48°和35°,当IPA45°时,RIRS治疗下盏结石成功率高,利于残余结石的排空。叶利洪等[25]的研究发现肾盂输尿管与肾下盏夹角对输尿管软镜碎石术的疗效有显著影响,这主要是因为IPA(采取ELBAHNASY的测量方法)过小,内腔镜偏转不足,导致不能进入肾下部分。2014年,JESSEN等[26]的回顾性研究,发现IPA(采取ELBAHNASY的测量方法)在结石排空组与结石残余组之间的差异有统计学意义,IPA超过30°时,软镜均能顺利进入下盏处理结石,小于30°时将明显降低手术成功率,因此IPA<30°的肾下盏结石患者术前应被告知结石清除是可能的,但存在二次手术干预的风险。2015年日本的一位学者INOUE[27]的回顾性分析研究,在多因素分析中仅有IPA(采取ELBAHNASY的测量方法)在结石排空组与结石残余组中有统计学差异,IPA<30°时,是影响术手术成功率及术后排石率的消极因素。国内学者杨嗣星等[28]回顾性分析了36例采用软性输尿管镜治疗IPA<30°肾下盏结石患者的临床资料,认为IPA<30°确实对软性输尿管镜钬激光碎石术治疗下组肾盏结石存在影响,但主要影响排石过程而非碎石。新型软性输尿管镜可以有效克服肾下盏IPA较小及漏斗部较长等困难,有效地粉末化下盏结石,几乎不存在残余结石。结合术前影像学分析及熟练的操作技巧,同时配合药物及物理排石手段可有效治疗IPA<30°的肾下盏结石。上述学者关于IPA对软镜治疗肾下盏结石疗效影响的观点不完全一致,可能与不同时期使用的软镜设备型号、测量方法、入组标准、研究方法及样本量不同等因素有关。但我们认为IPA仍是对软镜治疗肾下盏结石影响最重要的解剖参数,而关于IPA测量方法并无明确的标准,目前多数学者推荐ELBAHNASY和SAMPAIO的测量方法。
4.2 IL、IW对软镜治疗肾下盏结石的影响KILICARSLAN[24]通过多变量分析研究表明,IL参数无明显相关性,输尿管镜顶端6.7~7.2 cm镜体部分可作有效的二次偏转,有利于通过大多数肾下部分漏斗的长度,所以IL并没有影响手术的成功率;类似的研究还有RESORLU 等[8]回顾性分析发现,虽然IL在结石排空组与残石组中无统计学差异,但在结石残余组中IL值均是偏高的。但大多数学者认为IL过长是影响软镜治疗肾下盏的消极因素。JESSEN等[26]的回顾性研究,发现IL仅在单因素分析中有统计学意义,IL过长影响残余结石的排出,因此IL过长的肾下盏结石患者术前应被告知存在二次手术干预的风险;类似的研究还有INOUE[27]的回顾性分析研究,IL在单因素分析下有统计意义,IL27 mm时,影响手术成功率。GEAVLETE等[13]发现,当IL<3 cm 时,软镜治疗下盏结石成功率为88.2%,当IL≥3 cm时,其成功率为61.1%;SARI等[9]的回顾性研究发现,IL在治疗成功组和失败组中有明显的的统计学差异,过长的IL影响RIRS治疗肾下盏结石的成功率及术后排石率。
关于IW对软镜治疗肾下盏的影响如下述,2008年GEAVLETE等[13]发现肾下盏漏斗部宽度也与手术疗效密切相关:IW<0.5 cm是软镜治疗下盏结石的重要不利因素。2015年,KILICARSLAN[24]分析了36例经RIRS治疗的肾下盏结石患者的肾下盏解剖结构,通过多变量分析研究表明,仅IW是决定手术成功率的关键因素。同年,INOUE[27]的回顾性分析研究,IW仅在单因素分析下有统计意义,IW8 mm时,软镜更容易进入下盏,利于结石的排空。也有与上述观点相反的研究,RESORLU 、JESSEN、SARI等[8-9,26]的研究中,发现IW在结石排空组和结石残留组之间并无统计学差异,对RIRS治疗肾下盏结石的成功率及排石率影响不大。目前多数学者认为肾下盏漏斗部宽度不是影响软镜治疗肾下盏结石疗效的解剖学参数之一,有以下几个原因:首先是漏斗部的口径是可变的,特别是当液体灌流时,漏斗部口径变化比较大;其次是钬激光可以将结石粉碎成非常小的碎片甚至是粉末,而不需要进一步取石;最后,现代输尿管软镜尺寸允许它们进入非常狭窄的漏斗颈部。因此,除了罕见的病理性漏斗部狭窄的情况下,这种解剖特征对RIRS手术的影响减少。
4.3 CPH对软镜治疗肾下盏结石的影响早在2000年,TUCKEY等[7]提出CPH,并研究得出CPH<15 mm时,ESWL治疗肾下盏结石清除高达92%,是一个良好的预测指标;但是关于CPH对软镜治疗肾下盏结石影响的研究尚少。2012年,RESORLU[8]首次次研究了CPH与软镜治疗肾下盏结石疗效的相关性,发现CPH<25 mm时,软镜治疗肾下盏结石清除率为74.1%,虽然CPH在结石排空组与残石组中无统计学差异,但在结石残余组中CPH值是偏高的;2015年,INOUE[27]的回顾性分析研究,在单因素分析下CPH≥25 mm时,不利于残余结石的排出;随后,SARI等[9]对132名肾下盏结石患者进行了回顾性研究,发现CPH也是一个术前预测的指标,CPH≥20.2 mm时手术成功率高,当CPH临界值在20.2 mm时,其对应的结石排空敏感度为75.9%,特异度为59.2%。CPH比IPA更容易测量,并且CPH预测值的初始结果相当有前景,目前国内尚未有CPH与软镜治疗肾下盏结石疗效的相关研究,而国外相关研究少而且对于CPH与软镜治疗肾下盏结石疗效影响的结论不一致,未来还需积累更大的数据并进行多因素分析评估CPH的预测价值,不排除CPH也可以成为软镜治疗下盏结石效果的预测的解剖参数。
由目前国内外相关研究进展中可发现,输尿管软镜治疗肾下盏结石的成功率及术后残余结石排空率主要取决于IPA、IL、IW等解剖参数,而IPA是最重要的决定因素,CPH国外研究尚少,国内尚未见相关报道。虽然随着软镜及配套设备(激光、套石篮)推陈出新,配合适当的辅助治疗,对于处理≤2 cm直径大小的肾下盏结石的成功率有所提高,但依然存在有部分残余碎片的情况,而残余碎片可以为新结石的形成提供核心,结石刺激也更容易引起血尿、泌尿系感染、肾绞痛等并发症的发生,尤其感染性结石患者如伴结石残余,结石复发的可能性更大[29]。因此有必要进一步探讨肾下盏解剖结构在软镜治疗肾下盏结石中的影响,尤其是国内尚未研究的CPH,为此我们需要做更全面的研究,选取最合理和标准的测量方法,寻找最合适、关键的解剖参数,为广大泌尿外科医师更好地使用软镜治疗肾下盏结石提供临床指导。
5 小结与展望
综上所述,RIRS是目前治疗直径≤2 cm肾下盏结石的有效治疗方式[30],IPA、IL、IW为影响手术效果的关键解剖参数,目前国内外阐述了肾下盏解剖参数IPA、IL、IW对软镜治疗肾下盏结石影响的研究,但结论并非一致,而CPH解剖参数对软镜治疗肾下盏结石影响的研究,国外相关研究尚少,国内尚未有相当明确的相关研究文献来阐明。通过文献阅读,我们发现研究的局限:①在上述研究中,下盏解剖测量标准多样,缺乏统一;②缺乏术后复查,或复查影像学不标准;③随访时间及残余结石定义不一致;④大多数研究为回顾性分析而且样本量过小。为此,我们仍需进一步的前瞻性多中心研究分析各参数的评估价值,规范统一肾下盏解剖参数的测量,探讨患者的肾集合形态解剖学特征(IPA、IL、IW、CPH等)对软镜处理肾下盏结石的影响,从中寻找关键性的解剖参数,为输尿管软镜治疗小于2 cm肾下盏结石的临床研究提供一定的依据。
——可重复性或一次性输尿管软镜孰优孰劣?