9例矫正型大动脉转位合并室上性心动过速射频消融回顾性分析*
翁思贤 唐闽 方丕华 贾玉和 马亚哲 郭金锐 郭雨龙 刘可 张澍
矫正型大动脉转位(congenitally corrected transposition of the great arteries,ccTGA )是胚胎发育时心管左襻而形成的心脏畸形,其房室与大血管连接顺序变为:右房-形态学左室-肺动脉、左房-形态学右室-主动脉(形态学左室变功能右室、形态学右室变功能左室),从而达到生理性循环矫正的结果[1]。既往研究表明,ccTGA患病数约占先天性心脏病0.5%[2],每1 000个儿童中可见0.27~0.31个TGA者[3-4]。ccTGA常可出现各种类型室上性心律失常,国内外均有学者报道相关病例的射频消融治疗[5-11]。但是,由于超过90%[2]ccTGA患者合并诸如室间隔缺损(VSD)、房间隔缺损(ASD)、Ebstein畸形、心脏传导系统变异[12]等异常而给ccTGA合并室上性心动过速(SVT)的射频消融治疗带来了极大的困难。鉴于此,笔者回顾性分析9例ccTGA合并SVT患者的病例特点、电生理检查及射频消融结果等。
1 资料与方法
1.1 研究对象
连续入选2011年1月到2018年4月于本院诊治的ccTGA合并SVT患者,均有1次以上的窄QRS心动过速发作史。术前均完善心脏CT、超声心动图、心电图、化验等明确心脏畸形情况及心功能状况。
1.2 电生理检查
所有患者术前均停用抗心律失常药5个半衰期以上,并已签署相关知情同意书。局部麻醉及常规穿刺股静脉或右颈内静脉放置冠状窦电极(CS)、希氏束电极(HBE)和右室心尖部电极(RVA)后,用Bard多导电生理仪(Boston Scientific,美国)记录体表心电图与腔内电图信息。先后行心室、心房程序电刺激,必要时给予异丙肾上腺素后重复刺激,至诱发心动过速。SVT腔内电生理诊断与鉴别诊断参考目前公认的标准和方法[13]。
1.3 射频消融
明确诊断后,主要涉及到3类SVT射频消融:房室结折返性心动过速(AVNRT)、房室折返性心动过速(AVRT)、房性心动过速(AT)。①对于AVNRT者,常规穿刺股静脉放置消融导管至右心房,在X线透视或三维电解剖模型(若患者合并右旋心、右位心则常规融合CT三维重建图像)指导下,于常规慢径区域(后间隔冠状窦口与三尖瓣隔瓣间)标测到小A大V的靶点电图后,以功率滴定法进行消融(15~30 W,60 s,3次);若常规慢径区域消融无效,则通过抬高消融平面、或者以冠状窦静脉或穿刺房间隔途径至左房标测消融;若消融中出现稳定的慢交界心律、消融后重复电生理检查未诱发心动过速或出现≤1个回波则提示消融成功。②对于AVRT者,在X光或三维电解剖模型指导下,右侧旁道常规穿刺股静脉放置消融大头至形态学二尖瓣,酌情使用SR0长鞘(Abbott,美国)支撑;左侧旁道则选择主动脉逆行法或穿刺房间隔法至形态学三尖瓣消融;靶点判定为心动过速或起搏标测下,前传心室或逆传心房最早点;消融功率选取25~35 W,消融时间120 s以上,消融成功标准为阻断旁道前传和逆传、不能诱发心动过速。③对于AT者,常规穿刺股静脉放置消融导管至右心房,建立三维电解剖模型,结合X光透视行AT激动顺序标测,寻找心房最早激动点;若怀疑AT起源于左心房,则经房间隔穿刺途径至左心房行三维激动顺序标测;理想靶点为消融导管局部双极电图碎裂、单极电图呈QS型,较最早体表P波起始提前30 ms;消融功率选择20~35 W,有效靶点消融时间60 s以上;消融成功标准为术后不能诱发AT。
1.4 手术效果判定
手术即刻成功定义为消融术后电生理检查未诱发心动过速;远期疗效判定视术后24 h、3个月、6个月、1年后复查心脏超声、普通心电图、24 h动态心电图及症状而定。随访以电话和门诊为主。
2 结果
2.1 基本资料
共计9例病人入选研究,其中女性4例,年龄19~65岁、病史2~35年不等。3例既往有1次以上射频消融病史。术前影像学检查结果示(S,L,L)(situs solitus with L-looping of the ventricles and the aorta anterior and leftward)型7例(正位心6例、右旋心1例)、(I,D,D)(situs inversus with D-looping of the ventricles and the aorta anterior and rightward)2例(右位心1例、中位心1例)[2];其中2例合并ASD、2例合并VSD、2例合并瓣膜病(VHD)、1例合并肺动脉高压(PAH);心功能2例II~III级(NYHA分级),其余正常。
2.2 电生理检查及射频消融结果
术中电生理检查结果:4例AVNRT,3例AVRT,2例AT。术后1例HV间期延长至100 ms,其余无明显改变。复发1例,其余随访3~75个月未见心动过速复发(表1)。
2.2.1AVNRT 4例电生理检查证实均是慢快型AVNRT。其中病例3于常规慢径区域(冠状窦口前方)标测到小A大V靶点电位,放电过程中交界反应良好,消融成功。病例1和病例7于常规慢径区域消融效果不佳,后分别经穿间隔、ASD缺口途径于左后间隔消融成功。病例9(图1)为中位心合并内脏反位,解剖结构较为复杂,故使用EnSiteNavx三维电解剖融合CT建模,先后于右后间隔、左后间隔侧消融效果不佳,仍可诱发心动过速,遂抬高消融平面,于高位His束附近标测到小A大V靶点图伴粗钝H波(考虑远场H波),放电消融交界反应良好,巩固消融后未再诱发心动过速。
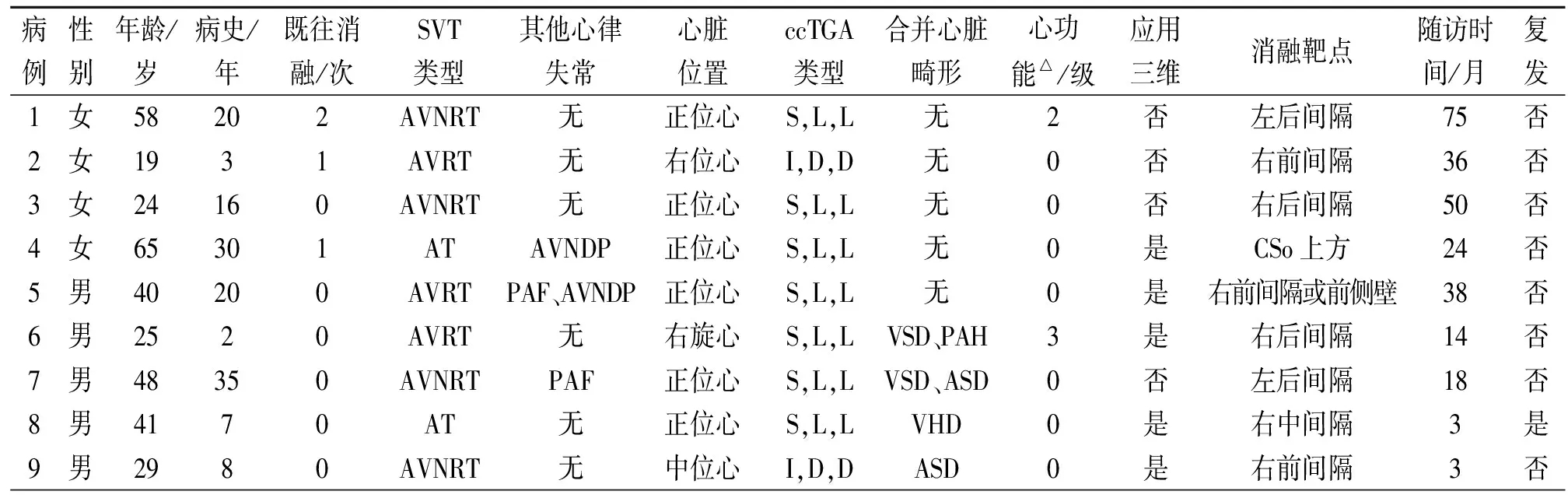
表1 临床、电生理检查及射频消融资料
注:△为NYHA分级;AVNDP=房室结双径路;S,L,L=内脏正位,心室左袢,主动脉左前;I,D,D=内脏反位,心室右襻,主动脉右前(与S,L,L镜像关系);PAF=阵发性心房颤动; CSo=冠状窦口

A:S1S2刺激诱发AVNRT(Abl d置于希氏束位置);B:左前斜45°透视靶点图;C:左房+右房三维电解剖模型融合CT建模:绿点为消融有效点,黄点为希氏束位置;D:靶点腔内电图:黑色箭头所示为H波(粗钝);E:消融时出现交界心律;F:全心腔三维电解剖模型融合CT建模:患者为中位心合并心房反位,AP位相当于正位心的LAO,RL位相当于RAO 。LAO=左前斜45°;RAO=右前斜30°;RL=右侧位;AP=前后位;his=希氏束;CS=冠状窦电极;ABL=消融导管;LA=左房;RA=右房;LV=左室;RV=右室;PA=肺动脉;Ao=主动脉
图1病例9(AVNRT)的消融成功靶点
2.2.2AVRT 3例电生理检查结果显示旁道位置均位于右心房形态学二尖瓣区,其中病例5电生理检查时可见AV跳跃现象,但未诱发AVNRT、无回波现象,且频繁发作PAF。病例2为右位心,心动过速发作时His上A波领先冠状窦口(CSo)约60 ms,于二尖瓣环靠前区行RS2刺激可使A波提前,仔细标测前间隔部位可见逆传心房最早激动点,放电10 s即阻断旁道。病例5在心室起搏下、于形态学二尖瓣区约11~12点位置标测到逆传心房最早激动点,在SR0长鞘支撑下即刻消融成功。病例6为右旋心,应用Carto三维电解剖模型融合CT建模,于形态学二尖瓣环前间隔区标测到前传心室最早激动点,放电消融后旁道前传阻断,反复电生理检查未诱发心动过速。
2.2.3AT 2例电生理检查证实为右房AT,其中病例4术中出现AV跳跃、间歇回波。病例4在Carto电解剖模型指导下,于CSo上缘标测到较体表心电图P波起点提前约30ms激动点,放电消融可终止心动过速,但仍可诱发,遂穿间隔至左后间隔标测到同样提前体表心电图P波起点30ms靶点,反复消融仍可诱发心动过速,返回右房继续于CSo巩固消融,后未再诱发AT。病例8于右房中间隔处标测到最早激动点,穿间隔至左房对应处也可标测到较早激动点,消融可终止心动过速,但巩固消融时频繁可见快交界反应,考虑该病例His位置较低、毗邻AT靶点,遂终止手术,术后3个月随访复发。
2.2.4消融的靶点分布及消融前后AH、HV间期的变化 见图2及表2。

A:ccTGA患者房室连接关系[2];B:7例(S,L,L)型ccTGA患者左前斜45°下靶点分布;C:2例(I,D,D)型ccTGA患者右前斜30°下靶点分布。RA=右房;LV=形态学左室;LA=左房;RV=形态学右室;MV=二尖瓣环;TV=三尖瓣环;CS=冠状窦;His=希氏束;AS=前间隔;MS=中间隔;PS=后间隔
图2靶点分布示意图

表2 消融前后AH、HV间期变化/ms
3 讨论
ccTGA患者形态学左室变成功能右室、形态学右室变成功能左室,其房室-大血管连接顺序变为:右房-形态学左室-肺动脉、左房-形态学右室-主动脉。此外,ccTGA常因合并心脏位置、结构等异常而加大了SVT射频消融的难度。自Eisenberger等[6]开始尝试使用Carto三维对ccTGA合并SVT进行射频消融以来,三维标测融合CT建模[9]成了该类复杂心脏畸形合并SVT患者治疗首选,此项技术使得术者能更加直观地辨认心脏各腔室,尤其对于合并右位心、右旋心等的ccTGA患者,获益更大。本组患者55.5%(5/9)使用三维标测技术,2例右位心和右旋心患者,应用三维+CT融合建模后均获得了消融的成功。研究表明,(S,L,L)型ccTGA患者房间隔、室间隔较(I,D,D)型患者更易出现排列紊乱而致传导系统异常[12];此外,紊乱排列的房间隔增加了其传导的各向异性及异常传导肌束的发生,使其更容易成为心律失常起源点,这与本组9例SVT合并ccTGA患者(7例S,L,L型,2例I,D,D型)消融靶点均靠近间隔侧的结果不谋而合,这也为相关SVT射频消融提供了较好的消融策略。
ccTGA合并双径现象似乎更为常见。Liao等[7]报道了9例AVNRT合并ccTGA的射频消融,其中7例靶点位于右后、中间隔常规慢径区域,1例于右室流出道标记到H波并于其下方消融成功,1例穿间隔至左后间隔消融成功,这是迄今为止报道的最大系列。而本组患者中66.7%出现双径现象(6/9),其中4例AVNRT患者中,仅1例于常规慢径区域消融成功,2例于左后间隔、1例于右房前间隔His下方消融成功。此提示,左右后间隔周围区域、也就是传统慢径的左右后延伸区[14],仍然是ccTGA合并AVNRT患者的首选消融靶点,若消融效果不佳(交界反应不好或仍可诱发)则可于前间隔、右室流出道等毗邻希氏束的位置尝试消融,但也明显加大了术后传导阻滞的风险,如本组病例9于右房前间隔记录到较为粗钝的H波,消融前后HV间期从40 ms增至100 ms,提示损伤了His束。借鉴国内Xue等[15]对临近His束的旁道采取不同能量的起搏方式以区分H波属远场或近场电位、从而避免消融时损伤His束的思路,或许能对此类消融靶点临近His束的AVNRT患者有所帮助。ccTGA还可合并双房室结,其电生理特点为:窦律或交界律可记录到3种形态QRS波;主房室结和副房室结均可介导AVNRT发生,心动过速下QRS波形态可有2种或以上;于2个不同且分离的解剖区域记录到His电位;在2个区域消融均可见交界心律[5]。(S,L,L)型患者更易合并双房室结,其发生率在10%左右[7]。本组9例患者中,电生理检查未见双房室结现象。
目前国内外对于ccTGA合并房室旁道的报道主要见于形态学三尖瓣环区域[11,16-17],且多旁道常见,与其合并Ebstein畸形相关。而本组3例旁道均位于形态学二尖瓣环区,且均为单一旁道,未见Ebstein畸形。右房室旁道合并ccTGA的消融与传统右侧旁道消融类似,可适当使用长鞘、冷盐水导管等以获得更好的支撑力、消融深度等[14]。对于ccTGA合并AT患者,国内外鲜有报道。Guo等[9]报道了3例ccTGA前间隔起源的AT,均可于肺动脉窦内消融成功,这与非ccTGA者于无冠窦消融His束旁AT有着相似之处[18]。本组2例AT,1例于CSo上方标测到最早激动点,但不局限,后经“左右夹攻”法消融成功,提示间隔起源的AT,若右房标测较早的区域不局限,可于左房侧对应位置加强消融;另1例则因靶点毗邻His束而放弃巩固消融致其复发,对于此类His束位置较低患者,肺动脉窦口是否适合作为备选靶点尚待进一步探索。
ccTGA合并SVT的患者,若条件允许,应首选三维电解剖模型融合CT建模,可增加手术的成功率;此类患者的术中定位,应更加关注左右房间隔侧的标测,以缩小靶点范围;若右房间隔面消融效果不佳,可于左房间隔面寻找更好的靶点或对应位置巩固消融。

