胰腺癌患者立体定向体部放射治疗非共面锥形射束与共面扇形射束照射的剂量学差异
陈飞虎,柏晗(通信作者),代智涛
1 云南省肿瘤医院·昆明医科大学第三附属医院放射治疗科 (云南昆明 650118);2 第二军医大学附属长海医院 (上海 200433)
胰腺癌作为消化系统常见的恶性肿瘤,其早期临床症状和体征不明显,一旦患者确诊为胰腺癌,多数已为中晚期,手术切除率不足20%,且预后效果差[1]。因此,放射治疗已成为治疗中晚期胰腺癌患者的主要方法。
对于中晚期胰腺癌患者,主要传统分次放射治疗技术有三维适形放射治疗(3DCRT)和调强放射治疗(IMRT),其技术特点是分次剂量低、治疗周期长、毒副反应大,肿瘤的局控率和患者生命质量的改善有很大局限性[2]。有研究表明,传统分次放化疗模式与单纯化疗相比,总生存率无明显差异[3-5]。对此,Swaminath和Chu[6]做了试验研究并报道,精确的立体定向体部放射治疗(SBRT),能更好地降低周围正常组织的照射剂量,毒副反应减小;同时,低分次、大剂量的分割模式也显著缩短了治疗周期,还能有效克服癌细胞的放射性抗拒。一项多中心胰腺癌放射治疗的前瞻性研究,利用带有呼吸门控的瓦里安Turebeam直线加速器,采用拉弧调强(rapidarc)照射技术,处方为6.6 Gy/f*5 f,最终49例患者的中位生存期、无进展生存(PFS)和总生存(OS)率均改善明显,无严重不良反应[7]。
此外,螺旋断层放射治疗系统(Tomotherapy)和立体定向放射外科系统(Cyberknife)也可做SBRT治疗[8-11],但关于这两种系统计划设计的剂量学对比,鲜有报道。因此,本研究结合以往临床试验研究结果,采用6.5 Gy/f*5 f、7 Gy/f*5 f、7.5 Gy/f*5 f的分次治疗模式,对扇形射束与非共面射束治疗胰腺癌患者的剂量学差异进行评价,为中晚期胰腺癌患者选择合适的放射治疗方式提供剂量学依据,现报道如下。
1 资料与方法
1.1 一般资料
选取2015年1月至2017年6月第二军医大学附属长海医院放射治疗科收治的13例无法手术的局部晚期胰腺癌患者作为研究对象,肿瘤体积19.03~100.61 cm3,平均58.45 cm3。所有患者均为首程放射治疗,基于大孔径CT模拟定位图像,分别制定Cyber和Tomo放射治疗计划,对两种不同计划间的剂量学差异进行评价。
纳入标准:所有选取患者经磁共振成像(MRI)、正电子发射计算机断层显像技术(PET-CT)及病理学活检,均已确诊为局部晚期胰腺癌,根据TNM分期标准进行肿瘤临床分期,其中Ⅱ期8例,Ⅲ期5例,临床资料齐全。排除标准:卡氏评分(Karnofsky Performance Status,KPS)<70分患者;发生远处转移患者;有其他严重的器官功能障碍患者;对放射治疗不耐受患者。
1.2 体位固定和CT模拟定位
患者均采用仰卧位,双手自然摆放于身体两侧,用真空负压袋内固定。CT模拟定位时采用荷兰Philips 16排大孔径CT模拟机进行扫描,扫描条件为120 kVp、400 mAs、1.5 mm 层厚无间隔螺旋扫描,扫描螺距为0.938。主图像采用平扫,在患者吸气末屏气的情况下扫描,扫描的界限为肿瘤上下界各自增加15 cm。辅助图像采用碘造影剂增强扫描,在患者呼气末屏气的情况下扫描,界限为肿瘤上下界各自增加5 cm。扫描完成后,通过射波刀数据管理系统(CDMS)导入患者CT影像,进行影像配准融合,然后由肿瘤临床医师进行靶区勾画,勾画完成后制定Cyber放射治疗计划;同时将勾画好靶区的图像文件打包发送到云南省肿瘤医院放射治疗科,制定Tomo放射治疗计划。
1.3 靶区与危及器官(OAR)的勾画
每例患者由同一主管医师勾画靶区,并按照ICRU83号文件进行靶区勾画和OAR的勾画,根据临床标准确定原发肿瘤靶区体积(Tumor),Tumor包括CT、PET/CT或MRI检查图像确定的可见原发病灶,对于立体定向放射治疗,AAPM TG101报告明确定义的肿瘤GTV=CTV,且射波刀具有呼吸追踪定位系统,因此这里不做CTV及PTV的勾画,但对于Tomo的计划设计,根据Chang等[11]的报道,我们在靶区Tumor的基础上,均匀外扩5 mm形成计划靶区(PTV),且PTV不外扩至OAR以内[12-13]。
OAR的勾画包括胃、小肠、十二指肠、肝脏、脾脏和双侧肾脏,由于射波刀和Tomo刀的剂量梯度在治疗靶区边缘迅速跌落,因此正常组织器官的轻微移动可使它进入高剂量区域,故OAR的勾画必须精准。
1.4 放射治疗计划的设计
将勾画好的靶区、OAR结构和CT图像分别传输至Tomo planning station和Multiplan计划工作站,所有患者的Tomo计划和Cyber计划分别由同一名指定好的物理师完成,并由副高职称以上的物理师和医师确认。患者PTV处方剂量为6.5 Gy/f*5 f(5例)、7 Gy/f*5 f(4例)、7.5 Gy/f*5 f(4例),处方剂量覆盖95%及以上的靶区体积,最大剂量点Dmax不作要求,但110%处方剂量线必须严格控制在靶区以内。OAR的剂量限值标准参考AAPM TG101报告[12]。
1.5 放射治疗计划的评估
比较两种放射治疗计划的靶区和正常组织器官剂量-体积直方图(dose-volume histogram,DVH)、机器跳数(Mu),剂量学评价指标主要包括肿瘤靶区(Tumor和PTV)观察指标和OAR限值指标。
肿瘤靶区的评价包括D2%(2%靶区体积所受剂量)、D98%(98%靶区体积所受剂量)和VDx(肿瘤靶区的覆盖率)。
OAR限值指标包括:(1)脊髓Dmax(脊髓≤0.035cc体积所受最大剂量)、D<0.25cc(脊髓0.25cc体积所受最大剂量)、D<1.2cc(脊髓1.2cc体积所受最大剂量);(2)小肠Dmax(小肠≤0.035cc体积所受最大剂量)、Dmean(小肠所受平均照射剂量)、D<5cc(小肠5cc体积所受最大剂量);(3)胃Dmax(胃≤0.035cc体积所受最大剂量)、Dmean(胃所受平均照射剂量)、D<10cc(胃10cc体积所受最大剂量);(4)十二指肠Dmax(十二指肠≤0.035cc体积所受最大剂量)、Dmean(十二指肠所受平均照射剂量)、D<5cc(十二指肠5cc体积所受最大剂量)、D<10cc(十二指肠10cc体积所受最大剂量);(5)肝脏Dmean(肝脏所受平均照射剂量);(6)肾脏Dmean(肾脏所受平均照射剂量)。
1.6 统计学处理
采用SPSS 22.0统计软件进行数据分析,计量资料以±s表示,采用t检验,P<0.05为差异有统计学意义。
2 结果
两种计划D2%、D98%和VDx比较,差异有统计学意义(P<0.05),而且Tomo计划的总跳数明显高于Cyber计划。从VDx角度,Tomo计划靶区覆盖率更高,但这两种计划的靶区覆盖率均为95%以上,达到临床需求。因此,两种计划靶区处方剂量的覆盖率并无明显优劣体现。见表1。
两种计划除胃Dmean比较,差异无统计学意义(P>0.05),其他OAR各项指标参数比较,差异均有统计学意义(P<0.05),Cyber计划脊髓Dmax、D<0.25cc和D<1.2cc显著优于Tomo计划;与Tomo计划比较,Cyber计划小肠Dmax和D<5cc也明显更低;与Tomo计划比较,Cyber计划胃Dmax和D<10cc具有明显优势;与Tomo计划比较,Cyber计划十二指肠Dmax、Dmean、D<5cc、D<10cc和左右肾脏Dmean也明显更低;Cyber计划只有肝脏Dmean和小肠Dmean不如Tomo计划。见表2。
表1 Cyber和Tomo计划靶体积(Tumor、PTV)剂量学参数比较(±s)
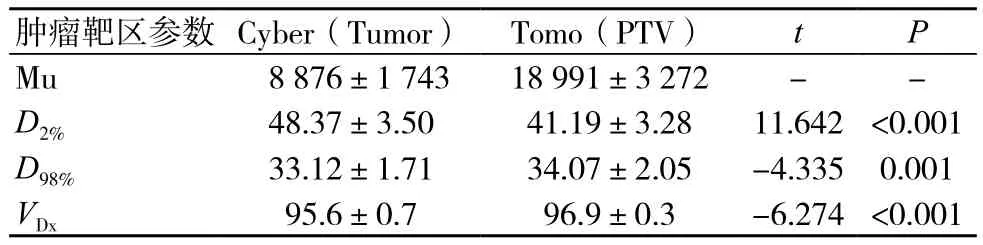
表1 Cyber和Tomo计划靶体积(Tumor、PTV)剂量学参数比较(±s)
注:Tumor为原发肿瘤靶区体积;PTV为计划靶区体积;VDx为100%处方剂量线的靶区体积覆盖率;D2%和D98%的单位为Gy,VDx的单位为%
Mu 8 876±1 743 18 991±3 272 - -D2% 48.37±3.50 41.19±3.28 11.642 <0.001 D98% 33.12±1.71 34.07±2.05 -4.335 0.001 VDx 95.6±0.7 96.9±0.3 -6.274 <0.001
表2 Cyber和Tomo计划OAR剂量学参数比较(±s)

表2 Cyber和Tomo计划OAR剂量学参数比较(±s)
注:Dmax为≤0.035cc的体积剂量;Dmean为整体积平均剂量;D<xcc为≤ xcc的体积剂量,x取0.25、1.2、5和 10;Dmax、Dmean和D<xcc的单位均为Gy
脊髓Dmax 5.47±1.58 13.11±2.67 -13.653 <0.001 D<0.25cc 5.09±1.49 12.63±2.52 -14.287 <0.001 D<1.2cc 4.59±1.31 11.94±2.34 -15.200 <0.001小肠Dmax 19.79±4.76 27.84±5.51 -8.459 <0.001 Dmean 3.53±0.93 2.57±0.72 2.998 0.011 D<5cc 14.04±3.38 19.00±3.38 -8.137 <0.001胃Dmax 19.52±3.72 31.60±3.80 -16.368 <0.001 Dmean 4.88±1.50 5.34±2.18 -1.206 0.251 D<10cc 11.90±2.81 17.90±2.88 -11.337 <0.001十二指肠Dmax 16.56±5.09 23.36±5.29 -10.383 <0.001 Dmean 4.02±1.25 4.98±1.52 -5.090 <0.001 D<5cc 9.50±3.33 14.05±4.07 -8.847 <0.001 D<10cc 7.69±2.91 11.51±3.89 -7.332 <0.001肝脏Dmean 3.22±1.09 2.58±1.43 3.133 0.009左肾Dmean 2.85±1.00 4.39±1.81 -3.712 0.003右肾Dmean 2.39±0.65 3.54±1.51 -3.889 0.002
除上述统计表,本研究进行了两种计划DVH曲线剂量比较,其结果见图1~3。图1显示处方剂量为7 Gy/f*5 f的平均DVH曲线;图2显示处方剂量为6.5 Gy/f*5 f的平均DVH曲线;图3显示处方剂量为7.5 Gy/f*5 f的平均DVH曲线。3种处方剂量的平均DVH曲线均表明具有相同的剂量分布趋势,肿瘤靶区(Tumor和PTV)均显示为Cyber计划低剂量区域更低,高剂量区域更高,而Tomo计划靶区内收缩更紧,该结果与表1中D2%和D98%的统计数据一致。所有OAR的DVH曲线均显示Tomo计划的低剂量区域更低,而高剂量区域更高;对于OAR高剂量点的控制,Tomo计划和Cyber计划都能满足AAPM TG101报告中OAR剂量限值的要求,显然Cyber计划更具绝对优势。

图1
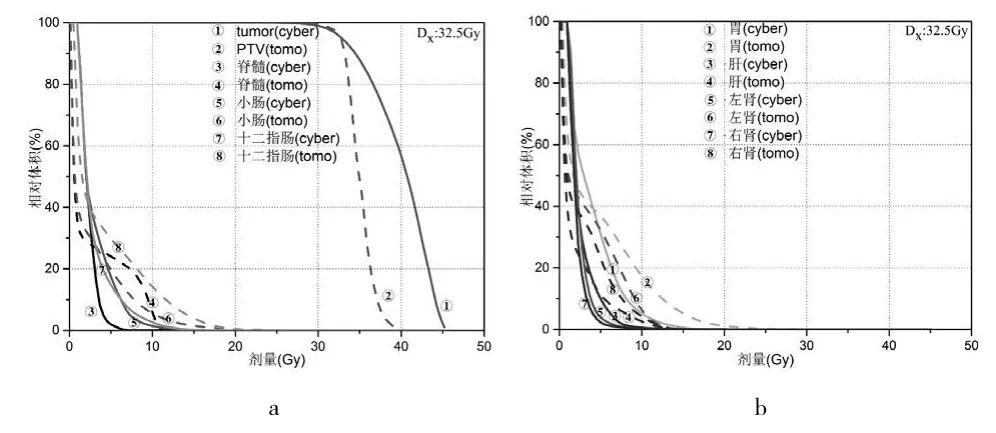
图2
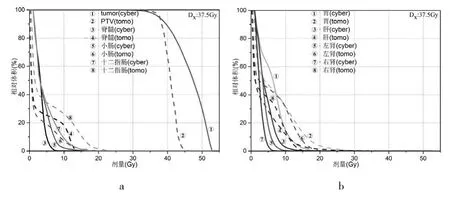
图3
3 讨论
同步放化疗是中晚期胰腺癌患者的标准治疗模式,胰腺癌患者的放射治疗也从适形照射到固定野调强、再到容积调强技术,以及发展至今的螺旋断层放射治疗和射波刀的SBRT技术。随着放射治疗技术的不断发展,SBRT技术相比常规的分次治疗模式,具有分次剂量高、治疗周期短、毒副反应小的技术特点。已有研究报道这种低分次、大剂量的分割模式不但显著缩短了治疗周期、减小了毒副反应,还能有效克服癌细胞的放射性抗拒,从而可能提高治疗效果,提高胰腺癌患者的PFS和OS[6]。
本研究汲取以往临床试验研究经验[6-7],采用3种SBRT分次治疗模式,比较分析Tomo和射波刀的计划设计方案,统计扇形束与非共面射束治疗晚期胰腺癌患者的剂量学差异。最终结果已经表明Tomo计划靶区内收缩更紧,这是由扇形射束与非共面射束照射差异所致,说明Tomo计划相比Cyber计划更容易满足靶区内剂量均匀,且计划靶区覆盖率也明显更高,减少了肿瘤靶区的漏照范围,但Tomo计划不具备呼吸追踪定位功能,射波刀所独有的呼吸追踪定位功能能弥补这一缺点,可以提高靶区内剂量照射的准确性,只要计划靶区处方剂量达到95%以上,均能满足临床需求。
此外,本研究主要观察了两种计划OAR的剂量学差异,结果表明Cyber计划更能有效控制OAR的高剂量区,且所有OAR均显示为Cyber计划的低剂量区域更高、高剂量区域更低。这主要由以下两方面原因所致:(1)Tomo计划的PTV是通过GTV外扩0.5 cm形成;(2)Cyber计划的非共面布野特点。由于Tomotherapy不具备呼吸追踪定位功能,为避免治疗时靶区的漏照,Tomo计划只能通过GTV外扩形成PTV,造成PTV更加贴近周围重要OAR,因而OAR高剂量区的剂量得不到有效控制;另外Cyber计划的非共面照射特点可以使靶区边缘剂量更加迅速跌落,从而更加有效地保护了周围邻近重要组织器官,但这也造成了OAR低剂量区的剂量更高。
另外值得注意的一点,几乎所有OAR的各项指标都显示Cyber计划优于Tomo计划,只有肝脏Dmean和小肠Dmean完全相反,这可能是由于Cyber计划只能通过患者身体前侧设置布野路径,造成患者前侧OAR的平均剂量高于后侧,但两种计划设计方案都能满足临床需求。
综上所述,本研究进行扇形射束和非共面射束两种计划设计方案的比较,最终结果已经表明Cyber计划更优于Tomo计划,主要体现为:(1)Cyber计划更容易满足AAPM TG101报告中OAR剂量限值标准;(2)非共面射束使靶区边缘跌落更加迅速,周围邻近危及器官能得到更好的保护;(3)射波刀具备呼吸追踪定位功能,不需要GTV外扩形成PTV,显著缩小靶区治疗范围,邻近OAR进一步得到保护。因此,对于中晚期胰腺癌患者,射波刀立体定向放射治疗可作为一种更优的治疗方式供患者选择。

