复方丹参黏附微丸与普通微丸中隐丹参酮与丹参酮ⅡA体外溶出对比研究*
张 强,陈笑南,田湾湾,梁 军,李鹏跃,杜守颖
(北京中医药大学中药学院,北京 100029)
复方丹参制剂作为《中国药典》收载的名优中成药,可用于气滞血瘀所致的胸痹,症见胸闷、心前区刺痛及冠心病心绞痛见上述症状者[1]。复方丹参方由丹参、三七、冰片配伍组成,其中丹参为君药。由于复方丹参方中各有效成分存在体内溶出困难、口服吸收较差、胃肠道内不稳定的问题[2],因此本课题组将其剂型优化为黏附微丸,以期增加复方丹参制剂在体内的滞留时间,提高其生物利用度。结合实验室前期研究[3-4],本实验进一步以丹参酮ⅡA为代表的脂溶性成分为研究对象,对比不同工艺制备的3种不同复方丹参微丸 [冰片包合复方丹参黏附微丸(BI-FDAP)、冰片不包合复方丹参黏附微丸(BE-FDAP)、普通微丸(FDP)]中隐丹参酮与丹参酮ⅡA的体外溶出度,评价复方丹参黏附微丸的缓释作用。
1 材料
1.1 试药 FDP、BI-FDAP、BE-FDAP(实验室自制),隐丹参酮对照品(中国药品生物制品检定研究院,批号:111562-201212),丹参酮ⅡA 对照品(中国药品生物制品检定研究院,批号:110745-201318),乙腈(美国 Fisher公司,色谱级),磷酸[赛默飞世尔科技(中国)有限公司,色谱级],纯净水(杭州娃哈哈集团),其余试剂均为分析纯。
1.2 仪器 LC-20AD型高效液相色谱(HPLC)仪(PDA检测器,日本岛津公司),Sartorius BS 110S型电子分析天平(北京赛多利斯科学仪器有限公司),KQ5200DA型数控超声波清洗器(昆山市超声仪器有限公司),ZRS-8G智能溶出仪(天津天大天发仪器公司),SHB-型水循环多用真空泵(上海振捷实验室设备有限公司)。
2 方法
2.1 复方丹参微丸中隐丹参酮与丹参酮ⅡA含量测定方法的建立
2.1.1 色谱条件 流动相为乙腈(A)-0.05%磷酸(B),梯度洗脱:0~10 min,61%~80%A;10~20 min,80%A;20~25 min,80%~61%A。进样量为 10 μL,检测波长270 nm,流速为1 mL/min,柱温25℃。
2.1.2 对照品溶液的制备 精密称取隐丹参酮4.21 mg置于10 mL容量瓶中,甲醇溶解并定容至刻度,浓度为0.421 g/L;精密称取丹参酮ⅡA 5.24 mg置于10 mL容量瓶中,甲醇溶解并定容至刻度,浓度为0.524 g/L。分别精密移取隐丹参酮、丹参酮ⅡA 2 mL置于10 mL容量瓶中,甲醇定容至刻度,即为混合对照品溶液。
2.1.3 黏附微丸供试品(BI-FDAP与BE-FDAP)溶液的制备 复方丹参黏附微丸研细过80目筛,备用。精密量取5 mL去离子水置于100 mL具塞锥形瓶中,精密称取过筛粉末0.1 g,均匀撒在溶液表面,溶胀6 h,精密量取5 mL甲醇至锥形瓶中,称取质量,超声5 min,重复上述过程3次,第4次加入甲醇后超声30 min,称取质量,补足失重。取5 mL上清液置于离心管中,9 000 r/min离心10 min,上清液过0.45 μm滤膜。
2.1.4 FDP供试品溶液的制备 精密称取微丸细粉(过80目筛)0.1 g,移取25 mL甲醇,称定质量,超声30 min,甲醇补足失重,上清液过0.45 μm滤膜。
2.1.5 方法学考察 1)专属性考察:按照“2.1”项下色谱条件分别检测混合对照品溶液、供试品溶液及阴性样品溶液,色谱图见图1,表明该方法专属性良好。2)线性关系考察:精密吸取对照品储备液,加甲醇稀释配制成系列不同浓度的对照品溶液,测定峰面积。以浓度为横坐标、峰面积为纵坐标,绘制标准曲线,并列回归方程分析。隐丹参酮的回归方程为:Yˆ=38 201X+9 462.9,r=0.999 9。丹参酮ⅡA 的回归方程为Yˆ=45 222X+14 337,r=0.999 9。表明隐丹参酮在 1.648 μg/mL~84.2 μg/mL、丹参酮ⅡA 在2.096~104.8 μg/mL 范围内线性关系良好。3)精密度考察:取混合对照品溶液连续进样6次,测定峰面积,隐丹参酮与丹参酮ⅡA的RSD值为0.48%和0.42%,表明仪器的精密度良好。4)稳定性考察:取复方丹参黏附微丸与FDP供试品溶液,分别于0、1、2、4、8、12 h 测定峰面积。隐丹参酮与丹参酮ⅡA的RSD值均低于3.0%,表明两种成分在12 h内稳定性良好。5)重复性考察:分别按照“2.3”与“2.4”项下供试品溶液制备方法,平行制备6份复方丹参黏附微丸与FDP的供试品溶液,测定隐丹参酮与丹参酮ⅡA的峰面积,计算RSD值。隐丹参酮RSD值分别为3.51%、2.03%、0.37%,基本符合要求。丹参酮ⅡA的RSD值分别为3.14%、1.44%、0.61%,基本符合要求。6)加样回收率考察:取复方丹参微丸研细,过80目筛,备用。精密量取5 mL水置于100 mL具塞锥形瓶中,精密称取过筛粉末0.05 g,均匀撒在溶液表面,溶胀6 h,精密量取5 mL混合对照品甲醇溶液至锥形瓶中,按照供试品溶液制备方法进行操作,隐丹参酮的回收率分别为95.51%、98.34%;丹参酮ⅡA的回收率分别为96.12%、106.15%,均符合要求。
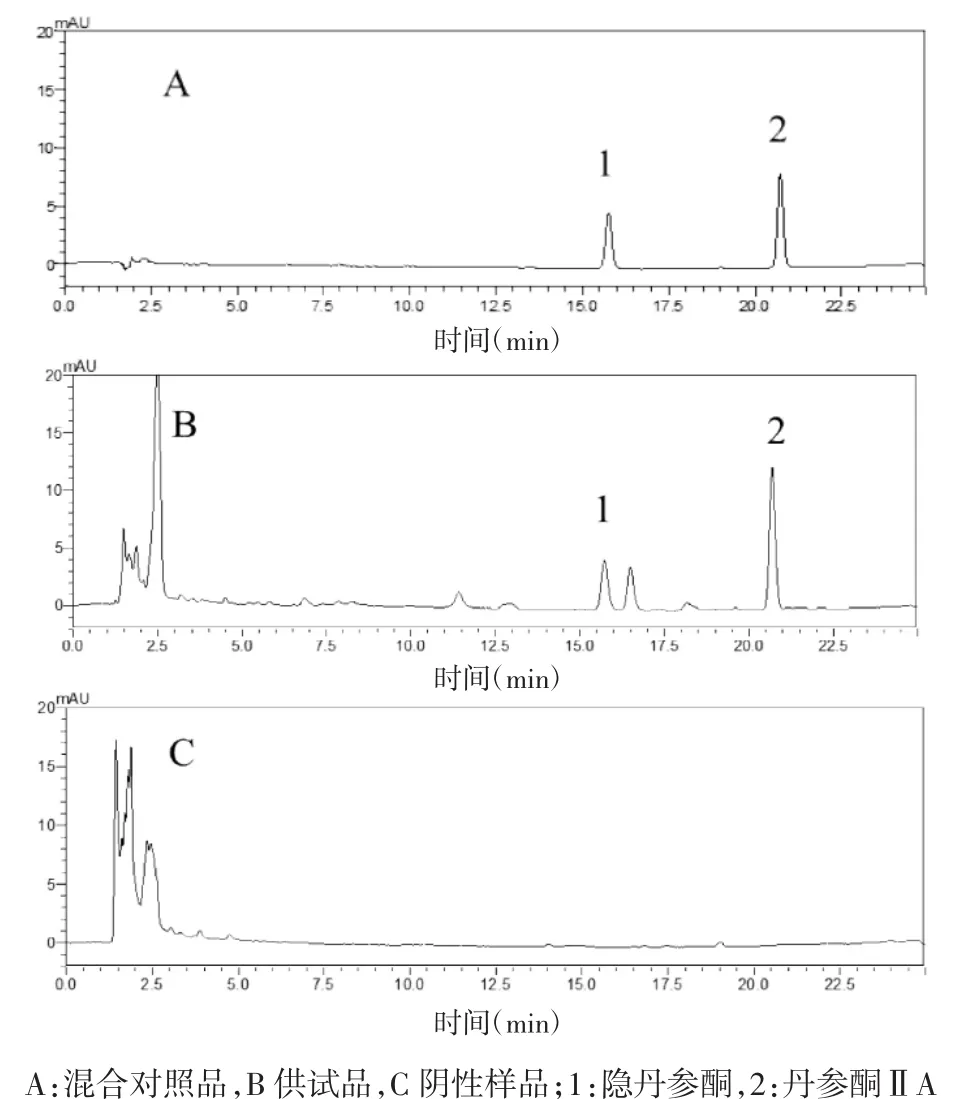
图1 复方丹参微丸中隐丹参酮与丹参酮ⅡA色谱图Fig.1 Chromatogram of cryptotanshinone and tanshinoneⅡA in Fufang Danshen Pellets
2.2 复方丹参微丸中隐丹参酮与丹参酮ⅡA含量测定 按照“2.1”项下建立的含量测定方法分别测定BI-FDAP、BE-FDAP以及FDP中隐丹参酮与丹参酮ⅡA的含量。
2.3 复方丹参微丸中隐丹参酮与丹参酮ⅡA溶出度研究
2.3.1 复方丹参微丸中隐丹参酮与丹参酮ⅡA累积溶出度的研究 实验采用2015版《中国药典》四部溶出度与释放度测定法第一法进行测定[5]。精密称定复方丹参微丸0.8 g,以0.2%十二烷基硫酸钠缓冲液(pH为6.8)为溶出介质,体积为500 mL,转速为 100 r/min,温度(37.0±0.5)℃。分别在 0.5、0.75、1、1.5、2、3、4、6、8、10、12、14 、24 h 取样 1.5 mL,加0.5 mL乙腈涡旋3 min混合均匀,0.45 μm滤膜过滤,每次取样后补加1.5 mL同温度溶出介质,HPLC测定,计算累积释放度。2.3.2 复方丹参微丸中隐丹参酮与丹参酮ⅡA累积溶出度的计算 累积溶出度的计算方法:Qn=500×;累积溶出百分率 (%)=×100%。式中Qn为第n点的累积含量(μg),Cn为第n点测得的药物质量浓度(μg/mL),Ci为第i(i≤n-1)个取样点测得的溶出液中药物质量浓度。
以时间为横坐标,累积溶出度为纵坐标,绘制溶出度曲线。
选择3种溶出动力学模型方程:零级方程、Higuchi方程、Peppas方程,其方程见表1。

表1 拟合模型及方程Tab.1 Fitting models and equations
t表示释药时间,Mt(mg)代表在t时间点累积释药量,M∞(mg)为最大药物累积释放量,Mt/M∞为t时累积释放率。式中k为药物释放速率常数,式中n表示释药参数。Higuchi方程认为药物的释放是基于Fick’s定律的扩散过程(即Fickian扩散),药物从基质中的释放遵循每单位面积的释药量与时间的平方根成正比;Ritger-Peppas模型中,可根据n分析成分的释放机制。Peppas方程中n<0.43,符合Fickian 扩散释药机制,n>0.85,符合溶蚀机制,0.43~0.85间,扩散和溶蚀并存。对溶出实验数据进行溶出方程拟合,探讨3种制剂中隐丹参酮与丹参酮ⅡA的体外释药机制。
2.3.3 3种制剂中隐丹参酮与丹参酮ⅡA相似因子分析 相似因子是根据溶出数据计算出的分析相同成分不同条件下溶出行为是否具有相似性的数据处理方式。计算公式如下Tt)2](-0.5)×100},其中,Rt及 Tt分别为 t时间参比及受试制剂累积溶出率,n为取点数目。
3 结果
3.1 复方丹参微丸中隐丹参酮与丹参酮ⅡA含量测定结果 隐丹参酮与丹参酮ⅡA在3种复方丹参微丸中含量测定结果见表2。
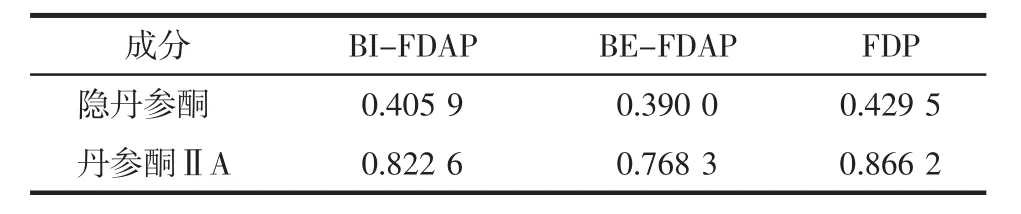
表2 3种微丸中隐丹参酮与丹参酮ⅡA含量测定表Tab.2 Contents of cryptotanshinone and tanshinoneⅡA in three kinds of pellets mg/g
3.2 溶出实验结果 3种复方丹参微丸中隐丹参酮与丹参酮ⅡA溶出曲线与最佳拟合方程见图2。两种黏附微丸中,隐丹参酮的溶出趋势较为平缓,与FDP相比呈现出一定的缓释作用。3种微丸中隐丹参酮的最终累积溶出度分别为(40.34±3.01)%、(42.41±1.37)%、(64.05±4.06)%。丹参酮ⅡA 在3个复方丹参制剂中溶出均比较缓慢,3种微丸的溶出曲线接近重合,BI-FDAP、BE-FDAP、FDP的累积溶出 度 分 别 为 (44.08±2.83)% 、(42.03±0.92)% 、(45.68±5.22)%,最终溶出度基本一致,溶出曲线仍呈上升趋势。

图2 3种微丸中隐丹参酮与丹参酮ⅡA体外溶出曲线Fig.2 Dissolution curve of cryptotanshinone and tanshinone IIA in vitro in three kinds of pellets
溶出曲线的最佳拟合方程见表3。结果显示,隐丹参酮在两种黏附微丸的溶出行为更符合Higuchi方程,FDP中更符合Peppas模型,且n<0.45,因此隐丹参酮在3种制剂中均符合Fickian扩散。丹参酮ⅡA在3种微丸中的溶出行为更符合Higuchi方程,属于Fickian扩散。
3.3 相似因子分析结果 3种复方丹参微丸中隐丹参酮与丹参酮ⅡA相似因子(f2)分析结果见表4。一般认为,f2值越接近100,相似程度就越高。当f2值在0~50时,认为两制剂体外溶出行为有显著性差异,f2值≥50即可认为两者的溶出过程一致。隐丹参酮的溶出行为两种黏附制剂更为相似,相似因子 68.31;BI-FDAP与 FDP的相似因子为 30.06;BE-FDAP与FDP的相似因子为36.36,表明隐丹参酮在黏附微丸和FDP的溶出具有明显差异。丹参酮ⅡA在3种制剂中两两制剂间相似因子均大于60,BI-FDAP与BE-FDAP相似因子为60.76;BI-FDAP与FDP相似因子为76.48;BE-FDAP与FDP相似因子为63.59,3种复方丹参微丸中丹参酮ⅡA的溶出行为无差异。

表3 3种微丸中隐丹参酮与丹参酮ⅡA溶出曲线拟合方程Tab.3 Fitting equation for the dissolution curve of cryptotanshinone and tanshinoneⅡA in three kinds of pellets
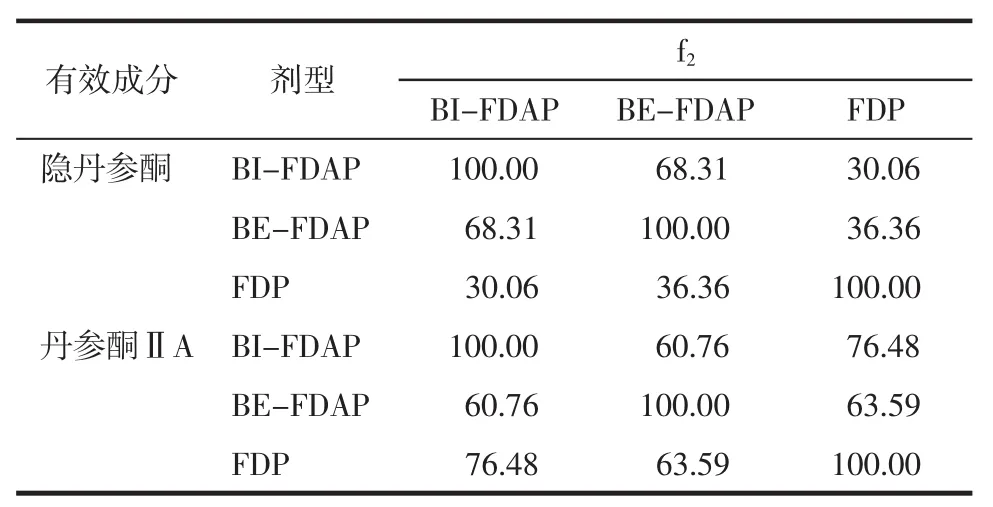
表4 3种微丸中隐丹参酮与丹参酮ⅡA体外溶出相似因子比较Tab.4 similar factors in vitro dissolution of cryptotanshinone and tanshinone IIA in three kinds of pellets
4 讨论
为了解决复方丹参制剂在体内生物利用度低的难题,本课题组经过剂型优化将其制备为复方丹参黏附微丸,并对其黏附性能进行评价,表明制备的黏附微丸可以延长在体内的滞留时间[6]。为了进一步阐明复方丹参黏附微丸的缓释作用,实验室前期以复方丹参片为参比制剂,分别对比冰片中龙脑、三七中三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1、人参皂苷Rd及丹参中丹酚酸B、丹参酮ⅡA在复方丹参黏附微丸中的体外溶出度,同样表明复方丹参黏附微丸具有一定的缓释作用[3-4]。本实验排除了片剂与微丸的干扰因素,进一步以复方丹参FDP为参比制剂,对比丹参中脂溶性成分在黏附微丸中的体外溶解度,更加准确地评价黏附微丸的缓释作用。
由溶出实验结果可知,3种制剂中丹参脂溶性成分隐丹参酮与丹参酮ⅡA的累积溶出度均较低,原因是由于两者为脂溶性成分,在水中溶解度较小。因此在其溶出介质加入十二烷基硫酸钠以增加其在体外的溶出量,考虑十二烷基硫酸钠为表面活性剂,液相色谱柱为十八烷基,实验表明当测试样品中含有表面活性剂且样品量较大时,经多次测定,表面活性剂会在色谱柱的筛板及硅胶的表面形成一层膜,进而影响色谱柱的效能,可能造成色谱峰变宽、拖尾等后果,为降低十二烷基硫酸钠对色谱柱的影响,本实验选择了低浓度的十二烷基硫酸钠溶出介质(0.2%十二烷基硫酸钠),同时样品经过乙腈稀释,进一步降低样品中十二烷基硫酸钠的浓度。
对比的3种不同工艺制备的微丸中,丹参类脂溶性成分隐丹参酮与丹参酮ⅡA在两种黏附微丸中的溶出曲线基本重合,其溶出行为无明显差异。而与FDP的比较发现,隐丹参酮的f2<50,表明FDP与黏附微丸存在明显的差异性,黏附微丸表现出明显的缓释作用。而丹参酮ⅡA的溶出曲线3种制剂基本重合,制剂间的f2>50,表明FDP与黏附微丸溶出行为一致。
隐丹参酮在黏附微丸与FDP中溶出过程的差异,可能与加入的黏附材料有关。黏附制剂是指在原有制剂工艺的基础上加入黏附材料,利用其独特的黏附性能增加药物在体内的滞留时间,从而延长在体内的吸收,提高药物生物利用度的一种给药系统[7]。课题组选定卡波姆934P、壳聚糖和羟丙基甲基纤维素(HPMC K100M)为黏附材料[8],制备黏附微丸。这3种材料均具有一定的黏附性能,郭莹等[9]使用卡波姆934P与乙基纤维素共同作为黏附材料制备的葛根素黏附微球生物黏附性良好。黎迎等[10]以壳聚糖作为黏附材料制备的三七总皂苷生物黏附微丸黏附性良好。上官盈盈等[11]使用羟丙基甲基纤维素制备口腔黏附片,其黏附性能良好。
丹参酮ⅡA与隐丹参酮为丹参中的脂溶性成分,而丹参酮ⅡA在黏附微丸与FDP的溶出行为比较差异不大,即黏附微丸的缓释作用对于丹参酮ⅡA不明显。其原因可能为丹参酮ⅡA本身的溶出较困难,1 h的累积溶出度不到10%,4 h的累积溶出度仅为20%左右,较低的溶出度成为限制溶出行为的主要因素,无法体现出黏附微丸的缓释作用。结合实验室前期体内药动学研究,比格犬口服复方丹参黏附微丸后,丹参酮ⅡA与隐丹参酮的药时曲线下面积(AUC)均明显高于FDP,黏附微丸的生物利用度明显提高,体内滞留时间增长表明黏附微丸具有缓释作用。
本实验建立了测定不同工艺制备的复方丹参微丸中隐丹参酮与丹参酮ⅡA含量测定方法以及其体外溶出度的考察方法,并对3种微丸(BI-FDAP、BE-FDAP、FDP)中隐丹参酮与丹参酮ⅡA的体外溶出度进行对比,对黏附微丸的缓释作用进行评价。结果表明与FDP相比,复方丹参黏附微丸具有一定的缓释作用,为制备提高复方丹参生物利用度的新型制剂提供了依据。此外,由于脂溶性成分溶出度低的特性,在评价其黏附作用时,结合体内及体外数据会更加全面。

