奎宁的热解机理、动力学及贮存期研究
肖卓炳,宋 科,刘建兰,田春莲
吉首大学 林产化工工程湖南省重点实验室,张家界 427000
奎宁,是一种天然的生物碱类(Alkaloids)化合物,无臭味,微苦,易溶于乙醇、氯仿、乙醚中,微溶于水和甘油,主要存在于茜草科植物金鸡纳树及其同属植物的树皮中,占树皮生物碱总量的70%,故又名金鸡纳碱[1]。1817年,法国药剂师Caventou和Pelletier合作从金鸡纳树皮中分离得到了奎宁单体,后来被证实就是存在于金鸡纳树皮中的抗疟疾有效成分[2]。到目前为止,疟疾仍是全球儿童致命的疾病之一[3]。奎宁的抗疟活性主要表现在,能影响疟原虫的生长和繁殖[2-4];抑制原虫的蛋白合成[5];干扰其糖代谢[6]。除了抗疟作用外,奎宁还可用于治疗免疫失调类疾病[7,8],如红斑狼疮、类风湿性关节炎。另外,2004年美国FDA批准奎宁用于治疗口腔和咽喉疾病以及癌症[9]。国内外对其药理、提取、分离纯化、化学合成、含量检测等均有大量研究,但未见有对其热稳定性及其分解机理进行研究。鉴于在新药开发和临床应用中的重要性,探讨奎宁的热稳定性规律、揭示其降解机理,能够为改进提取和合成工艺、选择合适剂型、提高制剂质量、药物的合理使用等提供重要科学依据[10-12]。
1 材料方法
1.1 样品
奎宁标准品,由西安飞达生物技术有限公司提供,纯度在99%以上。
1.2 实验方法
1.2.1 热重分析
热重分析实验在德国NETZSCH 公司的 STA-409-PC 型同步热分析仪上进行。称取8~10mg奎宁晶体粉末,采用10 ℃/min的线性动态升温速率从室温升至800 ℃,同时以高纯度动态氮气作为保护气体,氮气的流量为35 mL/min,以配套的70 μL氧化铝制陶瓷坩埚盛样。测试过程中热分析系统自动采集数据,同时得到样品的热重(TG)曲线和微分热重(DTG)曲线。
1.2.2 傅里叶红外光谱分析
热分解逸出气体的红外光谱由德国Bruker公司的TENSOR 27型傅里叶变换红外光谱仪检测,将升温过程产生的气体经传输管(保持毛细传输管温度在220~250 ℃之间)导入红外光谱仪气体检测腔(输气线路及光谱仪气室均保持200 ℃),在4 000~600 cm-1之间扫描逸出气体的红外光谱。
1.3 热分析动力学方法
本研究采用普适微分Achar法和积分Coats-Redfern法同时对热重数据和微分热重数据进行动力学分析[12,13],两者所采用的方程如下所示:
(1)
(2)
式中:g(α)—积分形式机理函数;f(α)—微分形式机理函数;T—热力学温度,K;Ea—表观活化能,kJ/mol;A—指前因子,min-1;R—气体常数,J/(mol·K);β—升温速率,K/min;α—转化分数。
分别以ln[g(α)/T2]对1/T和ln[dα/dt/f(α)]对1/T作图,采用最小二乘法进行线性回归可得到一条直线,从截距和斜率可求算出活化能(Ea)和指前因子(A)。
2 结果与分析
2.1 奎宁的热解机理推断
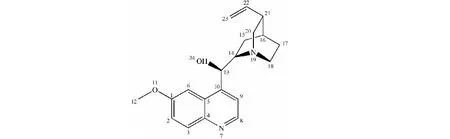
图1 奎宁分子的结构Fig.1 Molecular structure of quinine
图1为奎宁分子的平面结构。由图2(a)所示,奎宁在219.93 ℃之前,热重曲线和微分热重曲线一直都平滑无降低,说明在此之前奎宁一直处于稳定状态而未分解。219.93 ℃之后,TG曲线和DTG曲线开始降低,奎宁开始发生分解,热分解共分为两步,第一步由219.93 ℃至389.93 ℃,结合实验失重率58.67%(见图2(a)和表1)初步推断化学键断裂情况[13-16],推断可能首先是O11-C12、C13-O24这两个化学键的断裂,其次与C10相连支链上的原子相继发生断裂,这些化学键断裂形成小分子气体逸出,造成的理论失重率为55.26%,与实验失重率相吻合;第二步分解在389.93 ℃开始,一直到800 ℃时结束,该过程TG曲线下降缓慢,而DTG曲线基本保持水平,主要是残余骨架中苯并吡啶环的深度裂解碳化造成的缓慢失重过程,过程将产生大量挥发性气体产生,而残留物中的氢和氧受热继续分离[17]。
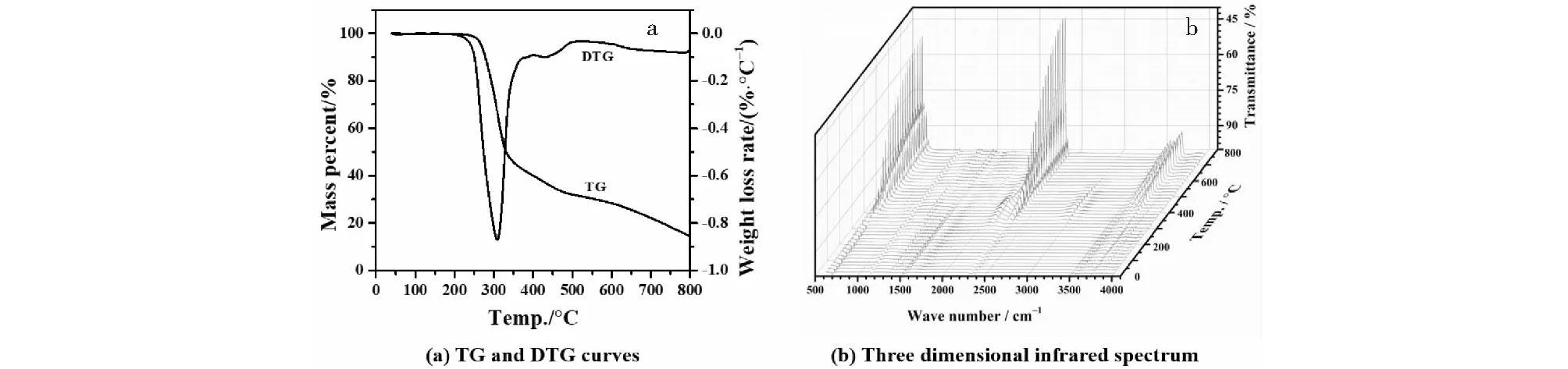
图2 奎宁晶体在10 ℃/min下测定的(a)热重-微分热重曲线和(b)热分解过程逸出气体的三维红外光谱图Fig.2 (A) TG and DTG curves at 10 ℃/min of quinine and (B) three dimensional infrared spectrum of evolved gases from the thermal decomposition

表1 奎宁各步热分解的特征参数
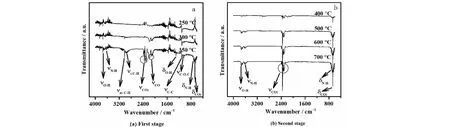
图3 奎宁(a)第一步和(b)第二步热分解过程中不同温度下的逸出气体的红外光谱曲线Fig.3 Infrared spectrum of evolved gases from the thermal decomposition of quinine (A) at first stage and (B) at second stage
图2b为奎宁热分解时逸出气体随温度变化的红外吸收光谱,分别选取250、300、350 ℃处的红外光谱解析第一步分解时逸出气体的官能团,经解析其主要的波数、振动类型及对应的吸收基团(见图3a),首先温度低于300 ℃时,检测到O-H(3 741 cm-1)、C-H(2 954~3 019 cm-1)和CO(2 102~2 183 cm-1)等官能团的伸缩振动峰,印证了之前推断奎宁第一步分解分子中O11-C12、C13-O24这两个化学键的优先断裂的推断,它们在断裂之后形成了醇类和CO;当温度为350 ℃时,除了发现上述官能团振动并进一步增强外,还检测到CO2(2 305~2 362 cm-1,667 cm-1)、N-H(3 627 cm-1,715 cm-1)和C-O-C(1 056 cm-1)的伸缩振动和弯曲振动,说明与C10相连支链上的原子相继发生断裂并裂解,形成了CO、CO2、醇类、醚类和胺类等物质。选取400 ℃、500 ℃、600、700 ℃处的红外光谱解析第二步分解时逸出气体的官能团,这四个温度处的吸收峰波数基本相一致,仅随时间的增加对应吸收处的吸光度增大,说明它们为同一种类气体,产自同一步骤的热解,仅检测到O-H(3 741 cm-1)、N-H(3 627 cm-1,715 cm-1)和CO2(2 305~2 362 cm-1,667 cm-1)等简单基团的伸缩振动和弯曲振动峰,印证了该步骤属于残余骨架中苯环、吡啶环的深度裂解碳化过程,形成了CO2、H2O、NH3等气体。至此,如图4所示,奎宁的热解过程可以做以下描述。

图4 不同温度范围内奎宁热分解机理推断Fig.4 Inference for the thermal decomposition mechanism of quinine at various temperatures
2.2 热解动力学
2.2.1 最概然动力学模型
由于奎宁晶体在219.93~389.93 ℃之间,晶体分子中与苯并吡啶环相连基团的化学键先后发生了断裂,先后释放了醇类、CO、CO2、醚类、胺类等物质,且分解失重速度快;在第二步失重即389.93 ℃之后的区间中,残余分子骨架中苯并吡啶环的深度裂解碳化过程较为缓慢,且无明显的失重台阶和微分失重峰,过程较复杂。因此本研究对第一步(219.93~389.93 ℃)分解进行动力学分析。
采用普适Achar法和Coats-Redfern法对10 ℃/min的TG-DTG曲线进行动力学处理,微分法和积分法两者的计算可以同时进行,相互印证,所需数据如表2所示。
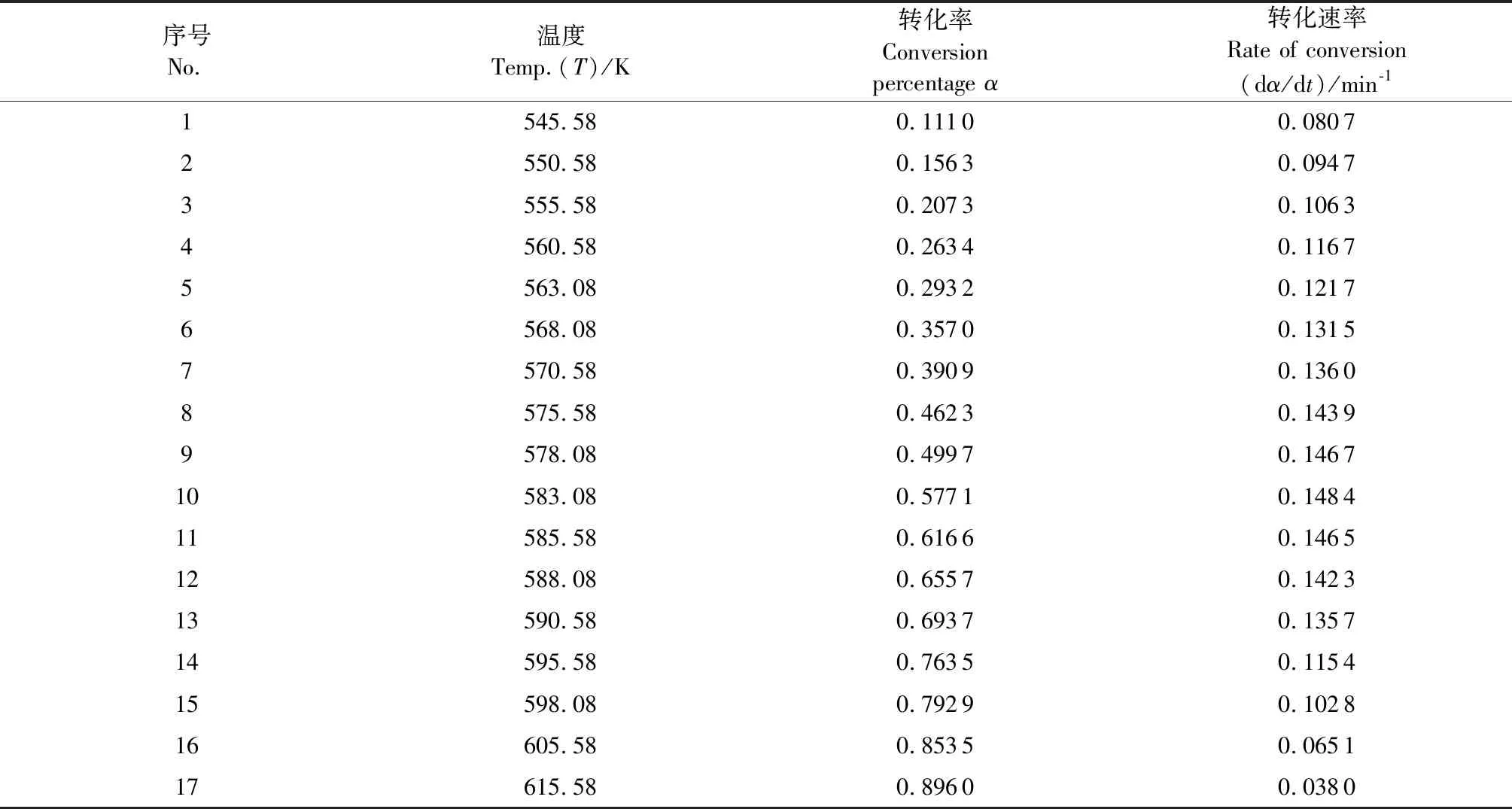
表2 采用Achar、Coats-Redfern法计算所需的失重数据 (β=10 ℃/min)
将表2中数据T、α、dα/dt代入40种常用机制函数[18,19],求得对应的f(α)和g(α)的值,再代入积分法Coats-Redfern方程和微分法Achar方程,经最小二乘法线性拟合,计算出Ea、lnA和r,数据见表3。当线性相关性较好(接近1),两种方法所得Ea和lnA最为接近时,所对应编号的机制函数即为该反应最可能的反应机制函数,相应的Ea和A即为该反应的活化能和指前因子。

表3 采用Coats-Redfern、Achar法求得的具有较好线性相关的动力学参数 (β=10 ℃/min)
由表3所示,经过40组函数模型的线性回归分析,发现奎宁分子第一步分解只有5组模型的相关性比较好(接近于1),因此奎宁热分解最可能的机制函数将在这几组函数模型中产生。
2.2.2 动力学三因子
将表3中Achar法和Coats-Redfern法计算所得两组数据对比可知,当失重机制函数为36号时,不但线性相关性较好(r接近于1),而且两种方法所得Ea和lnA最为接近。
表4比较了在不同方法所得动力学参数,可以确定奎宁第一步热分解为化学反应控制机制,符合反应级数方程,反应级数n=2,Ea=159.85kJ/mol,lnA=32.79,f(α)=(1-α)2,g(α)=(1-α)-1-1。

表4 奎宁的热分解动力学参数
2.3 奎宁贮存期的推断
根据求算得到的奎宁晶体第一步分解时的表观活化能Ea和指前因子A,则在一定反应温度Tc下的反应速率常数k=Ae-Ea/RTc,进一步求算得到分解反应速率常数k的负对数值pk。在贮存温度(室温25 ℃)下,根据药品pk值和药品商品规定贮存期的相关性,即pk<7.5的区间内,贮存有效期为1.5~2a;在7.5
经计算在室温下(25 ℃)贮存,奎宁降解反应速率常数的负对数pk为13.76,处于pk>10.5的区间内,进而推断奎宁的贮存期为4~5a。
3 结论
通过热重-红外联用分析并结合量子化学计算,可知奎宁晶体的热分解分两步,第一步从219.93 ℃到389.93 ℃,奎宁晶体分子中与苯并吡啶环相连基团的化学键先后发生了断裂,先后释放了醇类、CO、CO2、醚类、胺类等物质,且分解失重速度快;第二步从389.93 ℃至800 ℃,残余分子骨架中苯并吡啶环的深度裂解碳化过程较为缓慢,且无明显的失重台阶和微分失重峰,形成了CO2、H2O、NH3等气体,分解机理经热重数据和红外光谱解析对比能够相互验证,吻合。通过对奎宁第一步分解过程的热分析数据进行动力学分析,发现微分Achar法与积分Coats-Redfern法的结果相互验证,基本一致,可以确定第一步热分解为化学反应控制机制,符合反应级数方程,反应级数n=2,Ea=133.16kJ/mol,lnA=29.17,f(α)=(1-α)2,g(α)=(1-α)-1-1。最终,根据奎宁的热分解动力学参数推断在室温(25 ℃)下,奎宁的贮存期为4~5a。此结果可以为目前大量含奎宁药品的质量监控和评价提供依据。

