离心分离大质量数差混合物的实验研究方法
潘建雄,周明胜,裴 根,姜东君,孙启明
(清华大学 工程物理系,北京 100084)
气体离心法作为一种能耗低、分离系数大、规模灵活的分离方法,现已成功应用于工业化生产浓缩铀和稳定同位素分离[1-3]。利用离心法生产同位素产品时,工作介质一般要求为纯净物。针对离心分离混合物,国内外学者开展了相关研究。1980年前后,Fuhse[4]、Kai[5]、Makihara等[6]开展了离心分离气体混合物的研究,探究了小分子量气体对离心分离性能的影响。2004年,郑直[7]基于双组分气体模型,对相对分子质量相差大的混合气体的流场、丰度场进行了数值研究。2006年,张彤等[8]、贾兴国等[9]利用数值模拟的方法,研究了小分子量气体对离心级联中组分分布情况的影响,并提出通过附加供料氟利昂C6F12的方式,可实现用离心级联净化原料的目的。2014年,Cheltsov等[10]以SF6为介质,利用离心级联生产硫同位素,通过级联的多次分离,有效去除了S2F10,获得了超纯SF6产品。
在实际中,由于混合物中重气体组分与轻气体组分性质接近,较难通过其他方法分离,因此难以测定轻、重气体组分的分离效果。本文尝试寻找容易分离的轻、重气体组分作为混合物分离介质,通过实验获得轻、重气体组分的分离效果,以评估混合物的离心分离性能。
1 离心分离介质的选取
气体离心法的分离介质需满足一定的要求[11],经过对不同气体物性参数的调研[12-14],选取了2组轻、重气体介质。第1组,C7F14作为重气体组分,SF6、Xe作为轻气体组分;第2组,CCl3F作为重气体组分,C2H4作为轻气体组分。
1.1 C7F14和SF6/Xe
C7F14的相对分子质量为350.05,常温下为无色、透明、低沸点的液体,无腐蚀性,稳定性好,570 K温度下不分解。天然C7F14同位素组成及其丰度列于表1,由于氟只有1种稳定同位素,碳有2种稳定同位素(14C含量微小,不作考虑),故主要的同位素组分为12C7F14和12C613CF14,其他同位素组分丰度很小,可视为二元分离。

表1 天然C7F14的同位素组成Table 1 Isotopic component of natural C7F14
SF6的相对分子质量为146.06,Xe的相对分子质量为131.29。SF6、Xe化学性质稳定,具有热稳定性、无毒、无腐蚀性,适合用于离心分离。
在-100 ℃下,C7F14为固态,饱和蒸气压几乎为0,而此温度下,SF6的饱和蒸气压为5.3 kPa,Xe的饱和蒸气压为157.9 kPa,通过调制-100 ℃的酒精/液氮混合物能将轻、重气体组分顺利分开。
1.2 CCl3F和C2H4
CCl3F即氟里昂-11,相对分子质量为137.37,与某些稳定同位素离心分离介质(GeF4、BCl3)的相对分子质量接近,且化学性质不活泼、较稳定,是一种廉价的制冷剂,可作为稳定同位素离心分离介质的模拟介质。
C2H4的相对分子质量为28.06,化学性质稳定,价格低廉,且易获取。
在-115 ℃下,CCl3F为固态,饱和蒸气压为4 Pa;C2H4为气态,饱和蒸气压为49.9 kPa。通过调制-115 ℃的酒精/液氮混合物能轻松将二者分开。
2 混合气体离心分离实验装置
2.1 单机分离实验平台
利用实验室现有的包含国产离心分离专用设备在内的单机分离实验平台,开展了混合气体离心分离实验,其原理如图1[2]所示。
在常温下,将离心分离介质通入专用设备,为保证供料流的稳定性,在供料瓶处并联一稳压容器。利用液氮冷阱收集专用设备分离出的精、贫料。由于混合气体分离的特点,单机分离实验得到的精、贫料均为轻、重气体组分的混合物,需在分离实验结束后进行分馏操作,将轻、重气体相对分开后再进行取样。

图1 单机分离实验平台原理示意图Fig.1 Schematic diagram of single centrifugal experiment system
2.2 分馏装置
通过采用分馏法彻底分开精、贫料中的轻、重气体组分,以获得各组分气体的含量。本文建立的分馏装置示意图如图2所示。为达到较好的分馏效果,设计了分馏取样流程。以C7F14/SF6混合介质为例,分馏取样流程如下。
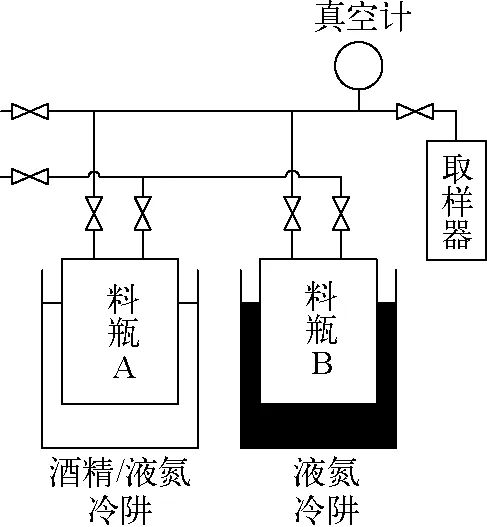
图2 分馏装置示意图Fig.2 Schematic diagram of fractional distillation unit
1) 将待分馏的C7F14/SF6混合介质利用液氮冷冻在料瓶A中;
2) 利用-100 ℃的酒精/液氮混合溶液初步解冻料瓶A,将挥发出的SF6气体用液氮冷冻收集到料瓶B中,此时C7F14仍冷冻在料瓶A中;
3) 待料瓶A中的SF6完全转移到料瓶B后,对料瓶进行解冻;
4) 在相同体积、相同温度下测量料瓶A、B中的气体压强并取样。
测得的压强比即为混合气体中C7F14和SF6的摩尔比。
3 基本全分离系数/全净化系数计算
根据Kai所提出的多元分离系数定义[15-16],任意两组分i、j之间的全分离系数γij为:
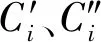
针对混合物分离,借鉴二元离心分离理论中分离系数的定义,引入全净化系数Df作为表征净化效果的参数。定义精料混合气体中轻气体组分的质量分数为xP,贫料混合气体中轻气体组分的质量分数为xW。全净化系数Df由下式定义:

4 混合气体离心分离实验
4.1 C7F14/SF6混合气体分离实验
以SF6摩尔含量为20%的C7F14/SF6混合气体为供料,通过改变供料流量、分流比θ等流体参数,进行了一系列单机实验,实验结果列于表2。由表2可知:1) 单独考虑C7F14、SF6组分的分离,二者的基本全分离系数均低于作为单一工作介质时的基本全分离系数;2) 综合考虑混合气体的分离,C7F14/SF6混合气体的全净化系数在6附近,随供料流量的增大,全净化系数变小。

表2 C7F14/SF6混合气体单机分离结果Table 2 Experimental result of C7F14/SF6 mixture
4.2 C7F14/Xe混合气体分离实验
以Xe摩尔含量为20%的C7F14/Xe混合气体为供料,选取供料流量为30 g/h、分流比为0.5进行对比实验,实验结果列于表3。由表3可知:1) 与C7F14/SF6混合气体分离实验类似,单独考虑C7F14、Xe组分的分离,二者的基本全分离系数均低于作为单一工作介质时的基本全分离系数;2) 相比C7F14/SF6混合气体,C7F14/Xe混合气体轻、重组分相对分子质量相差更大,混合气体的全净化系数明显增大,能达到12.19。

表3 C7F14/Xe混合气体单机分离结果Table 3 Experimental result of C7F14/Xe mixture
4.3 CCl3F/C2H4混合气体分离实验
为探究平均分子量较小的混合气体离心分离性能,进行了CCl3F/C2H4混合气体离心分离实验,以C2H4摩尔含量为10%的混合气体为供料,实验结果列于表4。由表4可知:1) C2H4相对分子质量小,离心分离C2H4效果不明显;2) CCl3F和C2H4的相对分子质量相差较小,CCl3F/C2H4混合气体的全净化系数均低于C7F14/SF6混合气体和C7F14/Xe混合气体。在分流比为0.5的情况下,CCl3F/C2H4混合气体的全净化系数可达5.27。
综合以上3组混合气体分离实验分析,二元混合气体的全净化系数远大于纯净气体的同位素分离系数,混合物中气体组分间相对分子质量相差越大,全净化系数越大;混合气体组分的离心分离系数低于单一介质离心分离时的系数。
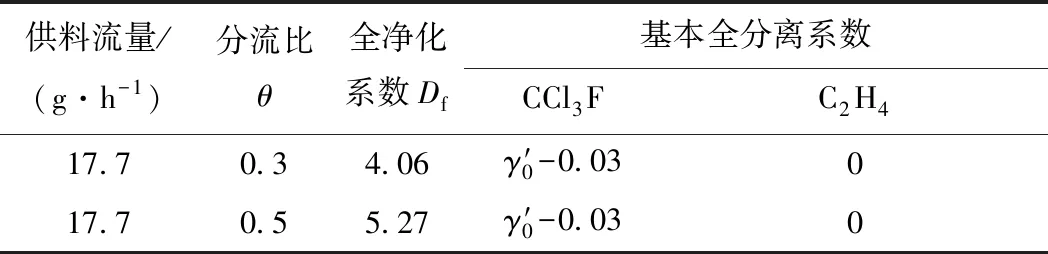
表4 CCl3F/C2H4混合气体单机分离结果Table 4 Experimental result of CCl3F/C2H4 mixture
5 结论
本文提出了一种实验方法,即通过使用易于分离的轻、重气体组分作为离心介质,来评估离心分离混合物性能,并引入全净化系数的概念,评估组分气体间的分离效果。该实验方法能得到二元混合气体的全净化系数及其各自组分的基本全分离系数。通过开展C7F14/SF6、C7F14/Xe、CCl3F/C2H4混合气体离心分离实验,验证了该实验方法的可行性。从已有的实验结果可发现。
1) 二元混合气体的全净化系数大。重气体组分更多地进入贫料,轻气体组分更多地进入精料,使得最终精、贫料中轻气体组分含量较供料发生明显变化。
2) 离心分离混合气体中,两种轻、重气体组分的基本全分离系数均低于各自单独分离时的基本全分离系数。对于任一组分,另一种组分的混入会降低该组分的离心分离效果。
针对离心分离混合物,可运用本方法开展更为系统的实验研究。

