吗啉的CO2吸收及核磁共振波谱实验研究
陆未央,王淑娟,Qi Yang
吗啉的CO2吸收及核磁共振波谱实验研究
陆未央1,王淑娟1,Qi Yang2
(1. 清华大学能源与动力工程系,北京 100084;2. CSIRO Manufacturing Flagship,Clayton VIC 3168,Australia)
吗啉(MOR)是一种环状胺,具有作为CO2吸收剂的潜力.本研究对吗啉溶液进行CO2吸收实验和核磁共振(NMR)波谱实验,通过吸收容量及不同CO2担载下NMR图像的变化规律,反映MOR-CO2-H2O系统化学反应的变化趋势,评价MOR溶液的吸收表现.吸收实验结果表明MOR的吸收容量为0.48mol CO2/mol胺,与5M MEA的结果接近.定量NMR实验结果反映了各组分峰的化学位移及变化规律.定量13C NMR实验结果表明系统各组分的摩尔分数变化规律符合反应机理假设.
吗啉;CO2捕集;吸收容量;核磁共振波谱
在化学吸收法捕集CO2的研究中,为解决传统吸收剂乙醇胺(MEA)高再生能耗、易降解等问题[1-2],寻找吸收性能和稳定性更好的吸收剂是一大研究方 向[3].哌嗪(PZ)的反应速率远高于MEA,被广泛应用于有机胺吸收剂的添加剂或者混合吸收剂的组分,以提高吸收剂的吸收速率[4-5].吗啉(MOR)是一种结构与PZ接近的环状胺,与PZ具有相似性质.PZ与MOR的结构如图1所示.MOR具有高热稳定性,反应速率常数约为MEA的3倍,低于PZ[6],因此MOR是一种有潜力的CO2吸收剂.
本文对MOR溶液进行CO2吸收实验,对富液进行滴定和核磁共振(NMR)波谱实验.通过吸收容量及不同CO2担载下NMR图像的变化规律,反映MOR-CO2-H2O系统化学反应的变化趋势,评价MOR溶液的吸收表现.MOR为环状二级胺,本研究关注的MOR吸收CO2的总包反应为式(1)和(2)[7],系统首先生成氨基甲酸盐MORCOO-和质子化胺MORH+,当CO2担载增大时开始生成碳酸氢盐HCO3-.
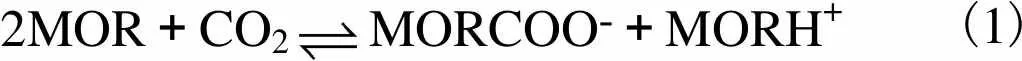
2MOR+CO2MORCOO-+MORH+(1)

MOR+CO2+H2OHCO3-+MORH+(2)
1 实验方法
1.1 实验药品及仪器
CO2吸收实验采用Sigma-Aldrich公司生产的99%纯度的MOR和BOC公司生产的99.9%纯度的CO2.滴定实验采用Sigma-Aldrich公司生产的1.18M的HCl溶液以及0.1%浓度的甲基橙指示剂,采用OAKLON公司生产的pH计测量溶液的pH值.NMR实验采用Bruker Avance Ascend 400核磁共振波谱仪及其标准样品重水-1,4-二氧六环,其结构如图2所示.
图2 标准样品重水-1,4-二氧六环的结构
1.2 实验装置
CO2吸收实验的实验装置如图3所示.将反应器置于水浴加热系统,通入CO2气体,将磁力转子置于反应器内进行搅拌,气体经吸收后排出反应器.吸收剂为2M MOR,通入纯CO2气体,气体流量为20mL/min,反应温度为40℃,磁力搅拌装置转速为900r/min.反应器入口和出口分别连接补水装置和冷凝管,以保持反应器内的水平衡.
滴定实验的实验装置如图4所示.采用1.18M的HCl溶液以及0.1%浓度的甲基橙指示剂滴定待测样品,直到酸与有机胺恰好完全反应,吸收实验中吸收的CO2被释放出来.带有色溶液的滴定管5与反应器和连通器相连,待滴定步骤结束后打开阀门测量CO2体积.连通器为敞口容器,读取滴定管5的示数前调整连通器高度使得有色溶液的液面平齐,HCl滴定前后滴定管5的示数之差即为CO2体积.

1—CO2气瓶;2—补水装置;3—反应器;4—磁力搅拌装置;5—水浴加热系统;6—冷凝管

1—HCl滴定管;2—反应器;3—磁力搅拌装置;4—阀门;5—带有色溶液的滴定管;6—连通器
1.3 实验步骤
配置100mL的2M MOR溶液,取50mL进行CO2吸收实验,其余50mL新鲜溶液用于后续实验步骤.将MOR溶液置于CO2吸收实验装置反应器,控制反应温度保持40℃,通入纯CO2气体,气体流量为20mL/min,进行反应18h至溶液饱和.分别取定量的富液和新鲜溶液混合,配置不同CO2担载的溶液.各样品的溶液配比如表1所示,其中新鲜溶液为0号样品,富液为10号样品,CO2担载随编号增大而增大.
从各样品中取5mL溶液进行滴定实验,再取少量溶液进行NMR实验.将样品加入滴定实验装置反应器,加入0.1%的甲基橙指示剂.保持阀门关闭,滴入1.18M的HCl溶液开始滴定,当待测溶液恰好变为粉色时滴定结束,再加入过量酸保证样品吸收的CO2充分释放.读取滴定前后滴定管5的示数即可获得CO2的体积.通过式(3)~(6)可从滴定实验结果计算样品的CO2担载.
表1 滴定及NMR实验所采用的样品溶液配比
Tab.1 Solution ratios used in titration and NMR experiment

样品编号012345678910 富液/mL00.91.82.73.64.55.46.37.28.19.0 新鲜溶液/mL9.08.17.26.35.44.53.62.71.80.90
式中:amine为胺的摩尔数;acid为酸的浓度;acid为恰好完全反应时酸的体积;为压力;为CO2的体积;为CO2的摩尔数;为理想气体常数;为温度;5为滴定前后滴定管5的示数变化;acid,total为加入酸的总体积;为CO2担载.
NMR实验采用标准样品重水-1,4-二氧六环,测量各样品的1H和定量13C NMR图谱,即以定量13C NMR图谱各组分的峰面积计算溶液各组分的摩尔比.NMR实验的操作参数为共振频率400.13MHz (1H)和100.62MHz(13C),采样32次,扫描前延迟3.73s.
2 结果与讨论
2.1 各样品的CO2担载与pH值
滴定及NMR实验中各样品的CO2担载和溶液pH值如表2所示.结果表明MOR的吸收容量为0.48mol CO2/mol胺,与5M MEA的结果接近[8].随着CO2担载的增大,溶液pH值从11.37逐渐减小到8.15.
表2 滴定及NMR实验所采用的样品的CO2担载和pH值

Tab.2 CO2 loading and pH of the solutions used in titration and NMR experiment
2.2 定量13C NMR实验结果
对MOR分子中的C原子进行编号,如图5所示.各样品的NMR实验结果如图6和图7所示,图中最下方为新鲜溶液0号样品,标准样品重水-1,4-二氧六环的13C和1H NMR峰分别出现在66.83ppm和3.70ppm.对富液的13C NMR图谱,氨基甲酸盐的峰出现在163.04ppm、66.79ppm和44.53ppm,分别对应羧基上的C原子、C1和C2,碳酸氢盐的峰出现在160.60ppm.有CO2担载的样品均检测出氨基甲酸盐,这与反应机理(1)一致.随着CO2担载的增大,从3号样品开始检测出碳酸氢盐,即CO2担载为0.16左右时碳酸氢盐的浓度高于检出限.新鲜溶液中C1和C2的化学位移分别为67.29ppm和44.98ppm,随着CO2担载的增大,C1和C2的峰逐渐右移,最大偏移量约为3ppm.NMR无法区分MOR和质子化MOR,两者的NMR图谱表现为同一个峰.

图5 MOR分子中的C原子编号示意
2.3 定量1H NMR实验结果
对新鲜溶液的1H NMR图谱,MOR的峰发生裂分,各自的中间峰出现在3.57ppm和2.70ppm,分别对应连接C1和C2的H原子.对MOR分子,连接在同一个C原子上的两个H原子并非化学等价,实验结果仅出现一个峰,原因可能是溶液中的MOR分子的环状结构进行翻转,使得同一个C原子上的两个H原子所处的化学环境对调,这个转换的弛豫时间远小于扫描间隔.随着CO2担载的增大,MOR分子上H原子的峰逐渐左移.对富液的1H NMR图谱,不同化学环境的H原子得到明显区分,连接C1的H原子化学位移为3.71ppm和3.45ppm,连接C2的H原子化学位移为3.17ppm和3.03ppm.1H NMR没有检测出连接N原子上的H原子和碳酸氢根上的H原子.

图6 MOR吸收实验不同CO2担载样品的13C NMR图谱
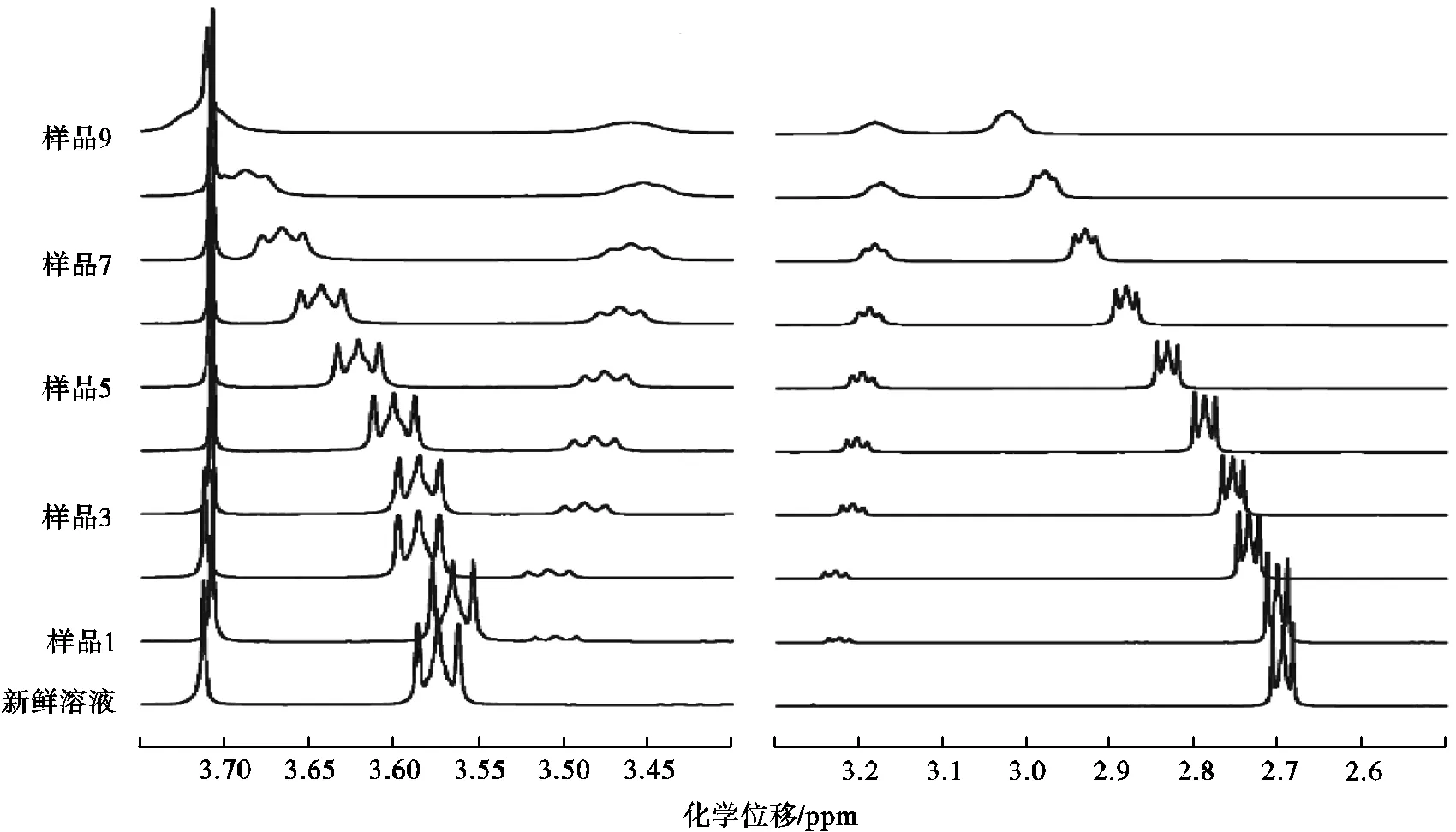
图7 MOR吸收实验不同CO2担载样品的1H NMR图谱
2.4 定量13CNMR实验结果
定量13C NMR的计算结果如图8所示,横坐标为样品编号,纵坐标为组分的摩尔分数.本研究中各组分的浓度较高,NMR图谱上表现为波峰高于基线噪音信号,定量13C NMR具有一定准确性.结果表明富液中氨基甲酸盐和碳酸氢盐的摩尔分数分别为36.77%和26.80%,总和为63.57%,即新鲜溶液有63.57%的MOR发生反应.氨基甲酸盐的摩尔分数随CO2担载的增大先增大后减小,从7号样品开始随CO2担载的增大而减小,即CO2担载在0.38左右时氨基甲酸盐的摩尔分数开始减小.系统各组分的摩尔分数变化规律符合反应机理(1)和(2)的假设.
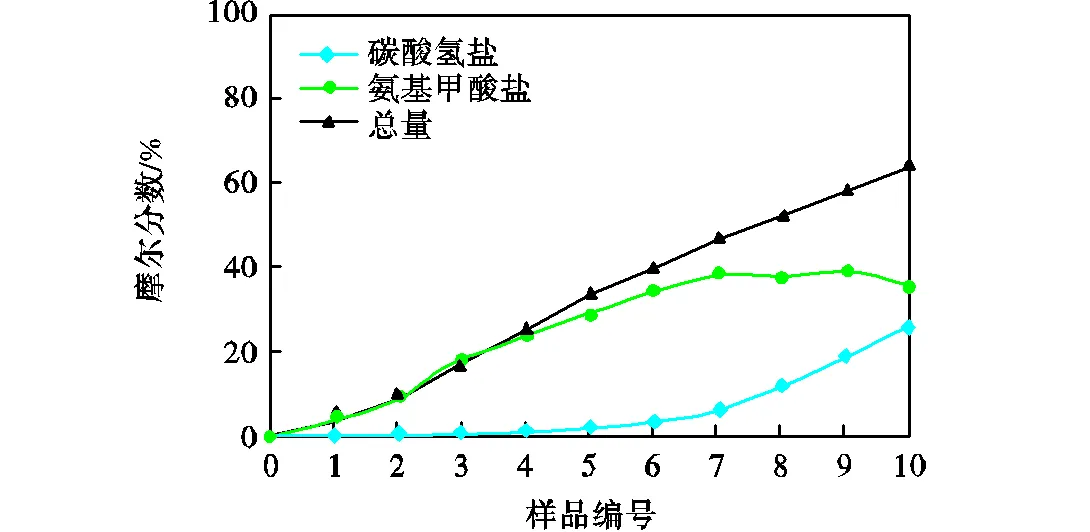
图8 定量13C NMR计算各样品氨基甲酸盐和碳酸氢盐的摩尔分数
3 结 论
作为环状胺吸收剂,MOR的CO2吸收与NMR实验研究对评价MOR吸收表现、明确MOR吸收CO2的反应机理有重要意义.吸收和滴定实验结果表明MOR的吸收容量为0.48mol CO2/mol胺,与5M MEA的结果接近,pH值变化为11.37~8.15.定量13C NMR实验结果表明富液氨基甲酸盐的峰出现在163.04ppm、66.79ppm和44.53ppm,碳酸氢盐的峰出现在160.60ppm,新鲜溶液中C1和C2的化学位移分别为67.29ppm和44.98ppm.定量1H NMR实验结果表明新鲜溶液和富液的1H NMR图谱的MOR峰发生裂分,新鲜溶液的同一个C原子上的两个H原子仅检测出一个峰,可能是因为溶液中MOR分子的翻转,富液的对应原子的峰得到明显区分.定量13C NMR实验结果表明富液中氨基甲酸盐和碳酸氢盐的摩尔分数总和为63.57%,氨基甲酸盐的摩尔分数随CO2担载的增大先增大后减小,在CO2担载0.38左右时开始减小,系统各组分的摩尔分数变化规律符合反应机理的假设.
[1] Jaud P,Bonnivard R G,Kanniche M,et al. Technico-economic Feasibility Study of CO2Capture,Transport and Geo-sequestration:A Case Study for France[R]. France:Peer Reviewed Papers,2004.
[2] Ciferno J P,DiPietro P,Tarka T. An Economic Scoping Study for CO2Capture Using Aqueous Ammonia[R]. DOE/NETL Report,2005-2.
[3] 魏思雨,韩 瑞,苏彦麟,等. 介孔骨架包裹纳米碳酸钙循环吸收CO2性能研究[J]. 燃烧科学与技术,2018,24(2):132-138.
Wei Siyu,Han Rui,Su Yanlin,et al. CO2sorption enhancement of nano calcium carbonate wrapped with the mesoporous skeleton[J].,2018,24(2):132-138(in Chinese).
[4] Rochelle G,Chen E,Freeman S,et al,Aqueous piperazine as the new standard for CO2capture technology[J].,2011,171,725-733.
[5] Muhammad A,Mutalib M I A,Murugesan T,et al. Thermophysical properties of aqueous piperazine and aqueous(n-methyldiethanolamine plus piperazine) solutions at temperatures(298. 15 to 338. 15)K[J].,2009,54:2317-2321.
[6] Matin N-S,Remies J E,Neathery J K,et al.The equilibrium solubility of carbon dioxide in aqueous solutions of morpholine:Experimental data and thermodynamic modeling[J].,2013,52:5221-5229.
[7] da Silva E F,Svendsen H F. Computational chemistry study of reactions,equilibrium and kinetics of chemical CO2absorption[J].,2007,1(2),151-157.
[8] 徐志成. 1,4-丁二胺/N,N-二乙基乙醇胺体系吸收二氧化碳的研究[D]. 北京:清华大学能源与动力工程系,2014.
Xu Zhicheng. CO2Absorption with Aqueous BDA/DEEA Blended System[D].Beijing:Department of Energy and Power Engineering,Tsinghua University,2014(in Chinese).
Experimental Study on the CO2Absorption and Nuclear Magnetic Resonance Spectra of Morpholine
Lu Weiyang1,Wang Shujuan1,Qi Yang2
(1. Department of Energy and Power Engineering,Tsinghua University,Beijing 100084,China;2. CSIRO Manufacturing Flagship,Clayton VIC 3168,Australia)
Morpholine(MOR) is a cyclic amine with potential use as a CO2absorbent. In this study,MOR solution was subjected to CO2absorption and nuclear magnetic resonance(NMR)spectroscopy experiments. The systemic MOR-CO2-H2O chemical reactions and absorption performance of the solution were observed in terms of absorption capacity and variations in NMR images under different CO2loadings. The results of absorption experiments showed that the absorption capacity of MOR was 0.48 mol CO2/mol amine,which was similar to that of 5M MEA. Qualitative NMR results reflected the chemical shifts and changes in the peaks of each component. The results of quantitative13C NMR experiments showed that the molar fraction of each component of the system was in accordance with the assumptions of the related reaction mechanism.
morpholine;CO2capture;absorption capacity;nuclear magnetic resonance(NMR)
TK0
A
1006-8740(2019)02-0149-05
2018-10-19.
国家自然科学基金资助项目(51576108).
陆未央(1990—),男,硕士研究生,tmdmk2@126.com.
王淑娟,女,博士,副教授,wangshuj@tsinghua.edu.cn.
10.11715/rskxjs.R201810010

