水热法制备纳米线研究进展
张仕龙,李震东,徐瑞成,陈 刚,2,符春林,2
(1.重庆科技学院冶金与材料工程学院,重庆 401331;2.纳微复合材料与器件重庆市重点实验室,重庆 401331)
1 引 言
纳米结构是提高材料性能的一种重要手段。其中,纳米线具有众多优势:易单晶化,可降低空穴-电子复合率;大比表面积,增加了边界效应,降低了电导率;有利于器件的小型化、集成化[1-3]。纳米线的制备总体上可分为物理法、化学法和综合法[4-5],其中化学法又分为化学气相沉积法(CVD)[6-7]、水热法[8-10]、模板法[11]等。而水热法具有制备条件简单、适用面广、具有可控性和调变性等优点而备受青睐。
水热法(又称高温水解法)是指将一定形式的前驱物放置在高压釜水溶液中,在高温、高压条件下进行反应,再经分离、洗涤、干燥等后处理的制备纳米线及纳米粉体的方法[12-15]。其最大优点是一般不需高温烧结即可直接得到纳米线,并可制备出固相反应难以制备出的熔点低、蒸气压高、高温分解的物质。相对于气相法和固相法,水热法得到的粉末纯度高、分散性好、均匀、形状可控、利于环境净化等[16-21]。然而,水热法中工艺条件会显著影响纳米线的结构和性能[22-24]。本文将综述采用水热法制备纳米线时矿化剂、反应温度和反应时间这些重要工艺参数对纳米线结构和性能的影响。
2 矿化剂的影响
矿化剂是水热法生长晶体时采用的催化剂。常用的矿化剂有强酸、强碱、有机溶剂等,水也是一种矿化剂[25]。在水热反应的过程中,在高温高压下水处于超临界状态,能显著提高反应物的活性。矿化剂浓度和种类对纳米线的形成和结构有重要作用[26-27]。
矿化剂的种类直接影响纳米线的形成,例如,同样制备银纳米线,美国克莱姆森大学的杨志强博士等以柠檬酸钠做矿化剂[28];中国中南大学陈超华博士等以Na2S作为矿化剂[29];美国杜克大学的李波博士等人以NaBr做矿化剂[30]。三者都制备出银纳米线,但是银纳米线的直径却有显著区别(如图1所示):采用Na2S作为矿化剂制备的银纳米线直径约为200 nm,采用柠檬酸钠做矿化剂时银纳米线的直径约为80 nm;而采用NaBr做矿化剂时,银纳米线的直径减小到约为20 nm。矿化剂除了影响纳米线的直径外,还会影响纳米线的形貌,一般而言,加入矿化剂会使纳米线表面变得更加光洁,并使得纳米线的团聚减少[31-32]。

图1 不同矿化剂种类时合成银纳米线的SEM图(a)柠檬酸钠[28];(b)Na2S[29];(c)NaBr[30]Fig.1 SEM image of silver nanowires with different mineralizer(a)sodium citrate[28]; (b)Na2S[29]; (c)NaBr[30]
东华大学史向阳教授等人分别采用二甲亚砜(DMSO)、甲醇、水做矿化剂制备金纳米线,在DMSO中形成了球形金颗粒,在甲醇中形成了金纳米线与金颗粒的混合物,在水中则得到金纳米线[33]。采用不同的矿化剂所得到的纳米线的尺寸和光滑度不同。例如,辽东学院马正先教授分别采用十六烷基三甲基溴化铵(CTAB)、十二烷基硫酸钠(SDS) 和聚乙二醇6000 (PEG6000)三种矿化剂,得到形貌有显著区别的硼酸镁纳米线(见图2)[34]:加入CTAB和SDS时得到规则的碱式硼酸镁纳米线;加入PEG6000时得到竹叶状的碱式硼酸镁,长径比大。
除了矿化剂的种类会影响纳米线的形成,同一种矿化剂,分子量与浓度不同,也会对纳米线产生较大的影响。Burke等采用不同分子量(Mw=2000、1300、800)和不同浓度(8 mol/L、6 mol/L、4 mol/L和2 mol/L)的聚乙烯亚胺(PEI)水热合成ZnO纳米线,发现Mw=2000和Mw=1300时只有浓度为2 mol/L产生均匀的纳米线,而Mw800时则在任意浓度产生均匀的纳米线[35]。纳米线的尺寸与PEI(Mw=800)的浓度有直接关系:当浓度为8 mol/L、6 mol/L和2 mol/L时,ZnO纳米线的平均长度分别为11 μm、8 μm和2.5 μm,平均直径分别为90 nm、40 nm和60 nm,即随着PEI浓度的增高,纳米线的长度增长,纳米线的直径先变小再变大。

图2 采用CTAB(a)、SDS(b)和PEG6000(c)制备的硼酸镁纳米线SEM照片[34]Fig.2 SEM images of magnesium borate nanowires prepared using CTAB (a), SDS (b) and PEG6000 (c) [34]
采用水热法制备纳米线时,矿化剂浓度的升高会促进纳米线的形成,但是超过某一临界值又会反过来影响纳米线的形貌与抑制纳米线的形成。中南大学陈超华博士等人采用水热法制备银纳米线时(如图3所示)[28]:随着Na2S浓度的增加银纳米线逐渐增多,非银纳米线结构逐渐减少;当Na2S浓度继续增加,最终产物中纳米线的外表不再光滑,并且直径差距增大。华中科技大学的陈大鹏等人同样发现了这一规律(如图4所示)[36]:随着Na2S浓度增加,纳米线的尺寸变大。其他研究者采用水热法制备纳米线也得出了这一结论[37-40]。

图3 不同Na2S浓度制备纳米线的SEM照片[28],(a)0.1 mol/L; (b)0.2 mol/L; (c)1 mol/L; (d)2 mol/LFig.3 SEM images of nanowires prepared with different Na2S concentrations[28], (a)0.1 mol/L; (b)0.2 mol/L; (c)1 mol/L; (d)2 mol/L
3 反应温度的影响
反应温度直接影响晶粒的生长。一方面,温度过高会导致杂相的产生;另一方面,在晶体的生长过程中,由于各个晶粒的生长速度存在差异,生长快的晶粒会吞并生长较慢的晶粒,从而引起晶粒尺寸存在差异[41]。因此,反应温度对晶体的生长起着至关重要的作用,温度太高不利于形成稳定晶型,温度太低又不足以提供纳米线生长的动力[42]。

图4 不同Na2S浓度制备的银纳米线SEM图[36],(a)0.10 mmol/L; (b)0.15 mmol/L; (c)0.30 mmol/LFig.4 SEM images of Ag nanowires prepared at different Na2S concentrations[36], (a)0.10 mmol/L; (b)0.15 mmol/L; (c)0.30 mmol/L

图5 不同水热温度制备MnO2的比表面积[45]Fig.5 Specific surface area of MnO2 prepared at different hydrothermal temperatures[45]
燕山大学韩娜教授等采用水热法制备银纳米线时发现[43]:随着温度的升高产物中原本的银纳米颗粒逐渐变为银纳米线,温度越高银纳米线的含量越高(当温度达到160 ℃时,基本无银颗粒生成);温度过高时(例如升温至180 ℃),反应体系活性过大,分子运动比较剧烈导致PVP难以稳定吸附在晶体的(100)晶面上,从而难以生成银纳米线。Muchuweni在制备氧化锌纳米线时发现[44]:在低温下,横向和轴向生长速率之间的竞争导致了低纵横比的杆状纳米结构的生长;而在高温下,轴向生长速率比横向生长速率高,得到了高纵横比、像线一样的纳米结构。而温度越低,其光学透射比越高,电阻越小,电阻率越高;随着温度的升高,光学透射比减小,电阻增加,电阻率降低。辽宁工程技术大学杨绍斌教授在研究水热温度对MnO2纳米线结构和电容性能的影响时发现[45]:MnO2纳米线的晶粒和直径随水热温度升高而增大,比表面积随着温度的升高而减小(如图5所示)。随着水热温度的升高,MnO2的电荷转移电阻(Rct)先降低后升高,扩散阻抗(W)也先降低后升高,Rct和W值达到最小,从而较小极化,有利于提高MnO2的倍率性能[46]。
Hamdi[47]、冯欧阳[48]、杨露[49]等在采用水热法制备纳米线过程中也发现,纳米线的生长速率、微结构、力学性能、电阻率等都强烈依赖于反应温度。纳米线的直径过大或者过小,其性能都不一定最佳,因此,选择合适的水热反应温度,得到最佳的纳米线尺寸与形貌,对于材料的性能研究具有重要意义。
4 反应时间的影响
在水热法中,除了矿化剂与水热反应温度外,水热反应时间也是影响纳米线形貌和性能的一个重要因素[50]。在Ge等采用水热法制备CuSe纳米线的过程中发现[51]:反应初期只有纳米颗粒,随着反应时间的增长,纳米线的数量增多。
王双甲等研究水热反应时间对氧化锌纳米线的形貌和性能的影响[52]:当水热反应时间为12 h时,所制备ZnO纳米线含较多杂质(见图6a),这可能是由于反应不彻底所致。水热反应时间延长到24 h时,所制备ZnO纳米线长径比较小,形貌均匀度较差(见图6b)。当水热反应时间为36 h时,所制备ZnO纳米线呈现花簇状生长,无杂质,形貌较好(见图6c)。当水热反应时间为48 h 时,所制备ZnO纳米线的形貌较差且杂质较多(见图6d),这可能是由于水热反应时间过长,ZnO部分重新溶解于偏弱酸性反应体系中,造成晶体受损或产率下降。Polsong[53]研究也发现,适当延长水热反应时间能促使ZnO纳米线的结晶化更加完整。除了反应时间外,易早等[54]也发现,反应温度、浓度、pH等也会对ZnO纳米线的形貌产生影响。反应速率随着反应温度的增加而加快,并且纳米线的尺寸也更加均一,与我们前面所得到的结论相符合;而随着pH的增大,纳米线的形貌会发生显著变化,由细线状变为花朵状;而随着浓度的改变,不仅会影响ZnO纳米线的生长速率,也会影响其表面形貌。由于浓度、pH等实验条件对不同纳米线的形貌影响不一样,因此,对于具体的影响规律,还需要我们去探究。

图6 不同反应时间的ZnO纳米线形貌图[52](a)12 h;(b)24 h;(c)36 h;(d)48 hFig.6 Morphology of ZnO nanowires with different reaction time[52] (a)12 h;(b)24 h;(c)36 h;(d)48 h

图7 (a)~(h) 不同水热时间的CH3NH3PbI3纳米线形貌图及尺寸分布; (i)纳米线平均尺寸与水热时间的关系Fig.7 (a) - (h) Morphology and size distribution of CH3NH3PbI3 nanowires at different hydrothermal time; (i) Relationship between average size of nanowires and hydrothermal time
此外,在Phuruangrat[55]、Mohammed[56]等诸多学者的研究都发现:随着反应时间的增加,纳米线长径比增加,比表面积增加,表面变得更光滑;当反应时间过长时,纳米线横向过度生长,纳米线长径比降低,纳米线变为纳米棒,会影响纳米线形成,也会影响材料的性能。因此,选择合适的水热反应时间,得到尺寸合适的纳米线,对于纳米材料的研究与应用具有重要意义。
5 水热法制备CH3NH3PbI3纳米线
有机-无机杂化钙钛矿是目前最有发展前景的光伏材料,在了解到水热法如何调控纳米线形貌的基础上,本文作者采用水热法制备出CH3NH3PbI3纳米线,并通过实验数据验证水热法制备工艺对纳米线形貌的影响。包括水热温度,水热时间对纳米线形貌的影响。
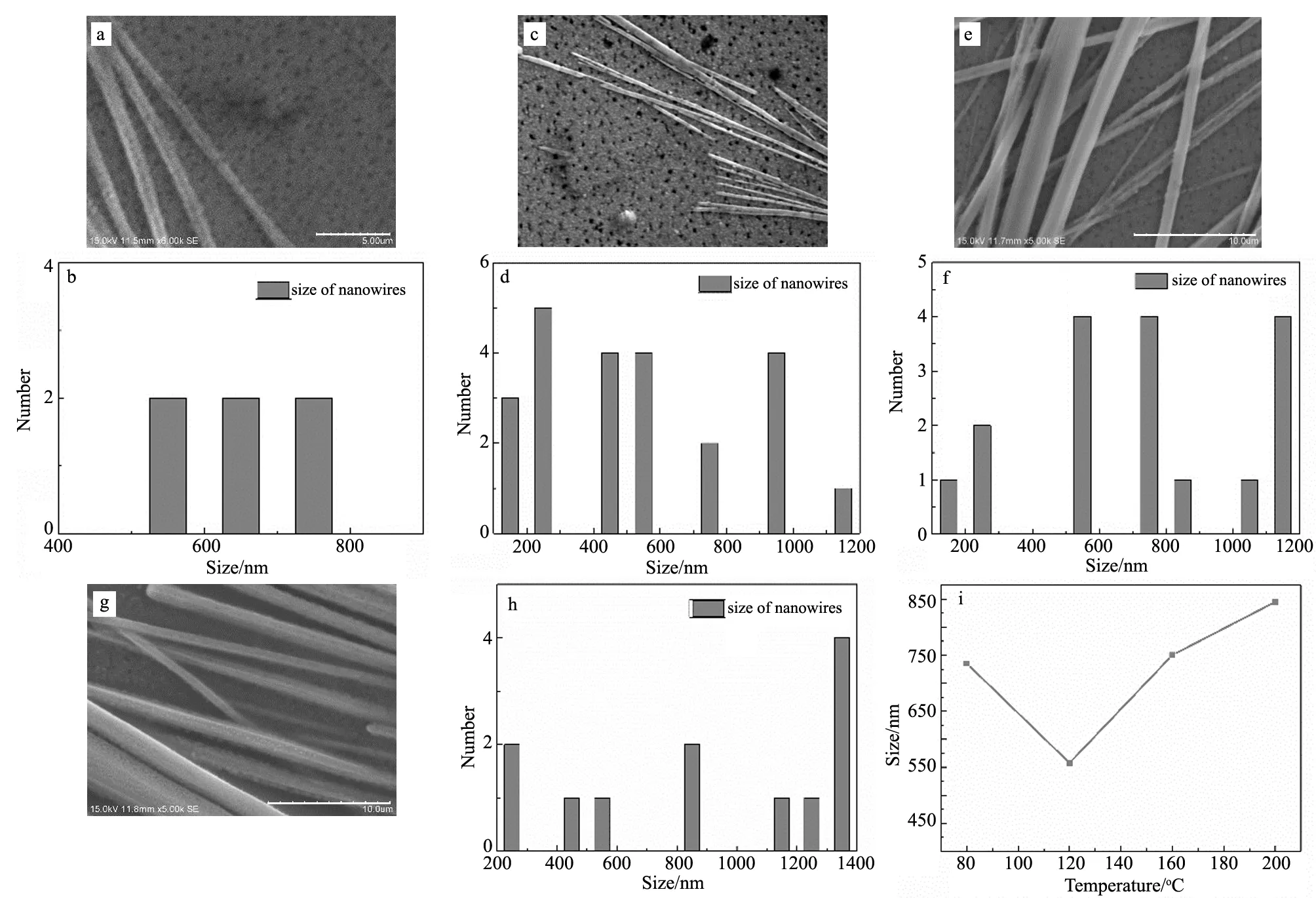
图8 (a)-(h) 不同水热温度的CH3NH3PbI3纳米线形貌图及尺寸分布; (i)纳米线平均尺寸与水热温度的关系Fig.8 (a)-(h) The morphology and size distribution of CH3NH3PbI3 nanowires at different hydrothermal temperature; (i) The relationship between the average size of nanowires and hydrothermal temperature
图7 (a)~(h)分别为不同水热时间CH3NH3PbI3纳米线的形貌图及纳米线的尺寸分布,图7 (i)为随着时间的变化,CH3NH3PbI3纳米线平均尺寸的变化。从图7 (i)中可以看出,随着水热时间的延长,纳米线的尺寸变得更加细小,当水热时间为70 min时,其平均纳米线尺寸达到了450 nm。虽然随着时间的进一步延长,一部分纳米线出现了分解的情况,但这是由于有机无机杂化钙钛矿本身不稳定的原因导致的。并且,其尺寸的变化,符合预测的结论,即随着时间的增加,纳米线的尺寸变小。
同样,研究了不同水热温度下的CH3NH3PbI3纳米线的尺寸变化规律,并找出尺寸变化与水热温度的关系。图8 (a)~(h)为不同水热温度的CH3NH3PbI3纳米线的形貌及尺寸分布图,图8 (i)为随着温度的变化,CH3NH3PbI3纳米线平均尺寸的变化图。通过研究发现,随着水热温度的升高,纳米线的平均尺寸先降低后升高,在温度为120 ℃时,尺寸最小,为557.89 nm,当温度超过120 ℃时,随着温度的继续升高,纳米线的尺寸持续变大,当温度为200 ℃时,其平均尺寸达到了850 nm。也与我们预测的结果一致。纳米线尺寸增大的原因可能是由于水热温度的升高,晶粒长大,导致纳米线的整体尺寸增大。通过我们的实验发现,采用水热法制备CH3NH3PbI3纳米线,尺寸随着实验因素的变化是符合我们的预期的。
6 结 语
纳米线由于特殊的各向异性结构和丰富的构效调控能力而受到广泛研究[57],它有利于器件的小型化、集成化;通过调控其尺寸可以有效优化材料及器件的性能。在制备纳米线的方法中,又以水热法制备条件简单、适用面广为广大学者所采用。而在水热法制备纳米线的过程中,通过改变矿化剂的种类与浓度、水热反应时间、水热法反应温度可以有效地调控纳米线的尺寸,从而改善纳米线的性能。虽然关于水热法制备纳米线的研究有一定的成果,但仍有许多工作有待开展,如:(1)研究其它反应条件(如溶剂浓度、pH值等)对纳米线形貌和性能的影响,并找出纳米线的生长机制和形貌变化的普适性规律。(2)研究不同表面形貌纳米线的性能。(3)在理论上较准确地预测纳米线形貌和不同表面形貌纳米线的性能。

