液质联用定量血清中维生素D、A、E的方法*
李金蓉,阮亮亮,2,3△,杨文初
(1.上海枫林医药医学检验有限公司特检部,上海 200031;2.上海医药临床研究中心,上海 200031;3.上海生物样本库工程技术研究中心,上海 200031)
脂溶性维生素是人体必需的营养成分,在人体的生理、病理上起着至关重要的作用。越来越多的研究证据表明,脂溶性维生素A、D、E与人体多种生理代谢性疾病相关联。最近的大量研究表明,维生素D缺乏除会引起传统认识到的儿童佝偻病外[1],还与冠心病,糖尿病,小儿头疼,癌症等众多疾病关系密切[2-5]。维生素D的检测已成为目前最为活跃的疾病标志物检测领域之一。维生素A除与视力的发育及功能,性腺功能等有关外[6-7],最新研究表明,维生素A在慢性的移植抗宿主疾病中具有改善皮肤的纤维化的功效[8]。维生素E作为抗氧化剂,普遍认为具有抗衰老的作用,最新发现维生素E缺乏也会导致卵巢激素的缺乏,从而会引起相关的疾病[9-10]。目前,检测维生素的方法主要有免疫分析法、高效液相色谱法、液质联用LC-MS/MS法等[11-13]。LC-MS/MS方法相比于免疫分析法具有特异性和灵敏度高等优点。因此,液质联用的方法已经广泛被运用在测量生物标记物方面。现今,已经有部分研究运用液质联用的方法同时分析脂溶性维生素A、D、E[14-16]。这些方法,在分析时间、灵敏度、方法成本等方面尚有诸多不足。此外,这些维生素是人血清内源物质,无法找到不含这些分析物的人空白血清配制校正标准做定量标准曲线,从而增加了一般方法的临床应用难度。本文首次提出并验证了以代替基质为基础的LC-MS/MS法,在5 min时间里完成了四种成分的同时准确定量,节省了试剂成本和时间成本。通过方法学验证,证明了方法适用于人血清中25-羟基维生素D2(25OHVD2)、25-羟基维生素D3(25OHVD3)、维生素A、维生素E的同时定量。
1 材料与方法
1.1仪器与试剂 液相色谱为LC20AD XR HPLC pumps 及SIL-20AC XR 自动进样器;质谱为AB Sciex QTrap5500型质谱仪。分析天平为赛多利斯公司CPA225D型;氮吹仪为Zymark公司Turbo Vap型;多管涡旋振荡器为Scientific Industry公司产品;离心机为Thermoscientific公司CL31R型。25OHVD2、25OHVD3、2H3-25-Hydroxy维生素D2、2H6-25-Hydroxy维生素D3购买自IsoSciences公司;维生素A购买自Sigma-Aldrich;维生素E购买自Dr.Ehrenstorfer GmbH公司;2H6-Retinol,购买自ISOREAG公司;维生素E-d6:购买自Toronto Research Chemicals公司。试剂如环己烷、甲醇、甲酸,甲酸铵均购买自sigma-Aldrich公司。水为Millipore生产双蒸水。
1.2方法
1.2.1工作液的配制 四种化合物的标准曲线工作液(SWS1~SWS8)及最低检测线、低、中、高4个水平的质控工作液(QWS-LL、QWS-L、QWS-M、QWS-H),按表1中浓度由高浓度逐级溶剂稀释配制。
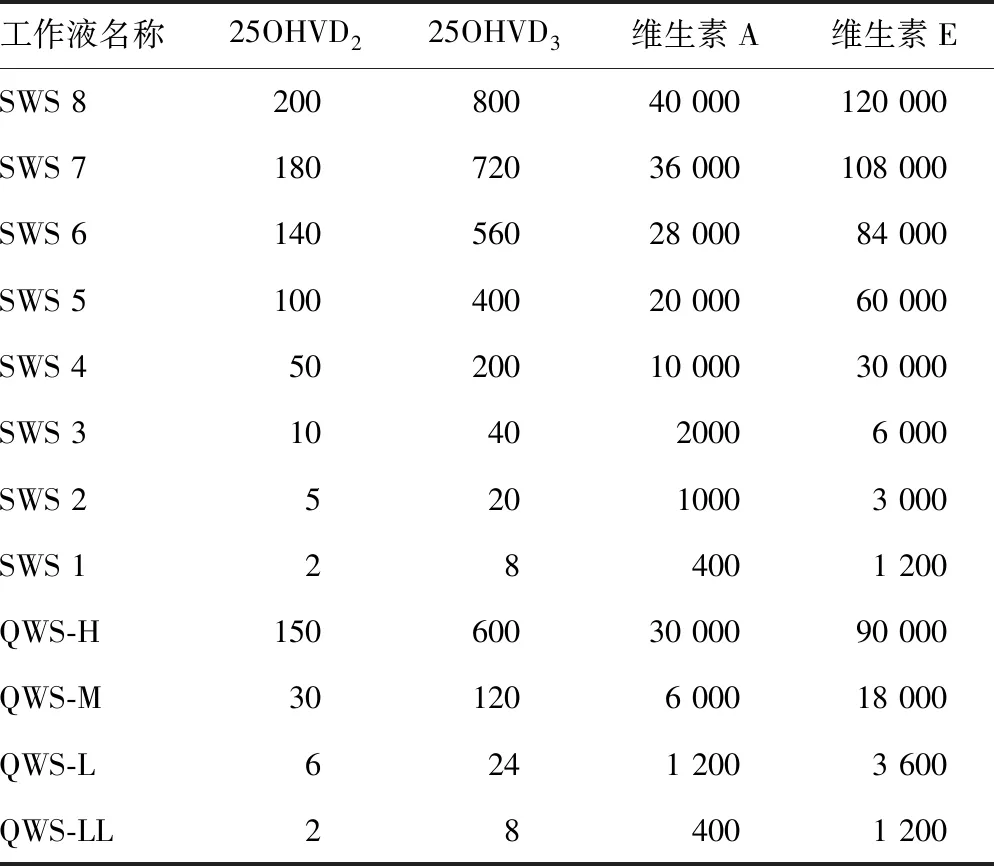
表1 标准曲线工作液和质控工作液名称和浓度(ng/mL)
1.2.2代替基质及其效能的平行试验验证
1.2.2.1代替基质及其配制按本实验室自行开发的方法配制 代替基质由实验室易得的化学品配制而成。
1.2.2.2平行试验验证 (1)取6份至少6个不同来源的混合血清,添加工作液,对得到的样品进行标准加入法分析,外推得到本底浓度,从而得到各点的理论浓度,此数据用作为浓度的参照值。(2)用代替基质做标准曲线,对上述样品进行定量,测得浓度;(3)计算代替基质测定结果的准确度,从而验证代替基质的可行性。
1.2.3质控样品的配制
1.2.3.1分析批代替基质质控的配制 分析批质控样品包括最低检测线质控(LLOQ)、低浓度质控(LQC)、中浓度质控(MQC)和高浓度质控(HQC)4个水平,由表1中各质控工作液25 μL依次加入到100 μL替代基质中配制而成。每个分析批次均新鲜配制。
1.2.3.2血清质控样品的配制 高血清质控样品(HQC-Sr)是将标曲工作液中的最高浓度点以工作液∶血清=1∶20的比例加入血清中混匀所得。中血清质控样品(MQC-Sr)为血清样品测试得到的本底浓度。
1.2.4样品处理
1.2.4.1校准曲线及批内质控品的处理方法 25 μL标曲工作液,或代替基质质控工作液分别加入100 μL替代基质中,加入200 μL内标溶液,涡旋混匀,加入900 μL环己烷,涡旋5 min,高速离心5 min;转移800 μL上清至另一离心管,氮气吹干;加入100 μL 80%甲醇水溶液复溶,涡旋离心后,取上清进样分析。
1.2.4.2血清样品的处理方法 25 μL甲醇加入100 μL血清样本中,加入200 μL内标溶液,涡旋10 s,加入900 μL环己烷,涡旋5 min,高速离心5 min;转移800 μL上清至另一离心管,氮气吹干后加入100 μL 80%甲醇水溶液进行复溶,涡旋离心后,取上清进样分析。
1.2.5LC-MS/MS方法参数 实验使用APCI离子源,多反应监测模式(MRM)进行选择离子扫描定量,质谱参数如下。雾化气(Gas 1):70 psi;喷雾电压:3 V;气帘气(CUR):25 psi;碰撞气(CAD):Medium;离子源温度(TEM):550 ℃。各化合物及其内标的过渡离子对如下,25OHVD3:383.4→365.3,25OHVD2:395.3→209.1,维生素A:269.0→93.0,维生素E:431.4→165.2;d3-25OHVD2:398.3→230.2,d6-25OHVD3:389.4→371.3,维生素E-d6:437.5→171.1,维生素A-d6:275.1→175.8。液相分离选用Thermo scientific公司Accucore色谱柱C18,50×2.1 mm,2.6 μm;流动相A为0.2%甲酸-1 mmol/L甲酸铵甲醇溶液,流动相B为0.2%甲酸-1 mmol/L甲酸铵水溶液;流速:0.5 mL/min;柱温:40 ℃,自动进样器温度:4 ℃。洗脱步骤如下:0~1.5 min有机相比例从70%升至95%,保留1.8 min,然后在0.2 min时间内升至100%有机相,保留1.6 min,之后回到初始有机相比例,停留0.5 min。最终在5 min时间里完成分析。代表性的图谱见图1。样品浓度分别为25OHVD2:20 ng/mL,25OHVD3:80 ng/mL,维生素A:4 000 ng/mL,维生素E:12 000 ng/mL。
2 结 果
2.1代替基质的可行性平行试验验证 如表2所示。内源性物质常规的定量方法为标准加入法,此测定结果在这里作为参照标准。用代替基质所做的标曲,得到相关系数r>0.990 0。用此标曲定量标准添加法的样品,得到的值与标准加入法对比,以评价代替分析物的可用性。4种化合物的用替代基质测定的偏差均在±20%以内。由此证明所配制的替代基质可以作为定量真实血清样本的替代基质,结果可靠。
2.2血清基底值测试 方法的可靠性必须通过真实的血清质控品来验证。本实验中以替代基质配制四个水平LLOQ、LQC、MQC、HQC的质控和两个水平的真实血清质控MQC-Sr(混合血清本底值)/HQC-Sr(标准加入一定量的混合血清值)各平行6份,按照样品前处理方法处理。上机测试得到血清MQC/HQC的实测浓度值。此值作为后期日内及日间准确度与精密度及稳定性测试的标准值。加入此两个水平的质控样本的目的一是为了说明方法适用于临床真实样本的测试,另一方面也说明了混合了不同来源的人血清样本中几乎不含对定量有干扰的物质。说明方法具有特异性。各化合物血清本底测试值由于篇幅限制未呈现。
2.3日内及日间准确度与精密度 为了考察方法的日内及日间准确度与精密度,配制了6个水平的质控品考察实测值与理论值之间的偏差。分别在3个不同的分析批及不同天对6个水平的质控品进行比较。根据测试结果,准确度与精密度的偏差均在±20%以内,符合生物样本分析的评判标准。见表3。
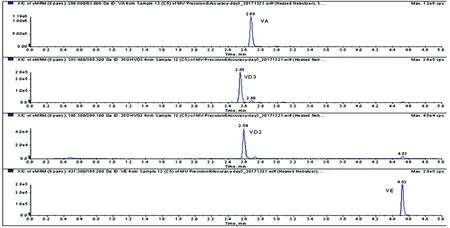
图1 4种化合物在5 min的LC-MS/MS的代表性色谱图
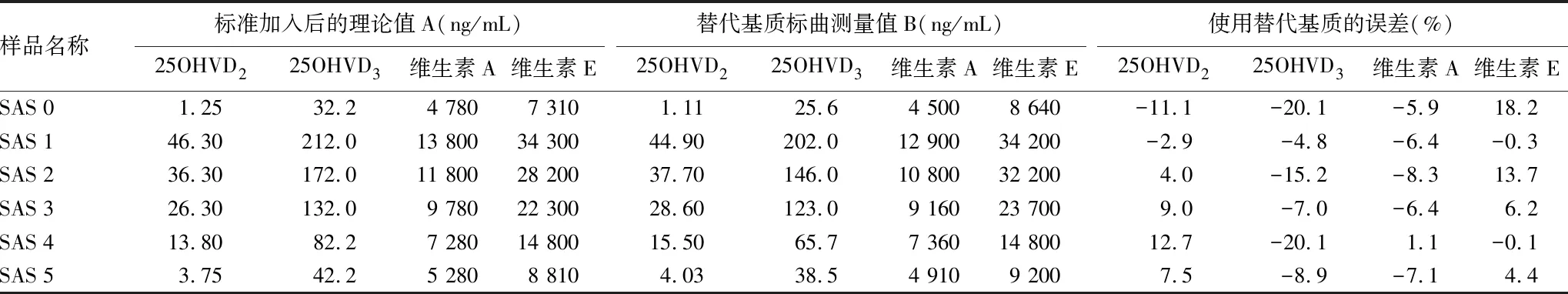
样品名称标准加入后的理论值A(ng/mL)25OHVD225OHVD3维生素A维生素E替代基质标曲测量值B(ng/mL)25OHVD225OHVD3维生素A维生素E使用替代基质的误差(%)25OHVD225OHVD3维生素A维生素ESAS 01.2532.24 7807 3101.1125.64 5008 640-11.1-20.1-5.918.2SAS 146.30212.013 80034 30044.90202.012 90034 200-2.9-4.8-6.4-0.3SAS 236.30172.011 80028 20037.70146.010 80032 2004.0-15.2-8.313.7SAS 326.30132.09 78022 30028.60123.09 16023 7009.0-7.0-6.46.2SAS 413.8082.27 28014 80015.5065.77 36014 80012.7-20.11.1-0.1SAS 53.7542.25 2808 8104.0338.54 9109 2007.5-8.9-7.14.4
2.4稳定性
2.4.1储备液稳定性 实验中考察了储备液在-20 ℃冰箱1个月的稳定性,结果符合新旧比对偏差在±10%以内的评判标准。此外,还考察了储备液在室温放置6 h的稳定性,结果也符合差异±10%以内的评判标准,说明使用的储备液在一个月的时间内是保持稳定的,且室温放置6 h及以内不会影响检测结果。
2.4.2工作液的室温稳定性 接近LLOQ的浓度点放置在室温6 h,与新鲜配制的相同浓度点比较,结果符合偏差在±10%以内的评判标准。本实验中使用的工作液自开始验证配制后储存在-20 ℃冰箱到完成验证实验1个月的时间里保持稳定,说明工作液在1个月的时间里是稳定的。由此,方法中使用的工作液放置在室温 6 h及以内,以及储存在-20 ℃冰箱1个月时间均不会对结果产生显著影响。
2.4.3短期稳定性 考察替代基质质控LQC和HQC及血清质控MQC-Sr和HQC-Sr共四个水平在室温放置24 h的稳定性。由实验结果得知,250HVD2,25OHVD3及维生素E三种成分的替代基质质控和血清质控在室温放置24 h均稳定。维生素A替代基质质控在室温放置24 h不稳定,每次分析需要新鲜配制。而血清质控是稳定的,说明真实样本即使在室温放置24 h依然呈稳定状态。限于篇幅,数据未列出。为了考察维生素A替代基质质控品的稳定性状态,接着又考察了其2、4、6 h,稳定性。由数据发现,维生素A在2 h里都会有近30%的降解,进一步说明维生素A的替代基质质控需新鲜制备,不适用于室内保存。
2.4.4冻融稳定性 考察了血清MQC-Sr和HQC-Sr两个浓度水平,将早先配制好储存在冰箱的HQC-Sr及MQC-Sr放置室温解冻后,再次存储回-20 ℃冰箱冷冻至少12 h以上再次解冻,依次循环3次考察其经过3次冻融循环后浓度与理论浓度之间的偏差。经过试验,得知血清在经过3个冻融循环后,依然可以保持稳定。不影响检测结果。满足生物分析方法学±20%以内的评判标准。限于篇幅,数据未列出。
2.4.5长期稳定性 考察了真实的血清质控品放置在-20 ℃冰箱1个月的稳定性状态。由于短期稳定性考察中维生素A替代基质质控品在室温放置不稳定,这里还考察了替代基质质控品在-20 ℃冰箱放置3 d的稳定性。由表4得到,血清质控在-20 ℃冰箱放置1个月的时间里仍然稳定,且4种成分的替代基质质控放置在-20 ℃冰箱3 d时间里也是稳定的。
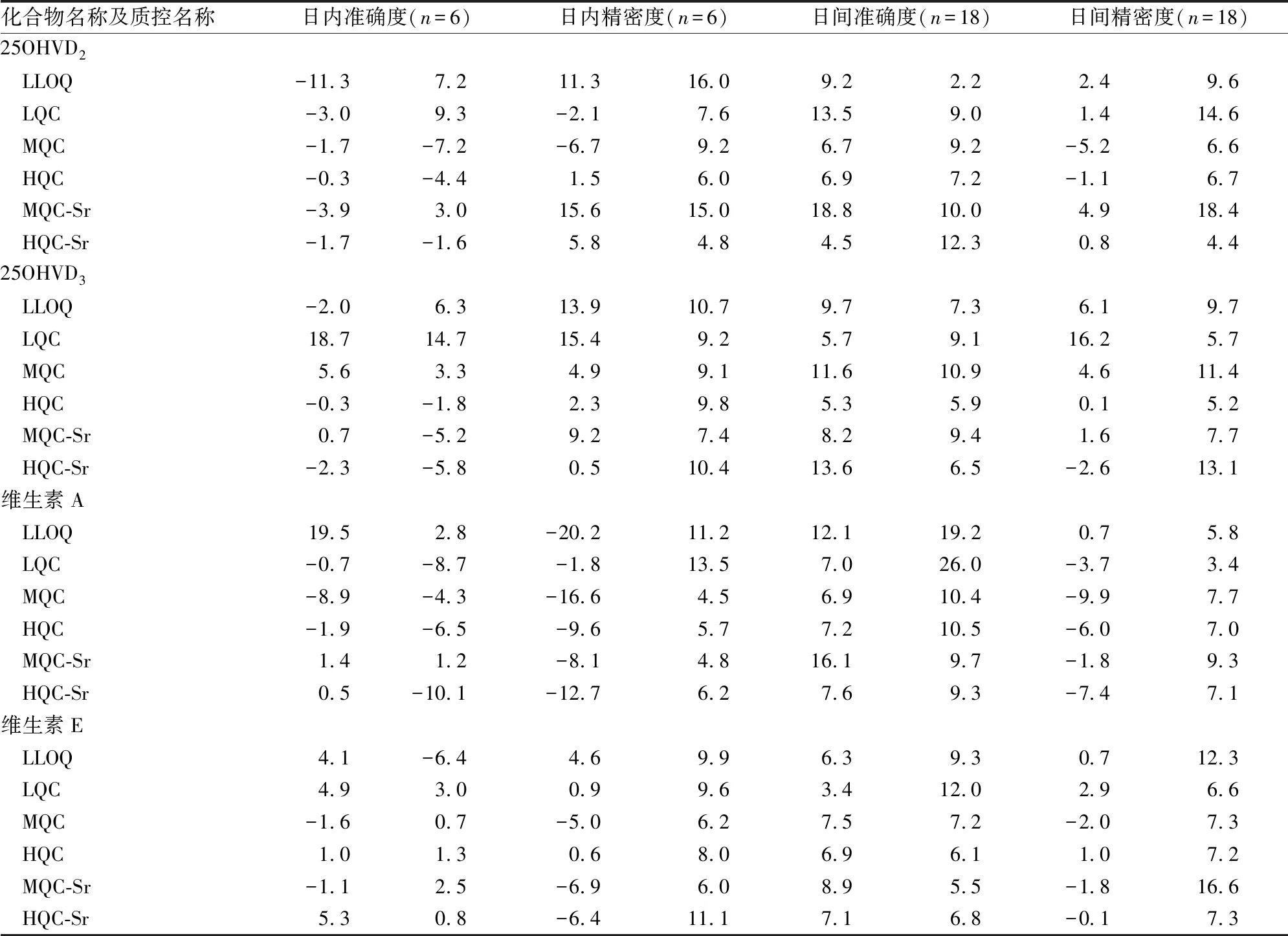
表3 日内及日间准确度与精密度(%)
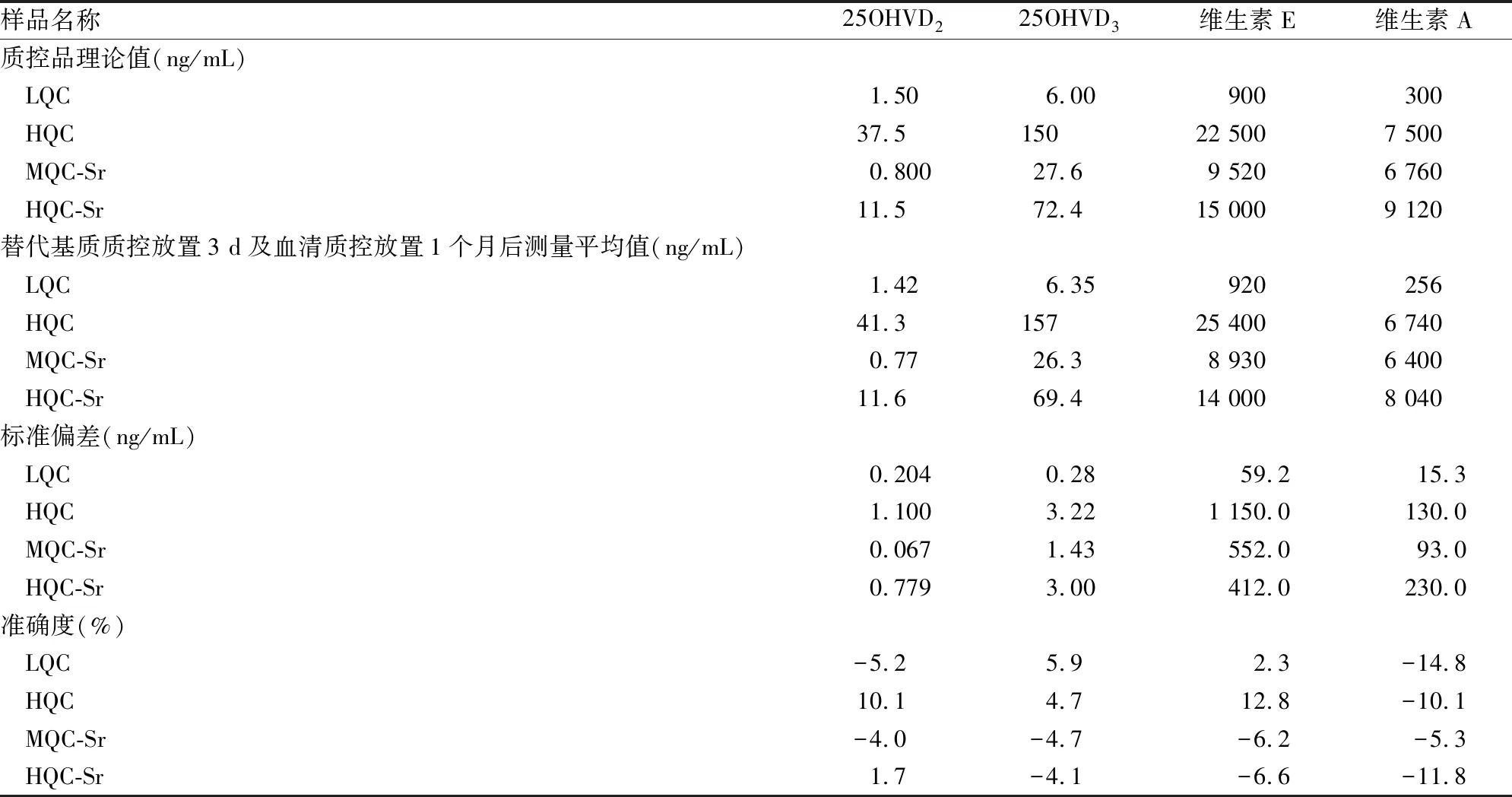
表4 4种化合物的长期稳定性(n=6)

续表4 4种化合物的长期稳定性(n=6)
3 讨 论
同时高效、精确定量人血清中25OHVD2、25OHVD3、维生素A、维生素E四种脂溶性维生素是一挑战性课题。原因一,四种物质在血清中含量分布很宽,从25OHVD2的纳克级以下,到维生素E的微克级以上,因此要求方法的线性范围宽。本方法即可灵敏地定量到低浓度的25OHVD2,也可检测到高浓度维生素E;原因二,作为内源性化合物的空白基质的不可得到性。市面上尚无包含这四种维生素的标准品和质控品,即使有,方法的成本也会很高,直接影响方法的广泛应用性。对内源性生物标志物的定量,如果空白基质无法得到,通常采取代替分析物或代替基质法。以同位素为基础的代替分析物法,尽管方法发展较容易,但成本较高,而且后续样品分析因不可用标曲直接定量而较麻烦。选用代替基质法,一旦代替基质的可用性得到证明,方法应用到样品分析则如常规定量分析一样,无附加步骤。但代替基质需反复筛选,以期其性能满足分析要求。经过大量筛选优化实验,本实验室制得了一种易得且性能可靠的代替基质。通过实验,其可用性得到证实。该方法使用了自配易得的替代基质来制备校准品和质控品,缩减了成本,提高了经济效益,使得方法更加实用。其三是方法的灵敏度和样品用量。由于25OHVD2的浓度很低,为达到准确定量,一般报道的方法样品用量都较大。而本方法只需100 μL血清就能达到较低的检测限,完全满足临床样本的分析要求,减轻了患者的痛苦。经过方法学验证,证明了该方法具有灵敏度高、可靠、稳定、耐用、快速等优点。本方法适用于临床样本的分析。目前该方法已在本实验室服务于临床样品分析。

