高效液相色谱法测定化妆品中的对甲苯磺酸异丙酯及GCMS确证
曾 苑,陈悦铭,黄少瑶,李仲唐,叶晓争
(广州质量监督检测研究院,广东广州 511447)
棕榈酸异丙酯和肉豆蔻酸异丙酯是广泛用于医药及化妆品的制造原料,对甲苯磺酸异丙酯是棕榈酸或肉豆蔻酸在与异丙醇酯化反应制备棕榈酸异丙酯和肉豆蔻酸异丙酯过程中,对甲苯磺酸作为反应催化剂的同时,也会与异丙醇发生酯化反应,产生对甲苯磺酸异丙酯这种基因毒性的副产物。欧洲药品管理局(EMA)、美国食品药品管理局(FDA)发布的基因毒性杂质限度指南的最终版[1]、基因毒性杂质指南草案[2]都对对磺酸酯类物质的基因毒性做出了明确的规定。目前,对于对甲苯磺酸异丙酯文献报道主要集中其应用[3]、药品中的检测[4-5],尚无关于化妆品中对甲苯磺酸异丙酯含量测定的方法文献报道。本文采用高效液相色谱法建立了化妆品中对甲苯磺酸异丙酯的检测方法。图1、图2分别是对甲苯磺酸异丙酯的化学结构式,对甲苯磺酸和异丙醇反应生成对甲苯磺酸异丙酯的过程。
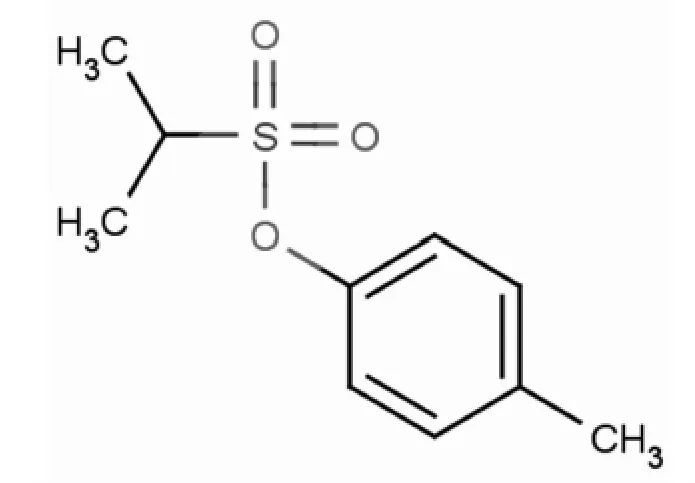
图1 对甲苯磺酸异丙酯的化学结构式

图2 对甲苯磺酸异丙酯的形成过程
1 实验部分
1.1 仪器与试剂
1260高效液相色谱仪(美国Agilent公司);Agilent7890A-5975C气相色谱-质谱联用仪,菲罗门SuperLu C18(250×4.6 mm,5μm)色谱柱;BSA224S-CW 电子天平(德国SARTORIUS公司);2600TH超声波清洗器(上海安谱科学仪器有限公司);AllegraX-30R高速离心机(美国BECKMAN COULTER公司)。
对甲苯磺酸异丙酯对照品(CAS:2307-69-9,北京百灵威科技有限公司,含量:90.0%);乙腈(色谱纯,美国 Fisher Chemical公司);溴化四丁基铵(分析纯,广州化学试剂厂);0.22μm有机相微孔滤膜(上海安谱实验科技股份有限公司);实验室用水为Milli-Q超纯水。
1.2 标准溶液的配制
称取0.0100 g对甲苯磺酸异丙酯标准物质用乙腈定容至100 mL容量瓶中,溶液浓度为0.10 mg·mL-1。分别吸取10、50、100、200、500、1000 μL 的对甲苯磺酸异丙酯标准溶液至 10 mL容量瓶中,用5 mol· L-1磷酸四丁基溴化铵(pH值=4.0)溶液∶乙腈(50∶50)定容,得到浓度分别为 0.1、0.5、1.0、2.0、5.0、10.0 μg·mL-1的对甲苯磺酸异丙酯标准溶液,于 4℃下储存备用。
1.3 样品的前处理
称取样品0.5 g(准确至0.01 g)于15 mL离心管中,加入5mL乙腈,涡旋振荡混匀后超声提取10min,再用离心机10000 r·min-1离心3 min,取上清液过0.22μm有机相微孔滤膜于进样瓶中待测备用。
1.4 高效液相色谱条件
色谱柱:菲罗门 SuperLu C18(250×4.6 mm,5 μm)色谱柱;流动相:5 mmol· L-1磷酸四丁基溴化铵(pH值=3.0)溶液∶乙腈 =50∶50;进样量为10 μL;流速为 1.0 mL·min-1;时间为 15 min;柱温为30℃;测定波长230 nm。分别对待测液进行测定。
1.5 GCMS确证条件
色谱条件:色谱柱:毛细管柱(HP-5 30 m×0.32 mm×0.25μm),固定相为5%苯基-甲基聚硅氧烷;载气:氦气;流速:1.0 mL·min-1;程序升温:起始温度为 100℃,维持 1 min,以20℃/min的速率升温至200℃,维持10 min,20℃/min的速率升至240℃,保持1 min;进样口温度:220℃;分流比10∶1;进样体积:1.0μL;溶剂延迟4 min。
质谱条件:离子源参数:电子轰击电离源(EI源),电子能量为80 eV,离子源温度为250℃。扫描模式:选择离子扫描,目标化合物对甲苯磺酸异丙酯的选择离子(m/z)(91、172、214)。
2 结果与讨论
2.1 萃取溶剂的选择
对比考察了乙腈、乙酸乙酯、甲醇对化妆品中的对甲苯磺酸异丙酯的提取效果,加标浓度为10μg·mL-1,回收率结果见
表1。结果表明,三者都有不错的提取效率,但乙酸乙酯与某些水包油型的膏霜类产品不互溶适用性较差,以乙腈作为提取溶剂时,杂质干扰最少,故选用乙腈为萃取溶剂。
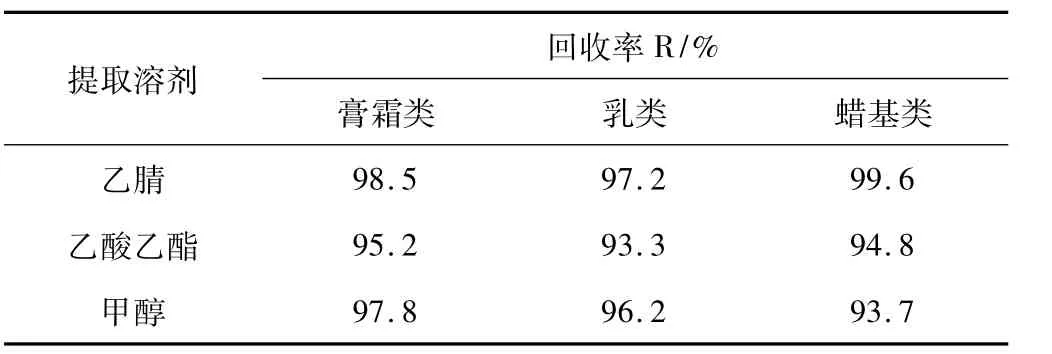
表1 不同溶剂提取3种基质化妆品中对甲苯磺酸异丙酯的回收率
2.2 检测波长的选择
取10.0μg·mL-1的对甲苯磺酸异丙酯标准溶液在选定波长215、230、254和280 nm进行测定,获得对甲苯磺酸异丙酯的色谱图和光谱图,通过比较得出,对甲苯磺酸异丙酯在230 nm处有最大吸收波长,故选定本次实验检测波长为230 nm。对甲苯磺酸异丙酯标准溶液光谱图见图3。

图3 对甲苯磺酸异丙酯吸收光谱图
2.3 色谱柱的选择
经查ACD/Lab,对甲苯磺酸异丙酯的 ACD/Log P值为2.18,Log P值是油水分配系数,Log P值越大,说明该物质越亲脂,反之,越小,则越亲水,即水溶性越好。由此可知对甲苯磺酸异丙酯的非极性大于极性,本次实验选用菲罗门SuperLu C18(250×4.6 mm,5 μm)色谱柱,SuperLu的硅胶基质纯度达99.999%,硅烷基键合于硅胶表面,使其具有适中的疏水性以及亚甲基选择性,非极性端基封尾有效减少分析物与残留硅醇基的作用,分析非极性化合物的有最大保留作用。色谱图见图4。

图4 对甲苯磺酸异丙酯标准溶液液相色谱图
2.4 流动相的选择
对甲苯磺酸异丙酯含有磺酸基(-SO3H),不仅是酸性官能团,也是可离子化的官能团,而在反相色谱中,样品的保留情况和其官能团的离子化状态关系密切,中性态和离子态之间的保留时间往往可以有高达30倍的差异。酸性条件(低pH值)有利于酸性分析物的保留,而碱性条件有利于碱性分析物的保留。因此,本次实验使用了不同比例的5 mol· L-1磷酸四丁基溴化(pH 值 =3.0)溶液 - 乙腈(90∶10),(70∶30),(50∶50)进行试验,结果发现,在5 mol· L-1磷酸四丁基溴化(pH值=3.0)溶液-乙腈(50∶50)时,实现基线分离的同时可保持很好的峰形,故选用5mol· L-1磷酸四丁基溴化(pH值=3.0)溶液-乙腈(50∶50)为本次实验的流动相。
3 方法学验证
3.1 线性范围与检出限
本方法研究校准曲线范围时,考察0.1~10μg·mL-1的线性宽度。配制浓度为 0.1、0.5、1.0、2.0、5.0、10.0 μg·m L-1的标准溶液。实验结果表明,在0.1~10μg·mL-1的范围内对甲苯磺酸异丙酯具有良好的线性关系,以浓度为横坐标X轴,以峰面积为纵坐标Y轴,得到线性方程y=23.28x-0.171,相关系数为0.9999。在本实验条件下,向空白样品中添加一系列浓度的对甲苯磺酸异丙酯标准溶液,根据仪器的灵敏度和样品处理步骤中稀释倍数,最终确定本方法检出限为如下:当称样量为0.5 g,定容体积为5 mL时,对甲苯磺酸异丙酯的检出限为1.0 μg·g-1。
3.2 方法的回收率与精密度
选取具有代表性的膏霜类、乳液类和蜡基类阴性化妆品样品分别进行3个水平(方法检出限、2倍方法检出限、10倍方法检出限)的加标回收实验,6次平行实验的结果见表2。在加标浓度范围内,化妆品中的对甲苯磺酸异丙酯平均回收率为95.2% ~101.2%,精密度 RSD 为1.2% ~2.1%;加标回收率和精密度实验结果符合GB/T27404-2008《实验室质量控制规范食品理化检测》的要求,方法具有准确可靠性和稳定可靠性[6]。

表2 对甲苯磺酸异丙酯加标回收实验测定结果
3.3 GCMS 法确证
由于化妆品的种类繁多,基质也各不相同,而液相色谱在定性方面存在不足,为避免假阳性样品的出现,本研究建立了对甲苯磺酸异丙酯GCMS确证方法。对于阳性样品或疑似阳性样品进行确证实验,以保证检测结果的准确性。确证条件见“1.5”,阴性样品加标浓度5 μg·g-1时的质谱图见图5。

图5 对甲苯磺酸异丙酯阴性样品加标浓度5μg·g-1时的提取离子质谱图
3.4 实际样品的检测
为验证方法的实用性,采用本方法对从广州市场购买的40种护肤品样品进行分析。试验结果表明,所有化妆品样品均未检测出本研究所分析的对甲苯磺酸异丙酯。
4 结论
建立了化妆品中对甲苯磺酸异丙酯的高效液相色谱检测法和GCMS确证方法,优化了色谱分离条件和样品前处理条件,最终选择乙腈溶液进行提取,菲罗门SuperLu C18(250×4.6 mm,5μm)色谱柱等度洗脱。结果显示,该方法的加标回收率(95.2% ~101.2%)和精密度(1.2% ~2.1%)良好,目标化合物的方法检出限为1.0μg·g-1。该方法前处理简单、适用性好,有利于化妆品中对甲苯磺酸异丙酯残留情况的监测,可为生产企业把控产品质量提供科学依据和技术支持。

