HPLC测定千里光提取物及千柏鼻炎胶囊中金丝桃苷在大鼠体内的血药浓度及药动学研究
朱雪飞
(江苏省扬州市食品药品检验检测中心,江苏 扬州 225000)
千柏鼻炎胶囊收载于《中国药典》2015版一部,由千里光、卷柏、羌活、决明子、麻黄、川芎、白芷7味制成,具有清热解毒,活血祛风,宣肺通窍之功效,临床主要用于风热犯肺、内郁化火、凝滞气血所致的鼻塞、鼻痒气热、流涕黄稠,或持续鼻塞、嗅觉迟钝;急慢性鼻炎、急慢性鼻窦炎见上述证候者[1]。千里光为菊科植物千里光SenecioscandensBuch.-Ham.的干燥地方部分,具有清热解毒,明目,利湿的功效[2]。金丝桃苷是千里光中的指标性成分[3],也是千柏鼻炎胶囊中的主要药效成分之一[4]。金丝桃苷具有抗肝肾损伤、抗抑郁、抗炎症、抗癌、抗氧化应激与抗细胞凋亡等药理作用[5-9]。关于千里光提取物及其复方制剂中金丝桃苷的药动学差异的比较尚未见报道,本研究为了考察复方中金丝桃苷的体内过程是否受中药配伍的影响,考察了大鼠灌胃千里光提取物和千柏鼻炎胶囊后的药动学特征,初步评价复方中其他中药配伍对金丝桃苷药动学特征的影响,以揭示中药复方配伍的合理性。
1 材料
日本岛津LC-20AT高效液相色谱仪(包括SPD-20A紫外检测器);N2000双通道色谱工作站(浙江大学智能信息工程研究所);高速冷冻离心机(美国Sigma公司);快速混匀器(江苏金坛仪器厂);岛津AUW220D分析天平(岛津);微量移液器(美国Thermo公司);BuchiR旋转蒸发仪(瑞士Buchi公司);HH系列数显恒温水浴锅(江苏金坛仪器厂);冷冻干燥机(德国Marin Christ公司)。金丝桃苷对照品(中国食品药品检定研究院,批号:111521-201205);千里光提取物(自制,HPLC法测得金丝桃苷含量为0.8312 mg·g-1);千柏鼻炎胶囊(广州白云山奇星药业有限公司,国药准字Z44022415,批号:160707,HPLC法测定金丝桃苷含量为0.7135 mg·g-1);乙腈(色谱纯,美国TEDIA);纯净水(自制)。清洁级SD雄性大鼠(扬州大学动物实验中心提供),体重250 g左右,适应性饲养1周。
2 方法
2.1 色谱条件
色谱柱:Kromasil C18(250×4.6mm,5μm);流动相:乙腈-0.2%醋酸水溶液(14∶86);检测波长:360 nm;流速:1mL·min-1;柱温30℃;进样量20μL。
2.2 千里光提取物的制备(同千柏鼻炎胶囊的制备工艺)
称取千里光药材适量,加10倍量水煎煮2次,第一次3h,第二次1.5h,合并煎液,滤过,滤液减压浓缩至适量,真空干燥后即得。经HPLC法测得金丝桃苷的含量为0.8312 mg·g-1。
2.3 对照品溶液的配制
精密称取金丝桃苷对照品适量,加乙腈醇制成每1mL含0.1364 mg的溶液,即得。
2.4 血浆样品的预处理
精密吸取血浆0.1mL,加0.2mL乙腈沉淀蛋白,涡流振荡1min,12000r·min-1高速离心5min,取上清0.45μm微孔滤膜滤过,20μL进样。
2.5 药动学研究
将SD雄性大鼠12只随机分成2组,每组6只,给药前禁食18h,自由饮水,将千里光提取物和千柏鼻炎胶囊(内容物)分别用1%CMC-Na分散,分别灌胃给药,给药剂量按金丝桃苷折算均为10 mg·kg-1,并于给药后给药前和给药后0.083,0.25,0.5,0.75,1,1.5,2,3,4,6,8,12,24 h眼眶后静脉丛取血,置肝素化的EP管中,分离血浆待预处理后测定。
2.6 统计学处理
采用DAS2.0药动学软件进行数据处理,血浆中金丝桃苷的峰浓度Cmax及达峰时间Tmax由实测数据直接得出。
3 结果
3.1 方法的专属性
空白血浆、空白血浆中加入金丝桃苷对照品、灌胃千里光提取物及灌胃千柏鼻炎胶囊的血浆样品色谱图见图1。由图可见,金丝桃苷与其他内源性成分分离效果良好,无干扰。

A.空白血浆;B.血浆中加入金丝桃苷对照品;C.灌胃千里光提取物后的血浆样品;D.灌胃千柏鼻炎胶囊后的血浆样品;1为金丝桃苷
图1 大鼠血浆样品中金丝桃苷的HPLC色谱图
3.2 线性范围及检测限
精密吸取金丝桃苷对照品溶液适量,置于1mL离心管中,加入大鼠空白血浆100μL,配制成金丝桃苷浓度分别为0.341,0.682,1.364,3.410,6.820,13.640 μg·mL-1的血浆样品,按2.4项下方法操作,进样分析,以峰面积(Y)对血药浓度(X)进行线性回归得Y=81.013X+1257(r=0.9998)(n=6),血浆中金丝桃苷在0.341~13.64 μg·mL-1之间线性关系良好,血浆中金丝桃苷检测限为0.079 μg·mL-1。
3.3 准确度实验
精密吸取100μL空白血浆置于1mL离心管中,18份,分3组,精密加入不同量的金丝桃苷对照品,使分别为1.364,3.410,6.820 μg·mL-1的低、中、高浓度样品,按 2.4项下方法操作,测定金丝桃苷含量,计算回收率,结果见表1。

表1 金丝桃苷回收率实验(n=6,x±s)
3.4 精密度实验
分别取金丝桃苷浓度为1.364,3.410,6.820 μg·mL-1的3种质量浓度的血浆样品在2.5项下的色谱条件下于日内和日间各测定5次,计算日内及日间精密度,结果见表2。
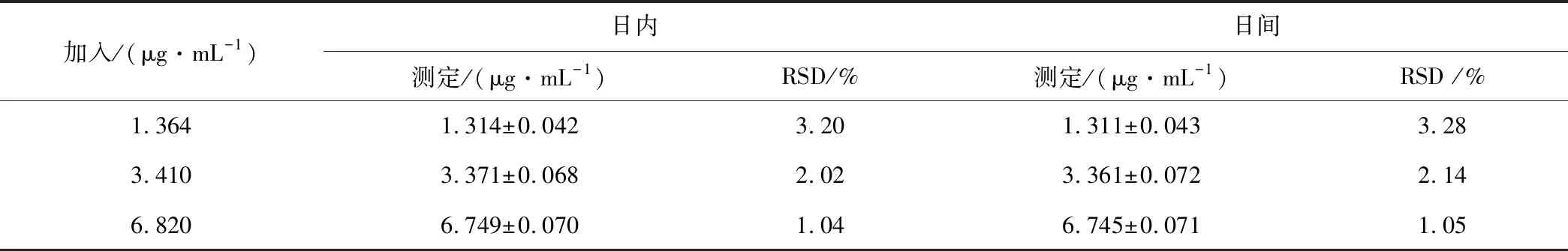
表2 金丝桃苷精密度实验(n=6,x±s)
3.5 提取回收率
取上述的金丝桃苷浓度为1.364,3.410,6.820 μg·mL-1的血浆样品(n = 6) ,按2.4项下方法处理,测定得到峰面积平均值A1;另取大鼠空白血浆100 μL,除不加对照品溶液,其他操作同“2.4”,向上清液中加入适量的金丝桃苷对照品溶液,使其浓度也分别为1.364,3.410,6.820 μg·mL-1的样品,测定得到峰面积平均值A2,计算得低、中、高3个质量浓度的血浆样品中山奈酚的提取回收率(R=A1/A2×100%)。结果为3个浓度的提取回收率分别为87.2%,89.3%,90.5%,其RSD分别为3.52%,2.79%,2.43%。
3.6 稳定性实验
分别考察了灌胃给药后大鼠血浆样本在室温、预处理后、反复冻融及长期冷冻条件下金丝桃苷的稳定性。结果表明,样本室温放置24h、预处理后样品室内(4℃)放置3d、反复冻融3次及-20℃冷冻储藏1月均有良好稳定性。
3.7 药动学参数
用DAS2.0药动学软件对测得的血药浓度数据拟合计算,结果表明千里光提取物和千柏鼻炎胶囊中的金丝桃苷在大鼠体内的药动过程均符合2房室模型,主要的药动学参数见表3,其平均药-时曲线见图2。

图2 金丝桃苷在大鼠体内的药-时曲线(-◆-千柏鼻炎胶囊灌胃;-▲-千里光提取物灌胃)表3 金丝桃苷在大鼠体内的主要药动学参数

参数千柏鼻炎胶囊千里光提取物t1/2β/h68.573±20.1969.315±17.54t1/2Ka/h5.105±0.892#1.150±0.273AUC0→t/(μg·h·mL-1)0.008±0.0030.006±0.003AUC0→∞/(μg·h·mL-1)0.040±0.006#0.023±0.002Tmax/h11Cmax/(μg·mL-1)2.277±0.234#1.821±0.179
注:与千里光提取物组比,#P<0.05。
4 讨论
分别比较了甲醇、乙腈、6 %高氯酸、三氯乙酸等有机溶剂,通过综合比较杂质干扰及提取回收率因素,发现乙腈沉淀蛋白效果最好。同时考察了不同体积比的血浆-乙腈(1∶2,1∶3,1∶4)对金丝桃苷测定的影响,发现血浆-乙腈(1∶2)时沉淀蛋白效果已经符合要求,如继续加大乙腈体积,则可能会对样品的检测浓度带来影响。
曾尝试采用2015版中国药典一部所载的千柏鼻炎胶囊中金丝桃苷的测定方法,即流动相乙腈-0.2 %醋酸水溶液(15∶85),用于本药动学研究中血浆样品的金丝桃苷检测,但通过前期的摸索研究,金丝桃苷与某内源性成分难以完全分离,故调整流动相为乙腈-0.2 %醋酸水溶液(14∶86)。
在本研究中,两组大鼠分别灌胃给予千里光提取物和千柏鼻炎胶囊后,金丝桃苷的药动学研究显示,其药-时曲线均符合二房室模型。但灌胃千柏鼻炎胶囊后金丝桃苷的Cmax为千里光提取物的1.25倍,AUC0→∞为1.74倍。上述结果表明,千柏鼻炎胶囊中的其他中药配伍对金丝桃苷的体内过程有较大的影响,即中药配伍能提高金丝桃苷口服吸收的生物利用度。此结果也从侧面表明中药在临床上配伍应用有其内在的合理性,但其具体机制有待进一步的深入研究。

