土壤中的微生物腐蚀研究进展
何奕,杜翠薇,徐大可,张达威,刘智勇
(1. 北京科技大学 新材料技术研究院,北京 100083;2. 腐蚀与防护教育部重点实验室,北京100083;3. 中国科学院金属研究所,沈阳 110016)
微生物广泛存在于各种自然环境、工业环境和极端环境中。许多材料如碳钢、不锈钢等对微生物都是敏感的。在金属腐蚀中约有20%的损失是由微生物引起的[1],每年,我国由于微生物腐蚀导致的损失高达约500亿人民币,严重危害着人们的生产生活。为了防止微生物腐蚀的发生,找到针对微生物腐蚀既环保又有效的防腐措施,必须清楚地认识其腐蚀行为。
土壤中含有大量的微生物,包括细菌、真菌、藻类等。一克土壤中约含有 1010个细菌,由大约 4000个种类构成[2]。在微生物腐蚀中,细菌是研究最多的,它们通过土壤粒子和其他潮湿的表面形成生物膜,通过胞外聚合物结合到一起。土壤微生物会引起材料的孔蚀、间隙腐蚀、选择性去合金腐蚀、沉积层下腐蚀等多种不利现象的发生,其中涉及到石油化工、造纸、核电站等多种企业和部门[3]。土壤中细菌形成的生物膜既可以抑制金属的腐蚀,也可以促进金属的腐蚀。
1 微生物腐蚀的机理
1.1 生物能量学机理
顾停月和徐大可[5-7]从生物能量学的角度出发,提出了生物阴极催化硫酸盐还原机理(Biocatalytic Cathodic Sulfate Reduction Mechanism,BCSR)。该机理的主要新观点为:微生物腐蚀金属的目的是为了获得能量。其具体反应方程式如下[8]:
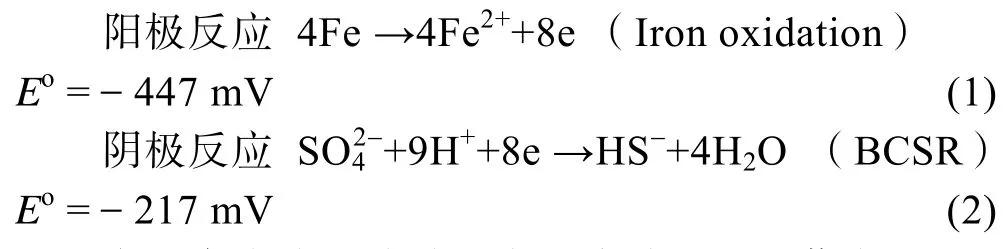
由反应(1)和(2)可得,硫酸盐还原菌(Sulfate Reducing Bacteria,SRB)在发生生物阴极催化硫酸盐反应时,ΔEo=+230 mV。根据公式 ΔGo=-nFΔEo<0可知,该反应能够在热力学上自发进行,且为一种放热反应。由腺苷酰硫酸 APS这种途径进入到硫酸盐还原菌细胞质内的 SO42-在细菌内酶的催化作用下被还原(如图 1所示),反应中铁为电子供体,SO42-在反应中得到电子。从动力学上来讲,细菌内的酶为整个腐蚀反应的进行提供了基础。硫酸盐还原菌在进行厌氧呼吸时,碳源(乳酸)为该反应提供电子。
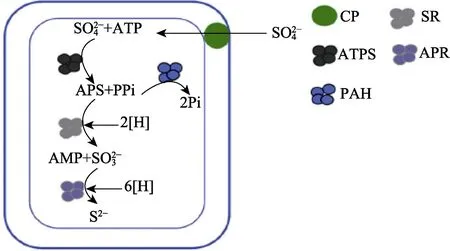
图1 异化硫酸盐的还原作用
以上的实验结果证明了生物阴极催化硫酸盐还原理论。根据该理论,可以合理解释产甲烷古细菌[6]和硝酸盐还原菌[9]也是为了获取生命必须的能量,从而对金属材料的表面造成了一定的腐蚀。
为获得能量进而腐蚀金属,以硝酸盐还原菌(Nitrogen Reducing Bacteria, NRB)为例:
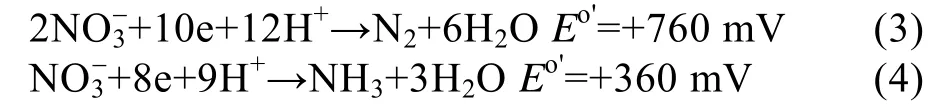
反应式(3)和(4)为NRB细胞质内可能发生的还原反应。在热力学上,将还原成NH3和N2的反应是可以自发进行的。与SRB相比,通过腐蚀,铁可以为NRB提供更多的能量。
虽然从生物能量学上讲,微生物可以获取更多的能量。然而在利用这些能量的过程中,生物膜的导电性、金属的表面形貌及其细菌对金属的吸附能力等这些因素都会对腐蚀过程造成重要的影响。为了更清楚地了解 MIC,在研究过程中必须考虑到生物电化学(即细胞外电子异相传递动力学)和生物膜的导电性等问题。
甲品种R1R1r2r2r3r3与感病品种(基因型为r1r1r2r2r3r3)杂交后,得F1为杂合子R1r1r2r2r3r3,实际上r2r2r3r3始终为纯合,因此分析过程中可以不考虑这两对基因。F1自交得F2,它们的基因型可能是R1R1、 R1r1、 r1r1,因为R1比r1片段短,所以分析电泳结果可以得出: 植株1为R1R1、植株2为r1r1、植株3为R1r1,因此由图中的扩增结果可以推测可抗病的植株有植株1和植株3;
1.2 生物电化学原理
近年来,微生物燃料电池(Microbial Fuel Cell,简称MFC)领域的快速发展,促进了人们对于生物电化学的认识,加深了人们对微生物腐蚀金属整个过程的了解[10]。根据BCSR理论,微生物腐蚀与生物阴极微生物燃料电池的最大区别在于不同种类的电子供体。微生物腐蚀的电子供体来源于金属的腐蚀,而生物阴极微生物燃料电池的电子供体则来自碳源的氧化。根据生物阴极催化硫酸盐还原机理,微生物主要是通过电子传递链获得电子,主要分为以下三种形式。
1)电子的直接传递。电子的直接传递是指细菌的细胞壁通过跟金属表面相接触,将电子以细胞的色素C(Cytochrome C)等膜蛋白的方式进行直接传递。此方式是微生物电子传导的重要途径。目前研究已经证实细胞色素C和铁硫蛋白存在于细胞外膜上,并作为电子传递的直接通道,使电子的传递变得更加快速。
2)细菌纳米线。Reguera等[11]在2005年首次提出纳米导线(Pili)这一概念,此理论通过导电原子力显微镜发现硫地杆菌的“菌毛蛋白”(Geopili)。这种蛋白通过具有导电性的细丝把电子传递给金属氧化物,同时将与内膜、周质或者外膜相关的蛋白电子导出到胞外,利用这种方式多血红素细胞色素能够将电子传递到菌毛上。整个过程中,电子流入和流出的相关机制还不是很详细,能够确定的是细菌通过形成生物纳米线(Pili)与金属表面形成电子传递的通道。
3)通过介体转移。电子在可溶性化合物中的传递,是一种间接的传递方式。Lojou等[12]指出,利用可溶性的氧化还原电子穿梭体可以有效地降低其传递活化能,提高电子转移速率。这些中介体可直接作用于金属离子,从而形成螯合物,并将这些螯合物传递给细胞膜上的酶或自身充当电子载体[13]。SRB腐蚀金属的三种电子转移方式如图2所示[14]。
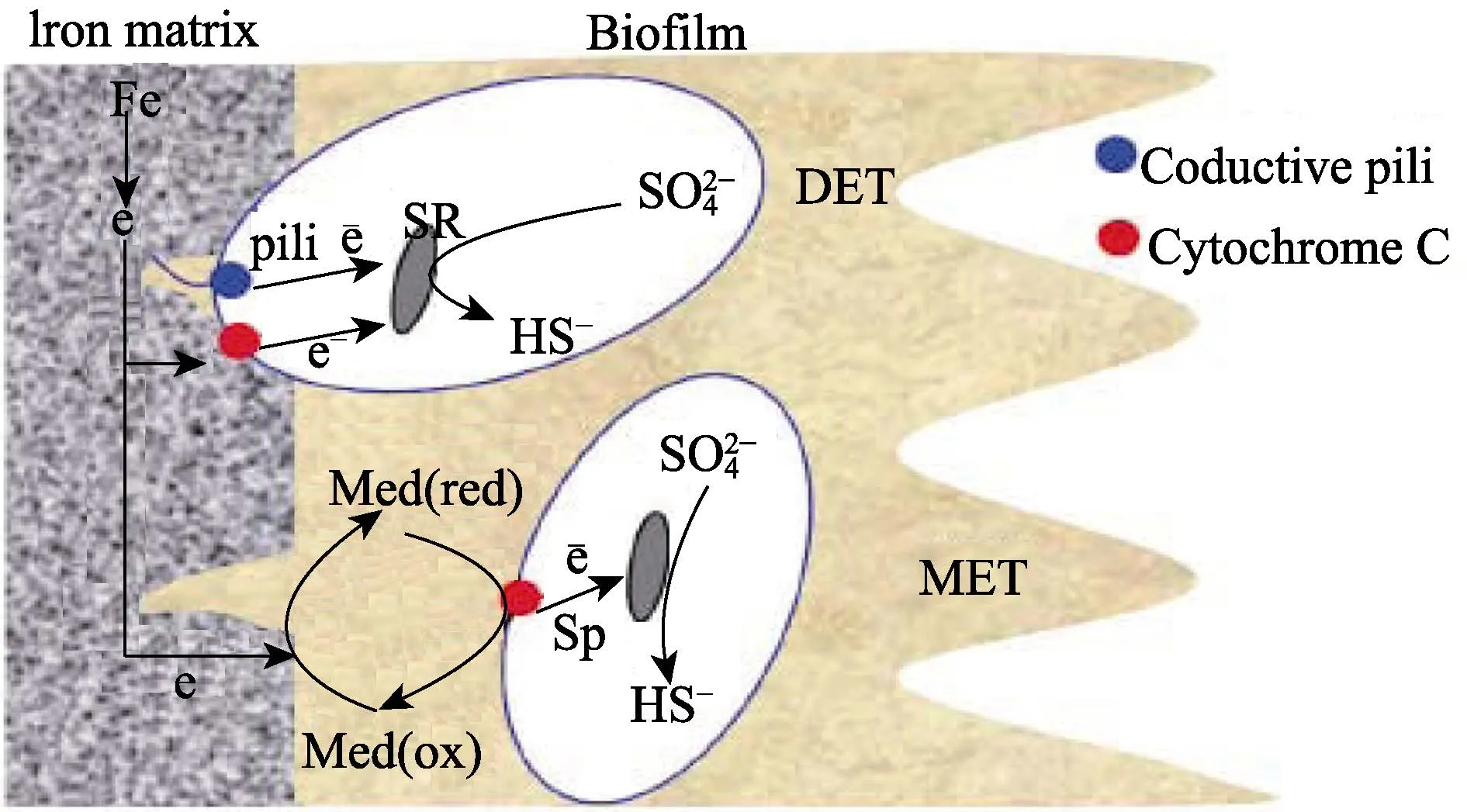
图2 SRB腐蚀金属的三种电子转移方式
由于所有的电子转移过程中都有多种酶和蛋白的参与,因此可利用基因工程的方法抑制某些蛋白和酶的表达,研究金属 MIC中可能的电子传递载体,并根据研究结果确定金属腐蚀过程中的电子传递的方式,从而寻找抑制微生物腐蚀的新方法,指导抗菌剂的研发与生产、输油管道的选材以及抗菌材料的进一步发展。
2 环境因素
细菌所需的营养物质一般包括:Na+、K+、Mg2+、Ca2+、、Cl-、、、,有的还需要Fe2+的存在。土壤中的Cl-浓度、Fe2+浓度、氧浓度、温度、pH值等,都会影响细菌对材料的腐蚀行为[15]。
2.1 氧的影响
在曝氧期间,金属的腐蚀速率与厌氧时相比明显高很多,形成的点蚀更深[16]。Hardy[17]等人研究发现,当表面覆盖有硫化物的生物膜接触空气之后,碳钢发生了严重的孔蚀。提出这可能与生物膜在阳极区和阴极区的差异有关,但对于反应机理还不清楚。Vonrege和Sand[18]在含SRB的介质分别测定覆盖有生物膜的37钢暴露在氧气中的腐蚀率,实验发现,37钢的最大穿透深度在无氧和有氧交替变化的条件下,要比在严格厌氧条件时的大,但对其机理并没有给出合理的解释。
2.2 pH值的影响
溶液中 H+能够与细胞膜中的酶相互作用,从而影响细菌活动和细胞壁上酶的活性,因此溶液pH能够影响微生物腐蚀过程[19]。目前,对硫酸盐还原菌(SRB)的各项研究(生理、生化)表明,该种细菌能够较快地适应新环境,适合其生长的pH值较为广泛,一般在5.5~8.5之间,其中最佳范围为7.0~7.5。因此当SRB所处的环境pH值较高时,将会抑制细菌的生长和繁殖,通过该方法可以控制微生物引起的腐蚀[20]。赵阳国等[21]研究发现,pH<7时,Fe2+不能同H+作用产生H2被SRB利用。吴文菲等[22]研究了pH对微生物还原硫酸盐的影响,发现在pH在7.0附近时,细菌的生长率最高。当环境温度、溶液盐度等条件相对适宜时,即便 pH减少到 4.0,仍存在 40%的硫酸盐去除率,可见SRB对pH的适宜能力很强。
2.3 温度的影响
在一定的温度范围内,温度升高时,细胞的生长速率也会随之增加[20]。范梅梅等[23]在研究嗜热菌对X60钢的腐蚀行为时发现,在30~75 ℃之间,随着温度的升高,腐蚀速率也逐渐增加(如图3所示)。冯颖等人[24]关于温度对中温 SRB还原反应的影响实验证明,36 ℃是最适合还原反应的环境温度。当温度高于 33 ℃,此时温度对细菌还原反应影响不大,但低于 30 ℃时,温度对还原反应抑制效果明显,并且随着温度的降低,这种抑制作用越强。

图3 温度对X60钢腐蚀速率的影响
3 研究现状
3.1 加速腐蚀现象
微生物促进金属腐蚀的机理一般可概括为以下几种:生物膜使金属表面形成氧浓差电池;生物膜产生具有腐蚀性的代谢物;生物膜对金属表面的钝化膜、腐蚀产物膜以及防腐蚀涂层具有破坏性;生物膜通过代谢消耗介质中的缓蚀剂等,从而加剧金属的腐蚀[25]。
N. Bolton[26]等在研究短小芽孢杆菌对不同类型钢材的腐蚀影响时发现,该种细菌能够在很大程度上促进镀锌钢的腐蚀(如图4所示),但对碳钢的腐蚀影响并不大。同时也指出,关于镀锌钢的点蚀机理虽然也有相关研究,但具体原因还未解释清,推测该腐蚀反应与生物膜和种群密切相关。但是,细菌的种类不同,微生物腐蚀机理也存在差异[27]。
R.F. Jack[28]等研究枯草芽孢杆菌时发现,浸泡初期碳钢的腐蚀速率被加速。随浸泡时间的延长,其腐蚀速率逐渐降低。他认为枯草芽孢杆菌之所以能加速腐蚀速率,是因为菌落膜内的次生代谢产物有可能是加速腐蚀的原因。

图4 镀锌钢在短小芽孢杆菌作用下发生点蚀
Xu Dake[29]等人研究C1018钢在地衣芽胞杆菌作用下的腐蚀行为时发现,将C1018钢于37 ℃下放置在地衣芽孢杆菌中3、7天,平均质量损失分别为(如图 5所示):0.24、0.89 mg/cm2。在无菌条件下,C1018钢于37 ℃下放置在地衣芽孢杆菌中7天的质量损失为0.05 mg/cm2。实验结果表明,地衣芽孢杆菌加速了碳钢的腐蚀,原因是地衣芽孢杆菌的生物膜相当于催化剂,促进了点蚀的发生。

图5 C1018在地衣芽胞杆菌作用下3、7天的平均质量损失
3.2 抑制腐蚀现象
微生物抑制腐蚀的主要机理如下:微生物代谢消耗材料表面的阴极去极化剂;微生物可以分泌抗菌素,减少金属的腐蚀;微生物的代谢产物在金属表面形成膜,如钝化膜或分泌具有粘性的缓蚀剂类等物质;通过介质中的有机物将电子直接传递到电极表面,抑制金属的腐蚀。
E. Juzelianas[30]等人研究蕈状芽孢杆菌分别对铝、锌、钢的腐蚀影响,电化学阻抗谱结果表明,该细菌对铝的腐蚀起到抑制作用,对锌的腐蚀则有促进作用,但并不影响钢的腐蚀。然而,他们未对上述现象的原因给出具体的解释。
A. Rajasekar和Y.P. Ting[31]研究在有机、无机介质中巨大芽孢杆菌和假单胞菌对304不锈钢腐蚀的影响时发现,在无机介质中,巨大芽孢杆菌和假单胞菌会使腐蚀电位(Ecorr)和点蚀点位(Epit)降低。无机介质中的 NO3-以及 HPO42-、H2PO4-能促进细菌的代谢过程,形成钝化膜,减少不锈钢的腐蚀速率。在有机介质中,巨大芽孢杆菌和假单胞菌都会促进不锈钢表面点蚀的形成。根据电化学原理和表面分析,浸泡初期没有产生抑制层时,铁部分溶解,溶解的铁会和K2HPO4及KH2PO4发生反应生成盐,堆积在试样表面。
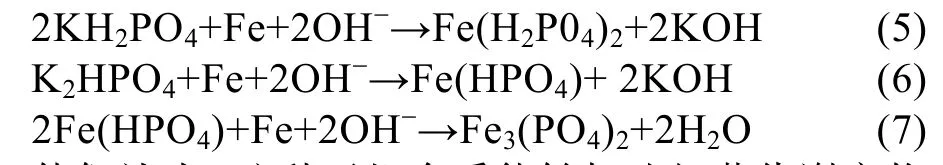
他们认为,这种无机介质能够加速细菌代谢产物的形成,形成一种磷酸铁盐钝化膜,从而抑制不锈钢的腐蚀。对于为何在有机介质中,两种细菌均可以加速不锈钢的点蚀,没有作出解释。
参阅文献资料可知,关于土壤微生物的腐蚀行为,由于所用材料、介质的不同,并且有些研究不够深入,仅仅描述所发生的腐蚀现象及腐蚀行为,而对腐蚀规律则没有进行深入研究,而且部分结果相异,研究中提出的腐蚀机理不尽相同,不具有可比性。
4 结语
生物膜在土壤微生物腐蚀中具有重要的地位和作用。生物膜在金属表面的形成很难避免,微生物腐蚀往往是菌体生命活动中其他因素(产生表面活性剂或酸性代谢产物、产生蛋白催化酶、消耗氧气、分解有机物质、参与电子传递等)和生物膜对金属基体的综合作用。在细菌的生长过程中,生物膜在金属表面的形成、与金属基体如何作用等,还需要更加深入地研究。未来的发展趋势将更着重于微观机理的研究,综合利用先进的技术来进一步揭示微生物腐蚀的微观机制,为达到更好的防护目的做准备。
装备环境工程2019年3期
