含NaCl超细水雾抑制甲烷爆炸实验研究*
杨 克,张 平,邢志祥,纪 虹,周 越,王 壮
(1.常州大学 环境与安全工程学院,江苏 常州 213164; 2.常州大学 石油工程学院,江苏 常州 213106)
0 引言
采煤、天然气输送等相关领域经常发生瓦斯爆炸,为防止瓦斯爆炸事故,学者们对甲烷抑爆技术进行了大量实验和理论研究。超细水雾作为1种低成本、无污染的资源,能够降低火焰温度,减弱热传播[1-3],而添加剂的引入可以更好地改善超细纯水雾抑爆效果[4]。因此,研究含添加剂的超细水雾对甲烷爆炸抑制效果具有重要意义。
Cao等[4-5]用质量浓度分别为5%,8%,15%的含氯化钠超细水雾来进行体积分数分别为6.5%,8%,9.5%甲烷的爆炸试验,研究发现NaCl可有效提高超细纯水雾抑制甲烷爆炸效果,且含5%氯化钠超细水雾抑爆效果较好;Joseph等[6]进行了含添加剂超细水雾抑制甲烷爆炸的试验研究,发现添加NaCl,KCl或KHCO3可使超细纯水雾的抑爆效率大幅提高,其中K+消除自由基的能力是Na+的2倍;Zhang等[7]通过试验研究不同添加剂对甲烷抑爆效果的影响,发现抑爆效果按照纯水、NH4H2PO4,KH2PO4,KCl,CH3COOK,KNO3,K2C2O4的顺序增强;Yu等[8-9]进行了含NaCl带电水雾减弱甲烷爆炸超压的试验研究,发现带电水雾使雾场更分散、更稳定,可以延迟超压峰值到达时间;刘江虹等[10]比较了分别含CaCl2,NaCl,KCl,FeCl2细水雾的灭火性能,发现根据质量比其灭火性能依次减弱;许红利等[11]进行了含添加剂细水雾高原灭火效果影响的试验研究,结果表明在低压低氧的情况下,质量浓度为1.5% FeCl2和10% NaCl的细水雾对柴油池火的灭火效率较高。前人对含氯化钠细水雾研究较多,但主要集中于扑灭各类火灾,对含氯化钠超细水雾抑爆研究较少,且大多未详尽考虑到氯化钠浓度对抑爆甲烷效果的影响。
基于此,本文将着重考虑氯化钠浓度对抑爆甲烷效果的影响。首先,测量含不同浓度氯化钠超细水雾粒径;然后,分析含不同浓度氯化钠超细水雾对甲烷爆炸平均火焰传播速度、爆炸超压、平均升压速率等指标的影响;最后,进行对比分析,确定最佳浓度。以期进一步推动含添加剂超细水雾抑制甲烷爆炸的研究。
1 实验设计
1.1 实验装置
此次实验所用的装置主要由超细水雾发生装置(平均雾化率为0.035 mL/s)、气体输送系统(40 L甲烷气瓶、40 L压缩空气气瓶)、信号采集与数据处理系统(信号采集卡为USB-1608FS-Plus,采集卡最大频率为400 kS/s)、高速摄像系统(实验采用1 000 fps,可记录帧数为4 896 帧,共4.896 s)、反应空间管道(管道内腔尺寸为50 mm×50 mm×1 000 mm,内部空间容量为2.5 L)、点火装置(实验采集高压脉冲点火器,双电极点火电压设为6 kV)等构成。具体构造如图1所示。
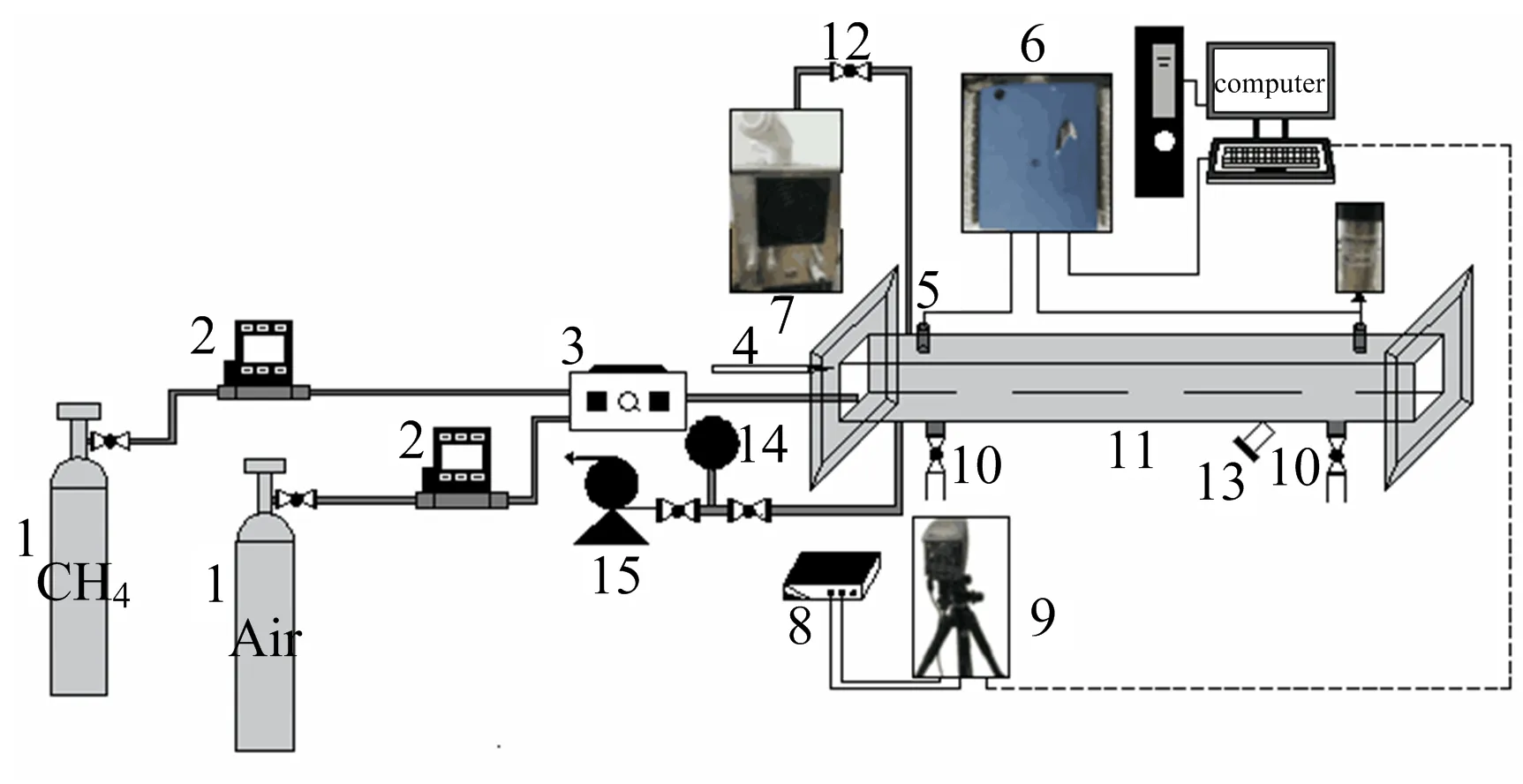
1.高压气瓶;2.质量流量控制器;3.预混装置;4.点火装置;5.压力传感器;6.压力数据采集卡;7.超细水雾系统;8.同步控制器;9.高速摄影仪;10.污水排放口和控制阀;11.爆炸管道;12.控制阀;13.光电传感器;14.真空计;15.真空泵图1 实验系统构造Fig.1 Construction of the experimental system
1.2 试验方法
实验的目的是研究含不同浓度NaCl超细水雾对甲烷爆炸抑制效果的影响。实验内容包括粒径测试和甲烷抑爆实验,粒径测试主要为测量超细纯水雾和含不同浓度NaCl超细水雾粒径(NaCl浓度分别为2.5%,5%,7.5%,10%,12.5%);甲烷抑爆试验中,以通雾量为0.7 mL的含不同浓度NaCl超细水雾作用于体积分数为9.5%甲烷,每次实验记录压力和火焰数据。实验进行2~3次。
2 实验结果与分析
2.1 NaCl浓度对超细水雾粒径分布的影响
在外界条件不变的情况下,对浓度分别为0%,2.5%,5%,7.5%,10%,12.5%的含氯化钠超细水雾进行粒径测试,观察不同NaCl浓度下,超细水雾粒径的变化。
表1为含不同浓度NaCl超细水雾的粒径分布。表1中,SMD(Sauter Mean Diameter)为表面积平均直径,μm;VAD(Volume Average Diameter)为体积平均直径,μm。由表1可以看出,当NaCl浓度为0%~5%时,超细水雾的SMD,VAD,中径值(V50)随NaCl浓度增加而增加;当NaCl浓度为5%~10%时,超细水雾的VAD,SMD,V50随NaCl浓度的增加而减小;当NaCl浓度超过10%时,超细水雾的VAD,SMD,V50几乎保持不变。相比于超细纯水雾,含NaCl超细水雾特征参数V10,V50,V90略有增加,但总体涨幅不大;当NaCl浓度为5%时,超细水雾特征参数变化最明显,从整体上来看,NaCl浓度的变化对水雾粒径影响较小,含NaCl超细水雾粒径主要集中在4.384 μm左右,所以NaCl粒径的变化并不是抑爆效果增强的主要原因。含氯化钠超细水雾抑制甲烷爆炸主要体现在其热分解的自由基中断甲烷链式反应上。

表1 含不同浓度NaCl超细水雾的粒径分布Table 1 Particle size distribution of ultrafine water mist with different concentrations of NaCl
2.2 含不同浓度氯化钠超细水雾抑爆甲烷效果分析
将通雾量为0.7 mL,分别含0%,2.5%,5%,7.5%,10%,12.5%的NaCl超细水雾作用于体积分数为9.5%的甲烷,观察火焰、最大爆炸超压、平均火焰传播速率以及平均升压速率随不同浓度含NaCl超细水雾的变化。表2为含不同浓度NaCl超细水雾抑爆效果。

表2 含不同浓度NaCl超细水雾抑爆效果Table 2 Explosion suppression effect of ultra-fine water mist containing different concentrations of NaCl
2.2.1 含不同浓度氯化钠超细水雾对火焰影响
火焰传播动态如图2所示。图2(a)为超细纯水雾作用于体积分数为9.5%甲烷火焰传播变化图。由图2(a)可以看出,在时间为60~90 ms时,火焰锋面由持平转为斜平面,靠近管道下方管壁的火焰出现延伸,传播速度大于管道上方管壁火焰,火焰传播速度减小,主要是气体被点燃初期受热膨胀,且超细水雾的受热蒸发吸热降温作用;在时间为90 ms时,火焰传播速度逐渐增大,主要是水雾进入管道反应区,与自由离子发生碰撞,发生对流扰动。当火焰传播到管道另一侧时,由于燃烧能量波的积聚,火焰速度增大,火焰冲破封闭薄膜。图2(b)为含2.5%NaCl超细水雾作用于体积分数为9.5%甲烷火焰传播变化图。由图2(b)可以看出,在时间为30~200 ms阶段,火焰传播整体速度较小,70 ms时为“指形”火焰向“郁金香”火焰转变的临界点,火焰传播速度最小;在火焰点燃240 ms之后,火焰由“郁金香”转为“指形”。发生这些变化的原因是,水雾微粒吸热汽化速度变快后产生的反向气流对火焰反应区产生扰动,引发火焰峰面积增大,火焰由指形转为贴壁两侧火焰传播速度快的微凹形湍流“郁金香”火焰,又由于含氯化钠超细水雾微粒吸热降温效果,以及阻碍链式反应的作用机理,火焰传播的反向气流速度减减慢,致使对称涡流消失,局部贴壁火焰传播速度回归正常,微凹形“郁金香”火焰短暂出现后再次消失[12]。直至火焰点燃1 100 ms以后,火焰传播受封闭薄膜的阻碍,火焰传播速度略有停滞,在火焰点燃后1 230 ms时,轰破薄膜。由图2可以看出,在火焰点燃360 ms时,超细纯水雾作用下火焰传播距离明显大于含2.5%NaCl超细水雾作用下火焰传播的距离。因此,含氯化钠超细水雾能更好地减小火焰传播强度。

图2 火焰传播动态变化Fig.2 Dynamic change of flame propagation
图3为不同喷雾条件下平均火焰传播速度变化以及较纯甲烷相比下降值变化图。由图3可以看出,当NaCl浓度为0%~2.5%时,平均火焰传播速度随其浓度的增加呈上升趋势;当NaCl浓度为2.5%~12.5%时,平均火焰传播速度随其浓度的增加呈下降趋势。表3为不同浓度NaCl作用下平均火焰传播速度的变化。由表3可以看出,含2.5%NaCl平均火焰传播速度较纯甲烷爆炸平均火焰传播速度下降了53.7%,抑制甲烷火焰传播效果最差的是12.5%氯化钠,其平均火焰传播速度较纯甲烷爆炸仍下降了43.6%,远超过超细纯水雾作用下降的效果,主要是在吸热降温的基础上,氯化钠热分解产生的离子与火焰反应区的自由基发生反应,阻碍甲烷链式反应,降低火焰传播速度。
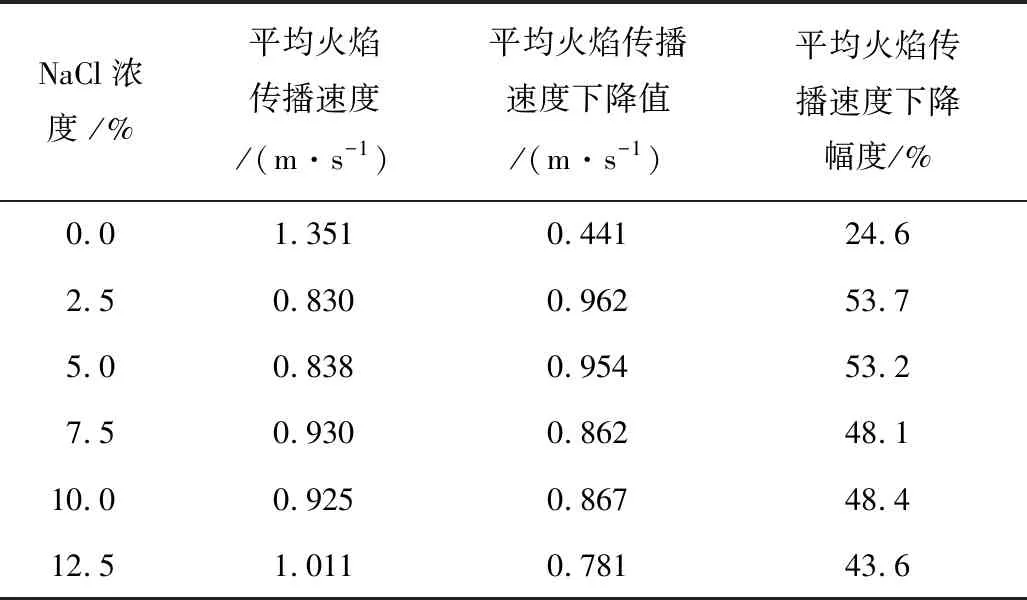
表3 不同浓度NaCl作用下平均火焰传播速度的变化Table 3 Changes in average flame propagation speed withdifferent concentrations of NaCl

图3 不同浓度NaCl下平均火焰传播速度的变化Fig.3 Curve of the average flame propagation speed under different concentrations of NaCl
2.2.2 含不同浓度氯化钠超细水雾对爆炸超压的影响
表4是NaCl浓度分别为0%,2.5%,5%,7.5%,10%,12.5%作用下最大爆炸超压的变化状况。图4为不同喷雾条件下最大爆炸超压变化以及较纯甲烷相比下降值变化。从表4中发现,超细纯水雾的添加使得甲烷最大爆炸超压较纯甲烷自由爆炸的最大爆炸超压下降了1.168 kPa。针对5个不同的NaCl浓度的甲烷抑爆实验,其爆炸超压分别下降了5.786,4.164,5.170,3.144和2.096 kPa,其中,含2.5%NaCl超细水雾下降幅度最大,最大爆炸超压较纯甲烷自由爆炸下降了63.4%。在浓度大于10%的NaCl作用下,甲烷最大爆炸超压下降值较小,占纯甲烷自由爆炸时最大爆炸超压的23%,约为是纯水雾作用下最大爆炸超压下降值的2倍。由图4可知,与纯水超细水雾单独作用相比,含氯化钠超细水雾作用下的最大爆炸超压更小,抑爆效果更佳。由此可见,添加NaCl能够大幅提高超细水雾对甲烷的抑爆能力。

表4 不同浓度NaCl作用下甲烷最大爆炸超压的变化Table 4 Changes in maximum explosion overpressure with different concentrations of NaCl

图4 不同浓度NaCl对最大爆炸超压的变化Fig.4 Curve of the maximum explosion overpressure under different concentrations of NaCl
图5是NaCl浓度分别为0%,2.5%,5%,7.5%,10%,12.5%超细水雾作用下对应的压力随时间变化曲线。由图5可知,不同浓度NaCl抑爆甲烷的压力曲线与纯甲烷自由爆炸的压力曲线都呈现双波峰,其中,仅2.5%NaCl浓度对应的甲烷最大爆炸压力在第1波峰。火焰传播初期,化学反应迅速加剧,燃烧产生的压缩波较大,导致第1波峰峰值较大;到火焰传播中后期,火焰传播速度减慢,导致第2波峰的爆炸超压小于第1波峰的峰值。当氯化钠浓度达到12.5%,其抑爆效果明显减弱,但其最大爆炸超压仍小于超细纯水雾。含12.5%的氯化钠抑爆效果减弱的主要原因是,随着氯化钠浓度的升高,溶液的比热容升高,超细水雾微粒吸热汽化速度变慢,而压力波传播速度很快,气化速度小于压力波积聚速度,压力出现显著上升。

图5 含不同浓度NaCl超细水雾对应的压力随时间变化Fig.5 Curve of pressure versus time for superfine water droplets containing different concentrations of NaCl
2.2.3 含不同浓度NaCl超细水雾对爆炸升压速率的影响
平均升压速率的计算公式如式(1)所示。
(1)
式中:v为平均升压速率,kPa/s;Pmax为最大爆炸压力,kPa;P0为初始压力,kPa;Δt为由初始压力增大到最大爆炸压力所用时间,s。
表5为不同浓度NaCl超细水雾作用下平均升压速率变化,图6为不同浓度NaCl超细水雾喷雾条件下平均升压速率变化以及较纯甲烷相比下降值变化。当NaCl浓度处于0~5%时,随着NaCl浓度的增大,甲烷爆炸的平均升压速率较纯甲烷自由爆炸的下降值增大;当NaCl浓度增大到5%时,甲烷爆炸的平均升压速率达到最小值,较纯甲烷自由爆炸的平均升压速率下降了71.7%;当NaCl浓度值为5%~12.5%时,随着NaCl浓度的升高,含NaCl的超细水雾抑制甲烷爆炸平均升压速率较纯甲烷自由爆炸下降值逐渐降低并趋于平稳。其中,纯水超细水雾的平均升压速率下降幅度要远小于抑爆效果较差的含12.5%NaCl超细水雾的升压速率下降幅度。
通过上述对含不同浓度NaCl超细水雾对抑爆性能影响的分析可知,总体而言,含NaCl超细水雾抑爆性能远强于超细纯水雾的抑爆效果,其中抑制甲烷爆炸效果最佳的是含2.5%NaCl超细水雾。
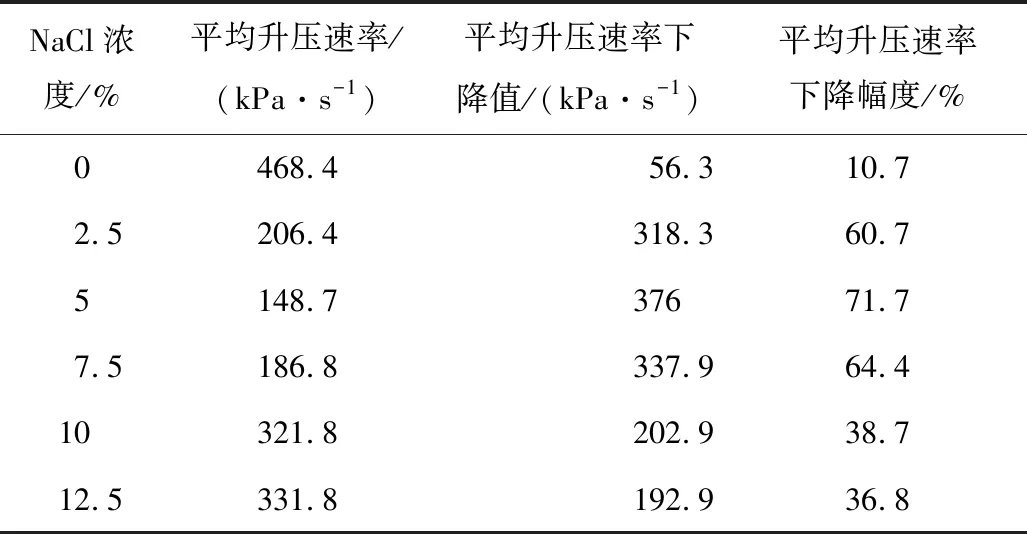
表5 不同浓度NaCl作用下平均升压速率的影响Table 5 Changes in average pressure rise rate with different concentrations of NaCl

图6 不同浓度NaCl对平均升压速率的变化Fig.6 Curve of the average pressure rise rate under different concentrations of NaCl
3 含NaCl超细水雾抑爆甲烷机理分析
含NaCl超细水雾抑爆甲烷是其物理和化学共同作用的结果。物理作用体现在含NaCl超细水雾粒径小,比热容较大,汽化潜热约为2 280 kJ/kg,导热系数小,使其蒸发速度快,减弱热辐射的传递,阻碍链式反应。化学作用主要体现在添加剂热分解产生的离子与火焰反应区的自由基(H原子以及自由基OH)发生反应,阻断链式反应进行。
众所周知,甲烷燃烧的机理如以下关键支链反应所示[13-14]:
OH·+CH4→CH3·+H2O
H·+CH4→CH3·+H2
O·+CH4→CH3·+OH·
所选用的NaCl受热分解产生Na·和NaO·自由基与CH4爆炸产生的OH·和H·自由基反应[7-8,15-16],可以中断链式反应并抑制爆炸:
Na·+OH·+M→NaOH+M
NaOH+H→Na·+H2O
NaOH+OH·=NaO·+H2O
NaO·+H·→Na·+OH·
NaO·+O·→Na·+O2
NaO2+CO→NaO·+CO2
Cl·+Cl·+M→Cl2+M
Cl2+H·→HCl+Cl·
HCl+H·→H2+Cl·
H·+OH·+Cl·→H2O+Cl·
含NaCl超细水雾抑制甲烷爆炸是水雾微粒的物理作用和NaCl热分解阻断链式反应的化学作用充分发挥协同抑爆效果,因此其抑爆性能要强于超细纯水雾的抑爆性能。
4 结论
1)NaCl浓度对超细水雾粒径影响不大,粒径的变化不是含氯化钠超细水雾抑爆效果增强的主要原因,主要是由于NaCl受热分解产生自由基与CH4爆炸产生的OH·和H·自由基反应使得抑爆效果显著增强。
2)通雾量为0.7 mL的超细纯水雾作用于体积分数为9.5%的甲烷,相比于9.5%纯甲烷自由爆炸,其火焰传播速率、最大爆炸超压以及平均升压速率分别下降了24.6%,12.8%和10.7%。
3)通雾量为0.7 mL的含NaCl超细水雾作用于体积分数为9.5%的甲烷,NaCl浓度为2.5%的超细水雾对甲烷爆炸的抑制性能最佳,相比于9.5%纯甲烷自由爆炸,其火焰传播速率、最大爆炸超压以及平均升压速率分别下降了53.7%,63.4%和60.7%,相比于超细纯水雾,分别下降了38.6%,58%和56%。

