基于多元统计分析的不同产地莪术饮片质量评价
顾丽亚, 胡 玮, 陆兔林,2∗, 郝 敏, 毛春芹∗, 季 德,2
(1.南京中医药大学药学院,江苏南京210023;2.江苏省中药炮制重点实验室,江苏南京210023)
莪术来源于姜科植物蓬莪术Curcuma phaeocaulis Valeton、广西莪术Curcuma kwangsiensis S.G.Lee et C.F.Liang或温郁金Curcuma wenyujin Y.H.Chen et C.Ling的干燥根茎,具有行气破血、消积止痛的功效[1]。现代研究表明莪术具有广泛的药理活性,包括抗炎、抗肿瘤、抗癫痫和抗菌等[2-9],倍半萜和姜黄素类成分是其发挥药理作用的主要物质基础。文献表明不同产地土壤、光照、水分、温度等环境因素有差异,造成中药次生代谢产物积累不同,影响药材品质,进而导致中药饮片质量不一[10-11]。莪术主产于广西、四川、浙江等地[12],作为临床常用的中药饮片,其品质好坏关系到用药的安全性和有效性。在质控方面,2015版 《中国药典》仅以挥发油得率为评价指标,不能全面评价莪术饮片的质量。目前,关于莪术饮片质量分析的文献较多,但研究主要针对莪术饮片炮制前后化学成分变化情况,不同产地各自收集的批次较少,不具有统计学意义[13-14]。
本实验采用HPLC法测定了30批不同产地莪术饮片中5个倍半萜类成分 (β-榄香烯、呋喃二烯、吉马酮、莪术醇、莪术二酮)和3个姜黄素类成分 (双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素)的含有量,结合聚类分析 (HCA)[15]、主成分分析 (PCA)[16-17]和正交偏最小二乘法(O2PLS-DA)[18]等多元统计分析方法,筛选出不同产地莪术饮片化学成分差异的标志性成分,系统、客观地评价质量差异,为其临床用药提供参考。
1 仪器与材料
1.1 仪器 Agilent 1260型高效液相色谱仪 (美国安捷伦公司);HL-350 A型高速多功能粉碎机 (上海塞耐机械有限公司);FA1104型电子分析天平(上海精密科学仪器有限公司);Mettler AG285电子分析天平 (瑞士梅特勒-托利多集团);KQ-500E型医用超声清洗器 (昆山超声仪器有限公司)。
1.2 试剂与试药 β-榄香烯对照品 (批号170802)、呋喃二烯对照品 (批号170510)、莪术醇对照品 (批号170515)均购于南京森贝伽生物科技有限公司;吉马酮对照品 (批号lw17040709)、莪术二酮对照品 (批号lw17101103)、姜黄素对照品 (批号lw17091410)、去甲氧基姜黄素对照品 (批号lw16090803)、双去甲氧基姜黄素对照品 (批号lw16090905)均购于南京良纬生物科技有限公司。乙腈 (色谱纯,德国Merck公司);甲醇 (色谱纯,山东禹王和天下新材料有限公司);甲酸 (色谱纯,美国Anaqua chemicals supply公司);无水乙醇 (分析纯,无锡市亚盛化工有限公司);Milli-Q超纯水 (南京汉隆实验器材有限公司)。
30批莪术饮片中,20批购于不同饮片生产企业,10批由浙江省瑞安市通明温郁金专业合作社提供药材,自行炮制。经南京中医药大学药学院陆兔林教授鉴定,植物基原分别为蓬莪术Curcuma phaeocaulis、广西莪术Curcuma kwangsiensis S.G.lae et C.F Liang或温郁金Curcuma wenyujin Y.H.Chen et C.Ling的干燥根茎。分别取净莪术参照2015版 《中国药典》制得浙江产地的莪术饮片。信息见表1。

表1 样品信息Tab.1 Information of samples
2 方法与结果
2.1 色谱条件 Agilent pro shell C18色谱柱(150 mm×4.6 mm,5 μm); 流动相0.5‰甲酸乙腈(A) -0.5‰甲酸水 (B), 梯度洗脱 (0~10 min,40%~50%A;10~20 min,50% ~75%A;20~25 min,75% ~95%A; 25~30 min, 95%A; 30~35 min,95% ~40%A; 35~40 min, 40%A); 柱温30℃; 体积流量 1 mL/min; 检测波长 216、415 nm;进样量10 μL。色谱图见图1。
2.2 溶液的制备
2.2.1 对照品溶液制备 精密称取β-榄香烯、呋喃二烯、吉马酮、莪术醇、莪术二酮对照品适量,加甲醇定容,分别配制成质量浓度为 2.714、0.508、 0.254、 0.496、 0.601 mg/mL 的倍半萜类混合对照品贮备液;精密称定双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素对照品适量,加甲醇定容,分别配制成质量浓度为 0.011、0.051、0.071 mg/mL的姜黄素类混合对照品贮备液。
2.2.2 供试品溶液制备 取莪术饮片适量,粉碎,过3号筛,精密称取0.5 g粉末,置于50 mL具塞锥形瓶中,加入20 mL的70%乙醇,称定质量,超声30 min(功率250 W,频率20 kHz),补足减失质量,过0.45 μm微孔滤膜。
2.3 方法学考察
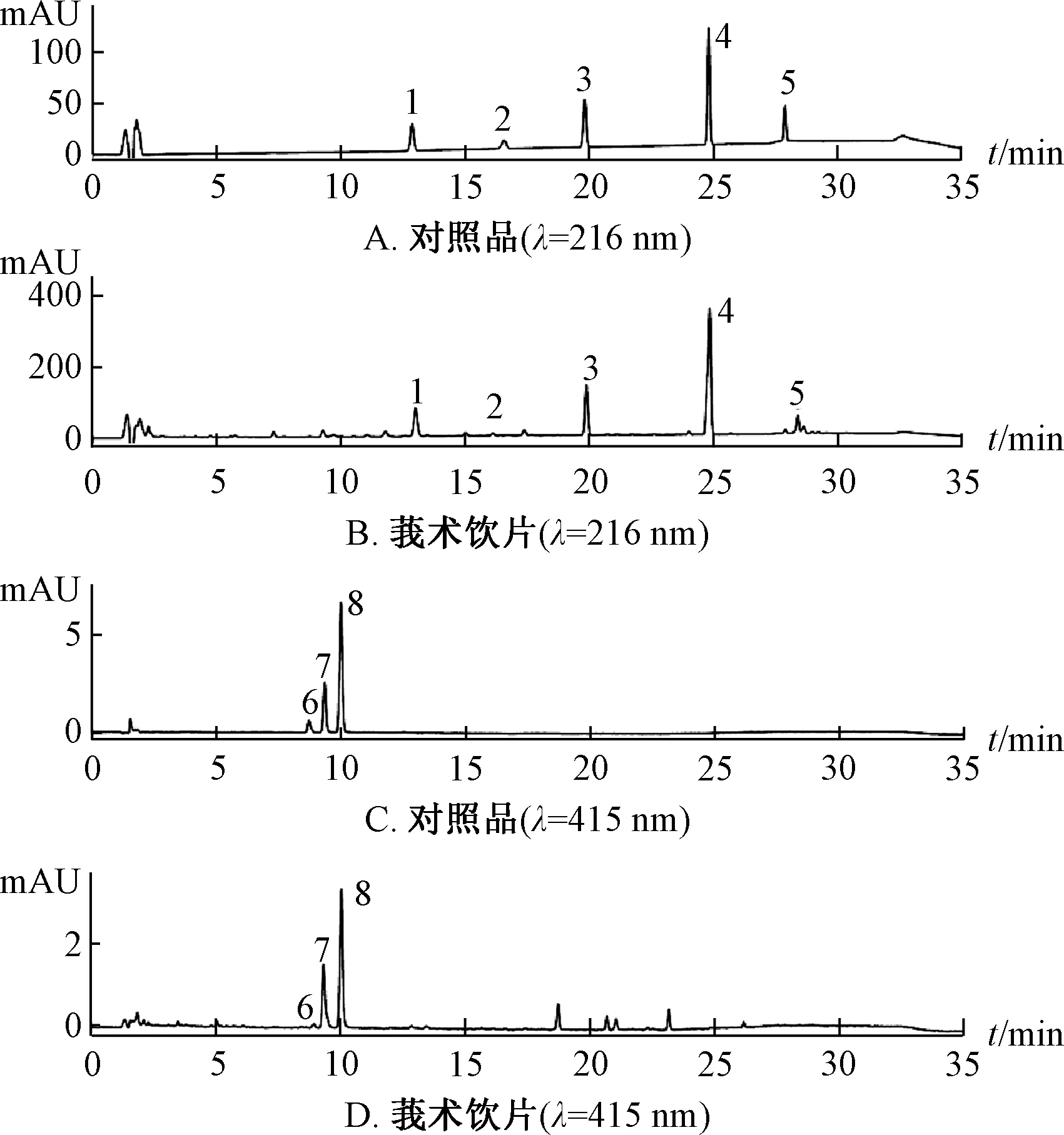
图1 各样品HPLC色谱图Fig.1 HPLC chromatograms of various samples
2.3.1 线性关系考察 依次精密吸取0.2、0.4、1.0、2.0、5.0 mL的混合对照品贮备液于10 mL量瓶内,加甲醇定容,制得系列对照品溶液。每个质量浓度分别进样2次,以峰面积平均值为纵坐标(Y),对照品质量浓度为横坐标 (X),进行回归,结果见表2。
2.3.2 精密度试验 精密吸取上述对照品溶液10 μL,连续进样 6次, 测得 β-榄香烯、 呋喃二烯、吉马酮、莪术醇、莪术二酮、双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素峰面积RSD值分别为0.89%、0.22%、0.27%、0.88%、0.83%、0.92%、1.15%、0.64%,表明仪器精密度良好。
2.3.3 重复性试验 选择同一批莪术粉末 (S3),平行6份,按 “2.2.2”项下方法制备供试品溶液,在 “2.1” 项色谱条件下进样,测得 β-榄香烯、呋喃二烯、吉马酮、莪术醇、莪术二酮、双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素质量浓度RSD值分别为1.46%、0.37%、0.72%、1.56%、1.39%、0.93%、1.88%、1.05%,表明该方法重复性良好。
2.3.4 稳定性试验 选择供试品 (S3), 按“2.2.2”项下方法制备供试品溶液,分别于0、2、4、6、12、24 h在 “2.1”项色谱条件下进样,测得β-榄香烯、呋喃二烯、吉马酮、莪术醇、莪术二酮、双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素峰面积RSD值分别为1.43%、0.51%、1.00%、0.90%、0.94%、0.47%、0.90%、0.39%,表明供试品溶液在24 h内稳定性良好。

表2 各成分线性关系Tab.2 Linear relationships of various constituents
2.3.5 加样回收率试验 精密称定9份已知质量浓度的供试品 (S3)粉末各0.25 g,每3份分别精密加入供试品中各成分含有量50%、100%、150%对照品溶液,按 “2.2.2”项下方法制备供试品溶液,在 “2.1”项色谱条件下进样,计算加样回收率。结果表明,β-榄香烯、呋喃二烯、吉马酮、莪术醇、莪术二酮、双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素的加样回收率分别为99.75%、98.96%、 99.36%、 98.32%、 97.82%、 99.23%、96.87%、97.67%,RSD分别为 1.23%、1.51%、0.90%、0.85%、0.47%、0.98%、1.90%、1.24%。2.4 样品含有量测定 30批莪术饮片按 “2.2.2”项下方法制备供试品溶液,每个样品平行3份,在“2.1”项色谱条件下进样,计算平均含有量,结果见表3。
2.5 多元数据分析 使用simca-p14.1软件对30批样品进行HCA分析。以莪术饮片8种化学成分的含有量为变量,采用组间Ward联结法,将欧式距离平方和作为样本测度,结果见图2。表明,3个产地的莪术饮片明显聚为3类,四川与广西产地的莪术更为接近,总体来说,温莪术各成分含有量相对其他2个主产地较高。
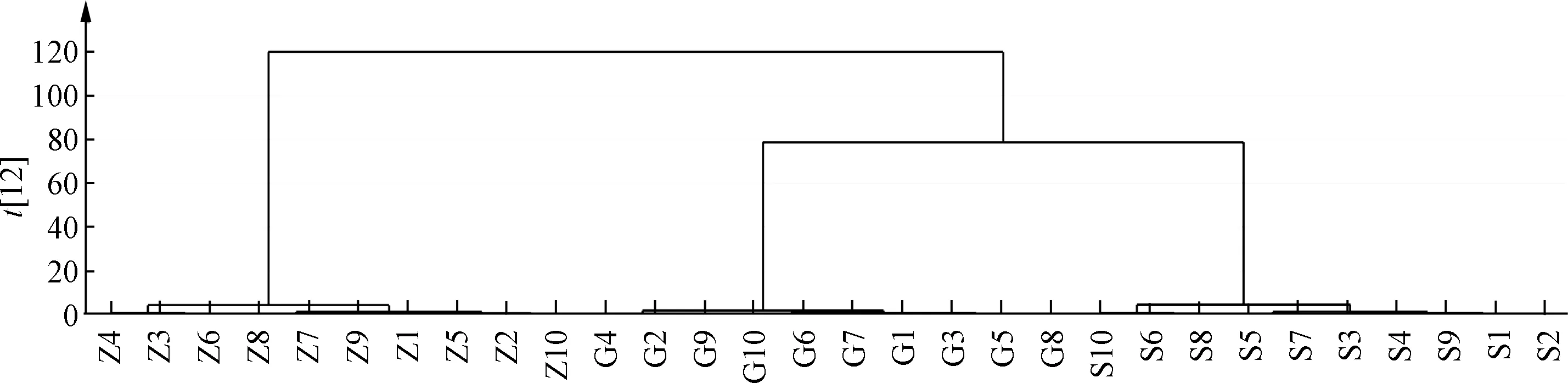
图2 30批样品聚类树状图Fig.2 Dendrogram of thirty batches of samples
为了进一步探讨3个产地莪术饮片之间的差异,使用非监督模式识别方法PCA对含有量测定数据进行分析,见图3。根据得分矩阵图,第一主成分的贡献率为59.5%,第二主成分的贡献率为31.8%,累计贡献率高达91.3%,表明模型拟合能力良好,能较全面的体现样品之间的差异。30批莪术饮片被分为3类,PCA分析与HCA分析结果相似。
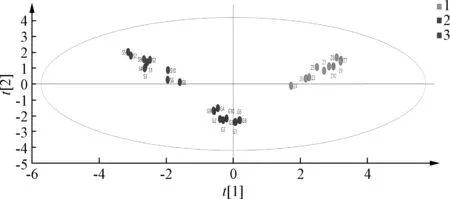
图3 30批样品主成分分析图Fig.3 PCA plot for thirty batches of samples
最后,采用监督模式识别方法O2PLS-DA对不同产地莪术饮片进行分析,见图4。该O2PLS-DA模型, R2Xcum=0.992, R2Ycum=0.935, Q2cum=0.92。其中,R2Xcum反映X矩阵结实率,R2Ycum概括模型的稳定性,Q2cum体现模型的预测性;R2Ycum和Q2cum的值越接近1,模型的稳定性和预测性越好。结果表明,该模型稳定可靠,30批样品聚类较好,分离显著,与PCA分析、HCA分析结果相互验证。结合变量重要性投影值 (VIP),筛选出对莪术分类贡献较大的主要成分,见图5。一般认为,VIP>1的变量对分类起着关键作用,而且值越大对分类的贡献越大。由图可知,VIP>1.0的有5个变量,按VIP值大小依次为姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素、莪术二酮、呋喃二烯。

图4 30批样品O2PLS-DA得分图Fig.4 O2PLS-DA score plot of thirty batches of samples

图5 30批样品O2PLS-DA模型中8个主成分的VIP值Fig.5 VIP values of eight chromatographic peaks in O2PLS-DA model of thirty batches of samples
3 讨论
在供试品溶液制备方面,考察了不同的提取方式,结果表明,超声和索氏回流提取效率相近,但前者更节约时间,因此选择超声提取。结合参考文献,分别考察了不同溶剂 (30%、50%、70%、90%乙醇)、提取时间 (15、30、45、60 min)、液料比 (20、40、60、80),确定最佳供试品溶液制备方法为40倍量70%乙醇超声提取30 min。同时对色谱条件进行考察,包括色谱柱 (Hanbon ODS-2 C18色谱柱、Agilent pro shell C18色谱柱)、流动相系统 (乙腈-水、乙腈-甲酸水、乙腈甲酸-甲酸水)、梯度洗脱、体积流量、柱温、波长等,综合考虑基线噪声、对称因子、分离度、洗脱时间等因素,确定最佳色谱条件。
本实验采用HPLC测定了30样品中8种成分的含有量,该方法操作简便、准确度高、重现性好。结合模式识别方法对莪术饮片含有量进行深入分析,结果表明不同产地的莪术饮片可明显分为3类,表明不同产地的莪术饮片质量差异较大,其中姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素、莪术二酮、呋喃二烯等几个成分对分类的贡献较大,莪术醇、吉马酮、β-榄香烯等几个成分差异小。目前,2015版 《中国药典》规定莪术有3个基原,但不同产地莪术饮片有效成分的种类和含有量均存在较大差异,以期2020版 《中国药典》分列制订不同产地莪术饮片含有量的标准。本实验收集的莪术饮片产地有限,后续研究希望增加非道地产区的样本量,为不同产地、不同基原莪术饮片的区分及质量评价提供更加全面的理论依据。

