合成类蛋白酪氨酸磷酸酶1B抑制剂专利现状分析
沈芳,马永涛,张雄辉,李瑶
(国家知识产权局专利局专利审查协作天津中心,天津 300304)
随着全球经济的快速发展,工业化、城市化进程的不断推进,人们的饮食呈现高热量和高钠化的趋势,同时人们的体力活动越来越少,伴随而来的糖尿病患者群日益增大[1]。糖尿病是21世纪世界范围的一种多病因代谢性疾病,仅次于肿瘤和心血管疾病,据统计,预计到2022年全球糖尿病药物市场规模将达到1 240亿美元。我国的糖尿病市场规模也保持着稳定增长的态势,2017年中国2型糖尿病患者有1.2亿人,其中52.3%的患者未被确诊,预计到2028年该数字将增至1.6亿[1-3]。
目前治疗糖尿病的药物种类众多,根据作用靶点的不同,已上市药物主要包括胰岛素类、α-糖苷酶抑制剂、胰高血糖素样肽(GLP-1)受体激动剂、钠-葡萄糖共转运蛋白(SGLT-2)抑制剂等,目前正在研发的热门靶点涉及G蛋白偶联受体(GPR119)激动剂、11β-羟基固醇脱氢酶1(11β-HSD1)抑制剂、蛋白酪氨酸磷酸酯酶1B(PTP1B)抑制剂等[4-6]。
本文主要针对涉及合成类PTP1B抑制剂的专利现状进行分析,获取申请量、重要申请人、代表性专利等方面的信息,为糖尿病药物的科研单位及企业提供专利申请、专利布局等方面的参考。
1 PTP1B简介
蛋白酪氨酸磷酸酶和和蛋白酪氨酸激酶共同调节细胞内蛋白质的去磷酸化与磷酸化从而调节体内细胞生长、分化、增殖、代谢、凋亡等生理过程。在庞大的PTPs家族中蛋白质酪氨酸磷酸酶1B(PTP1B)是第1个于1988年被成功分离纯化的蛋白酶,它不仅是胰岛素和瘦素信号转导的关键生理调节因子,而且其与ER应激以及胰岛β细胞之间也有重要关联。胰岛素敏感度降低是2型糖尿病的重要标志,PTP1B可以通过作用于IR和IRS的关键酪氨酸残基,使其去磷酸化,从而抑制胰岛素的信号通路或导致胰岛素信号通路的终止,最终使胰岛素的敏感度降低,此外,PTP1B与肥胖、肿瘤也密切相关[7-9]。
近年来,PTP1B抑制剂吸引了众多科研单位和制药公司的密切关注,陆续开发了一些具有临床应用前景的小分子抑制剂,如:辉瑞公司的Ertiprotafib,Genaera公司的Trodusquemine,日本烟草公司的JTT-551,但上述药物最终因疗效不佳或不良反应而终止研发[10]。 因此,目前大多数PTP1B抑制剂尚处于初步研究阶段,主要通过有机合成、组合化学、分子模拟的方法,利用计算机辅助药物设计进行新药开发,通过高通量筛选,寻找具有抑制 PTP1B 活性的化合物,再对化合物进行结构改造,以期改善化合物的药代动力学性质以及不良反应,最后得到具有特异性、高效性的PTP1B抑制剂。
2 合成类PTP1B抑制剂的专利态势
本文的检索截止日期为2018年7月,所采用的数据库是中国专利文摘数据库(CNABS)、德温特世界专利索引数据库(DWPI)以及incopat专利数据库。检索策略是初步选择关键词和分类号对该技术主题进行检索,人工筛选得到涉及合成类PTP1B抑制剂的专利为535项。
2.1 申请量趋势 由图中可以看出,PTP1B抑制剂作为潜在的药物靶点,自1988年被成功分离纯化后,随着PTP1B蛋白三维结构的确定和公开发表,基于该靶点的药物设计得到了广泛的研究,一度成为国外研究的热点,从上世纪末开始至2004年的专利申请整体呈现快速上升趋势。然而之后随着早期进入临床的药物相继失败或中止研究,以及PTP1B靶点本身的局限性,被报道的该靶点研究项目和进入临床的候选药物越来越少,导致国外针对该靶点的抑制剂的研究长期处于低谷。相比之下,中国在该领域的起步较晚,自2002年开始逐步发展,申请量逐渐增加,尤其在2010~2015年期间,全球申请量的增长主要归因于中国申请量,究其原因,主要在于受国内鼓励发明创造的大环境影响,创新主体的知识产权保护意识显著提高,科研创新以及专利申请的积极性得到鼓舞,极大促进了国内申请量的提升。
2.2 主要申请人 由表1可知,全球申请量前十名的专利申请人中,国内和国外的申请人各占一半,除佛山市赛维斯医药科技有限公司以外,国内申请量最多的是中国科学院海洋研究所,国外申请量最多的是默克公司。

图1 合成类PTP1B抑制剂专利申请量年度分布

排名申请人申请量(项)1佛山市赛维斯医药科技有限公司452默克公司333诺和诺德公司274中国科学院海洋研究所245中国科学院上海药物研究所196华东师范大学137ISIS制药公司118山西大学109诺华公司1010第一三共株式会社8
对国内前五名申请人的专利申请法律状态进行统计分析,结果如表2所示。佛山市赛维斯公司的授权率为0,中国科学院海洋研究所、中国科学院上海药物研究所、华东师范大学、山西大学的授权率分别为81.8%、57.9%、100%、100%,表明上述4位申请人的专利申请质量较高,也反映出我国在该领域的研发实力在不断增强。
3 合成类PTP1B抑制剂的专利技术
目前,对于PTP1B抑制剂的药物设计主要集中在两个方向:一个是针对 PTP1B 的催化活性区设计得到磷酸酪氨酸(pTyr)模拟物,另一个是针对PTP1B酶的变构抑制位点设计得到非竞争性PTP1B抑制剂,前后由于催化位点具有正电性和保守性的结构特征,通常细胞渗透性差,作用特异性不强,后者由于变构抑制位点在PTP酶家族保守性较低,相较于磷酸酪氨酸(pTyr)模拟物在细胞渗透性和作用特异性方面具有一定优势[8]。本节根据抑制剂结构的不同,选取专利申请量较大的酰胺类、羧酸类、杂环类进行分析。

表2 国内主要申请人专利申请授权率
3.1 含有酰胺结构的专利申请 此类抑制剂大多是以含有草酰氨基基团的化合物为先导化合物进行结构改造,通过结构中的草酰氨基与PTP1B的精氨酸活性中心相互作用,形成盐桥,在适当位置引入大体积疏水基团进行结构修饰,依靠氢键作用和疏水相互作用,可以特异性识别PTP1B。
诺和诺德公司CN99806015以人工合成的生物素化33P-磷酸化的肽为底物,用胰岛素受体酪氨酸激酶在酪氨酸残基处33P-磷酸化,对化合物进行筛选发现草酰氨基苯甲酸(见图2)可作为竞争性、可逆转的、活性位点指导的抑制物,部分化合物对于PTP1B具有选择性抑制活性,而对其他PTP酶几乎没有影响。之后,该公司的专利申请AU6985300涉及草酰氨基取代的噻吩并吡喃衍生物(见图3),对PTP1B酶抑制的Ki值达0.8 μmol·L-1。

图2 草酰氨基苯甲酸衍生物

图3 草酰氨基取代的噻吩并吡喃衍生物
应用研究系统ARS股份公司的专利申请WO2003EP00808涉及取代亚甲基酰胺衍生物(见图4),优选化合物对PTP1B的IC50值少于5 μmol·L-1。华东师范大学CN201510083031涉及手性3,3-二取代氧化吲哚衍生物(见图5),表现出良好的PTP1B抑制作用,优选化合物的IC50值达到2.06 μmol·L-1。

图4 取代亚甲基酰胺衍生物

图5 3,3-二取代氧化吲哚衍生物
3.2 含有羧酸结构的专利申请 辉瑞公司开发的以PTP1B为靶点的药物Ertiprotafib(见图6)和日本烟草公司开发的JTT-551(见图7)均含有羧酸结构,曾进入临床阶段,但是由于临床效果不佳和毒副作用大而被终止[10]。

图6 Ertiprotafib

图7 JTT-551
应用研究系统ARS股份公司的专利申请AU2005231980涉及作为PTP1-B抑制剂的1,1′-(1,2-乙炔二基)双苯羧酸衍生物(见图8),对PTP1B的IC50值为0.51 μmol·L-1。赛诺菲-安万特公司AU2005263418报道了羧酸类抑制剂,以水杨酸为核心结构(见图9),对PTP1B酶IC50值为0.7~46 μmol·L-1。

图8 1,1′-(1,2-乙炔二基)双苯羧酸衍生物

图9 水杨酸类化合物
中国医学科学院药物研究所CN 20101013976涉及苯甲酰胺基羧酸类化合物(见图10),总结出抑制剂的药效团应至少包括两个芳基和一个羧基,采用药效团与骨架迁越相结合的设计策略,筛出在理论上强效结合的化合物,IC50值0.09~0.85 μmol·L-1。华东师范大学CN201410084085涉及4,4-二甲基石胆酸-2,3-骈N-芳基吡唑衍生物(见图11),基于石胆酸进行结构改造得到了一种结构新颖、PTP1B抑制活性显著提高的抑制剂,优选化合物的IC50达到0.42 μmol·L-1。

图10 苯甲酰胺基羧酸类化合物

图11 4,4-二甲基石胆酸-2,3-骈N-芳基吡唑衍生物
3.3 含杂环结构的专利申请 由于羧酸的电性较高,用杂环来替代羧酸以改善PTP1B抑制剂的细胞膜渗透性一直是人们研究的热点。
美国家用产品公司CN99808438涉及(2-酰氨基噻唑-4-基)乙酸衍生物(见图12),化合物在25 μmol·L-1浓度下对PTP1B的抑制率最高达到96.6%。霍夫曼-拉罗奇公司AU2005304040涉及氨基喹唑啉化合物(见图13),PTP1B抑制活性的IC50在1.09~91.79 μmol·L-1的范围内。

图12 (2-酰氨基噻唑-4-基)乙酸衍生物

图13 氨基喹唑啉化合物
诺华公司的一系列专利申请WO2006US46543、WO2007US65421涉及噻唑烷二酮类化合物(见图14),结构的共同特征是1,2,5-噻唑烷二酮邻近位置有一个羟基或取代的羟基进行取代,通过抑制PTPase-1B(PTP1B)和T细胞PTPase(TC PTP)来治疗由PTPase介导的疾病,对PTP1B的IC50范围为0.000 1~15 μmol·L-1。
中国科学院上海药物研究所CN200710037848涉及含唑类结构的小分子蛋白酪氨酸磷酸酯酶1B抑制剂(见图15),最优化合物抑制PTP1B的IC50值为2.48 μmol·L-1。华东师范大学、中国科学院上海药物研究所的共同申请CN201410078744涉及苯并杂环取代1,3,4-噁二唑类化合物(见图16),通过保留现有结构中的N-H,引入并杂环,从结构上增强了化合物的刚性,固定了化合物的构象,提升化合物与酶的结合能力,改善分子的亲水性,从而改善化合物的生物利用度。


图14 噻唑烷二酮类化合物
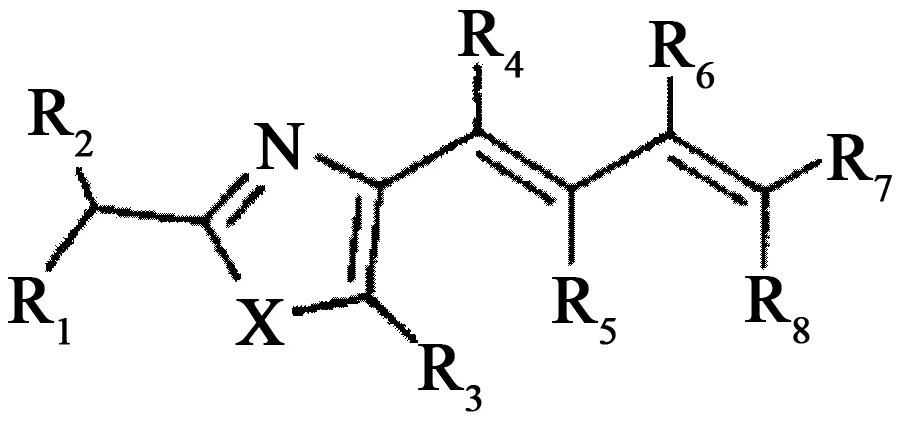
图15 含唑类结构的化合物
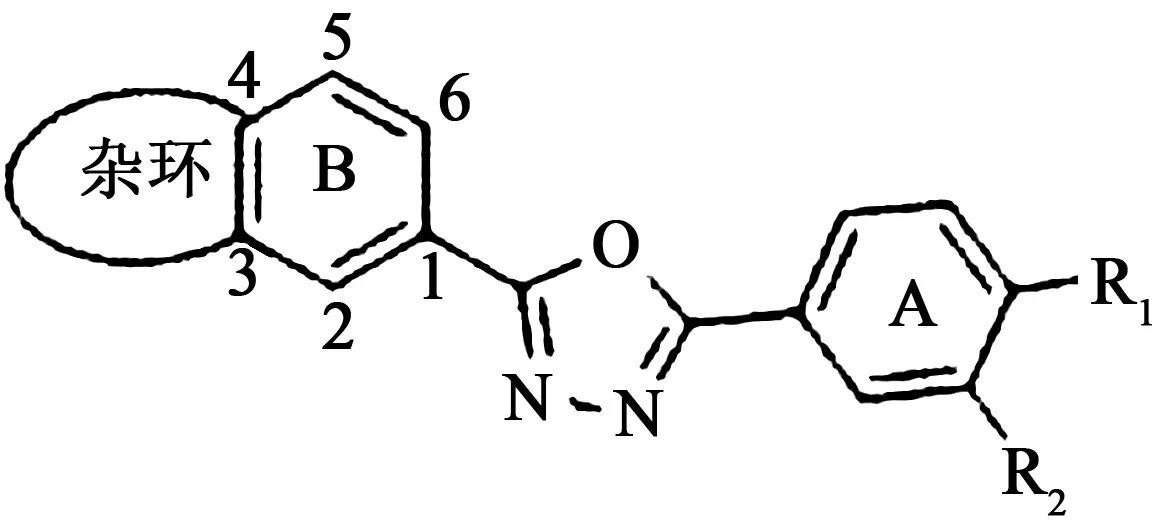
图16 苯并杂环取代1,3,4-噁二唑类化合物
4 总结
合成类PTP1B抑制剂的国外申请人起步早,大部分原研药申请人对专利进行了布局,国外申请人主要为大型制药公司,其在糖尿病药物领域均有上市药物,可见其专利转化度较好。然而鉴于PTP1B靶点结构本身的局限性,外国专利申请量从2004年以后就呈现下降趋势,逐渐进入衰退期,而中国随着知识产权意识的觉醒,从2002年开始申请量呈逐步上升趋势。国内申请人主要集中在高校/科研单位,缺乏企业的介入。通过对化合物结构进行深入分析发现,合成类PTP1B抑制剂涉及多种不同结构类型的化合物,说明由于目前此类抑制剂尚未有成功应用的先例,研发热点不集中,在该领域尚无系统的专利布局,国内外申请人都一直在探索发现新化学结构,这在一定程度上为国内申请人的研发和专利布局提供了机遇。
面对此种局面,国内申请人应当加大仿制药和原研药的研发投入,以进入临床的、具有PTP1B抑制活性的化合物作为先导化合物进行结构改造,积累一定方向性的研究基础,开发具有更好活性、靶向性或者药代动力学的药物,提升药物有效性或针对性。同时,应当对国外已有技术以及专利布局给予充分关注,深入研究重要申请人的技术脉络,一方面注意规避其专利雷区,另一方面,在充分利用国外申请人已有研发成果的基础上,发挥创造性,针对核心技术和专利进行进一步创新,可以围绕新剂型、新晶型、新工艺、新用途以及联合用药进行外围专利布局,形成一定的反制约,或通过交叉许可等方式为自身谋求利益。

