TiN-TiC复合材料的制备及其吸附性能
马玉洁 崔立峰

摘要:采用溶胶一凝胶法制备了具有优良吸附性能的TiN-TiC复合材料。采用X射线衍射仪,热重分析似,扫描电子显微镜,N2吸附一脱附仪和元素分析仪对该复合材料进行表征。结果发现,TiN-TiC复合材料具有介孔结构,比表面积为144.9m2·g-1,平均孔径为7.44nm。基于以上特性,研究了TiN-TiC复合材料对水中Cr(Ⅵ)的吸附能力。结果表明,在吸附温度为30℃、吸附时间为240min、初始Cr(VI)质量浓度为100mg·L-1、吸附剂投加量0.34g·L-1的條件下,TiN-TiC复合材料对Cr(VI)的吸附量为284.45mg·g-1。研究了相应的准一级、准二级动力学方程,结果表明,此复合材料对Cr(Ⅵ)的吸附动力学数据与准二级动力学方程有更好的相关性。
关键词:TiN-TiC;Cr(Ⅵ):吸附
中图分类号:TB 331文献标志码:A
随着我国电镀、皮革、染色、金属酸洗和铬酸盐加工生产等行业的快速发展,含铬废水的排放越来越多,环境污染日益严重。含铬废水中的Cr(VI)毒性最大,Cr(VI)是国际抗癌研究中心和美国毒理
TiN与TiC的化合物具有优异的物理化学性能,如高硬度、高密度、低电阻率、耐蚀性、化学性质稳定等,因此,TiN与TiC的化合物被广泛应用于涂层材料,电极材料和催化材料等方面。目前,制备TiN与TiC常用的方法是物理气相沉积、化学气相沉积和原子层沉积。关于溶胶-凝胶法制备TiN-TiC用作高效吸附剂的报道很少。
本研究中,采用溶胶一凝胶法制备出TiN-TiC复合材料,此方法易操作,可大批量生产。试验对合成的材料进行了表征。与此同时,将TiN-TiC用于对水中Cr(VI)的吸附,研究了其吸附性能。
1试验
1.1试验原料及设备
原料:尿素(CN2H4O)、表面活性剂(C19H42BrN,CTAB)、乙酸锌(Zn(CH3COO)2)、钛酸异丙醇(C12H28O4Ti)、乙酸(CH3COOH),均购于上海国药集团化学试剂有限公司;试验用水为二次去离子水。
设备:X射线衍射仪(X-ray diffractometer,XRD),N2吸附脱附仪(nitrogen absorption-desorption,BET),扫描电子显微镜(scanning electron microscope,SEM)和热重分析仪(thermos gravimetfic,TG)。
1.2TiN-TiC复合材料的制备
g-C3N4的制备:将一定量的CN2H4O粉末放在马弗炉中,550℃加热4h,升温速度为4℃·min-1,得到黄色块状g-C3N4。
TiN-TiC复合材料的制备如下:首先,将0.20g的CTAB溶解在15.00mL去离子水中,再加入1.60gg-C3N4于50℃的水浴中磁力搅拌30min;其次,2.25g Zn(CH3COO)2和3.14mL C12H28O4Ti分别溶于3.33mL CH3COOH中。将以上两种溶液混合均匀后加入处理后的CTAB超声30min;然后,放人50℃烘箱,形成凝胶后在120℃下烘干;最后,将黄色产物在900℃下煅烧120min,得到TiN-TiC复合材料。
1.3 TiN-TiC复合材料吸附性能测试
采用静态吸附法考察材料对Cr(VI)的吸附性能。取200.00mL Cr(VI)溶液,加入50mg吸附剂,转入水浴恒温振荡器中振荡一定时间后,离心取上层清液待测。吸附率和吸附量的计算公式:式中:η为吸附率;C0为Cr(VI)起始浓度;Ce为吸附平衡时Cr(Ⅵ)的起始浓度。
式中:Q为吸附量;V为溶液体积;C0为Cr(VI)起始浓度;Ce为吸附平衡时Cr(VI)的起始浓度;m为吸附剂用量。
2 结果与分析
2.1XRD表征结果及分析
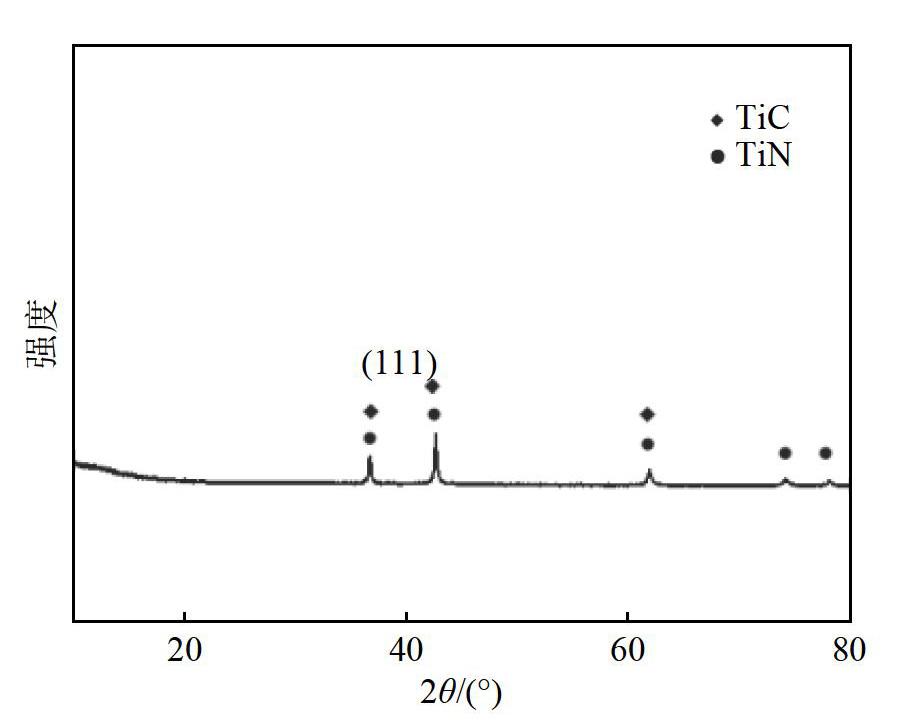
TiN-TiC复合材料的XRD谱图见图1,由图1可见,在所制备的复合材料中只有TiN和TiC两种相存在,该复合材料出现5个明显的衍射峰,分别对应TiN的(111),(200),(220),(311),(222)和TiC的(111),(200),(220)晶面,没有出现其他杂相。
2.2TG表征结果及分析
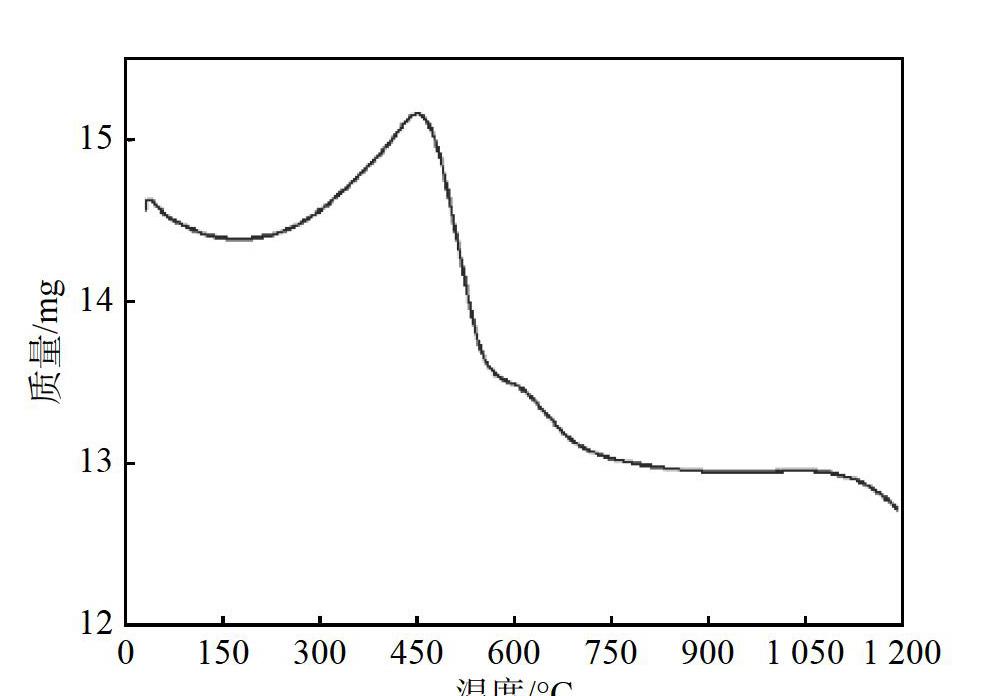
图2为TiN-TiC复合材料的TG曲线,是在空气氛围下以10℃·mm-1的加热速率,从50℃升高到1100℃进行测试得到的。从图2中可以明显地观察到发生质量损失的4个温度区间:低于200℃的区间,发生质量损失是因为样品中吸收的水蒸发和前驱物中无机成分的分解;在200-480℃,TiC与TiN分别发生氧化反应,导致质量增加;质量损失主要发生在480-700℃,可以清楚地看出,TiN-TiC复合材料的质量迅速下降;在最后一个温度区间内,曲线变得平缓,这表明该样品的质量在700℃后基本稳定,表明该物质没有发生相变。
2.3 SEM表征结果及分析
图3为TiN-TiC复合材料的SEM图。从图3中可以看出TiN-TiC复合材料的表面疏松,以簇状结构聚集在一起,趋于不规则形貌,没有游离的颗粒。
2.4 比表面积及孔径分析
图4为TiN-TiC复合材料的N2吸附脱附曲线和吸附支对应的孔径分布图。从图4(a)中可以看出,TiN-TiC复合材料的N2等温吸附一脱附曲线呈典型的Ⅳ等温线,具有H3-型滞回环,说明样品均为介孔结构。经BET法计算,TiN-TiC复合材料的比表面积为144.9m2·g-1。从孔径分布曲线图4(b)与表1结果可以看出,TiN-TiC复合材料的孔径分布较均匀,TiN-TiC的平均孔径较宽,为7.44nm。
2.5 元素分析
为了确定TiN-TiC复合材料中TiN与TiC组分的含量,本试验将样品干燥、研磨、过筛、包样,通过元素分析仪高温生成气体的方法对TiN-TiC复合材料中的C,N元素含量及C,N元素質量比进行了测定。从表2中可以看出,样品中C的质量分数占10.72%,N的质量分数占11.75%,元素质量比(C/N)为0.91,结果表明,这两种元素含量相近,说明TiN-TiC复合材料中TiN与TiC的质量比接近1:1。
2.6 吸附时间对吸附效果的影响分析
在吸附温度30℃、初始Cr(VI)溶液浓度为100mg·L-1、吸附剂投加量为0.34g·L-1、吸附时间为240min的条件下,TiN-TiC复合材料与活性炭对Cr(VI)的吸附量与吸附时间的关系见图5。由图5可见:随着吸附时间的延长,Cr(VI)吸附量逐渐增大;TiN-TiC复合材料的平衡吸附时间为180min,对应的平衡吸附量为284.45mg·g-1,吸附率为94.8%;活性炭的平衡吸附时间为120min,对应的平衡吸附量为261.90mg·g-1,吸附率为87.0%。可以说明,相同条件下,TiN-TiC复合材料比活性炭具有更高的吸附性。
2.7 吸附动力学
为了全面研究TiN-TiC复合材料对Cr(VI)的吸附动力学特性,需得到最合适描述此吸附过程的动力学模型,分别采用拟一级动力学、拟二级动力学方程对数据进行拟合。
式中:qe和qt分别为吸附平衡时和t时刻的吸附量;k1为拟二级吸附速率常数;t为吸附时间;k2为拟二级吸附速率常数。
拟一级动力学、拟二级动力学方程的拟合曲线见图6。由图6可见:TiN-TiC复合材料吸附Cr(VI)的拟二级动力学方程的相关系数为0.9908,高于拟一级动力学方程的相关系数。说明TiN-TiC复合材料对Cr(VI)的吸附符合拟二级动力学方程,准二级动力学模型包含了本吸附的多数过程,如外部液膜扩散、表面吸附等,能够更为真实地反映Cr(VI)在复合材料上的吸附机制。
3结论
(1)本试验通过溶胶-凝胶法合成TiN-TiC复合材料,该材料的比表面积和平均孔径分别为144.9m2·g-1和7.44nm,有利于吸附剂中有机分子的扩散或转移。
(2)TiN-TiC复合材料对Cr(VI)的吸附行为符合拟二级反应动力学方程。
(3)在吸附温度30℃、废水中Cr(VI)浓度为100mg·L-1、TiN-TiC复合材料投加量0.34g·L-1、吸附时间240min的条件下,复合材料对Cr(VI)的吸附量为284.45mg·g-1,对其去除率接近100%。相比于常用工业吸附剂(活性炭),TiN-TiC吸附Cr(VI)的效率较高,吸附量较大,且合成方法简便,是一种前景广阔的绿色吸附剂。

