导管接触性溶栓治疗下肢动脉硬化闭塞症合并血栓形成
战激光,赵堂海,解远峰,张 杰,逄晓军,秦少华
下肢动脉硬化闭塞症(arteriosclerosis obliterans,ASO)是血管外科常见疾病。近年来,随着腔内介入治疗的患者逐年增多,逐渐发现下肢ASO患者病变血管内继发血栓形成的情况较为常见[1],该研究对导管接触性溶栓 (catheter-directed thrombolysis,CDT)在下肢动脉硬化闭塞症合并血栓形成中的临床应用价值进行分析。
1 资料与方法
1.1 一般资料 选取2014年11月—2017年11月笔者所在科收治的下肢动脉硬化闭塞症合并血栓形成患者 62例(62条患肢),其中男38例,女 24例;年龄 61~79 岁,平均(70±5)岁。既往均有不同程度的下肢缺血病史,主要临床症状为间歇性跛行、静息痛等。患肢足部皮温平均值(16.68±0.72)℃,均无心房颤动病史。Rutherford临床分级:3级35例,4级21例,5级6例。踝肱指数(ankle brachial index,ABI)为 0.2~0.5,平均 0.32±0.12。患者入院后均完善双下肢动脉CTA检查,病变位于股浅动脉段(43/62)、腘动脉段(4/62)、股腘动脉段(15/62),膝下流出道血管均显示良好。术中均造影明确病变段血管管腔内存在继发血栓。
1.2 治疗方法术中逆行穿刺健肢股动脉,采取“翻山”技术,首先造影了解病变位置、长度以及远端流出道等情况,其次在路径图的引导下将导丝、导管引入病变远端正常血管管腔内(在通过病变段血管管腔时造影可见充盈缺损影像学表现,明确管腔内存在继发血栓)。若出现以下2种情况:(1)反复尝试导管无法到达远端真腔;(2)导丝、导管进入远端内膜下,无法返回真腔。则在路径图或B超引导下逆行穿刺胫后动脉或足背动脉,建立双向血管通路,将近端导丝牵引至远端真腔内[2]。选择略长于病变段长度的溶栓导管,导管到达预定位置后插入内芯,通过溶栓导管推入20万U尿激酶,置管成功后返回病房,开始规范溶栓治疗 48~72 h[3](具体时间根据溶栓效果及时调整):24 h持续泵入尿激酶40万U (经溶栓导管)、肝素1.25万U (经翻山鞘管);生理盐水50 ml+尿激酶20万U,经溶栓导管脉冲推入,2次/d;氯吡咯雷口服75 mg/d,拜阿司匹林口服100 mg/d[4];联合应用扩张血管、改善微循环类药物。溶栓期间监测患者凝血,1次/6 h,使活化部分凝血活酶时间(APTT)维持在75~100 s之间,并定期复查血常规,了解血小板的变化,预防肝素诱发的血小板减少症[5]。溶栓过程中根据溶栓效果及时调整溶栓导管位置或拔除溶栓导管,若造影发现病变血管残存狭窄闭塞段,则对狭窄闭塞段血管行经皮腔内血管成形术 (percutaneous transluminal angi-oplasty,PTA),扩张完毕复查造影,如残留狭窄仍>50%或产生夹层,则于相应部位放置适合血管周径的自膨式裸支架。
1.3 疗效评价及随访指标 记录患者住院过程中下肢皮温改变情况、血管搏动情况、间歇性跛行改善情况以及静息痛缓解程度,对比ABI指数变化。于术后3、6、12、18个月进行随访,观察记录患者病情改善及预后,并复查双下肢CTA。
1.4 统计学分析 采用SPSS 21.0软件,计量资料以±s表示,采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 治疗效果 59例患者患肢动脉得以开通,其余3例患者因术中导丝最终无法返回真腔而终止手术,其中22例患者术中植入支架,支架植入率37.3%(22/59)。59例患者与术前相比,患肢足背动脉均恢复搏动,间跛距离显著提高甚至无间跛症状,静息痛症状缓解。术后足部皮温平均值(28.38±0.70)℃,ABI指数平均值 0.85±0.10。足部皮温、ABI指数均较术前改善显著(P<0.05)。59例患者(59条肢体)均无穿刺点血肿、出血、垃圾脚、下肢深静脉血栓形成等并发症发生。
2.2 随访及预后 患者出院后均正规口服抗凝药物治疗,时间6个月,并定期监测凝血变化。于术后3、6、12、18个月进行随访,患肢动脉通畅率分别为98.3%(58/59)、94.9%(56/59)、86.4%(51/59)、83.1%(49/59)。随访过程中再次发生病变的患肢动脉经下肢动脉CTA检查证实为支架内再狭窄,入院行PTA(部分应用药物涂层球囊),症状均较入院时缓解。
2.3 其中1例患者治疗前后影像学对比 患者术前造影见股浅动脉起始处开始闭塞,远端未显影(图1)。置管溶栓48 h后股浅动脉全程显影,管腔节段性狭窄(图2)。给予球囊扩张、支架成型术后,股浅动脉、腘动脉显影良好(图3~4)。

图1 患者术前造影见股浅动脉自起始处开始闭塞,远端未显影

图2 置管溶栓48 h后股浅动脉全程显影,管腔节段性狭窄

图3 股浅动脉狭窄段给予球囊扩张、支架成型术后全程显影良好
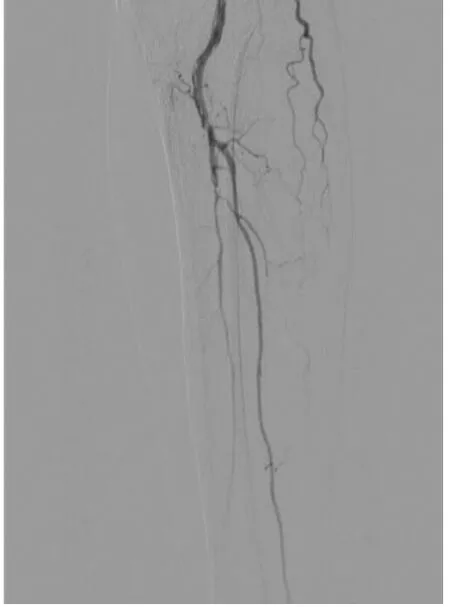
图4 腘动脉及膝下动脉显影良好
3 讨论
下肢动脉硬化闭塞症为动脉因粥样硬化病变而引起的慢性动脉闭塞性疾病,由于动脉粥样硬化性斑块、动脉中层变性和继发血栓形成而逐渐产生管腔闭塞,使下肢发生缺血[6]。
既往在下肢动脉硬化闭塞症合并血栓形成患者的治疗中,均于术中一期行球囊扩张、支架植入,支架植入率较高,患者负担较大,术后因附壁血栓透过支架网眼进入管腔造成肢体远端动脉栓塞的情况常有发生。导管接触性溶栓较传统介入手术具有一定的优势,因溶栓导管深入血栓内部,溶栓药物经侧孔溢出直接作用于血栓内部,溶栓效果确切。CDT可有效避免发生严重的缺血再灌注损伤,因溶栓的逐步再灌注,进而避免了因闭塞血管突然开通所导致的再灌注综合征[7]。在溶栓过程中,虽然破裂的碎栓有可能导致远端动脉二次栓塞,但通过调整溶栓导管的位置,均能有效避免垃圾脚的发生[8]。CDT最严重的并发症就是出血,尤以内脏出血及颅内出血最为凶险,想要获得满意的溶栓效果及较高的保肢率,就要承担较高的出血风险[9],但临床实践中,可以通过严格控制溶栓药物的使用剂量及溶栓时间、监测患者凝血变化来降低出血风险。以往在采用腔内治疗时经常面临导丝无法通过闭塞段或导丝进入内膜下最终无法返回真腔等问题,随着介入耗材的改进及介入技术的突飞猛进,手术成功率逐年提高。CDT可以暴露血管真实管腔形态,将长段病变转化成简单且容易处理的短段病变,降低了支架植入率[10],减轻患者的临床费用。
综上所述,CDT在下肢动脉硬化闭塞症合并血栓形成患者的治疗中具有较高的临床应用价值。

