辣木种子提取物对小鼠实验性肝损伤的保护作用
梁华峰, 张莉莉, 吴 帅, 朱正兰, 叶文才, 李满妹
(暨南大学药学院,广东广州 510632)
辣木Moringa oleifera Lam.为辣木科辣木属落叶乔木,又名油辣木、辣根树、鼓槌树等,原产于印度,现广泛分布于非洲、阿拉伯、东南亚等热带海洋气候区,我国广东韶关、云南、海南、贵州等地现有引种[1]。辣木是非洲和东南亚地区一种历史悠久的传统药物,其药效价值和营养价值在当地被广泛认可,辣木籽在民间常被用于醒酒和排毒,具有抗炎、抗菌、降血压、降血脂、调节血糖、抗肿瘤以及抗氧化等功能[2];辣木树叶或种子提取物可保护大鼠的肝损伤[3-5],但相关研究很少涉及其作用机理。因此,本实验建立小鼠急性酒精性肝损伤、小鼠四氯化碳致急性肝损伤模型,研究辣木种子提取物对小鼠肝脏的保护作用及机制,为治疗急性肝损伤提供依据。
1 材料
1.1 动物 SPF级雄性昆明小鼠,体质量20~22 g,购于广东省医学实验动物中心,许可证号SCXK(粤)2008-0002。小鼠饲养于25℃恒温动物房中,每天明暗交替12 h(7:00~19:00);自由饮水和饮食,适应性饲养7 d后进行实验。
1.2 试药 辣木种子提取物由本课题组制备,方法为辣木种子粉碎后按1∶10比例加水回流提取3次,每次 2 h,过滤后浓缩,即得。Pierce BCA protein assay kit购自美国Thermo公司;甘草酸苷片购自日本米诺发源制药株式会社 (批号15089);乳酸脱氢酶 (LDH)、丙二醛 (MDA)、谷丙转氨酶 (ALT)、谷草转氨酶 (AST)、碱性磷酸酶(ALP)、总超氧化物歧化酶 (T-SOD)、谷胱甘肽还原酶 (GR)、谷胱甘肽过氧化物酶 (GSH-Px)、谷胱甘肽 (GSH)、HE染色试剂盒均购自南京建成生物工程研究所;兔抗乙醇脱氢酶 1A/1B/1C(ADH1A/1B/1C) 抗体、 兔抗乙醛脱氢酶 2(ALDH2)抗体均购自美国Epitomics公司;小鼠抗β-actin抗体购自武汉博士德生物工程有限公司;辣根标记山羊抗兔IgG、辣根标记兔抗小鼠IgG均购自美国Proteintech Group公司。
1.3 仪器 MK3型酶标仪购自美国Thermo公司;IX51型倒置荧光显微镜购自日本Olympus公司;RM2235型切片机购自德国Leica公司;凝胶成像分析系统、PCR仪购自美国Bio-Rad公司;BS210S型电子分析天平购自德国Sartorius公司;3-18 K型台式高速冷冻离心机、2-5型离心机购自美国Sigma公司;ULTRA-TURRAX T8型组织匀浆机购自德国IKA Labortechnik公司。
2 方法
2.1 辣木种子提取物对小鼠肝组织ADH1和ALDH2 mRNA、蛋白表达的影响
2.1.1 分组及给药 24只小鼠随机分为对照组和辣木种子提取物组,每组12只,对照组灌胃10 mL/kg生理盐水,辣木种子提取物组灌胃500 mg/kg的提取物溶液 (10 mL/kg), 每天 1次,共7 d。最后1次灌胃后0.5 h,颈椎脱臼处死小鼠,取肝脏,提取mRNA,于-80℃冰箱中保存。
2.1.2 mRNA表达检测 Trizol提取肝组织匀浆中总RNA,紫外分光光度测定260、280 nm波长处的吸光度,计算OD260nm/OD280nm,总 RNA浓度=OD260nm×稀释倍数×0.040。采用RT-PCR法进行逆转录构建cDNA模板,逆转录反应条件参照试剂盒说明,通过NCBI网页找到所需基因序列,利用Primer premier 6.0设计特异性引物:ADH1正向5′-TTTTGTAGCCGAAGCGATCTG-3′, 反 向 5′-TACCACGGTGTACTGGGAGAA-3′, PCR 产物长度129 bp; ALDH2 正 向 5′-GACGCCGTCAGCAGG AAAA-3′, 反向 5′-CGCCAATCGGTACAACAGC-3′,PCR产物长度 189 bp;GAPDH正向 5′-AGGTCGGTGTGAACGGATTTG-3′, 反向 5′-TGTAGACCATGTAGTTGAGGTCA-3′, PCR 产物长度123 bp。
然后,通过PCR仪进行扩增,反应条件为95℃预变性5 min,95℃变性10 s,56℃退火10 s,72℃延伸10 s,共45个循环;熔解曲线条件为95℃ 5 s,65℃ 1 min,0.11℃/s升温至97℃,每升温5℃检测1次荧光,最后降温至50℃。
2.1.3 蛋白表达检测 肝脏加入RIPA裂解液进行裂解、提取蛋白,BCA法测定蛋白浓度。采用Western blotting法[6]进行聚丙烯酰胺凝胶电泳,转膜,5%脱脂牛奶溶液室温封闭1 h,4℃孵育一抗过夜,在摇床上用TBST洗涤3次,每次10 min,室温孵育二抗1 h,TBST再洗涤3次,通过ECL发光液检测ADH1、ALDH2蛋白表达,并根据灰度值计算两者蛋白表达相对量。
2.2 辣木种子提取物对急性酒精性肝损伤小鼠的作用
2.2.1 建模、分组及给药 60只小鼠适应性饲养1周后随机分为对照组、模型组、甘草酸苷组及提取物低、中、高剂量组,每组10只,对照组、模型组小鼠灌胃生理盐水,甘草酸苷组灌胃85 mg/kg甘草酸苷,提取物低、中、高剂量组分别灌胃125、250、 500 mg/kg 提取物, 给药量均为10 mL/kg,连续10 d,末次灌胃前12 h禁食不禁水。第10天灌胃30 min后,除对照组外各组小鼠灌胃18 mL/kg 50%乙醇。
2.2.2 取样及检测 50%乙醇灌胃8 h后乙醚麻醉小鼠,心脏采血至肝素抗凝管中,4℃、3 000 r/min下离心 15 min取血浆,测定 ALT、AST、ALP、LDH水平;肝组织在生理盐水中高速匀浆30 s,制备10%生理盐水肝匀浆液,4℃、12 000 r/min离心15 min,取上清液于新EP管中,作为肝组织匀浆液,根据相应试剂盒操作步骤测定GSH、MDA水平。
2.3 辣木种子提取物对四氯化碳致急性肝损伤小鼠的作用
2.3.1 建模、分组及给药 60只小鼠适应性饲养1周后随机分为对照组、模型组、甘草酸苷组及提取物低、中、高剂量组,每组10只,对照组、模型组小鼠灌胃生理盐水,甘草酸苷组灌胃85 mg/kg甘草酸苷,提取物低、中、高剂量组分别灌胃32.5、75、150 mg/kg提取物,连续15 d,末次灌胃前12 h禁食不禁水。第15天灌胃30 min后,对照组小鼠腹腔注射10 mL/kg橄榄油,其他各组小鼠腹腔注射10 mL/kg四氯化碳橄榄油溶液 (16 mg/kg)。
2.3.2 取样及检测 各组小鼠腹腔注射CCl4橄榄油溶液18 h后乙醚麻醉,心脏采血至肝素抗凝管中,4℃、3 000 r/min离心15 min取血浆,测定ALT、AST水平。同时取肝组织,一部分放入4%多聚甲醛溶液中固定,制成石蜡切片用于病理学检查;另一部分按 “2.2.2”项下方法匀浆,根据相应试剂盒操作步骤测定MDA、GSH、T-SOD、GR、GSH-Px水平。
再采用 RT-PCR 法检测 C/EBPα、 TNF-α、SREBP-1c、COX-2 mRNA表达,操作方法同“2.1.2” 项。 C/EBPα 正 向 5′-TTACAACAGGCCAGGTTTCC-3′, 反 向 5′-GGCTGGCGACATACAGTACA-3′, PCR 产物长度 187 bp; TNF-α 正向 5′-ATGAGCACAGAAAGCATGATC-3′, 反 向 5′-TACA GGCTTGTCACTCGAATT-3′, PCR产物长度110 bp;SREBP-1c 正 向 5′-TGTTGGCATCCTGCTATCTG-3′,反向 5′-AGGGAAAGCTTTGGGGTCTA-3′, PCR 产物长度 189 bp; COX-2正向 5′-GCACTTCACCCATCAGTT-3′, 反 向 5′-AGTTGCTCATCACCCCAC-3′,PCR产物长度 375 bp;GAPDH正向 5′-AGGTCGGTGTGAACGGATTTG-3′, 反向 5′-TGTAGACCATGTAGTTGAGGTCA-3′, PCR 产物长度123 bp。
然后,通过PCR仪进行扩增,反应条件为94℃预变性5 min,94℃变性30 s,退火30 s(C/EBPα退火温度51℃,30个循环;TNF-α退火温度50℃,40个循环;SREBP-1c退火温度51℃,28个循环;COX-2退火温度60℃,30个循环;GAPDH退火温度60℃,30个循环),72℃先延伸30 s再延伸7 min使产物延伸完全。反应结束后,取10 μL产物进行琼脂糖凝胶电泳,Bio-Rad凝胶成像系统拍照。
2.4 统计学分析 RT-PCR数据通过LightCycler 480软件进行处理,用target/reference比值表示;Western blotting数据通过Quantity one软件进行灰度分析。所有数据均采用Student’s t-test进行统计学分析,用 () 表示。以P<0.05表示差异有统计学意义。
3 结果
3.1 提取物对ADH1和ALDH2 mRNA、蛋白表达的影响 图1显示,与对照组比较,提取物组ADH1 mRNA、蛋白表达显著升高 (P<0.05),但对ALDH2无显著影响 (P>0.05)。
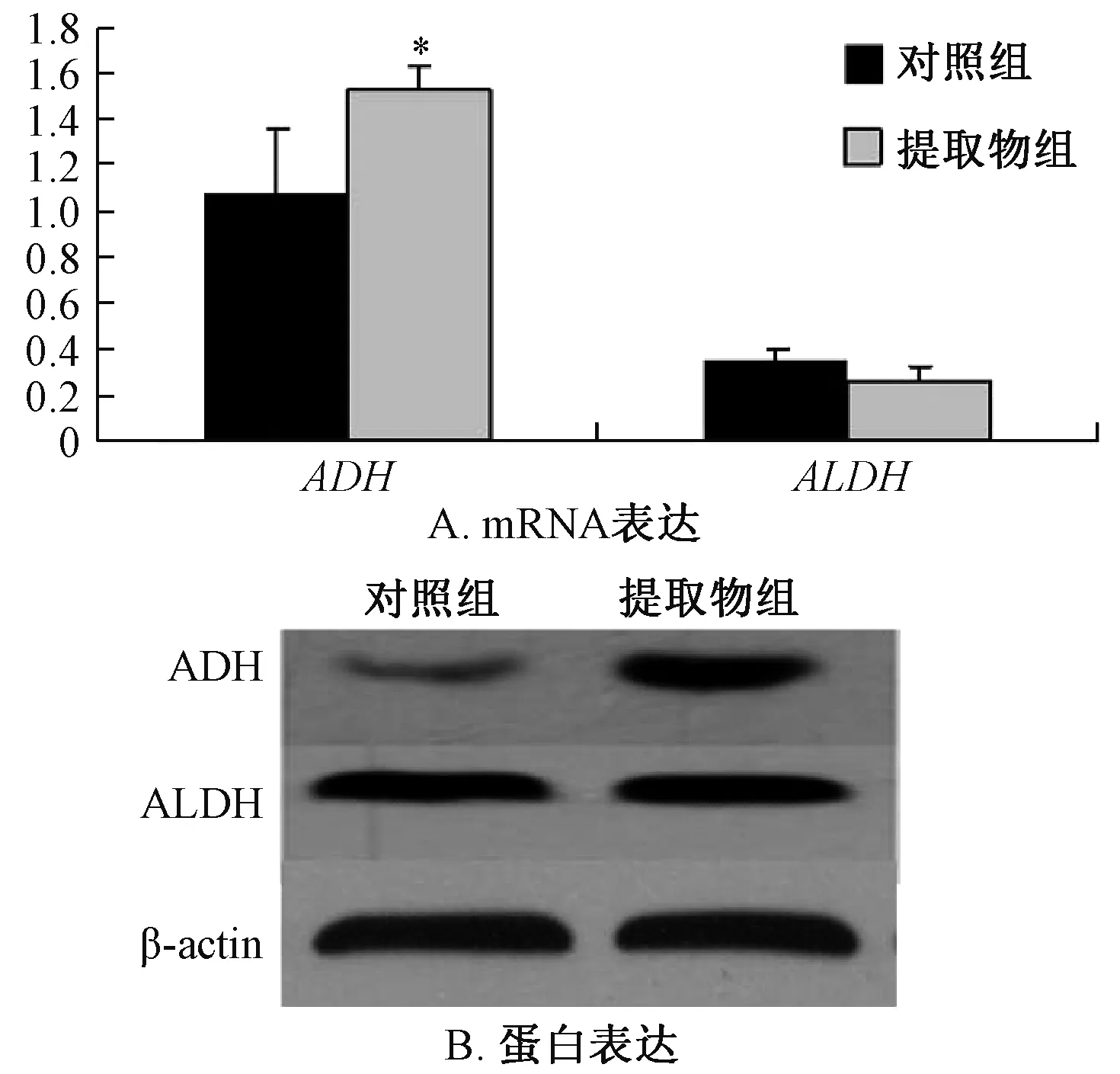
图1 提取物对ADH1和ALDH2 mRNA、蛋白表达的影响Fig.1 Effects of extract on the mRNA,protein expressions of ADH1 and ALDH2
3.2 提取物对急性酒精性肝损伤小鼠血浆ALT、AST、LDH、ALP水平的影响 表1显示,与对照组比较,模型组ALT、AST、LDH、ALP水平显著升高(P<0.01);与模型组比较,提取物组 ALT、AST、ALP水平显著降低 (P<0.05,P<0.01),并且中、高剂量组LDH水平也显著降低 (P<0.05,P<0.01)。
表1 提取物对ALT、AST、LDH、ALP、GSH、MDA水平的影响s, n=8)Tab.1 Effects of extract on ALT,AST,LDH,ALP,GSH and MDA levelss, n=8)
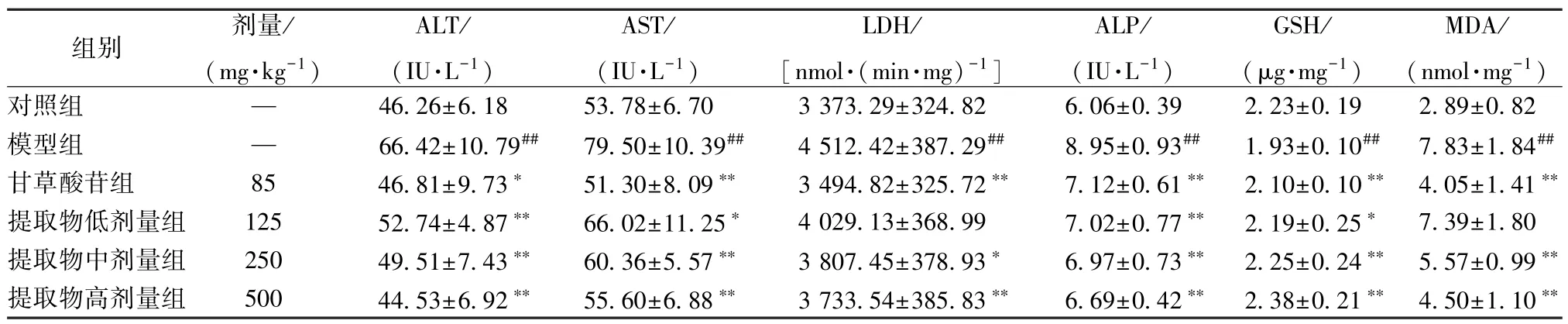
表1 提取物对ALT、AST、LDH、ALP、GSH、MDA水平的影响s, n=8)Tab.1 Effects of extract on ALT,AST,LDH,ALP,GSH and MDA levelss, n=8)
注:与对照组比较,##P<0.01;与模型组比较,∗P<0.05,∗∗P<0.01
组别 剂量/(mg·kg-1)ALT/(IU·L-1)AST/(IU·L-1)LDH/[nmol·( min·mg) -1 ]ALP/(IU·L-1)GSH/(μg·mg-1)MDA/( nmol·mg-1 )对照组 — 46.26±6.18 53.78±6.70 3 373.29±324.82 6.06±0.39 2.23±0.19 2.89±0.82模型组 — 66.42±10.79## 79.50±10.39## 4 512.42±387.29## 8.95±0.93## 1.93±0.10## 7.83±1.84##甘草酸苷组 85 46.81±9.73∗ 51.30±8.09∗∗ 3 494.82±325.72∗∗ 7.12±0.61∗∗ 2.10±0.10∗∗ 4.05±1.41∗∗提取物低剂量组 125 52.74±4.87∗∗ 66.02±11.25∗ 4 029.13±368.99 7.02±0.77∗∗ 2.19±0.25∗ 7.39±1.80提取物中剂量组 250 49.51±7.43∗∗ 60.36±5.57∗∗ 3 807.45±378.93∗ 6.97±0.73∗∗ 2.25±0.24∗∗ 5.57±0.99∗∗提取物高剂量组 500 44.53±6.92∗∗ 55.60±6.88∗∗ 3 733.54±385.83∗∗ 6.69±0.42∗∗ 2.38±0.21∗∗ 4.50±1.10∗∗
3.3 提取物对急性酒精性肝损伤小鼠肝组织GSH、MDA水平的影响 表1显示,与对照组比较,模型组GSH水平显著降低 (P<0.01),MDA水平显著升高 (P<0.01);与模型组比较,提取物组GSH水平显著升高 (P<0.05,P<0.01),并且中、高剂量组MDA水平显著降低 (P<0.01)。
3.4 提取物对四氯化碳致急性肝损伤小鼠血浆ALT、AST水平的影响 表2显示,与对照组比较,模型组ALT、AST水平显著升高 (P<0.01);与模型组比较,提取物组两者水平显著降低 (P<0.05, P<0.01)。
表2 提取物对ALT、AST、T-SOD、MDA、GSH、GR、GSH-Px水平的影响 ±s, n=8)Tab.2 Effects of extract on ALT,AST,T-SOD,MDA,GSH,GR and GSH-Px levels±s, n=8)
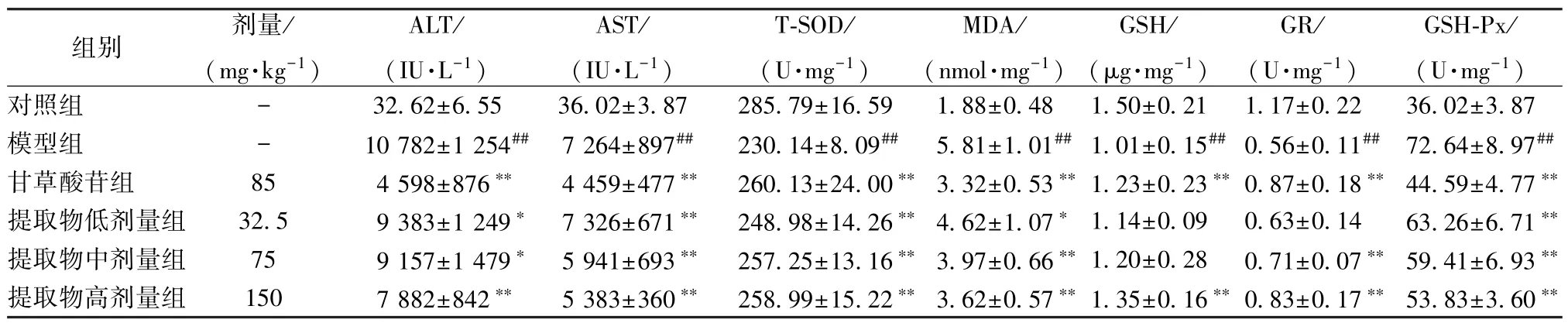
表2 提取物对ALT、AST、T-SOD、MDA、GSH、GR、GSH-Px水平的影响 ±s, n=8)Tab.2 Effects of extract on ALT,AST,T-SOD,MDA,GSH,GR and GSH-Px levels±s, n=8)
注:与对照组比较,##P<0.01;与模型组比较,∗P<0.05,∗∗P<0.01
组别 剂量/(mg·kg-1)ALT/(IU·L-1)AST/(IU·L-1)T-SOD/(U·mg-1)MDA/( nmol·mg-1 )GSH/(μg·mg-1)GR/(U·mg-1)GSH-Px/(U·mg-1)对照组 - 32.62±6.55 36.02±3.87 285.79±16.59 1.88±0.48 1.50±0.21 1.17±0.22 36.02±3.87模型组 - 10 782±1 254## 7 264±897## 230.14±8.09## 5.81±1.01##1.01±0.15##0.56±0.11## 72.64±8.97##甘草酸苷组 85 4 598±876∗∗ 4 459±477∗∗ 260.13±24.00∗∗ 3.32±0.53∗∗ 1.23±0.23∗∗ 0.87±0.18∗∗ 44.59±4.77∗∗提取物低剂量组 32.5 9 383±1 249∗ 7 326±671∗∗ 248.98±14.26∗∗ 4.62±1.07∗ 1.14±0.09 0.63±0.14 63.26±6.71∗∗提取物中剂量组 75 9 157±1 479∗ 5 941±693∗∗ 257.25±13.16∗∗ 3.97±0.66∗∗ 1.20±0.28 0.71±0.07∗∗ 59.41±6.93∗∗提取物高剂量组 150 7 882±842∗∗ 5 383±360∗∗ 258.99±15.22∗∗ 3.62±0.57∗∗ 1.35±0.16∗∗ 0.83±0.17∗∗ 53.83±3.60∗∗
3.5 提取物对四氯化碳致急性肝损伤小鼠肝组织TSOD、MDA、GSH、GR、GSH-Px水平的影响 表2显示,与对照组比较,模型组T-SOD、GSH、GR水平显著降低 (P<0.01),MDA、GSH-Px水平显著升高 (P<0.01);与模型组比较,提取物组TSOD水平显著提高 (P<0.01),MDA、GSH-Px水平显著降低 (P<0.05,P<0.01),并且高剂量组GSH水平显著升高 (P<0.01),中、高剂量组GR水平显著升高 (P<0.01)。
3.6 提取物对四氯化碳致急性肝损伤小鼠肝组织病理学的影响 图2显示,对照组小鼠肝细胞排列整齐、大小均一,细胞核呈圆形,界限清晰,分布在肝细胞中央,肝小叶结构正常;模型组小鼠肝细胞排列紊乱,细胞质疏松、肿胀,嗜酸性下降(嗜酸性细胞质容易和酸性染料伊红结合,染成粉红色),细胞核固缩,形态不一,小静脉周围可见大量点状或片状坏死,肝细胞索排列紊乱,肝小叶界限不清,肝细胞内呈现明显空泡状;提取物低剂量组小鼠肝细胞坏死有所减少,肝细胞排列较模型组稍紧密,细胞内空泡减少;提取物高剂量组小鼠肝细胞排列整齐、致密,肝细胞内无明显的空泡和疏松,肝小叶结构基本完整,结构清晰,肝细胞索排列整齐。
3.7 提取物对四氯化碳致急性肝损伤小鼠肝组织C/EBPα、 TNF-α、 SREBP-1c、 COX-2 mRNA 表达的影响 图3显示,与对照组比较,模型组C/EBPα、COX-2 mRNA 表达显著降低 (P<0.01), TNF-α、SREBP-1c mRNA表达显著升高 (P<0.01);与模型组比较,提取物组C/EBPα mRNA表达显著升高(P<0.05, P<0.01), SREBP-1c、 COX-2 mRNA 表达显著降低 (P<0.05,P<0.01),并且中剂量组TNF-α mRNA表达显著降低 (P<0.05)。
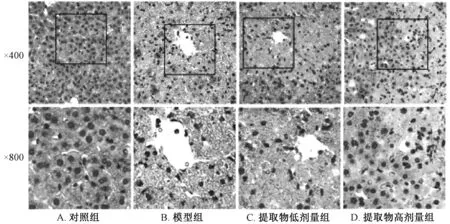
图2 提取物对肝组织病理学的影响 (HE染色)Fig.2 Effects of extract on liver histopathology (HE staining)
4 讨论
为了考察辣木种子提取物降低血液中乙醇体积分数的方式,本实验检测了与酒精代谢有关的乙醇脱氢酶 1(ADH1)和乙醛脱氢酶 2(ALDH2)mRNA、蛋白表达,发现连续 7 d给予小鼠500 mg/kg提取物后,ADH1 mRNA、蛋白表达均显著增加,但对ALDH2影响不明显。由此可知,辣木种子提取物能通过提高ADH1表达加速乙醇在肝脏的代谢,从而降低血液中乙醇体积分数。
研究显示,酒精性肝损伤与超氧离子和自由基大量生成有关[7-8],两者可攻击生物膜引起脂质过氧化,造成细胞膜和线粒体膜等功能障碍,从而导致细胞损伤或死亡,这个过程伴随转氨酶释放、脂质过氧化产物生成、抗氧化相关酶 (SOD、GR、GSH-Px)活性改变、抗氧化物质GSH水平变化等。本实验发现,辣木种子提取物能够不同程度降低急性酒精性肝损伤小鼠血浆转氨酶水平,缓解了ALP、LDH水平升高,呈现出对肝脏的保护作用;升高肝组织GSH水平,表明提取物能提高肝脏抗氧化水平,而肝组织MDA水平的降低提示脂质过氧化水平的降低。总的来说,辣木种子提取物可能通过加强小鼠肝脏的抗氧化平衡体系来减少酒精对肝脏的损伤。
由于四氯化碳肝损伤模型中肝脏病理学改变与人的肝脏疾病具有很高的相似性,故四氯化碳常用来复制人的肝病模型[9]。血液中转氨酶水平是衡量肝损伤的重要指标,其升高是CCl4肝损伤的重要表现,其中丙二醛 (MDA)水平反映机体脂质过氧化程度[10];总超氧化物歧化酶 (T-SOD)活力间接反映机体清除自由基能力[11];谷胱甘肽还原酶 (GR)能催化氧化谷胱甘肽 (GSSH)还原成还原型谷胱甘肽 (GSH),其主要作用是清除自由基,防止脂质过氧化反应发生,其水平也是衡量机体抗氧化能力的重要因素;谷胱甘肽过氧化物酶(GSH-Px)活性反映GSH抗氧化能力变化。
本实验发现,四氯化碳可使血浆ALT、AST水平显著升高,而辣木种子提取物可不同程度地缓解。同时,提取物能显著降低肝组织MDA水平,缓解四氯化碳致T-SOD活力下降,在抗脂质氧化、维持肝组织抗氧化水平方面具有一定作用;缓解GSH水平下降,增强肝组织GR活力,使GSH合成量增加、水平升高,可能与增强GR的活力和提高机体抗氧化能力有关;逆转四氯化碳致小鼠肝脏GSH-Px代偿性升高,减少因对抗自由基损伤而造成的GSH的损耗,提高GSH水平;明显改善四氯化碳对小鼠肝组织的病理损伤,可能与缓解炎症反应发生有关。
肝星状细胞 (HSC)的激活在肝脏疾病,如肝纤维化和肝硬化中发挥着主要作用,通过在活化的HSC中过表达C/EBPα可抑制HSC增殖,表明上调C/EBPα表达可以抑制HSC[12]。本实验发现,辣木种子提取物可明显上调C/EBPα mRNA表达,表明它对对小鼠肝损伤的保护作用可能与通过上调C/EBPα mRNA表达、抑制HSC激活有关。同时,C/EBPα还是COX-2的关键调节因子,高表达的COX-2能激活COX-前列腺素通路,造成细胞炎症和坏死;本实验发现辣木种子提取物可使COX-2 mRNA表达显著下降,可能与其参与C/EBPα调控有关。由此推测,辣木种子提取物抗炎作用可能与上调C/EBPα mRNA表达、抑制HSC激活、降低COX-2 mRNA表达有关。
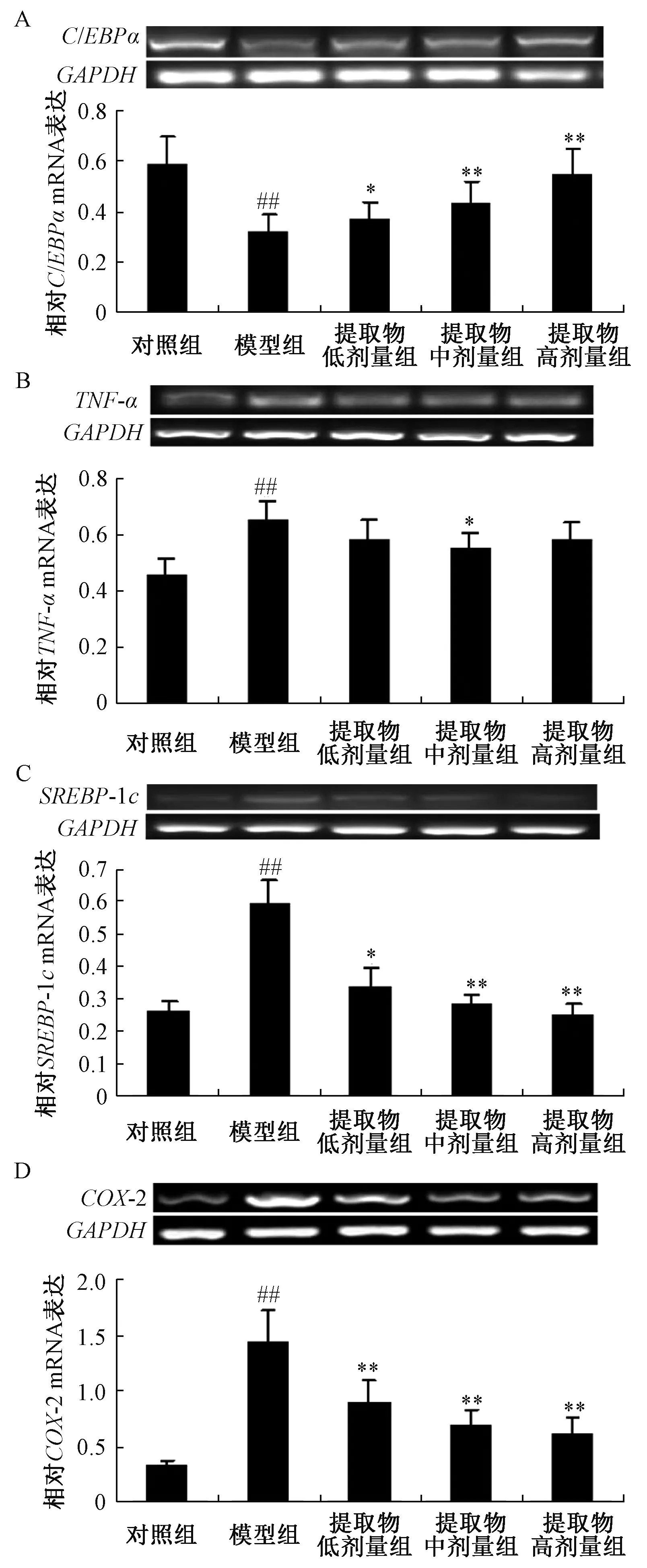
图3 提取物对 C/EBPα (A)、 TNF-α (B)、 SREBP-1c(C)、COX-2(D)mRNA表达的影响Fig.3 Effects of extract on C/EBPα (A), TNF-α (B),SREBP-1c(C) and COX-2(D) mRNA expressions
在正常情况下,机体内TNF-α活性极低,而在病理条件下它会大量表达,对机体造成损伤。本实验发现,四氯化碳造成了小鼠肝脏TNF-α mRNA表达明显提高,表明四氯化碳通过刺激Kupffer细胞大量表达TNF-α来损害肝细胞,而辣木种子提取物能降低其表达。由此可知,辣木种子提取物还可能通过抑制CCl4对Kupffer细胞激活、降低TNF-α表达来发挥肝脏保护作用。
SREBP-1c与肝脏脂肪变性密切相关,其过表达会造成脂肪酸合成酶 mRNA水平增加4倍;SREBP-1基因敲除小鼠血清甘油三酯水平显著降低,而其基因过表达时小鼠则表现出肝脏脂肪堆积、胆固醇合成相关基因的大量表达[13]。本实验发现,四氯化碳促进了小鼠肝脏SREBP-1c mRNA表达,而辣木种子提取物可下调其表达,推测它可能通过抑制肝损伤时SREBP-1c激活来抑制脂肪酸和胆固醇合成,从而减轻脂质代谢紊乱给肝脏带来的损伤。
综上所述,辣木种子提取物对小鼠实验性肝损伤 (急性酒精性肝损伤、四氯化碳致急性肝损伤)有明显保护作用,其机制可能涉及如下几个方面:(1)辣木种子提取物通过提高ADH1蛋白表达,从而加快乙醇的代谢; (2)辣木种子提取物通过上调C/EBPα mRNA表达,从而调控并抑制COX-2 mRNA表达,减缓炎症反应发生; (3)辣木种子提取物部分降低前炎症因子TNF-α mRNA表达,从而抑制炎症反应的发生; (4)辣木种子提取物通过下调SREBP-1c mRNA表达,从而抑制脂肪酸和胆固醇合成,减轻脂质代谢紊乱给肝脏带来的伤害。由此可知,日常服用辣木种子可预防和改善酒精或其他化学物质对肝脏造成的损伤。

