负压封闭引流治疗深度烧伤创面及对炎性因子、致痛因子的影响
黎鸿章,肖昌明,银西洋,邹 杰,杨 坤,刘 攀
深度烧伤创面若处理不当常易引发感染,若不能获得快速有效的治疗,不但需要反复植皮,还会增加患者痛苦[1]。资料显示,快速封闭深度烧伤创面,缓解组织缺血、水肿及创面渗出,恢复烧伤组织的外形及功能,避免再感染的发生,减少并发症是治疗深度烧伤创面(DBW)的关键[2]。研究证明,负压封闭引流(VSD)可实现全创面引流,持续清除创面渗出物,改善局部血液循环,避免细菌感染,为游离植皮和促进创面修复创造条件[3-4]。对于VSD的应用,临床多研究其对创面的修复效果,较少涉及其对血清炎性因子及致痛因子的影响。为降低DBW感染率,缓解患者疼痛,内江市第一人民医院于2015年1月—2017年12月应用VSD治疗DBW患者,在评价其疗效的同时探究其对血清炎性因子及致痛因子的影响。
临床资料
1入选标准
纳入标准:深度烧伤且创面感染者;对VSD敷料不过敏者;可耐受植皮修复手术者;知情同意者;肝肾功能正常者;有VSD适应证者。排除标准:无需植皮创面即可自行愈合者;植皮前使用VSD者;敏感体质者;感染性疾病者;免疫性疾病者;活动性出血伤口;无法配合治疗者;接受其他治疗者。本研究获得内江市第一人民医院伦理委员会批准。
2一般资料
2015年1月—2017年12月内江市第一人民医院治疗DBW患者106例,其中男性69例,女性37例;年龄25~59岁,平均44.5岁;体质量61.46~68.37kg,平均65.93kg;受伤至入院时间0.5~13d,平均5.65d。烧伤部位:躯干61例,四肢45例;创面面积33.80~62.50cm2,平均43.87cm2;烧伤深度:Ⅱ度49例,Ⅲ度57例;创面细菌培养均为阳性;火烧伤75例,热液烧伤31例。将上述DBW患者按照治疗方法分为VSD组和对照组各53例,两组一般资料具有均衡性(P>0.05)。见表1。
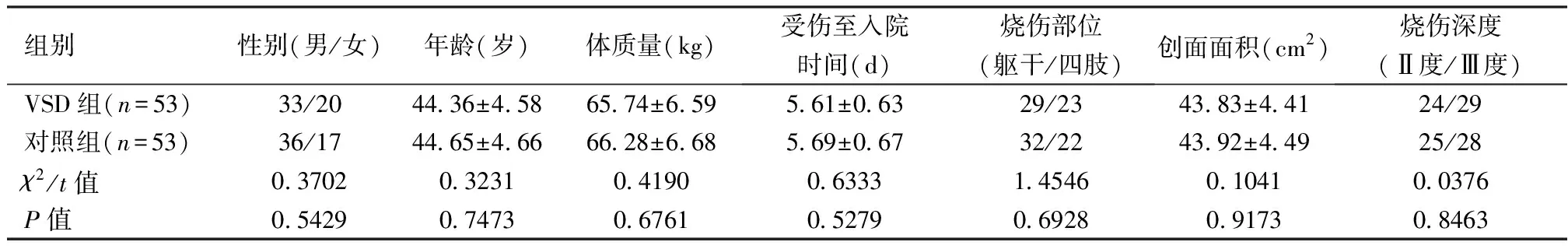
表1 两组一般资料比较
3方法
3.1VSD组 VSD组行VSD+游离植皮治疗。VSD:取负压敷料并按照创面大小、形状进行修剪,然后将其覆盖于已行游离植皮的筛状皮片上, 边缘间断缝合固定,确保敷料充分接触创面基底、筛状皮片,无死腔,以医用酒精清洁创面周缘,以半透性生物贴膜对创面进行封闭,并确保密闭充分,经Y型三通接头将所有引流管合并,并连接于引流管,经水封瓶与负压吸引器相连接。按照筛状皮片情况维持15~20kPa压力,接通负压,观察密闭性,若密闭性良好,则行持续负压引流,引流时间7~10d,待组织间隙封闭后行游离植皮。游离植皮:彻底清洁创面,死腔敞开,待长出新鲜肉芽组织后以过氧化氢、生理盐水彻底清洗,于患者腹部取与烧伤面积相同的中厚皮片,加工成筛状皮片并覆盖于烧伤创面,并加压包扎。植皮完成后抗生素常规抗感染治疗,术后1周左右检查植皮情况,若植皮面积坏死≥30%需再次植皮。
3.2对照组 采用常规清创和换药的方法,即:患者入院后清洁创面周围的皮肤,修剪创面上的水疱及污染严重的腐皮,盖以辅料,定期换药。游离植皮同VSD组。
4观察指标
观察两组治疗后7d创面愈合率、疼痛评分;创面完全愈合时间、住院时间、住院费用;治疗前及治疗后7d血清CRP(超敏C反应蛋白)、肿瘤坏死因子-α(TNF-α)、IL-8、补体C3a等炎性因子水平;血清5-羟色胺(5-HT)、脑内神经肽Y(NPY)、前列腺素E2(PGE2)等致痛因子水平。创面愈合率=(原有创面面积-现有创面面积)/原有创面面积×100%。创面完全愈合时间:以创面完全上皮化为愈合标准。以视觉模拟疼痛评分法进行评分:无痛,0分;可忍受的轻微疼痛,1~3分;尚可忍受疼痛显著且影响睡眠,4~6分;难以忍受的强烈疼痛,7~10分。以酶联免疫吸附法检测CRP、TNF-α、IL-8、补体C3a水平。以ELISA法检测血清5-HT、NPY、PGE2水平。检测按照试剂盒说明书进行。
5统计学分析
结 果
1两组创面愈合率、创面完全愈合时间、住院时间、住院费用比较
VSD组治疗后7d创面愈合率大于对照组,疼痛评分、创面完全愈合时间、住院时间及住院费用均少于对照组,差异有统计学意义(P<0.05)。见表2。
2两组治疗前后炎性因子情况比较
治疗前,两组CRP、TNF-α、IL-8、补体C3a水平差异无统计学意义(P>0.05);治疗后7d,两组CRP、TNF-α、IL-8、补体C3a水平均较治疗前降低,VSD组CRP、TNF-α、IL-8、补体C3a水平低于对照组,差异均有统计学意义(P<0.05)。见表3。
3两组疼痛因子情况
治疗前,两组血清5-HT、NPY、PGE2水平差异无统计学意义(P>0.05);治疗后7d,两组5-HT、NPY、PGE2水平均较治疗前降低,VSD组5-HT、NPY、PGE2水平低于对照组,差异均有统计学意义(P<0.05)。见表4。

表2 两组创面愈合率、创面愈合时间、住院时间、住院费用比较

表3 两组治疗前后血清炎性因子情况
治疗前后比较:#P<0.05

表4 两组治疗前后血清疼痛因子情况
治疗前后比较:#P<0.05
讨论
深度烧伤多存在严重组织缺损,常规非手术治疗难以自愈,故临床多行植皮治疗[5]。但因局部损伤严重,免疫功能减弱或丧失,不但易引发感染,降低植皮成活率,还会给患者带来较大的痛苦[6]。VSD是通过覆盖负压引流敷料,经负压引流出创面渗出物、坏死组织等物质,促进创面愈合的治疗方法[7]。在DBW的治疗中,VSD具有下述优点:(1)封闭性保护创面组织,抑制细菌增殖,避免二次感染;(2)引流创面渗出,缓解组织水肿,解除血管压迫,扩张毛细血管,改善创面血供,促进组织修复[8];(3)避免水平丢失,维持创面湿润,促进免疫细胞、抗炎因子运行至创面,在杀灭病原菌的同时提高局部抗感染能力,创面湿润还利于生成肉芽组织;(4)促进上皮细胞爬行,利于上皮组织生成[9];(5)促进生成成纤维细胞及血管内皮细胞,促进创面毛细血管生成;(6)提高胶原酶活性,促进移植胶原代谢,利于植皮成活[10]。牟晓欣等[11]证明,VSD、游离植皮联合治疗DBW可促进创面愈合,提高植皮成活率,避免局部感染。Huang等[12]认为,VSD可促进创口愈合,缩短治疗时间。在本研究中,VSD组创面愈合率、创面完全愈合时间、住院时间及住院费用均优于对照组,与上述研究一致。
研究证明,DBW的发生和免疫机制失衡,创口病原菌快速增值,炎性因子大量生成,补体激活关系密切[13]。创口炎性反应及免疫反应均可引发中心粒细胞、巨噬细胞等于创口聚集,生成炎性因子,推动感染进展[14]。在DBW发生发展进程中,炎性因子发挥着重要作用,炎性因子可打破抗炎性因子与促炎性因子间的动态平衡,增强促炎性因子活性,推动炎性反应进展[15]。研究证明,烧伤感染的发生发展不但和CRP、TNF-α、IL-8密切相关,还和补体C3a等炎性因子存在一定的关系[16]。资料显示,补体C3a可参与机体免疫调节与微生物防御反应,促进免疫病理性损伤反应[17]。在本研究中,治疗后VSD组CRP、TNF-α、IL-8、补体C3a等水平低于对照组,提示VSD有益于纠正免疫机制失衡,抑制炎性因子生成。因烧伤后炎性反应最严重的部位即为创面,负压封闭引流治疗能加强创面的引流,调节局部的炎性反应,降低烧伤患者全身的炎性反应水平,增强免疫力。
5-HT为重要的疼痛因子。研究证明,5-HT可介导肾上腺素β受体,促进其产生前列腺素,引发胺类物质增加并刺激交感神经纤维产生疼痛[18]。5-HT能够促进血小板生成,引发毛细血管痉挛及局部组织水肿,使伤害性感受器受到刺激并产生痛觉[19]。NPY可促进细胞膜去极化,通过肾素-血管紧张素系统提高血管及毛细血管的兴奋性,促使其剧烈痉挛,导致疼痛[20]。此外,NPY还能够提高肥大细胞活性,促使其分泌5-HT[21]。PGE2可促进炎性反应,引发周围伤害感受,加快痛觉在脊髓中的传导,加剧疼痛[22]。在本研究中,治疗后VSD组5-HT、NPY、PGE2水平及疼痛评分均低于对照组,说明VSD可抑制生成疼痛因子,有效缓解患者疼痛。
总之,VSD可通过覆盖负压引流敷料,经负压引流出创面渗出物、坏死组织等物质,促进DBW创面愈合及植皮存活,降低炎性因子及疼痛因子水平,缓解患者痛苦,缩短患者康复时间。

