白果内酯通过Nrf2/HO-1信号通路改善氧化应激所致体外血脑屏障损伤的研究
徐玮,梁文意,郭彩娟,黄亿健,李育平,贝伟剑,郭姣
( 广东药科大学中医药研究院 /广东省代谢病中西医结合研究中心,广东 广州 510006)
血脑屏障(blood brain barrier,BBB)完整性破坏是多种中枢神经系统疾病发展的根源[5-6]。内皮屏障功能异常导致组织水肿和功能障碍,这个过程涉及炎症、缺血再灌注损伤、糖尿病、动脉粥样硬化等。在疾病条件下,脑组织释放的一系列内源性炎症介质,包括组胺、缓激肽、血小板活化因子、生长因子、糖基化产物、细胞因子、活性氧,都有可能增加微血管通透性[7-8]。脑微血管内皮细胞是BBB形成的基础,其封闭特性可以部分归因于相邻内皮细胞之间连续的紧密连接(tight junctions,TJs)[9]。氧化应激失常是BBB破坏的诱因,当机体活性氧成分与抗氧化系统之间平衡失调,氧化应激反应将引起的一系列适应性的反应[10-11]。Nrf2/HO-1通路广泛参与神经系统等组织器官的抗氧化应激损伤[12-13]。本研究将探讨白果内酯是否通过Nrf2/HO-1信号通路保护H2O2诱导的氧化损伤引起BBB通透性增加。
1 材料与方法
1.1 主要试剂与材料
1.1.1 实验试剂 白果内酯 (Bilobalide,1108650-201507,中国食品药品检定研究院提供);依达拉奉(3-甲基-1-苯基-5-吡唑啉酮,48QIH-BE,东京化成工业株式会社);特级南美胎牛血清(S711-001S,Lonsera品牌);DMEM高糖培养基(C11960500BT)、DMEM低糖培养基(C11885500BT)、0.25% 胰酶(25200056),pH7.4磷酸盐缓冲液(PBS,8118127)均由Thermo Fisher Scientific公司提供;细胞培养抗生素(15140-122,北京索莱宝科技有限公司);CCK-8(40203ES60,上海翊圣生物技术有限公司);DMSO(W387520)、H2O2(31642)、Na-F(SLBL5470V)由Sigma-Aldrich公司提供;乳酸脱氢酶(LDH)活性检测试剂盒(A020-2)、一氧化氮(NO)含量检测试剂盒(A013-2)、还原型谷胱甘肽(GSH)含量检测试剂盒(A006-2)由南京建成生物工程研究所提供;RIPA裂解液(P0013B)、BCA蛋白定量试剂盒(P0010S)、总抗氧化能力检测试剂盒(S0116)由碧云天生物技术公司提供。
1.1.2 主要仪器及实验耗材 Eon微孔板分光光度计(BioTek);Mithras LB-940荧光酶标仪(Berthold Technologies);SW-CJ-1FD超净工作台(上海博讯实业有限公司医疗设备厂);DK-8D电热恒温水槽(上海一恒科技有限公司);8000直热气套式CO2培养箱(Thermo scientific);CKX41倒置相差显微镜(日本OLYMPUS);MERS00002电阻仪(Millipore);小型垂直蛋白电泳仪、小型Trans-Blot转印槽(美国伯乐);0.4 μm孔径Tranwell膜、细胞培养皿均由Corning公司提供;PVDF膜(ISEQ00010,Millipore)。
1.1.3 细胞株 永生化人脑微血管内皮细胞株(human cerebral microvascular endothelial cell line,hCMEC/d3)购自中国科学院细胞库;永生化人脑星形胶质细胞株(human normal glial cell line,HEB)购自广州吉尼欧生物有限公司。
1.2 方法
1.2.1 细胞培养 hCMEC/d3培养使用高糖DMEM,HEB培养使用低糖DMEM,培养基均需另加入10%(φ)胎牛血清,1%双抗。细胞置于5%(φ)CO2,37 ℃细胞培养箱培养。倒置显微镜观察细胞,细胞接种2 h可见细胞完全贴壁,细胞形态呈光亮的圆球形。接种8 h后,细胞延展生长,hCMEC/d3细胞形态呈梭形,HEB细胞形态呈星形,折光性强。
1.2.2 体外BBB模型建立[14-15]HEB细胞培养状态佳,且细胞生长密度达90%时,移去旧培养基,PBS润洗2次,用0.25%胰蛋白酶消化细胞,离心后将细胞重悬,细胞稀释成6×104个/mL。移取500 μL细胞悬液,滴在transwell培养室反面,轻柔吹打至细胞悬液完全均匀铺盖在膜上,并将transwell培养室倒置放于无菌的培养皿上,培养箱培养2 h,等待细胞贴壁。细胞贴壁后在培养板中加入1 mL培养基,将transwell培养室放回于细胞孔中。2 d更换1次培养基。待下室的HEB细胞生长融合至70%时,按照上述消化细胞方法将hCMEC/d3细胞重悬并用培养基稀释至1.5×105个/mL。移取1 000 μL细胞悬液,加在transwell上室,并用划“8”字的手法将细胞摇晃均匀。将细胞板放入5% CO2,37 ℃气套式细胞培养箱中培养。2 d更换1次培养基。
1.2.3 CCK-8 法检测细胞活性 取生长状态良好的hCMEC/d3细胞以2×105个/mL接种到96孔板,培养24 h后,运用不同浓度白果内酯(0.2、1、5、25、125、625 μmol/L)和依达拉奉(10 μmol/L)分别刺激细胞24 h,考察药物对hCMEC/d3细胞毒性的影响。再用H2O2诱导氧化损伤2 h,考察其对hCMEC/d3细胞增殖活力的影响。正常组、给药组和空白孔加入CCK-8试剂,继续置于培养箱中反应2 h。酶标仪450 nm波长处测定吸光度(A)值。通过公式计算细胞增殖活力,细胞活力=[A(含药孔)-A(空白孔)]/[A(无药物孔)-A(空白孔)]×100%。
1.2.4 BBB模型NO、GSH、LDH及总抗氧化能力测定 BBB模型建立成功后,模型分为6组:空白对照组、H2O2模型组(500 μmol/L)、白果内酯低中高剂量组(0.2、1、5 μmol/L);依达拉奉(10 μmol/L)阳性组。给予不同浓度白果内酯及依达拉奉预处理体外BBB模型24 h,利用H2O2(500 μmol/L)诱导2 h模拟氧化应激损伤。收集细胞培养上清液用于LDH活性测定,收集细胞裂解液用于NO含量、GSH含量及总抗氧化能力测定,细胞裂解液样品制备方法如下:用预冷PBS润洗transwell孔上层的hCMEC/d3细胞2次,每个transwell孔加入120 μL RIPA裂解液,4 ℃裂解20 min,细胞刮刀将细胞刮下,收集裂解液。4 ℃下12 000 r/min离心20 min,取上清。后续实验步骤严格按试剂盒说明书方法进行。
“白+黑”的工作模式让他和同事们出师大捷—11月1日当天就查处了天通苑某超市擅自改动散装食品有效期的案件,还连夜端掉某山区内一个无证加工酱鸭的黑窝点。郑全意带着队员们次日凌晨三点赶在回城区的路上,“拼命三郎”的“美誉”已被大家叫响了。
1.2.5 跨内皮细胞电阻值(TEER)的测定 体外BBB模型采用跨内皮细胞电阻仪(Millicell ERS)进行TEER测量,测电笔金属头部分使用前先用75%(φ)乙醇浸泡15 min,再用PBS冲洗3次。电阻测定时长电极垂直于tranwell板的下室,短电极垂直于tranwell板的上室。模型建立过程中每天监测TEER值,测量值应减去无细胞的transwell培养室的电阻值(Ω·cm2)。测定TEER结果为TEERhCMEC/d3=(TEERhCMEC/d3+filter- TEERfilter)×S(膜面积),单位:Ω·cm2。每个transwell培养室测量3次,并且每个实验组设置3个复孔,在相同的培养条件以获得平均TEER和标准偏差。
1.2.6 Na-F通透性的测定 体外BBB模型按照“1.2.4”分组给药24 h后在tranwell板上室加入0.1 mL含有1 mg/mL的Na-F及500 μmol/L H2O2的高糖培养基,2 h后从下室中吸取200 μL溶液,用多功能酶标仪测定其荧光A值,Ex(γ)=(485±10)nm;Em(γ)=(530±10)nm。通过稀释Na-F浓度为0.004、0.02、0.1、0.5、1 mg/L,制定Na-F标准曲线,将各组测定的A值代入标准曲线,计算各组溶液中透过BBB模型的Na-F量。
1.2.7 蛋白免疫印迹 药物处理后,按照“1.2.4”的方法收集细胞裂解液,并按BCA蛋白定量试剂盒方案进行蛋白定量,最终将蛋白浓度统一到相同浓度。按照蛋白∶5×SDS蛋白示踪缓冲液=4∶1混合均匀,85 ℃煮沸10 min,-20 ℃保存。取 20 mg 总蛋白用于上样。10%~15%聚丙烯酰胺凝胶电泳分离,运用“三明治夹心”湿法转膜,随后脱脂奶粉封闭1 h,TBST洗膜后分别加入Nrf2、HO-1、claudin-5、occludin、VE-Cadherin和GAPDH的兔单克隆抗体4 ℃下孵育过夜;TBST洗涤后加入抗兔二抗,室温孵育2 h;采用增强化学发光法成像,并运用Lane 1D凝胶成像分析软件进行灰度分析,目标条带灰度值与GAPDH内参灰度值相比,表示相关蛋白的相对表达值。
2 结果
2.1 体外BBB模型成功建立
文献报道细胞电阻大于300 Ω·cm2,代表体外BBB模型成功建立[15]。通过每天监测TEER值,发现体外BBB在第6天电阻值可达到300~500 Ω·cm2,第6~9天TEER值处于一个稳定状态,第9天才开始明显下降。说明在此研究中体外BBB模型已成功建立。
2.2 白果内酯对hCMEC/d3 细胞活力的影响
各浓度白果内酯给药处理24 h,如图1所示,给药组细胞活力与正常组比较,1 μmol/L白果内酯较正常组细胞活力增加10%(P<0.05),5 μmol/L白果内酯较正常组细胞活力增加30%(P<0.01)。25、125 μmol/L白果内酯对细胞活力无显著性影响,625 μmol/L白果内酯能引起hCMEC/d3细胞的活力降低21%(P<0.05),说明有一定毒性影响。

150100500细胞活力/%1234567****
1.正常组; 2~7.依次为白果内酯给药浓度0.2、1、5、25、125、625 μmol/L。与正常组比较:*P<0.05,**P<0.01。
图1白果内酯对hCMEC/d3细胞活力的影响
Figure1Effects of bilobalide on hCMEC/d3 cell viability
2.3 白果内酯对H2O2损伤hCMEC/d3细胞增殖活力的影响
如图2所示,模型组用H2O2干预血管内皮细胞2 h,细胞增殖活性显著下降 40%(P<0.05),而预先用白果内酯中剂量(1 μmol/L)和白果内酯高剂量(5 μmol/L)给药,能显著缓解H2O2引发的细胞活力下降,并呈浓度依赖性(P<0.05),细胞活力与正常组比较差异无统计学意义(P>0.05)。阳性对照药依达拉奉组与模型组相比,细胞活力显著增加(P<0.05)。
2.4 不同浓度白果内酯对H2O2损伤体外BBB相关氧化应激指标的影响
如图3所示,与正常组比较,模型组NO及GSH含量水平显著降低(P<0.05,P<0.01),LDH活性水平显著升高(P<0.01)。与模型组比较,白果内酯中剂量(1 μmol/L)和白果内酯高剂量(5 μmol/L)可显著提高NO含量(P<0.05,P<0.01),提高GSH含量(P<0.05,P<0.01)及总抗氧化能力(P<0.05,P<0.01);显著降低LDH活性(P<0.01),并呈现剂量依赖关系。依达拉奉阳性组与模型组相比,NO含量、GSH含量、总抗氧化能力显著增加(P<0.01),LDH活性显著降低(P<0.01)。

*###1234561.51.00.50.0细胞活力/%
1.正常组; 2.模型组; 3.白果内酯低剂量组; 4.白果内酯中剂量组; 5.白果内酯高剂量组; 6.依达拉奉组;与正常组比较:*P< 0.05; 与模型组比较:#P<0.05。
图2白果内酯对H2O2损伤hCMEC/d3细胞活力的影响
Figure2Effect of bilobalide on hCMEC/d3 cell viability injured by H2O2

0.50.40.30.20.10.0108642030020010003210123456NO含量/(μmol?g-1)GSH含量/(μmol?g-1)LDH活性/(U?g-1)总抗氧化能力/(mmol?g-1)####*######****############**#ABCD
1.正常组; 2.模型组; 3.白果内酯低剂量组; 4.白果内酯中剂量组; 5.白果内酯高剂量组; 6.依达拉奉组;与正常组比较:**P<0.01; 与模型组比较:#P<0.05,##P<0.01。
图3白果内酯对H2O2损伤BBB模型氧化应激损伤相关指标的影响
Figure3Effect of bilobalide on the oxidative stress injury related indicators of the BBB model injured by H2O2
2.5 白果内酯抵抗氧化应激损伤对体外BBB通透性的影响
通过测定TEER值和Na-F的透过量可以评价体外BBB的通透性[16]。电阻值测定结果发现(图 4),低、中、高剂量的白果内酯及依达拉奉预处理体外BBB,H2O2干预2 h后,模型组细胞电阻值显著降低(P<0.01),白果内酯组及依达拉奉组与正常组比较差异无统计学意义(P>0.05),与模型组比较差异有统计学意义(P<0.01)。Na-F透过浓度结果反映,与正常组比较,氧化损伤模型组Na-F透过含量显著增加(P<0.01)。与模型组比较,依达拉奉组Na-F的透过量显著降低(P<0.01),白果内酯中剂量和高剂量亦可显著降低Na-F的透过量(P<0.05,P<0.01),并呈剂量依赖性。

AB########****####12345640030020010006420Na-F透过浓度/(mg?mL-1)跨内皮细胞电阻值/(Ω?cm2)
1.正常组; 2.模型组; 3.依达拉奉组; 4.白果内酯低剂量组; 5.白果内酯中剂量组; 6.白果内酯高剂量组;与正常组比较:**P<0.01;与模型组比较:#P<0.05,##P<0.01。
图4白果内酯对氧化应激损伤体外BBB通透性的影响
Figure4Effect of bilobalide on blood-brain barrier permeabi-lity injured by oxidative stressinvitro
2.6 白果内酯对氧化应激损伤内皮细胞紧密连接蛋白的影响
为考察给予氧化损伤是否影响紧密连接蛋白的表达,白果内酯预处理能否起到保护BBB紧密连接的作用。实验结果证明(图5),与正常组相比,H2O2干预BBB 2 h,内皮细胞紧密连接相关蛋白claudin-5、occludin、VE-Cadherin的表达量均显著性降低(P<0.05,P<0.01)。而预先给予白果内酯或依达拉奉干预24 h,再给予氧化损伤,与模型组相比,白果内酯给药组claudin-5、occludin、VE-Caherin蛋白表达量均高于模型组(P<0.05,P<0.01),依达拉奉对Occludin和VE-Caherin蛋白表达也显著性增加(P<0.01)。

###########***#####**123456Claudin-5VE-CadherinGAPDHOccludinClaudin-5OccludinVE-Cadherin2.01.51.00.50.0相对蛋白表达量2.01.51.00.50.0相对蛋白表达量2.01.51.00.50.0相对蛋白表达量123456
1.正常组; 2.模型组; 3.依达拉奉组; 4.白果内酯低剂量组; 5.白果内酯中剂量组; 6.白果内酯高剂量组;与正常组比较:*P<0.05,**P<0.01;与模型组比较:#P<0.05,##P<0.01。
图5白果内酯对氧化应激损伤内皮细胞紧密连接蛋白的影响
Figure5Effect of bilobalide on tight junction proteins of endothelial cells injured by oxidative stress
2.7 白果内酯对H2O2诱导的体外BBB Nrf2/HO-1通路的影响
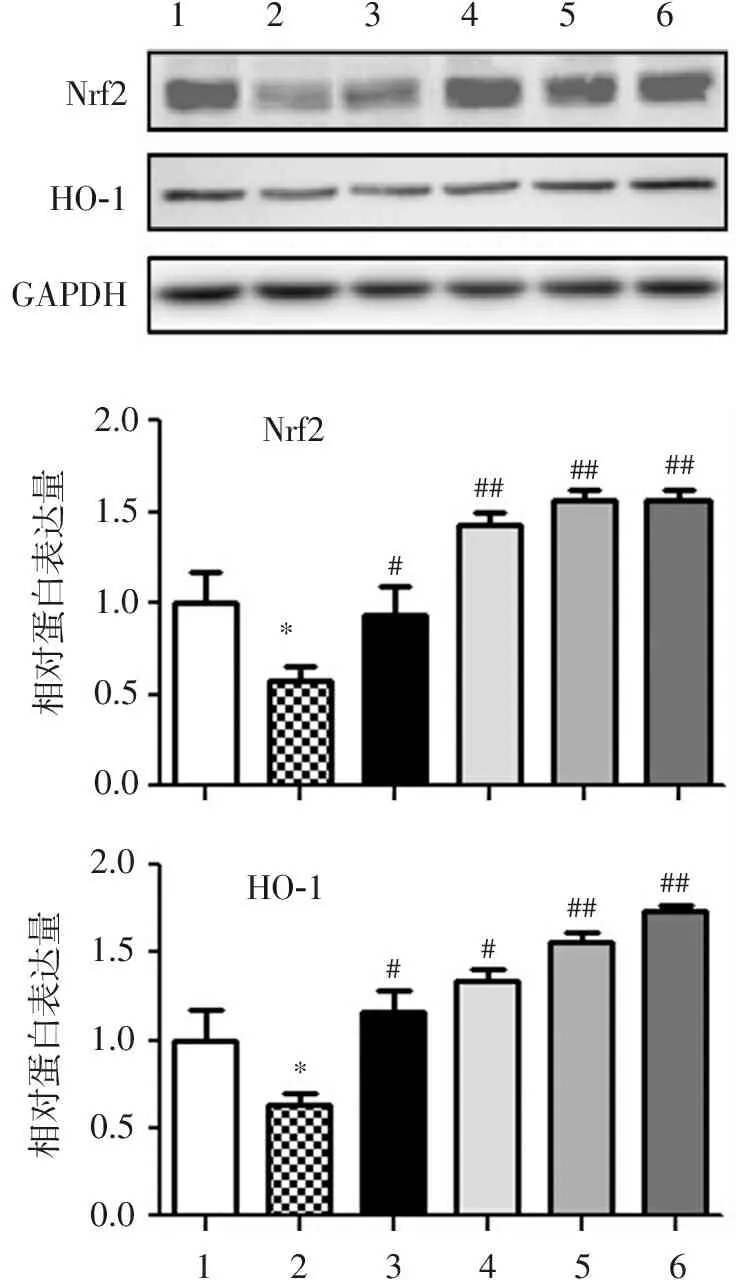
HO-1是细胞内的抗氧化酶,其表达受上游转录因子Nrf2的调节[26]。为验证白果内酯是否通过影响Nrf2/HO-1信号通路发挥其抗氧化作用,通过Western blot检测H2O2模型组及白果内酯给药组对体外BBB Nrf2、HO-1蛋白表达水平。实验结果显示(图6),H2O2干预体外BBB显著降低Nrf2、HO-1蛋白的表达(P<0.05),而白果内酯预处理,Nrf2、HO-1蛋白表达与模型组相比明显升高(P<0.01),并高于正常组水平。依达拉奉对Nrf2、HO-1蛋白的表达与模型组相比无显著影响(P>0.05)。
#############**123456HO-1GAPDHNrf2Nrf2HO-12.01.51.00.50.0相对蛋白表达量2.01.51.00.50.0相对蛋白表达量123456
1.正常组; 2.模型组; 3.依达拉奉组; 4.白果内酯低剂量组; 5.白果内酯中剂量组; 6.白果内酯高剂量组; 与正常组比较:*P<0.05; 与模型组比较:#P<0.05,##P<0.01。
图6白果内酯对H2O2诱导的体外BBB Nrf2/HO-1通路的影响
Figure6Effect of bilobalide on H2O2-induced Nrf2/HO-1 pathway in blood-brain barrierinvitro
3 讨论
活性氧(ROS)和其他自由基/氧化剂引起的氧化应激在动脉粥样硬化、糖尿病、缺血性中风及相关中枢神经系统疾病的发病机制中起关键作用[17-18]。当机体受到氧化损伤时,体内可产生各种抗氧化分子及酶用于清除体内产生的ROS,保护机体免受ROS的损伤[19]。GSH常被称为“抗氧化之母”,是机体内关键的非酶性抗氧化物,GSH含量是衡量机体抗氧化能力的重要生物标志物。LDH是细胞损伤标志物[18]。已有研究证明,依达拉奉通过清除细胞内ROS,拮抗H2O2下调细胞Nrf2/HO-1表达,从而抑制H2O2导致血管内皮细胞的损伤作用[20]。
hCMEC/d3细胞是永生化的人脑微血管内皮细胞系,其具备人脑内皮细胞的大部分形态和功能特征[21]。星形胶质细胞被证明是体内内皮细胞渗透性的关键调节剂,它可以帮助调节培养的内皮细胞更具有BBB结构特性[21]。因此体外BBB的构建可广泛用于药物对BBB通透性的评价。在体外BBB模型中,TEER降低和Na-F透过浓度的增加与BBB通透性的增加有关[22]。
本实验中,H2O2能引起BBB模型血管内皮细胞的NO、GSH水平和Nrf2/HO-1表达显著下降,说明细胞已发生氧化应激,消耗了大量的抗氧化物质,并导致细胞膜损伤,LDH从细胞内漏出,胞外LDH水平显著升高,细胞活力下降,并且此时BBB模型的TEER下降,荧光素纳透过增加,说明H2O2能引起BBB氧化应激损伤,并增加BBB模型通透性。
实验结果表明,阳性药依达拉奉和白果内酯预处理都可以提高氧化应激时的总抗氧化能力,提高内皮细胞的NO、GSH水平,减少LDH漏出,明显提高细胞活力,并且可以维持细胞正常的电阻值及较低的Na-F的透过。
实验结果还发现,H2O2干预BBB模型使紧密连接蛋白claudin-5、occludin及VE-Cadherin表达量下调,而给予白果预处理可逆转H2O2干预BBB模型引起的紧密连接蛋白claudin-5、occludin及VE-Cadherin表达量下调,解除H2O2干预对紧密连接蛋白的影响,说明白果内酯可通过抗氧化起到了保护BBB的作用。
Nrf2/HO-1 通路广泛参与神经系统等组织器官的抗氧化应激损伤,是机体最重要的内源性保护体系之一[23-24]。核因子E2相关因子2(Nrf2)是一种基本的亮氨酸拉链氧化还原敏感转录因子,可调节有害应激状态下细胞的氧化还原状态,相关文献已证明Nrf2可在各种中枢神经系统(CNS)疾病中提供神经保护作用[25]。在正常条件下,Nrf2通过其抑制剂Kelch样ECH相关蛋白1(Keap1)锚定于细胞质中。在氧化应激条件下,Nrf2从Keap1解离,转移至细胞核并激活多种抗氧化酶,例如谷胱甘肽过氧化物酶(GSH-Px)、血红素加氧酶-1(HO-1)、烟酰胺腺嘌呤二核苷酸磷酸(NADP+)等[26]。血红素氧合酶(HO)具有2种亚型:诱导型(HO-1)和组成型(HO-2)。HO-1是相关疾病的保护性基因,包括I/R损伤、阿尔茨海默病、高血压病、动脉粥样硬化和糖尿病;而组成型HO-2的遗传缺失会导致缺血性脑损伤加剧[27]。本实验结果发现,白果内酯预处理能上调Nrf2及HO-1蛋白的表达,缓解甚至抵消H2O2对BBB氧化损伤模型的损伤。
综上表明,白果内酯可通过抗氧化作用改善氧化应激所致BBB通透性的破坏,其作用机制可能是通过Nrf2/HO-1信号通路调节氧化还原状态,逆转H2O2氧化应激所致的紧密连接蛋白水平下调,维持正常BBB通透性。

