雷珠单抗联合玻璃体切割术对PDR患者血清VEGF-A和SDF-1表达的影响
罗 文,明 媚
作者单位:(435000)中国湖北省黄石市,鄂东医疗集团黄石市中心医院湖北理工学院附属医院
0 引言
增生性糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)是糖尿病常见的并发症之一,可引起玻璃体积血、视网膜牵拉性脱离、纤维血管膜增生等生理病理变化,若未及早诊治,可导致致盲,严重影响患者的身体健康[1]。目前,玻璃体切割术(vitrectomy,VT)是 PDR 常用的治疗方法,但其手术难度大,易导致术中创伤大而引起多种并发症发生,甚至影响手术疗效[2]。近年来,相关研究显示,视网膜新生血管异常与PDR发生发展有关,通过抗新生血管治疗可提高患者的治疗疗效,其中雷珠单抗是常用的抗新生血管药物[3]。而血管内皮生长因子(VEGF-A)、人基质细胞衍生因子1(SDF-1)是血管新生的重要因子,具有促进、加快血管新生的作用,其在PDR病情进展中具有重要的作用,但关于雷珠单抗联合VT对PDR 患者 VEGF-A、SDF-1 影响的报道较少[4]。对此,本研究通过给予PDR患者雷珠单抗联合VT治疗,探讨其对患者VEGF-A、SDF-1的影响,现报道如下。

表1 两组一般资料比较
表2 两组VEGF-A和SDF-1比较
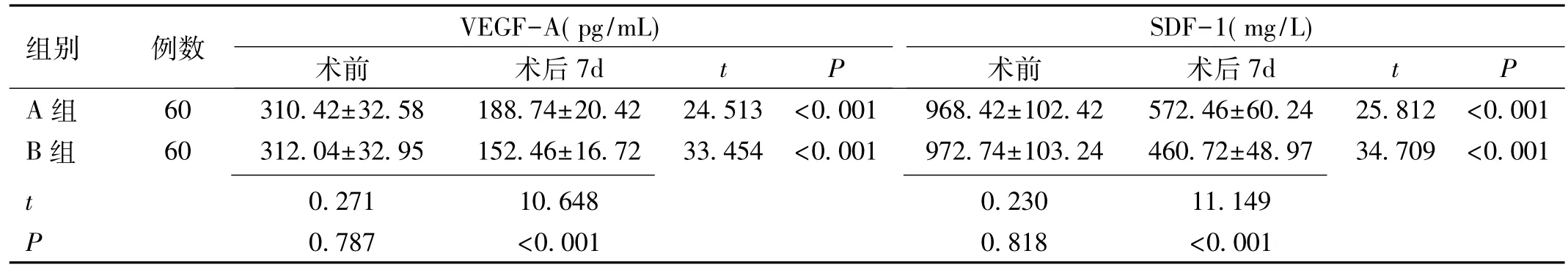
表2 两组VEGF-A和SDF-1比较
注:A组:给予玻璃体切割术治疗;B组:在A组基础上给予玻璃体腔注射雷珠单抗治疗。
组别 例数 VEGF-A(pg/mL)SDF-1(mg/L)术前 术后7d t P 术前 术后7d t P A 组 60 310.42±32.58 188.74±20.42 24.513 <0.001 968.42±102.42 572.46±60.24 25.812 <0.001 B 组 60 312.04±32.95 152.46±16.72 33.454 <0.001 972.74±103.24 460.72±48.97 34.709 <0.001 t 0.271 10.648 0.230 11.149 P 0.787 <0.001 0.818 <0.001
1 对象和方法
1.1 对象 前瞻性选取2017-01/2018-01本院收治的PDR患者120例150眼。纳入标准:(1)符合《中华眼科学》[5]中PDR诊断标准;(2)糖尿病病程>3a、糖尿病视网膜病变(DR)分期为Ⅳ~Ⅵ期;(3)年龄>18岁、无精神病病史;(4)签署知情同意书。排除标准:(1)术前1mo血糖控制不佳(空腹血糖>11.0mmol/L)、有雷珠单抗等抗VEGF-A治疗史;(2)有免疫、血液系统严重性疾病;(3)有心、肝、肾等严重性原发性疾病;(4)有高度近视及其他非PDR眼底病。本研究经伦理委员会审批通过,依据随机数字表法分为A组60例76眼和B组60例74眼,两组性别、年龄、病程、体质量指数、空腹血糖、糖化血红蛋白、DR分期、患侧比较,差异无统计学意义(P>0.05),见表1。
1.2 方法
1.2.1 治疗方法 B组先给予玻璃体注射雷珠单抗治疗,即VT术前3~5d托吡卡胺眼液点眼,消毒铺巾,散瞳至5~6mm,表面麻醉(盐酸奥布卡因眼液),开睑(开睑器),眼球固定(齿镊)等术前准备,对合并白内障者先行超声乳化术摘除晶状体,于颞下角巩缘下4mm处以4.5号针垂直于眼球壁进入玻璃体腔中心位置后,缓慢注射0.05mL(0.5mg)雷珠单抗,缓慢退出针头、无菌纱布覆盖、氧氟沙星滴眼液滴眼至VT手术;然后给予VT治疗,即再次行雷珠单抗注射相同的术前准备,于玻璃体三通道采用20G的MVR矛形穿刺刀行垂直穿刺、颞下建立灌注管、颞上及鼻上建立手术器械通道,常规切割中央玻璃体,运用剥膜钩、视网膜镊、眼内剪切除新生血管膜,解除牵拉,复位视网膜,期间注意操作尽量轻柔,保护周围无关组织及血管等,对大面积出血者采用球内电凝止血,完毕后行视网膜激光光凝,根据情况选择是否硅油或气体(C3F8)填充,术毕常规退出器械,无菌纱布覆盖,氧氟沙星滴眼液滴眼3d预防感染等处理。A组给予VT治疗,即不给予玻璃体注射雷珠单抗治疗,其余均同B组。
1.2.2 指标观察 比较两组 VT手术情况、并发症及VEGF-A、SDF-1、最佳矫正视力(BCVA)、黄斑中心视网膜厚度(CMT)。(1)VT手术情况,包括手术时间、电凝止血、术中出血等;(2)并发症,包括医源性裂孔、玻璃体积血(二次出血)、前房积血(二次出血)等;(3)VEGF-A、SDF-1,于术前、术后7d抽取外周静脉血3mL置入无菌试管中,分离血清(3000r/min、10min、离心半径 8.5cm)后,采用酶联免疫吸附法检测 VEGF-A、SDF-1水平;(4)BCVA、CMT,于术前、术后1d,3mo通过国际标准视力表检测BCVA[以最小分辨角对数(LogMAR)表示],并通过裂隙灯显微镜、光学相干断层扫描检测CMT。
统计学分析:采用统计学软件SPSS22.0进行处理,计量资料以珋x±s表示,组间比较采用独立样本t检验,同组时间差异采用配对样本t检验,多个时间差异采用重复测量方差分析,两两比较采用LSD-t检验;计数资料以%表示,组间比较采用χ2检验;等级资料的组间比较采用秩和检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组VEGF-A和 SDF-1比较 A组和B组术前VEGF-A、SDF-1比较,差异均无统计学意义(P>0.05),两组术后 VEGF-A、SDF-1明显低于术前,B组术后VEGF-A、SDF-1明显低于A组,差异均有统计学意义(P<0.001),见表 2。
2.2 两组VT手术情况比较 B组VT手术时间、电凝止血、术中出血明显低于A组,差异均有统计学意义(P<0.05),见表 3。

表3 两组VT手术情况比较

表4 两组并发症比较 眼(%)
表5 两组BCVA和CMT比较
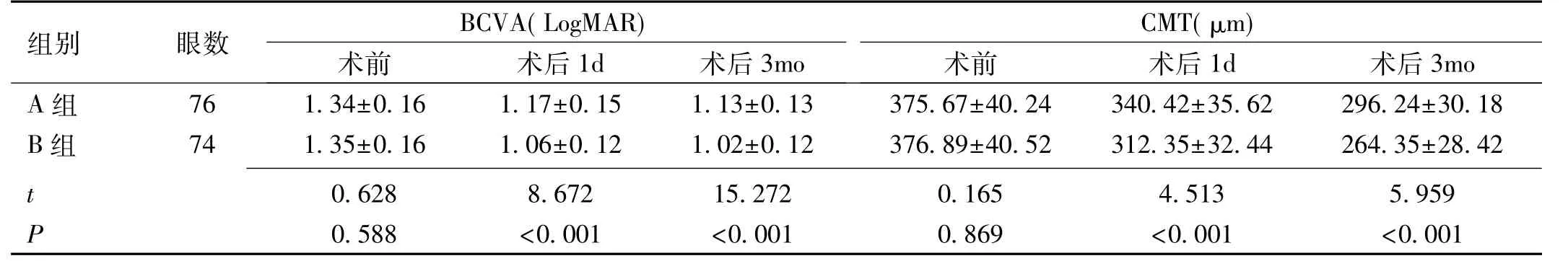
表5 两组BCVA和CMT比较
注:A组:给予玻璃体切割术治疗;B组:在A基础上给予玻璃体腔注射雷珠单抗治疗。
组别 眼数 BCVA(LogMAR)CMT(μm)术前 术后1d 术后3mo 术前 术后1d 术后3mo A 组 76 1.34±0.16 1.17±0.15 1.13±0.13 375.67±40.24 340.42±35.62 296.24±30.18 B 组 74 1.35±0.16 1.06±0.12 1.02±0.12 376.89±40.52 312.35±32.44 264.35±28.42 t 0.628 8.672 15.272 0.165 4.513 5.959 P 0.588 <0.001 <0.001 0.869 <0.001 <0.001
2.3 两组并发症比较 B组并发症发生率明显低于A组,差异有统计学意义(P<0.05),见表4。
2.4 两组BCVA和CMT比较 A组和B组术前BCVA、CMT比较,差异均无统计学意义(P>0.05),两组术后1d,3mo BCVA、CMT明显低于术前,差异均有统计学意义(A组:BCVA:t1d=6.758,P1d<0.001;t3mo=8.880,P3mo<0.001;CMT:t1d=5.718,P1d<0.001;t3mo=13.767,P3mo<0.001;B组:BCVA:t1d=12.473,P1d<0.001;t3mo=14.194,P3mo<0.001;CMT:t1d=10.696,P1d<0.001;t3mo=19.560,P3mo<0.001),B组术后1d,3mo BCVA、CMT明显低于 A 组,差异均有统计学意义(P<0.001),见表5。
3 讨论
PDR是由糖尿病高血糖损伤引发视网膜循环障碍而导致血-视网膜屏障受损所致,主要表现为视网膜增厚而引起视力下降,也是糖尿病患者主要的致盲疾病之一[6-7]。目前,VT是 PDR 有效的治疗方法之一,可有效清除玻璃体积血、解除玻璃体视网膜牵拉,并使脱离的视网膜复位,从而逐步恢复视力[8-9]。但PDR患者视网膜与增生膜、新生血管膜紧密粘连,影响患者的术后康复及手术疗效[10-11]。但VT在切割干净增殖膜及缓解、消除视网膜牵拉等过程中,其剥离难度大,加之视网膜存在广泛水肿,常易损伤到正常的视网膜而导致出血及医源性裂孔等并发症。
近年来,随着PDR病理生物学研究的不断进步,相关研究发现,PDR的病变特征是形成新生血管、增殖性纤维膜进入玻璃体,导致视网膜牵拉而使视网膜脱离出现缺血、缺氧症状[12-13]。而 SDF-1是趋化因子蛋白家族中的一员,具有趋化细胞生长、增殖的作用,VEGF-A则是一种特异性血管生成因子,可促使SDF-1等合成并共同参与PDR新生血管的增殖进程,且VEGF-A还能促进有丝分裂素与内皮细胞受体结合而引起内皮细胞增殖并形成新生血管及改变血管渗透性,从而加快血-视网膜屏障的破坏而促使 PDR 的发生发展[14-15]。而有研究显示,抗VEGF-A药物是PDR重要的治疗方法,其中雷珠单抗是一种重组的单克隆抗VEGF-A药物,具有靶向的抑制阻断所有VEGF-A亚型活性的作用,可有效抑制视网膜内血管新生,有利于提高患者的治疗疗效[16-17]。
本研究结果显示,A组和B组术后VEGF-A、SDF-1明显低于术前,B组术后VEGF-A、SDF-1明显低于A组,表明雷珠单抗联合VT能够有效降低了PDR患者VEGF-A、SDF-1,有效抑制患者视网膜血管的新生。分析原因是VT能够通过手术方式清除玻璃体积血,解除玻璃体视网膜牵拉,在一定程度上减少了积血、视网膜牵拉等对VEGF-A、SDF-1等血管新生因子的释放;而本研究于术前联合了雷珠单抗治疗后,可能由于其能够有效抑制阻断VEGF-A亚型的活性[18],不仅进一步减少了 VEGF-A的生成,还抑制了VEGF-A促进SDF-1合成的作用,使患者的SDF-1进一步降低。同时,本研究中,B组VT手术时间、电凝止血、术中出血及并发症发生率明显低于A组,A组和B组术后1d,3mo BCVA、CMT明显低于术前,B组术后1d,3mo BCVA、CMT明显低于A组,表明雷珠单抗联合VT能够有效减少VT创伤及并发症,有效改善患者BCVA、CMT。分析原因是本研究通过雷珠单抗联合VT更有效地降低了 PDR患者视网膜内 VEGF-A、SDF-1,使VEGF-A、SDF-1促进血管新生的作用下降,能够有效逆转虹膜及视网膜新生血管的形成,改善血管的通透性,使新生血管受到抑制发生不同程度的萎缩和消退,能够降低VT切割干净增殖膜及缓解、消除视网膜牵拉等操作难度,从而有效减少VT创伤及医源性裂孔、玻璃体积血(二次出血)、前房积血(二次出血)等并发症,为患者术后康复提供了良好的条件,有效改善了患者BCVA、CMT。
综上所述,本研究认为,雷珠单抗联合VT可有效降低PDR患者血清VEGF-A、SDF-1水平,有利于减少VT创伤及并发症,且可有效改善患者BCVA、CMT。但雷珠单抗注射的最佳时机还不确定,且本次研究纳入病例数较少,不足以代表所有病患情况,期待更大样本及更深入的研究。

