EDTA滴定法测定再生锌原料中的锌含量
范丽新 汤淑芳
(1 北矿检测技术有限公司,北京 102628;2 金属矿产资源评价与分析检测北京市重点实验室,北京 102628)
前言
目前世界上已探明的锌矿储量非常有限,因此再生锌原料就显得尤为重要,应当引起我们的重视。再生锌原料主要包括:热镀锌渣、锌灰,压铸锌合金生产过程中生产的含锌废料,报废的锌合金废料,烟道灰,瓦斯泥/灰,铜、铅、锌冶炼产生的含锌烟尘,进口的含锌物料等,是金属锌的重要来源。因此制定相应的再生锌原料化学分析方法,对促进保护环境和资源的综合利用具有重要的意义。
高含量锌的测定方法一般为EDTA滴定法[1-6],再生锌原料中含有较高含量的铁、锰、铅等共存元素,本文建立了使用氟化铵-盐酸-硝酸-硫酸溶样,过滤消除高含量铅的干扰,氨水沉淀分离铁、锰、铅等共存元素,滤液中加入掩蔽剂掩蔽少量干扰元素,从而准确地测定再生锌原料中锌含量,结果满意。
1 实验部分
1.1 主要试剂
锌标准溶液(5 mg/mL):称取5.000 0 g金属锌(wZn≥99.99%)溶于100 mL盐酸(1+1)中,移入1 000 mL容量瓶中,以水定容,摇匀。
铅标准溶液(5 mg/mL):称取5.000 0 g金属铅溶于100 mL硝酸(1+1)中,移入1 000 mL容量瓶中,以水定容,摇匀。
洗涤液:2 g氯化铵溶于100 mL水中,加3 ~4滴氨水,混匀。
硫酸铁溶液:称取100 g九水合硫酸铁溶解于1 000 mL硫酸(1+9)中,此溶液1 mL含三价铁约20 mg。
乙酸-乙酸钠缓冲溶液(pH=5.5):称取200 g三水合乙酸钠,溶于水中,加入18 mL乙酸,用水稀释至1 000 mL,混匀。
氟化铵溶液(200 g/L) 、甲基橙指示剂(0.5 g/L)、二甲酚橙指示剂(5 g/L,限2周内使用)、过硫酸铵溶液(200 g/L,当日配制)、氟化钾溶液(200 g/L)、硫代硫酸钠溶液(100 g/L)。
乙二胺四乙酸二钠(Na2EDTA)标准滴定溶液[c(C10H14N2O8Na2·2H2O)≈0.05 mol/L]:称取18.6 g乙二胺四乙酸二钠,加水微热溶解,冷至室温,移入1 000 mL容量瓶中,用水稀释至刻度,混匀放置3 d后标定。
Na2EDTA标准滴定溶液的标定:称取4份0.10 g(精确到0.000 1 g)金属锌置于250 mL烧杯中,加入10 mL盐酸(1+1),盖上表皿,低温溶解,取下冷却,加入1 mL硫酸铁溶液(200 g/L),加入3~5 g氯化铵、5 mL过硫酸铵(200 g/L),用氨水中和至沉淀完全并过量10 mL,加热微沸1~2 min,趁热用中速定性滤纸过滤,用500 mL烧杯承接滤液,用热的洗涤液洗涤烧杯和沉淀各2~3次,滤液保留。将沉淀用热的洗涤液洗至原沉淀的烧杯中,加入1~2 mL盐酸(1+1)溶解沉淀,加入5 mL过硫酸铵(200 g/L),用氨水中和至沉淀完全并过量10 mL,加热微沸1~2 min,取下,经原滤纸过滤于保留滤液的烧杯中,用热的洗涤液洗涤烧杯和沉淀各3~4次。将滤液煮沸并浓缩体积约100 mL,彻底破坏过剩的过硫酸铵,取下冷却。加入0.1 g抗坏血酸、1滴甲基橙指示剂(0.5 g/L),用氨水(1+1)和盐酸(1+1)调至溶液恰变红色,加入25 mL乙酸-乙酸钠缓冲溶液、5 mL氟化钾溶液(200 g/L)、5 mL硫代硫酸钠溶液(200 g/L)混匀。滴加2滴二甲酚橙指示剂(5 g/L),用Na2EDTA标准滴定溶液滴定至溶液由紫红色变为亮黄色即为终点。随同标定作空白实验。
按式(1)计算Na2EDTA标准滴定溶液对锌的滴定系数F:
(1)
式中:F为Na2EDTA标准滴定溶液对锌的滴定系数,g/mL;m1为称取金属锌质量,g;V1为标定时消耗Na2EDTA标准滴定溶液的体积,mL;V0为标定时滴定空白试剂溶液所消耗Na2EDTA标准滴定溶液的体积,mL。平行标定4份,结果保留4位有效数字,其极差值不超过0.000 010 g/mL时,取其平均值。否则重新标定。
1.2 实验方法
按表1称取试样(精确至0.000 1 g),置于250 mL三角烧杯中,用少量水润湿,加入1~3 mL氟化铵(200 g/L),再加入10 mL盐酸,盖上表面皿,置于电热板上低温加热5~10 min,再加入5 mL硝酸、5 mL硫酸(1+1) [注:如试料含碳较高,可加入2~5 mL高氯酸,对特别难消解的样品,还可以在冒浓白烟时滴加硝酸-硫酸混合酸(1+1)]。
当铅量小于12 mg时,继续加热至呈湿盐状,取下稍冷。加入20 mL硫酸(1+9),加热溶解盐类,稍冷,用水吹洗表面皿及杯壁,并稀释体积至60 mL左右。当铅量大于12 mg时,补加3 mL硫酸(碳高样品待碳消解完全后,取下稍冷再补加硫酸),加热至冒浓白烟,蒸至硫酸白烟出现回流,取下冷却。用水吹洗表面皿及杯壁,并稀释体积至50 mL左右,加热微沸10 min,冷却至室温,放置1 h。用慢速定量滤纸过滤,滤液用250 mL烧杯承接,用硫酸(2+98)洗涤烧杯及沉淀各4~5次,水洗烧杯及沉淀各1次,保留滤液。

表1 试料质量Table 1 Sample weighing of test material
加入3~5 g氯化铵、5 mL过硫酸铵(200 g/L),用氨水中和至沉淀完全并过量10 mL,加热微沸1~2 min,趁热用中速定性滤纸过滤,用500 mL烧杯承接滤液,用热的洗涤液洗涤烧杯和沉淀各2~3次,滤液保留(注:如溶液中含铁较低,加入氯化铵前适当补加硫酸铁溶液使溶液中含铁量约20 mg)。
将沉淀用热的洗涤液洗至原沉淀的烧杯中,加入1~2 mL盐酸(1+1)溶解沉淀,加入5 mL过硫酸铵(200 g/L),用氨水中和至沉淀完全并过量10 mL,加热微沸1~2 min,取下,经原滤纸过滤于保留滤液的烧杯中,用热的洗涤液洗涤烧杯和沉淀各3~4次(注:锰高样品,氢氧化物沉淀不易被盐酸溶解,可滴加一滴过氧化氢溶液)。
将滤液煮沸并浓缩体积约100 mL,彻底破坏过剩的过硫酸铵,取下冷却。加入0.1 g抗坏血酸、1滴甲基橙指示剂(0.5 g/L),用氨水(1+1)和盐酸(1+1)调至溶液恰变红色,加入25 mL乙酸-乙酸钠缓冲溶液、5 mL氟化钾溶液(200 g/L)、5 mL硫代硫酸钠溶液(200 g/L)混匀。滴加2滴二甲酚橙指示剂(5 g/L),用Na2EDTA标准滴定溶液滴定至溶液由紫红色变为亮黄色即为终点。
锌含量计算公式为:
(2)
式中:F为Na2EDTA标准滴定溶液对锌的滴定系数,g/mL;V3为试液消耗Na2EDTA标准滴定溶液的体积,mL;V2为空白试液消耗Na2EDTA标准滴定溶液的体积,mL;m2为试料的质量,g;0.581 6为镉量换算为锌量的系数;wCd由原子吸收光谱法测得的镉的质量分数(称取样品0.1 g于250 mL烧杯中,加入10 mL盐酸,盖上表面皿,低温加热5 ~10 min,加入5 mL硝酸,继续加热溶解并蒸至近干,取下稍冷。加入10 mL(1+1)盐酸,加热溶解盐类,取下冷却。用水吹洗表面皿及杯壁,移入100 mL容量瓶中,用水稀释至刻度,混匀。使用空气-乙炔火焰,于原子吸收光谱仪波长228.8 nm处,以水调零,分别测量试液和随同试料空白溶液的吸光度,减去空白溶液的吸光度,从工作曲线上查出相应的镉的质量浓度)。计算结果精确至小数点后两位。
2 结果与讨论
2.1 溶样方式的选择
再生锌原料种类较多,有些样品含硅高,有些样品含碳高,为样品消解完全,对溶样方式进行了研究(表2)。

表2 溶样方式的选择Table 2 Sample dissolution methods
1#、2#、4#硅的含量分别为5.92%、5.62%、1.49%。由表2可知,含硅量高的样品需要加氟化铵,否则会溶解不完全,使结果偏低,氟化铵的加入对锌的测定无影响。1#、2#、3#、4#、5#碳的含量分别为8.14%、2.58%、11.36%、3.76%、4.02%。实验表明,含碳量高的样品需要加高氯酸,否则溶解不完全。实验选定的溶样方式为盐酸+氟化铵+硝酸+高氯酸+硫酸。
2.2 样品所含杂质元素
对再生锌原料中主要成分的影响进行了干扰实验及消除干扰实验,表3为再生锌原料主要成分表。
2.2.1 铁的影响
铁高干扰Na2EDTA滴定锌,采用氢氧化物共沉淀消除其干扰,实际样品中的铁含量高低不一,本实验研究了氢氧化铁沉淀对锌的吸附情况。称取0.10 g金属锌(精确至0.000 1 g),分别加入不同量的铁,按照分析步骤进行滴定,并计算Na2EDTA标准滴定溶液对锌的滴定系数,结果见表4。

表3 再生锌原料主要成分表Table 3 Main components of regenerated zinc material

表4 铁的加入量对滴定系数的影响Table 4 Effect of iron addition on titration coefficient
实验证明,氢氧化铁沉淀对锌有一定的吸附作用,选择同步标定消除微量吸附的影响。表4结果表明,用洗涤液洗涤氢氧化铁沉淀后,其对锌的吸附量比较恒定,10~60 mg的铁量对锌滴定系数基本无影响,但铁的含量过低,会使氨水中和至沉淀完全观察不够明显。实验选择标定时加入20 mg铁,与样品进行同步标定。对铁含量较低的样品,则在样品消解后补加铁至20 mg。
有些样品锌含量较低,铁的含量相对较高,实验进行了较高含量的铁对较低含量锌的测定影响,实验结果见表5。

表5 较高含量铁对较低含量锌测定的影响Table 5 Effect of high iron content on determination of lower zinc content
由表5可见,较高含量的铁经过氢氧化铁沉淀分离对较低含量锌的测定无影响。
2.2.2 铅的影响
铅在pH值5~6时与EDTA 络合稳定,与二甲酚橙也生成稳定络合物,干扰锌的测定。
移取20.00 mL锌标准溶液,加入不同量铅,按不分离铅实验步骤进行测定,结果见表6。
结果表明,当试样中含铅量小于12 mg(称样量为0.20 g时,相当于6%的铅含量)时,经氢氧化铁沉淀过滤基本上能分离掉铅,当铅≥12 mg时,分离效果不佳。拟采用硫酸铅沉淀分离消除高含量铅的干扰。并研究了分离硫酸铅沉淀对锌测定的影响。移取20.00 mL锌标准溶液,加入不同量的铅标准溶液,以下按实验方法进行,结果见表7。

表6 铅对锌测定的影响Table 6 Effect of lead on the determination of zinc
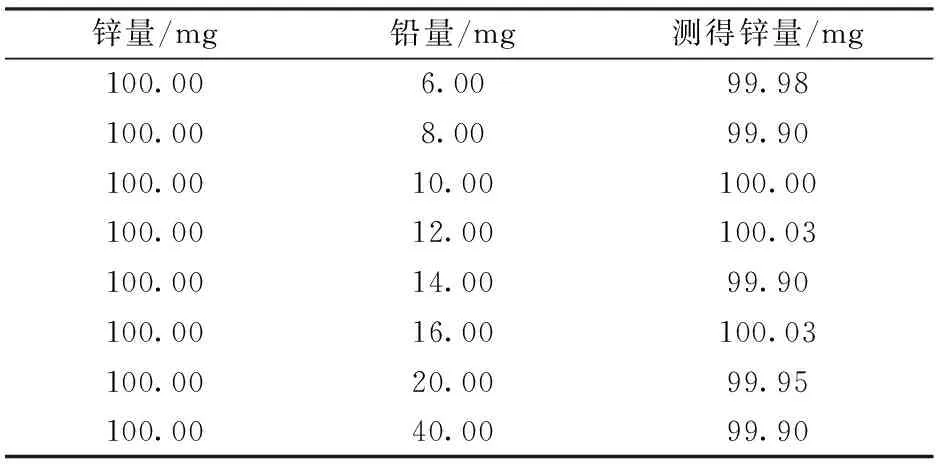
表7 分离铅对锌测定的影响Table 7 Effect of separation of lead on the determination of zinc
实验表明:当铅≥12 mg时,采用硫酸铅沉淀分离可消除铅的干扰。且铅含量低于12 mg时,硫酸铅沉淀分离也基本不影响锌的测定。
对样品4#(含铅量约24%)和6#(含铅量约13%)按不分离硫酸铅沉淀的实验步骤进行操作,分别测定氢氧化铁分离一次滤液及二次滤液中铅量。分别将第一次过滤滤液和第二次过滤滤液煮掉过硫酸铵后,加入10 mL盐酸,定容于200 mL容量瓶中,用ICP-AES法测定滤液中的铅量。表8结果表明,样品中含铅量较高时,氢氧化铁沉淀过滤只能分离掉部分铅(不定量),剩余部分的铅会通过第一次过滤及第二次过滤进入到滤液中,对锌的测定产生影响。
2.2.3 锰的影响
锰高干扰Na2EDTA滴定锌,采用加入过硫酸铵氧化-氢氧化物共沉淀消除其干扰。称取0.10 g金属锌(精确至0.000 1 g),分别加入不同量的锰,过滤时加入5 mL过硫酸铵,按照分析步骤进行滴定,并计算Na2EDTA标准滴定溶液对锌的滴定系数,结果见表9。
实验证明,5 mL过硫酸铵基本上能完全氧化20 mg以内的锰,锰含量超过20 mg终点变化不敏锐。
称取0.10 g金属锌(精确至0.000 1 g),分别加入30 mg和50 mg锰,过滤时加入不同量的过硫酸铵,按照分析步骤进行滴定,并计算EDTA标准滴定溶液对锌的滴定系数,结果见表10。

表8 一次滤液及二次滤液中的铅量Table 8 Lead content in primary and secondary filtrates

表9 锰的加入量对滴定系数的影响Table 9 Effect of manganese addition on titration coefficient

表10 过硫酸铵用量对锰沉淀的影响Table 10 Effect of ammonium persulfate dosage on manganese precipitation
实验证明,加大过硫酸铵的用量能消除更多锰的干扰,10 mL过硫酸铵基本上能完全氧化50 mg以内的锰,但是锰含量为50 mg时,氢氧化物沉淀对锌的吸附作用较大,使锌的测定结果偏低。
收集的一百多个再生锌原料试样中未发现锰含量超过20 mg(称样量为0.20 g时,相当于10%的锰含量),实验选择加入过硫酸铵(200 g/L)的体积为5 mL。
2.2.4 其它共存单元素对锌测定的影响
再生锌原料中其它共存元素还有硅、硫、碳、铝、铁、锰、镁、钙、铜、砷等,硅在溶样过程中以SiF4的形式挥散除去,硫和碳在溶样过程中挥发除去。氢氧化物沉淀分离时,可消除绝大部分铁、部分铝和钙、镁的干扰,过硫酸铵氧化-氢氧化物共沉淀可消除锰的干扰,滴定时,少量铜采用硫代硫酸钠掩蔽,残留铝、铁可采用氟化钾掩蔽。分别取100.00 mg及30.00 mg锌,按表11分别加入不同种类不同量的单元素,按实验步骤测定锌量,结果见表11。
结果表明,4 mg砷、10 mg铝、6 mg镁、20 mg钙对100 mg和30 mg锌的测定基本无影响。当镁超过6 mg(称样量为0.20 g时,相当于3%的镁含量)时,锌的测定结果偏低。收集到的样品中无含量高于3%的镁。

表11 共存单元素对锌测定的影响Table 11 The influence of coexisting elements on the determination of zinc
2.2.5 混合干扰元素对锌测定的影响
本实验也进行了混合共存元素对100.00 mg和30.00 mg锌的测定影响,实验结果见表12。
表12结果表明,所列共存元素在选定分析步骤下对锌的测定基本没有影响。

表12 混合干扰实验Table 12 Mixed interference test
2.3 滴定条件的选择
2.3.1 氨水用量对锌测定的影响
移取20.00 mL锌标准溶液,按照实验步骤进行测定,氢氧化铁沉淀完全后过量不同体积的氨水,结果见表13。

表13 氨水过量体积对锌测定的影响Table 13 The influence of excess volume of ammonia water on the determination of zinc
实验表明,氨水过量5~20 mL对锌的测定均无明显影响,实验选定氨水过量体积为10 mL。
2.3.2 抗坏血酸用量对锌测定的影响
移取20.00 mL锌标准溶液,按照实验步骤进行测定,滴定前加入不同量的抗坏血酸,结果见表14。

表14 抗坏血酸加入量对锌测定的影响Table 14 Effect of ascorbic acid addition on zinc determination
实验表明,抗坏血酸的加入量0.1~0.4 g对锌的测定基本无影响,实验选用加入0.1 g抗坏血酸。
2.3.3 氟化钾用量对锌测定的影响
移取20.00 mL锌标准溶液,加入10 mg铝,按照实验步骤进行测定,滴定前加入不同体积的氟化钾,结果见表15。

表15 氟化钾用量对锌测定的影响Table 15 Effect of potassium fluoride dosage on determination of zinc
实验表明,氟化钾的用量2~15 mL对锌的测定影响不大,实验选用加5 mL氟化钾。
2.3.4 硫代硫酸钠的用量对锌测定的影响
移取20.00 mL锌标准溶液,加入2 mg的铜,按照实验步骤进行测定,滴定前加入不同体积的硫代硫酸钠,结果见表16。
由于再生锌原料中铜的含量为0.03%~0.6%,5 mL硫代硫酸钠溶液足以掩蔽再生锌中的铜。实验选用加5 mL硫代硫酸钠。
2.4 一次过滤和二次过滤残渣中的锌量
按拟定的测定步骤对样品进行测定(4#、6#按实验方法分离铅测定)。将一次过滤和二次过滤残留渣用10 mL盐酸溶于100 mL容量瓶中,用水洗净滤纸,稀释至刻度,用ICP-AES法测定残留锌量,二次过滤残留锌量低于0.2 mg,与标定二次过滤残留锌量一致,对测定结果影响不大。一次过滤残留锌量在0.7~1.9 mg,误差范围比较大,实验选择二次过滤,结果见表17。

表16 硫代硫酸钠用量对锌测定的影响Table 16 The influence of sodium thiosulfate dosage on the determination of zinc
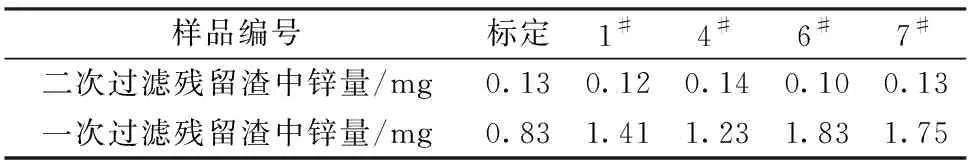
表17 过滤残留渣中的锌量Table 17 Zinc content in filtered residue
2.5 二次滤液中的铅量
按拟定的分析步骤对样品进行测定(标定中加20 mg铅,标定4#、6#按实验方法分离铅测定)。将二次过滤溶液煮至100 mL后,加入10 mL盐酸,定容于200 mL容量瓶中,用ICP-AES法测定滤液中的铅量,经多次实验,残留铅量低于0.01%,对测定结果不造成影响。对于含铅量较高的样品(铅量大于12 mg),实验选择先分离铅,实验结果见表18。

表18 二次滤液中的铅量(分离铅)Table 18 Lead content in secondary filtrate (separation of lead)
2.6 精密度实验
分别对不同锌量的再生锌样品进行了11次独立实验,相对标准偏差(RSD)在0.15%~1.0%,表明方法的重现性良好,结果见表19。
2.7 加标回收实验
在样品1#、2#和3#中分别加入不同量的锌标准溶液进行加标回收实验,加标回收率在99.1%~102%,表明结果准确、可靠,结果见表20。
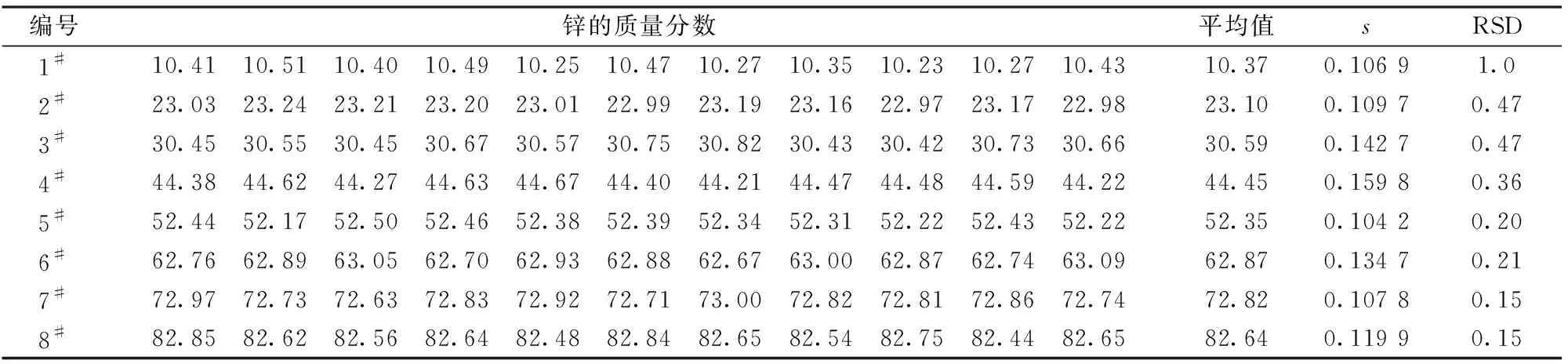
表19 精密度实验Table 19 Precision tests /%

表20 回收率实验Table 20 The analytical results for the recovery test
3 结论
通过实验表明,采用EDTA滴定法测定再生锌原料中的锌含量,能够消除铅、铁、锰等元素的干扰,同时优化了滴定条件。方法简便易行,分析结果准确可靠,能满足日常对再生锌原料中锌含量的检测要求。

