皮肤黑色素形成机理与干预机制
陈卓仪,刘晓英,郑雅婷,洪 婷,刘潭林,杜志云
(1. 广东工业大学,广东 广州 510006;2. 无限极(中国)有限公司,广东 广州 510000)
俗话说“一白遮三丑”,美白是现代广大女性关注的热门话题。由于皮肤的颜色主要由皮肤色素含量及分布决定,黑色素是最主要的决定因素。因此美白化妆品功效性评价往往通过皮肤黑色素含量的减少程度来进行评判。
皮肤的色素物质主要包括黑色素、胡萝卜素等。黑色素广泛存在于人的皮肤、黏膜、视网膜、软脑膜、胆囊及卵巢等处。其中,白种人皮肤含褐黑色素居多,肤色较浅;黄种人的皮肤以真黑色素居多,肤色较深。因此抑制真黑素和褐色素的形成是美白的主要途径之一。
1 黑色素的形成与调控
1. 1 黑色素形成机理
黑色素的形成主要涉及3种酶:酪氨酸酶(TYR)、DHICA氧化酶(TRP-1)和多巴色素异构酶(TRP-2)。酪氨酸酶是一种铜蛋白,是黑色素生成的关键酶,其活性中心的双核铜离子在酶催化中起重要作用。
黑色素生成的初始阶段是由苯丙氨基酸和酪氨酸在TYR的催化作用下氧化生成多巴醌(DQ)开始,DQ可以成为合成真黑素和褐色素的基质。第1个步骤是黑色素合成的关键步骤,剩余的反应可自发地在生理pH下进行。DQ形成后,DQ经过分子内除氨基生成白色多巴色素。白色多巴色素与DQ之间的氧化还原再产生多巴色素和多巴。多巴色素逐渐分解,大部分脱羟生成二羟基吲哚(DHI),而少部分生成二羟基吲哚羧酸(DHICA)。最后,DHI氧化成吲哚-5,6-醌(IQ),IQ、DHICA和白色多巴色素生成的吲哚-5,6-醌-2-羧酸(ICAQ)一起被氧化生成真黑素。其中TRP-1是催化DHICA氧化成真黑素的重要酶。另外,在谷胱甘肽或半胱氨酸的作用下,DQ转换成5-S-半胱氨酸多巴(5-S-CD)和少量的2-S-半胱氨酸多巴(2-S-CD)。之后反应生成谷胱氨酸多巴,进而被氧化生成半胱苯肼噻嗪(HBTA),生成褐色素[1-5]。真黑素与褐色素最终合成黑色素。
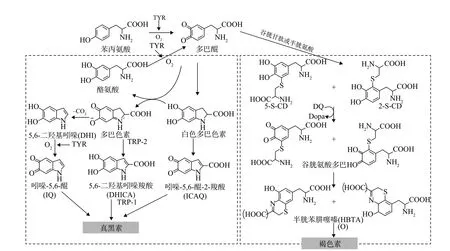
图 1 黑色素的生成路径(真黑色素和褐色素生成)[25]Fig. 1 Pathway of melanin production (eumelanin and pheomelanin)
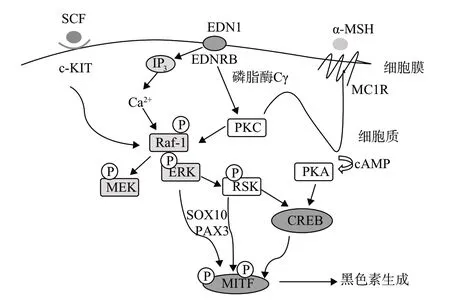
图 2 EDN1和SCF靶点的运作机制Fig. 2 The mechanism of EDN1 and SCF targets
1. 2 黑色素在细胞分子水平上的调控
内皮素1(EDN1)和干细胞因子(SCF)是最本质的导致黑色素在皮肤上发生不均匀色素沉积的靶点。相对于直接抑制酪氨酸活性,干预EDN1或SCF特有的细胞内通路是一个十分有效的路径。对皮肤黑变病、日光斑、黄褐斑或者与它们相关色素沉积的抑制也是有效的。
细胞内信号转导机制与EDN1、SCF、小眼畸形相关转录因子(MITF)、蛋白激酶A(PKA)、蛋白激酶C(PKC)、酪氨酸相关蛋白质-1(TYRP-1)、多巴色素异构酶(DCT)、酪氨酸激酶(TYK)和α-促黑色素细胞激素(α-MSH)等都有关[9]。
EDN1和SCF分别和它们的受体EDNRB、c-KIT结合,引起聚磷酸肌醇水解生成三磷酸肌醇(IP3),IP3可调动细胞内Ca2+,而甘油二酯通过活化磷脂酶Cγ,从而激活PKC。其中激活的PKC使苏氨酸蛋白激酶(Raf-1)发生磷酸化,磷酸化的Raf-1将信号传递到丝裂原活化蛋白激酶(MAPK)时,使MEK,ERK和RSK均按顺序被激活并发生磷酸化,最终磷酸化的RSK将信号传导至cAMP应答元结合蛋白(CREB),使其激活并发生磷酸化。磷酸化的CREB作用于MITF基因上并与其基因启动子结合,使MITF被转录并翻译,最终作用于TYR基因上,使TYR激活,导致黑色素的产生[10]。
于此同时,活化的PKC也通过α-MSH及其黑色素受体1(MC1R)造成cAMP的升高,cAMP能通过信号传导激活细胞内的PKA,而活化PKA也能引起CREB磷酸化,磷酸化的CREB同样作用于MITF基因上,导致黑色素的产生。
另外,SCF与其受体c-KIT结合,也通过二聚化和自身磷酸化调节酪氨酸激酶本身的活性。被激酶磷酸化的ERK和RSK也与其他转录因子SOX10,PAX3等结合,从而增加黑色素细胞特殊蛋白的基因和蛋白质水平的表达。
所以在正常人类黑色素细胞中EDN1和SCF两个信号之间发送信号,在细胞内信号通道内相互传递信 号[15],刺激表皮黑色素的合成与沉积。
2 黑色素的干预机制
2. 1 黑色素合成通路
黑色素的生成通过一系列细胞内的信号通道进行调控,主要有3个最常见的信号通道分别是cAMP-依赖信号通路、Wnt/β-连环蛋白通路和ERK信号通路,这3个常见的信号通路均参与了MITF监管调控黑色素生成[6-8]。MITF是黑色素在黑色素细胞主要的调节因子,通过绑定TYR,TRP-1和TRP-2基因表达的启动因子区域调节TYR,TRP-1和TRP-2的转录。
2. 1. 1 cAMP-依赖信号通路
MC1R是在黑色素细胞中生成黑色素的关键控制器。当α-MSH刺激MC1R时,它通过腺苷酸环化酶(AC)激活产生cAMP。cAMP进而激活PKA,PKA通过CREB的磷酸化激活MITF的基因表达。最后通过与TYR,TRP-1和TRP-2启动区域相互作用,MITF基因转录生成黑色素相关的蛋白。
一旦α-MSH与MC1R结合,黑色素原生成增加100倍[25]。除了α-MSH之外,β-MSH和促肾上腺皮质激素也通过这个方式促进黑色素生成。
2. 1. 2 Wnt或β-连环蛋白通路
Wnt配体与受体Frizzled结合激活后,一系列复杂的反应会引起β-连环蛋白(β-catenin)在细胞内的积累。在这个通道内,Wnt与G-蛋白耦合因子(Go/Gq)绑定,蓬乱蛋白(DVl)被吸收到质膜,从而导致糖原合成丝氨酸激酶-3β(GSK-3β)失活。随后,复合物被破坏,β-catenin的降解被抑制。稳定的β-catenin从而进入细胞核促进MITF基因的表达[19,20]。因此,Wnt通路是通过上调MITF活性来刺激黑色素的生成。
2. 1. 3 ERK信号通路
ERK信号通路也称为MAPK信号通路,涉及MAPK在内的许多蛋白。当一个信号分子SCF与细胞表面的受体c-Kit结合,Ras致癌基因会激活Raf激酶、MEK激酶和ERK1/2。被磷酸化的MITF泛素化和退化,从而消除相关蛋白基因的表达。因此,ERK信号通路是通过激活Ras致癌基因抑制正常和病变的黑色素细胞中黑色素的生成。
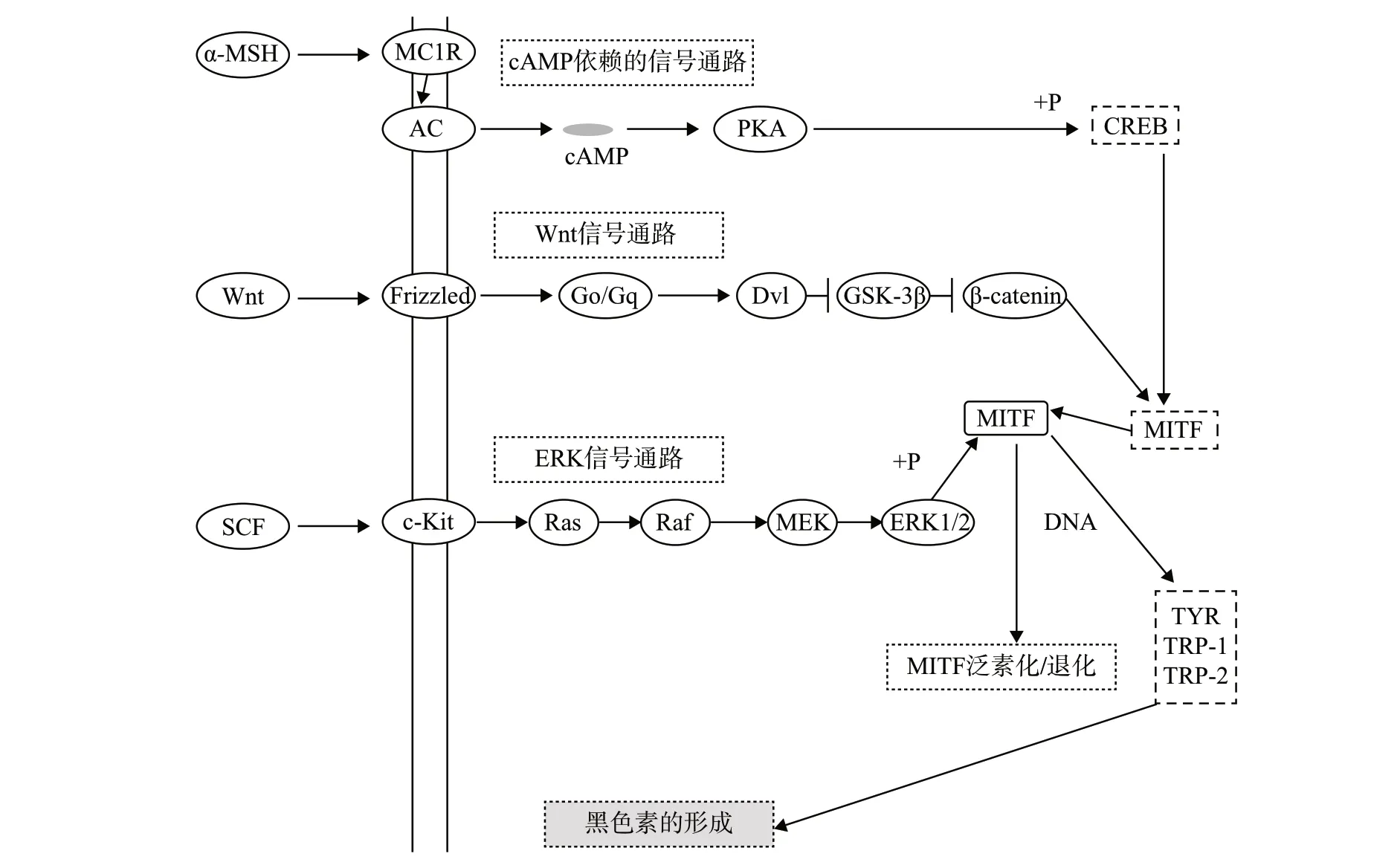
图 3 黑色素形成的信号通路[25]Fig. 3 Melanin formation signaling pathway
2. 1. 4 其他路径
1)通过增加表皮γδT细胞的白介素-13(IL-13)抑制TYR和DCT。2014年Han等[13]发现人参腺苷F1通过抑制人皮肤表面黑色素细胞或角质层的黑色素细胞中酪氨酸酶和DCT的mRNA表达,从而达到美白的效果。其中人参腺苷F1增加了人表皮上γδT细胞的IL-13的量,而IL-13对TRY和DCT的蛋白数量和它们在正常人表皮mRNA表达的减少有重要的作用。
2)通过调节降低环氧酶-2(COX-2)从而抑制黑色素的生成。COX-2是一种促进黑色素生成的诱导酶,UV促进COX-2的表达。Kim等[15]发现在黑色素细胞中COX-2降低可抑制TYR、TRP-1、TRP-2、gp100质粒DNA和MITF的表达,同时降低TYR酶的活性。并且COX-2的基因小干扰RNA(siRNA)明显地降低α-MSH,从而抑制其诱发黑色素细胞色素 沉积。
因此,COX-2是抑制黑色素生成和α-MSH诱发色素沉积的一个重要靶点,与COX-2的表达有关。COX-2的抑制剂可能在美白化妆品中对于色素沉积失常如雀斑、色素过多、色斑等的调节有作用。
3)糖基化。Diwakar等[26]通过皮肤活体组织和角质黑色素细胞在外源凝集素的板上混合培养,实验结果表明,黑色素细胞内黑色素含量的变化与糖蛋白的含量变化成正比,从而证明黑色素的生成与糖蛋白相关,但糖基化的路径还未知。
4)脂肪干细胞通过白介素-6(IL-6)调控抑制表皮黑色素细胞。2014年Kim等[27]发现,IL-6对人表皮黑色素细胞有直接的作用。他们通过将人类表皮黑色素细胞分成3组分别在脂肪干细胞条件培养基、人类皮肤纤维细胞条件培养基和对照培养基上进行培养。结果发现脂肪干细胞条件培养基和人类皮肤纤维细胞条件培养基都抑制了黑色素增殖和生成,但脂肪干细胞培养基比人皮肤成纤维细胞条件培养基对人黑色素细胞增殖、生成和酪氨酸酶活性更有效果。
之后将IL-6中和抗体与脂肪干细胞培养基混合培养人表皮黑色素细胞,再次测定黑色素细胞的生长和黑素生成。结果表明[27],IL-6中和抗体能显著影响脂肪干细胞培养基对表皮黑色素细胞的抑制作用,使人表皮黑色素细胞增殖, 黑素含量、酪氨酸酶活性和酪氨酸酶mRNA水平恢复正常。
所以,胚胎干细胞条件培养基通过降低黑色素合成的酶活性来抑制黑色素细胞增殖和黑色素生成,其中IL-6起到关键作用。
2. 2 黑色素运输路径干预
2. 2. 1 纤维母细胞(根源产生)
黑色素细胞与相邻细胞(皮肤角质形成细胞和成纤维细胞)之间的相互作用在人类皮肤颜色的调节中起着重要的作用。神经调节蛋白-1(NRG1)高度表达于菲茨帕特里克VI型皮肤的纤维母细胞,很大程度决定了人类的基本肤色。Choi等[29]研究参与调节黑色素细胞黑色素生成的NRG1活性基序,发现8基序增加黑色素的生成,却没有促进黑色素细胞的增殖,且产生这种效应的是最小的片段四肽。所以这种小生物活性肽只调节色素沉着而不刺激黑色素细胞增殖。
2. 2. 2 肌球蛋白(中间拦截)
调整actin-based肌球蛋白可以调节黑色素在表皮黑色素细胞的运输系统,Rab-肌球蛋白运输系统已经成为许多类型细胞的细胞器运输的一个基本机制。
2. 2. 3 黑色素沉积被巨噬细胞吞噬(后期消除)
巨噬细胞通过泛素蛋白酶体循环(UPS)调控皮肤黑色素细胞中控制黑色素合成的TYR的分解。对碳水修饰物的研究[22]已经表明内质网(ER)的TYR通过与内质网关联的蛋白质降解发生水解作用。内因子调节UPS和脂肪酸已经被证实通过调节,增加或减少酪氨酸可加速泛素酪氨酸酶水解,泛素酪氨酸酶又可以通过蛋白酶体进行加速或减速分解。
2. 3 黑色素的分解及代谢
黑色素排泄主要有2条途径:一是黑色素在皮肤内被分解、溶解和吸收后穿透基底膜,被真皮层的嗜黑色素细胞吞噬后,通过淋巴液带到淋巴结再经血液循环从肾脏排出体外;二是黑色素通过黑色素细胞树枝状突起,向角质形成细胞转移,然后随表皮细胞上行至角质层,随老化的角质细胞脱落而排出体外[23,24]。
2. 4 外在环境因素干预
皮肤色素沉着的外在调节主要受紫外线辐射的影响。色素沉着很大程度上是由于UVA,它使得黑色素的合成增加。在3~4 d紫外线辐射后,色素沉着延长,主要是由于UVA和UVB辐射,增加表皮黑色素的水平,黑色素生成保护皮肤[20]。一方面,紫外线辐射增加黑色素细胞增殖、树突数和黑素体转移,黑色素停留在角质形成细胞的细胞核上起保护作用,防止染色体受到光线辐射受损;另一方面,在角质形成细胞和黑色素细胞POMC表达肽中,MC1R和黑素酶增加。
2. 5 内在生理性因素调节
由于人口老龄化的增加,孤独、退休、健康问题和睡眠问题引起的压力变得越来越普遍。这些压力和睡眠不足会影响皮肤再生和皮肤状况,从而导致黑色素的生成。研究证实[4],压力和睡眠习惯都对面部皮肤状况有影响。因此,要正确地调节压力和睡眠,才能保持皮肤健康和活力。
另外,人正常表皮黑色素细胞中含有雌激素受体。在雌激素对其影响的研究中[28],TYR活性显示刺激了黑素酶。而雄性激素调节TYR活性,是皮肤色素沉着的关键调节因子。研究强调2种性激素在调节皮肤色素沉着的重要性,因为2种性激素都同时参与不同细胞因子的调控,引起皮肤色素沉着。
3 结论
综上所述,即使皮肤黑色素的机理研究已在多个方面取得显著进展,但在化疗药物的调控机制、糖基化路径和内质网中酪氨酸酶的研究等方面仍面临着巨大挑战。且市场大部分美白产品的研究仍相对较传统,在抑制黑色素细胞增殖分化方面的研究甚少。相信随着科技与研究的进步,黑色素机理通路等的研究会更加全面成熟,美白产品研究中的黑色素立体多途径复合干预,皮肤渗透技术等新思路也将会被广泛 应用。

