QuEChERS-高效液相色谱-串联质谱法同时测定有机肥料中10种氟喹诺酮类药物残留
赵 娜, 梁嘉诚, 时丽艳, 吕运开, 于丽青*
(1. 河北省产品质量监督检验研究院, 河北 石家庄 050091; 2. 河北大学化学与环境科学学院, 河北 保定 071000)
抗生素是一类化学物质,在低浓度下能杀灭或抑制其他微生物。大量研究表明,抗生素消耗增加会导致耐药细菌的出现和传播,导致抗生素治疗在人类和动物中失败[1]。鉴于抗生素耐药性的潜在危险,许多国家已经制定了限制使用这些药物的实用指南[2]。目前被广泛用于畜禽养殖业的抗生素按照化学结构可分为磺胺类、喹诺酮类、四环素类、氨基糖苷类、大环内酯类、β-内酰胺类等[3]。大部分抗生素在动物肠道中不能完全被机体吸收,约60%~90%的抗生素以其原形或者代谢产物被排泄到动物的粪便或尿液中[4]。这些动物排泄物与植物物质结合,可以人工发酵成有机肥料。在有机肥中,由于代谢物再转化为母体化合物,抗生素非常稳定,甚至含量增加。因此,兽药可以通过农业施用有机肥到达土壤环境,进一步影响土壤细菌群落的结构和功能[5,6]。此外,研究人员还指出,土壤中的兽药残留可以被蔬菜吸收,这可能对人类和动物造成潜在的健康风险。因此,建立一种同时检测多种兽药残留的方法,研究兽药在有机肥中的迁移机理,并获得更多的风险评估数据是很有必要的。
氟喹诺酮类药物(fluoroquinolones, FQs)具有广谱、高效、价格低廉,杀菌能力强、半衰期长等特点,已广泛用于动物和人类感染性疾病的预防和治疗[7,8]。不合理的用药导致药物原型或其代谢产物在粪便中残留,畜禽粪便经过发酵制成有机肥料施于农田土壤,氟喹诺酮进而被土壤植物和水生生物所吸收、富集,然后进入食物链,影响食品安全,最终将不同程度地被人类吸收,产生毒害作用[9]。目前,食品和环境基质(水、土壤和污水污泥)中兽药含量测定的分析方法已得到很好的发展[10-13]。然而,很少有人关注有机肥(粪肥)中兽药残留的分析。目前报道的有机肥样品中兽药残留的前处理方法主要包括液液萃取[14]和固相萃取[15-18]等,液液萃取法通常需大量的化学试剂,且操作复杂;固相萃取技术具有操作简单、价格低廉、易于自动化的优点,但常规的固相萃取吸附剂为非特异性吸附,吸附性和选择性较差,对复杂样品的净化和富集较难。
有机肥料的基质非常复杂,目标物易被干扰。因此,需要一种准确、高效和便捷的样品前处理方法将氟喹诺酮类药物从有机肥料中分离出来并富集检测。分散固相萃取样品前处理技术QuEChERS具有快速(quick)、简便(easy)、廉价(cheap)、有效(effective)、耐用(rugged)、安全(safe)等优点,此方法包含一个液液微萃取过程,可以除去那些会干扰色谱分析的基质成分。因此,QuEChERS技术具有净化有机肥料药物的潜力。近年来在兽药残留检测中应用日趋广泛[19,20]。
本文采用QuEChERS技术提取有机肥料样品,联用高效液相色谱-串联质谱(HPLC-MS/MS),实现了有机肥料中10种氟喹诺酮类药物残留的同时检测。该方法具有较高的准确度和精密度,可为定性和定量分析有机肥料中氟喹诺酮类药物提供一种准确、高效的检测方法,对市场上有机肥料的质量安全监管也具有较高的应用价值。
1 实验部分
1.1 仪器与试剂
高效液相色谱-质谱联用仪(美国Agilent公司);色谱柱Atlantis T3 C18色谱柱(250 mm×4.6 mm, 5 μm)(美国Agilent公司); HCT165离心机(湖南长沙易达仪器有限公司); CP214电子分析天平(奥豪斯仪器上海有限公司); SK-1快速混匀器(上海上登实验设备有限公司);氮吹仪(青岛海科仪器有限公司);真空冷冻干燥机(美国Virtis公司); 0.22 μm有机相滤膜(美国Pall公司)。
所有化学试剂无特殊说明外均为分析纯。乙腈(色谱纯)、磷酸氢二钠、磷酸二氢钠(天津市科密欧化学试剂有限公司);柠檬酸、柠檬酸钠、磷酸、乙二胺四乙酸二钠(Na2EDTA)(天津市恒兴化学试剂制造有限公司);无水硫酸镁(天津市光复精细化工研究所);甲酸(色谱纯)、氯化钠(天津市福晨化学试剂有限公司);西诺沙星(纯度≥99.9%)、氧氟沙星(纯度≥99.3%)、环丙沙星(纯度≥94.0%)、依诺沙星(纯度≥97.5%)、诺氟沙星(纯度≥99.1%)、沙拉沙星(纯度≥91.2%)、丹诺沙星(纯度≥94.0%)、洛美沙星(纯度≥99.4%)、二氟沙星(纯度≥96.1%)、恩氟沙星(纯度≥99.9%)、培氟沙星(纯度≥99.0%)(德国Dr. Ehrenstorfer公司)。
1.2 溶液的配制
Na2EDTA-Mcllvaine缓冲溶液(pH=4.0):准确称取34.6 g十二水合磷酸氢二钠、6.45 g柠檬酸和18.6 g乙二胺四乙酸二钠,置于烧杯内,加入400 mL超纯水,用玻璃棒不停地搅拌,用1 mol/L的氢氧化钠溶液调节pH值至4.0,转移至容量瓶,用超纯水定容至500 mL,即为0.1 mol/L的Na2EDTA-Mcllvaine缓冲溶液。
磷酸盐缓冲溶液(pH=7.2):称取12.8 g十二水合磷酸氢二钠和2.18 g二水合磷酸二氢钠,用超纯水溶解后稀释并定容至500 mL。
标准溶液的配制:分别称取20 mg 11种药物标准品,以0.2%(体积分数,下同)的甲酸水溶液做溶剂,配制11种药物的储备液(1 000 mg/L),储存在4 ℃的黑暗环境中。在实验前用0.2%甲酸水溶液逐级稀释储备液,得到工作溶液。分别精密吸取10 μL除内标物(西诺沙星)外的其他10种储备溶液,加入10 mL容量瓶中,用0.2%甲酸水溶液稀释、定容,即得质量浓度为1.0 mg/L的混合标准工作液。精密吸取10 μL 11种标准储备溶液,加入10 mL容量瓶中,用0.2%甲酸水溶液稀释至刻度,摇匀,即得质量浓度分别为1.0 mg/L的混合标准内标溶液,待用。
1.3 实验条件
1.3.1色谱条件
色谱柱:Atlantis T3 C18(250 mm×4.6 mm, 5 μm);柱温:40 ℃;进样量:5 μL;流速:0.5 mL/min;流动相:A为乙腈,B为0.2%甲酸水溶液;梯度洗脱程序见表1。

表 1 梯度洗脱程序Table 1 Gradient elution programTime/minφ(mobile phase A)/%φ(mobile phase B)/%0138751387104060134060151387251387 Mobile phase A: acetonitrile; mobile phase B: 0.2% (v/v) for-mic acid solution.
1.3.2质谱条件
离子源:电喷雾离子(ESI)源,正离子模式;离子源温度:150 ℃;检测方式:多反应监测模式(MRM);毛细管电压:3 500 V;喷雾压强:10.34 kPa;脱溶剂温度:350 ℃;脱溶剂气流量:3 L/min。10种兽药的其他质谱参数见表2。

表 2 10种氟喹诺酮类药物的质谱参数Table 2 Mass parameters of the ten fluoroquinolones
* Quantitative ion.tR: retention time.
1.4 样品预处理
将有机肥料样品冷冻干燥后粉碎,准确称取1.0 g,置于50 mL聚丙烯离心管中,加入5 mL Na2EDTA-Mcllvaine缓冲液(pH=4.0)和20 mL乙腈溶液,以2 000 r/min的速度涡旋混合,涡旋2 min后,加入1.0 g无水硫酸镁、0.5 g氯化钠、0.5 g柠檬酸钠,充分混匀,超声提取10 min后,以5 000 r/min的速度离心5 min,取5.0 mL上清液,于50 ℃氮吹至干。
加入0.5 mL流动相溶液(流动相A∶流动相B=4∶6, v/v),超声溶解,过0.22 μm滤膜后供高效液相色谱-质谱仪测定。
2 结果与讨论
2.1 样品提取时缓冲溶液的优化
本研究中测定的10种氟喹诺酮类药物均为酸碱两性化合物,在酸性或碱性条件下均可进行提取[16]。由于有机肥料基质的特殊性,在实验过程中如果直接向样品中加入乙腈提取溶液会使样品中氟喹诺酮类药物性质发生改变。因此,在加入乙腈提取溶液前可用缓冲溶液稀释,使之形成均相体系,以便目标化合物的提取。本试验对比了水和2种缓冲溶液(磷酸盐缓冲溶液和Na2EDTA-Mcllvaine缓冲溶液)在样品前处理时对目标化合物提取得到的色谱峰面积的影响,结果见表3。由表可知,Na2EDTA-Mcllvaine缓冲溶液提取样品时提取效率最高,得到的检测色谱峰面积最大,故选择Na2EDTA-Mcllvaine缓冲溶液(pH=4.0)作为样品提取时的缓冲溶液。

表 3 水和2种缓冲溶液提取的10种氟喹诺酮类 药物色谱峰面积Table 3 Peak areas of the ten fluoroquinolones extracted with water and two buffer solutions
2.2 色谱条件的优化
选择甲醇和乙腈作为流动相进行对比试验。结果显示:甲醇作为流动相时,组分色谱峰形易变宽,组分分离度低。而乙腈作为流动相时可明显改善酸碱化合物的峰形,流动相中加入甲酸可增强化合物的保留性,且色谱峰分离程度有所提高,故本试验选用乙腈和0.2%的甲酸水溶液作为流动相进行梯度洗脱。色谱条件优化后得到的10种氟喹诺酮类药物的色谱图见图1。
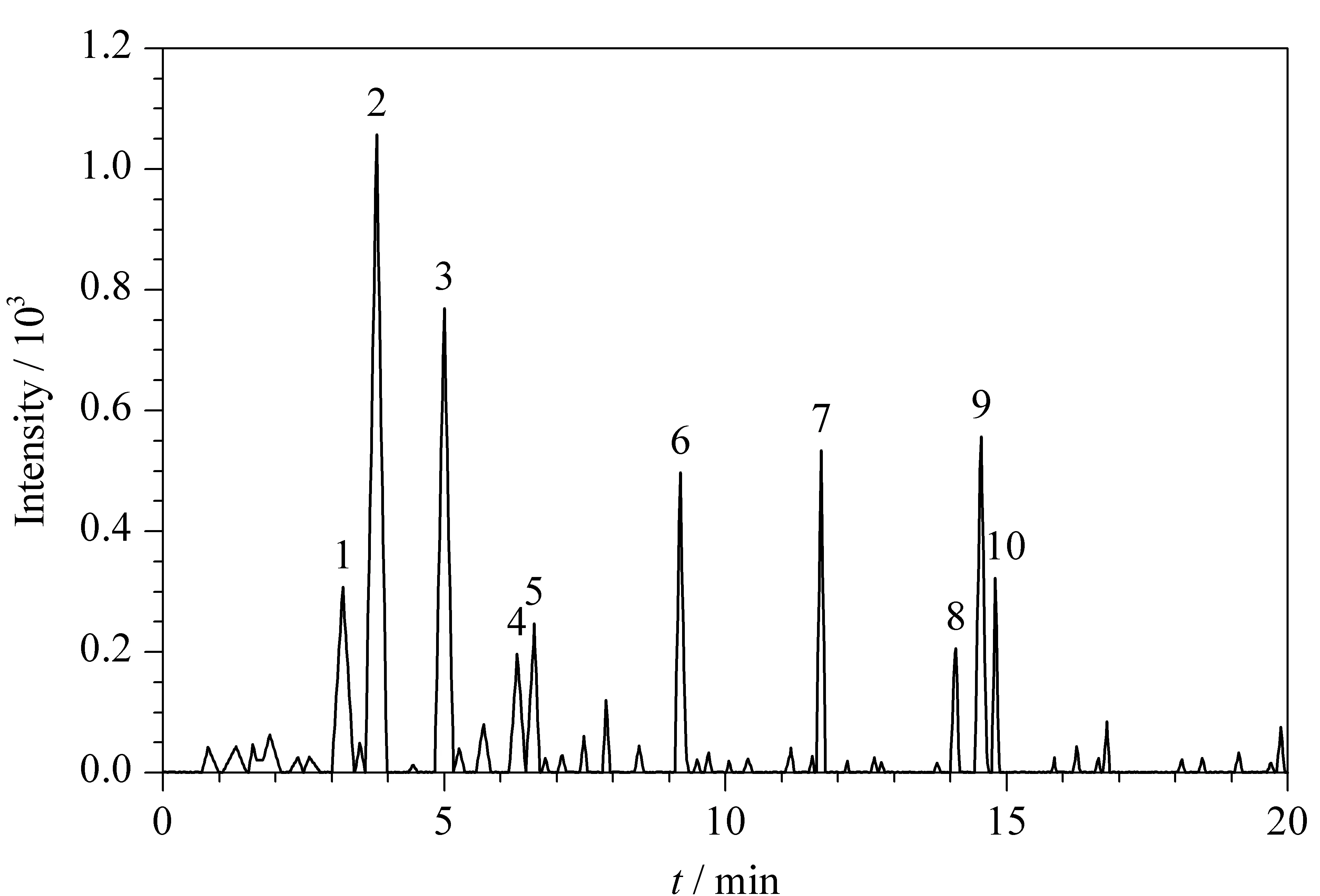
图 1 10种氟喹诺酮类药物标准溶液(300 μg/L)的色谱图Fig. 1 Chromatograms of the ten fluoroquinolone standard solutions (300 μg/L) Peak Nos. and retention times: 1. lomefloxacin hydrochloride, 3.2 min; 2. pefloxacin methanesulfonate, 3.8 min; 3. danofloxacin mesylate, 5.0 min; 4. ofloxacin, 6.3 min; 5. sarafloxacin hydrochloride, 6.6 min; 6. norfloxacin, 9.2 min; 7. enoxacin, 11.7 min; 8. difloxacin hydrochloride, 14.1 min; 9. enrofloxacin, 14.5 min; 10. ciprofloxacin hydrochloride, 14.8 min.
2.3 质谱条件的优化
氟喹诺酮类药物的分子结构中含有羧基和叔氨基,具有酸碱两性,在酸性溶液的条件下呈阳离子状态,在电喷雾正离子模式下,极易形成[M+H]+准分子离子。将所研究的10种氟喹诺酮类药物标准溶液分别单标进样,根据目标物的分子结构特征,采用一级质谱对目标物进行母离子全扫描,分析得到[M+H]+分子离子峰,然后二级质谱以分子离子为母离子。通过优化10种药物目标物的特征离子对、毛细管电压、雾化室温度、碰撞电压等质谱条件,选取相对丰度强、干扰小的离子对作为定性、定量离子。在进行MRM监测时选择信噪比最高的离子对进行检测,以提高质谱确证的准确性。
2.4 基质效应
基质效应是由基质中的共提干扰物与目标化合物竞争电离所致。通常会对目标化合物的灵敏度、准确度和分析方法的重现性等产生影响。根据基质标准曲线与溶剂标准曲线的斜率比值来评价基质效应,若比值在0.8~1.2范围内,则表明基质效应不明显。本文对10种氟喹诺酮类药物的基质效应进行了评价(见表4),可以看出,基质效应对各药物无明显影响。
2.5 方法学验证
2.5.1线性关系及检出限
将标准储备溶液逐级稀释,配制成质量浓度分别为20、50、100、200、300和500 μg/kg的混合标准溶液,在优化的色谱和质谱条件下进行分析。以各组分进样质量浓度(μg/kg)为横坐标、峰高为纵坐标绘制标准曲线,得线性方程(见表5)。由表可知,10种氟喹诺酮类药物的线性相关系数(r)均大于0.993 0,表明各目标物在相应的范围内线性关系良好。分别以3倍和10倍信噪比(S/N)确定检出限(LOD)和定量限(LOQ),分别为0.5~2.5 μg/kg和1.7~8.3 μg/kg。
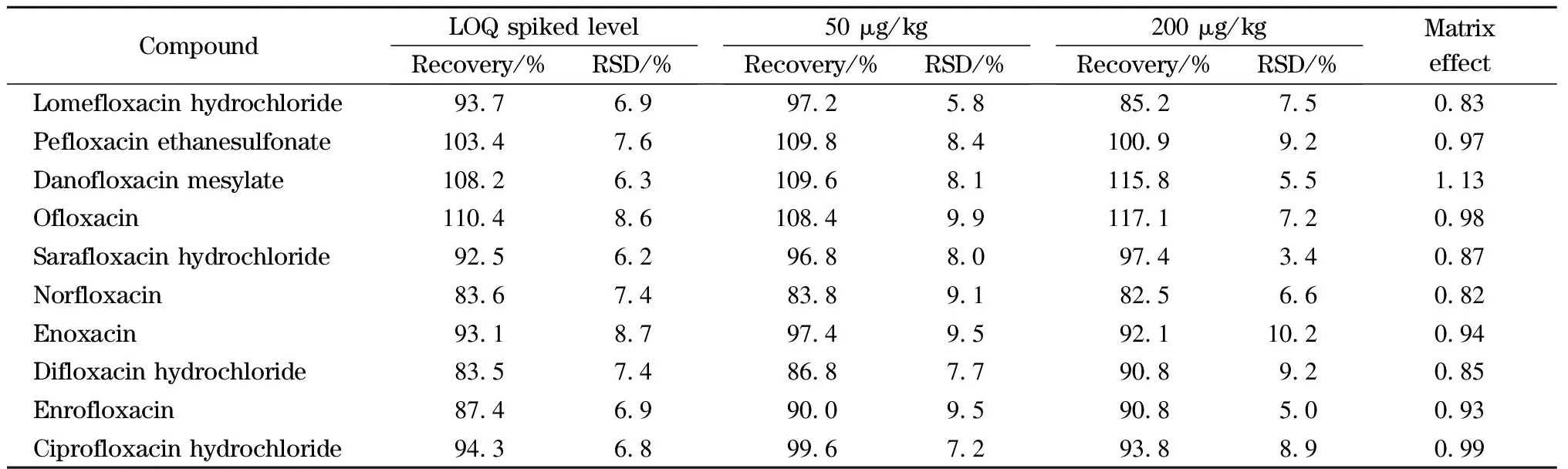
表 4 10种氟喹诺酮类药物的回收率和相对标准偏差(n=3)Table 4 Recoveries and RSDs of the ten fluoroquinolones (n=3)
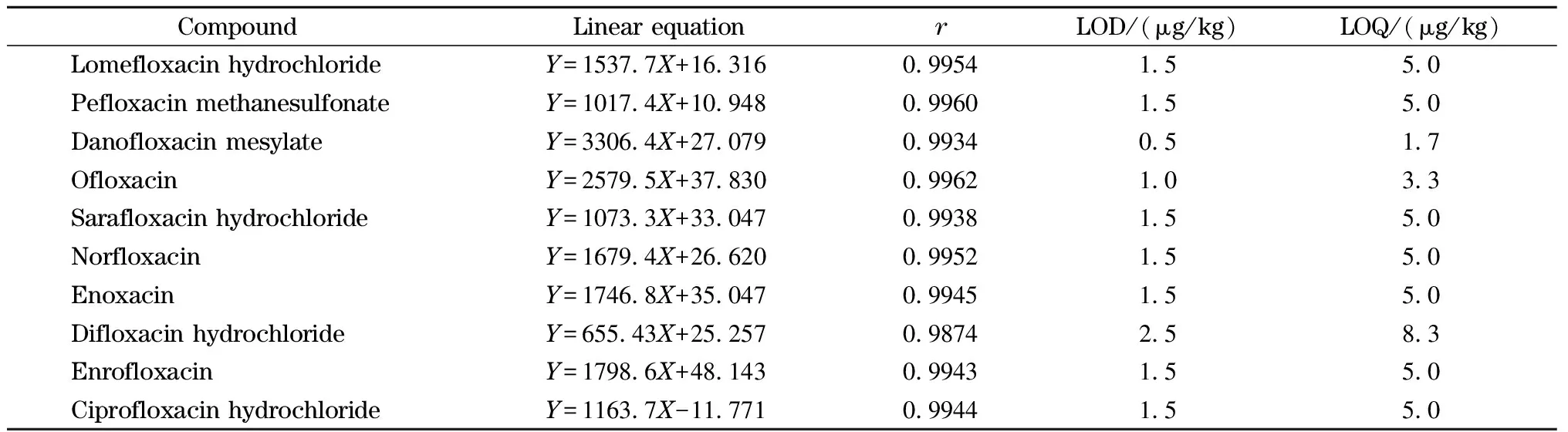
表 5 10种氟喹诺酮类药物的线性方程、相关系数、检出限和定量限Table 5 Linear equations, correlation coefficients (r), limits of detection (LODs) and limits of quantification (LOQs) of the ten fluoroquinolones
Y: peak height response value;X: mass concentration (μg/kg).
2.5.2方法回收率的确定
向有机肥料空白样品溶液中添加LOQ水平、50和200 μg/kg 3个水平的氟喹诺酮类药物混合标准溶液,每个浓度水平平行测定3次,以标准曲线定量,实验结果见表4。10种氟喹诺酮类药物的平均回收率为82.5%~117.1%,相对标准偏差为3.4%~10.2%,结果表明该方法有良好的重现性。
2.6 实际样品的测定
采用本研究建立的QuEChERS联用高效液相色谱-质谱测定方法,检测了市场上常见的9种有机肥料样品中的氟喹诺酮类药物残留浓度。测定结果(见表6)表明,市场上常见的有机肥料样品中药物残留主要为恩氟沙星、氧氟沙星、诺氟沙星和环丙沙星。这4种抗生素在有机肥料中普遍残留的质量浓度范围为63.0~1 368.4 μg/kg。为验证本方法的可靠性,对本方法中氟喹诺酮类药物的检出范围与文献[21]进行对比,发现两种方法的测定结果非常接近,表明本法适用于有机肥料中氟喹诺酮类药物残留的测定。
3 结论
本研究采用QuEChERS技术对有机肥料复杂基质样品进行前处理,有效降低了样品基质的干扰,并联用高效液相色谱-质谱技术,建立了可同时测定有机肥料中10种氟喹诺酮类药物残留的分析方法。该方法检测成本低、周期短、准确度高、重复性好、操作简单、快速,适用于有机肥料质量安全监测时大批量样品中氟喹诺酮类药物残留的筛查和确证。

