CO2熔盐电化学转化碳材料的电化学特性
谷雨星,杨 娟,汪的华
武汉大学资源与环境科学学院,湖北省资源与能源可持续利用技术示范型国际科技合作基地,武汉 430072
1 引言
传统水溶液中电化学还原CO2制备高能量密度燃料需较高的电势驱动,且为抑制析氢反应的发生和提高反应效率往往需要使用高活性、高选择性催化剂1。高温熔盐具有宽电化学窗口、良好的离子与热传导能力,高温下具有较快的反应动力学,副反应少,以其为媒介的电化学还原CO2过程是一种实现CO2捕集并同时制备高附加值碳材料和氧气的环保高效的方法2,3。该方法阴极所得产物多为表面富含含氧官能团的无定型碳材料4–8,前期研究和文献报道都表明,这类碳材料具有较优异的储能和化学吸附特性,可用作超级电容器电极材料3、锂离子电池负极材料9–11和污染物吸附材料3,12。目前,对该类碳材料的研究主要集中于制备条件和产物形貌调控13–17,而对其本征电化学性质方面的研究仍是空白。
粉末微电极(powder microelectrode)是由查全性等18建立的一种可用于研究微量粉体材料本征电化学特性的微(腔)电极技术,电极制备方法简单易操作,无需粘结剂、导电添加剂,具有用量少、极化小、抗外界干扰能力强等优点,已被成功地应用于电分析和电化学传感器19–21、催化剂与材料的储能特性及腐蚀性能测试等研究领域22–24。本文旨在通过采用粉末微电极循环伏安扫描技术,揭示在熔融三元碳酸盐(Li/Na/K2CO3)中不同温度及槽压下电化学还原CO2制备的碳材料(简称电解碳,Electrolytic-carbon,EC)所具备的独特电化学性质及其变化规律。
2 实验部分
2.1 试剂与仪器
试剂及材料:实验用 Li2CO3、Na2CO3、K2CO3、Na2SO4、(NH4)2SO4和四丁基高氯酸铵(Bu4NClO4)均为分析纯(≥ 99.0%),乙腈为色谱纯(≥ 99.8%),均购自国药集团化学试剂有限公司;实验用水为超纯水(电阻率> 18.2 MΩ·cm)。测试用多壁碳纳米管(MWCNTs)、石墨、乙炔黑(Acetylene black)购自阿拉丁试剂(上海)有限公司,还原氧化石墨烯(rGO)通过550 °C热还原Hummers法制备的氧化石墨(GO)制得。
仪器:金相显微图通过超景深三维显微镜VHX-5000 (日本基恩士)获得,循环伏安测试使用电化学工作站为CHI660E (上海辰华仪器公司)。
2.2 EC的制备及表征
EC的具体制备过程参考本课题组已发表的相关文献3,4,即在CO2气氛下,采用三元碳酸盐体系进行恒槽压电解制碳。体系中三元碳酸盐Li2CO3、Na2CO3、K2CO3的摩尔比为43.5 :31.5 :25。电解以SnO2棒(直径14 mm,长度20 cm)为阳极,镍片(长4 cm,宽3 cm)为阴极,通过改变电解槽压(3.5、4.5、5.5 V)和电解温度(450、550、650 °C)制备不同的EC。不同温度、不同槽压条件下制备的EC均为无定型碳材料,其形貌表征详见文献4,碳材料粒径范围为50 nm–2 μm,比表面积100–900 m2·g-1,氧含量测试采用X射线光电子能谱(XPS,Thermo Fisher),激发光源为Al-Kα。不同条件下制备 EC的比表面积及氧含量数据见表1 (比表面积数据来源于文献4)。
2.3 粉末微电极的制备及电化学测试
粉末微电极的制备方法参照文献18。将直径为100 μm的铂丝一端热封于玻璃管中,另一端用铜丝连接作为集流体引出;打磨电极端面制成铂微盘电极,然后将电极浸入微沸的王水中腐蚀,使铂溶解形成具有一定深度的微腔,制成空腔微电极(图 1c)。通过超景深三维显微镜测量,可知微腔直径为 100 μm,深度约为 77–78 μm (图 1d)。取适量制备的碳粉置于光滑的平板玻璃表面,以微电极研磨碳粉使其逐渐填满微腔,将所制得的电极用于后续电化学测试。制得的粉末微电极填充碳粉前后的光学照片如图 1a,b所示。以填充有碳粉的粉末微电极为工作电极,铂丝为对电极,饱和甘汞(SCE)电极作为参比电极,组成电化学测试体系,电解液选用阴、阳离子半径不同的Na2SO4、(NH4)2SO4和Na2S2O8溶液以及质子惰性电解质 Bu4NClO4-乙腈溶液,循环伏安(cyclic voltammetry,CV)测试扫描速率为 50 mV·s-1。图2为测试体系示意图,测试前体系通氮气除氧。

表1 不同EC的比表面积及氧含量Table1 Specific surface area and oxygen content of different EC.
3 结果与讨论
3.1 EC的电化学性质
图 3示出了几种典型碳材料和电解碳材料(450 °C-4.5 V-EC)在 10 mmol·L-1Na2SO4电解液中的循环伏安曲线。由图可见,几种通用碳材料在-0.6–0.6 V vs.SCE扫描电位区间内,CV曲线均接近于矩形,表现出明显的双电层电容特性,由负向正反扫时电流由充到放响应迅速。与之显著不同,在正向扫描阶段,450 °C-4.5 V-EC的CV曲线在-0.6 – -0.21 V范围内仍存在负向充电电流,表现出明显的“双电层充放电响应迟滞”现象。继续正向扫描,正向电流出现且迅速增大,随后出现明显的阳极电流峰。由于溶液中并无特殊的电活性反应粒子,这种特异行为只能由电解碳材料特殊的表面化学特性和/或其引起的特殊的界面反应特性所引起。

图1 粉末微电极填充碳粉前(a)、后(b)金相显微图,及微腔深度测量图(c),(d)Fig.1 Metallographic micrograph of powder microelectrode before (a) and after (b) filled with carbon,and the measurement of the microcavity depth (c),(d).

图2 粉末微电极及测试装置示意图Fig.2 The schematic diagram of the powder microelectrode and the experimental setup.

图3 不同碳材料CV测试对比Fig.3 Cyclic voltammogram of different carbon materials.
前期对450 °C-4.5 V-EC材料的研究表明,其表面含有较多的含氧官能团12。我们将450 °C-4.5 V-EC在550 °C 氩气气氛下热处理12 h,实现碳材料表面大部分酸性及中性含氧基团的脱除25。经XPS测试,450 °C-4.5 V-EC高温处理后的氧含量由最初的 16.3%降到 4.9%。处理后 450 °C-4.5 V-EC的CV测试如图4所示,其CV曲线与未处理的相比发生明显变化,扫描极化反向后 CV曲线没有明显的电流滞后及阳极电流峰出现,表现出普通碳材料的双电层电容性质。由此可见EC的这一电化学特性与其表面含氧官能团有密切的关系。
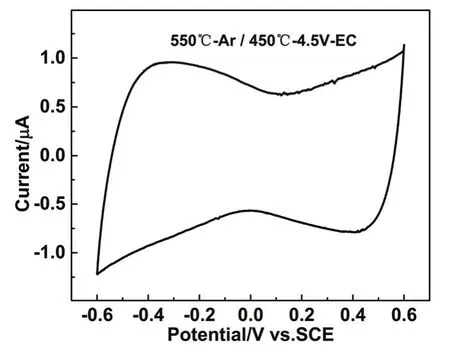
图4 550 °C 氩气气氛热处理12 h后450 °C-4.5 V-EC的CV曲线Fig.4 Cyclic voltammogram of 450 °C-4.5 V-EC after annealing at 550 °C under argon atmosphere.
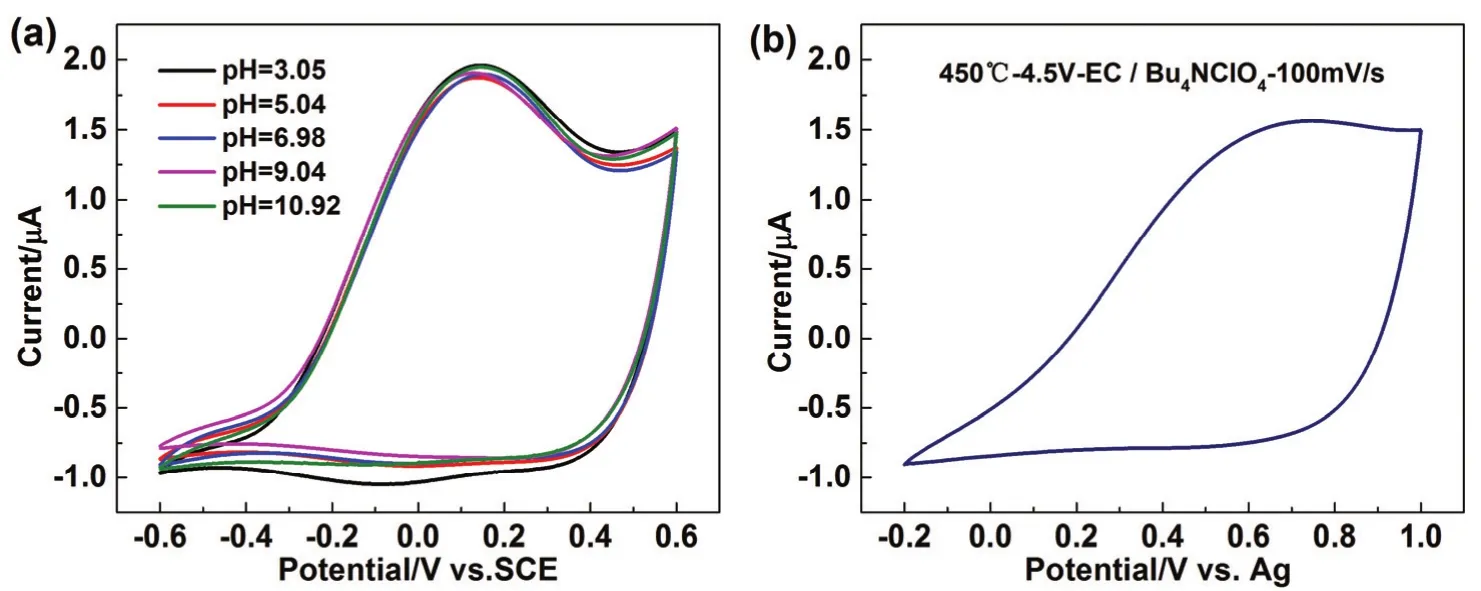
图5 450 °C-4.5 V-EC 在不同 pH 条件下(扫速:50 mV·s-1) (a)和 10 mmol·L-1 Bu4NClO4-乙腈电解液中(扫描速率:100 mV·s-1) (b)的CV 曲线Fig.5 Cyclic voltammograms of 450 °C-4.5 V-EC in different pH of 10 mmol·L-1 Na2SO4 aqueous solution at 50 mV·s-1 (a) and in 10 mmol·L-1 Bu4NClO4 at 100 mV·s-1 (b).
3.2 EC的电化学特性探究
一种可能的原因是这些含氧官能团具有一定的氧化还原活性,在水溶液电解液中发生有质子参加的氧化还原反应,故而实验测量了不同pH介质中的循环伏安曲线(图 5a)。由图可见,在不同pH条件下,450 °C-4.5 V-EC的特殊电化学性质表现基本不受影响,阳极峰的峰值电流大小不随pH的变化而变化。与其他具有含氧官能团如羧基、羰基等26,27的碳材料所表现出的有质子参与的官能团氧化反应过程明显不同。且如图5b所示,在质子惰性电解液中(10 mmol·L-1Bu4NClO4-乙腈),450 °C-4.5 V-EC特有的伏安曲线特征仍然存在。表明该充放电响应迟滞现象并非其表面含氧官能团氧化还原反应所致,而更可能与碳材料本身具有大量的酸性含氧官能团及其微纳米结构引起的界面过程有关。前期研究12表明,450 °C-4.5 V-EC材料的表面含氧官能团中有 86.6%为酸性基团—羧基,其pHPZC= 2.68,在较宽的pH范围内材料表面带负电。推测其与电解液中的阳离子存在比较强烈的特性相互作用,发生阳离子的特性吸附并且这一过程在动力学上比较缓慢,致使材料表现出不同的电容特性。为验证这种推测,考察了电位扫描速率的影响。如图6a所示,随着扫描速率的降低,正向扫描时电流为零对应的临界电位值逐渐负移,充放电迟滞现象明显减弱。当扫描速率低于10 mV·s-1时,CV曲线接近规则的矩形。这一现象表明,电解碳的特殊电化学性质与其独特的界面化学特性有关。扫描速率较快时,因材料存在对阳离子的特性吸附,在浓度较低的电解液中阳离子扩散速率受限,从-0.6 V开始正向扫描,前阶段因特性吸附EC表面阳离子脱附缓慢且吸附仍在继续;因此存在明显的负向充电电流。直到电位高于-0.21 V后阳极极化增强,电极表面荷正电,静电斥力作用使阳离子快速脱出产生正向电流并出现峰值(0.1 V处),图7给出了该过程中不同电位处碳材料表面离子的分布状态。而当扫描速率降低时,电位变化较缓慢,碳材料表面阴阳离子有足够的时间完成吸脱附交换,不会出现暂态条件下扫描速率反向后充电电流响应滞后的现象。提高电解质浓度(100 mmol·L-1Na2SO4),充放电响应迟滞现象消失(图 6b)。表明电解碳的电化学行为确与离子在其界面处缓慢特性吸脱附有关。值得指出的是,在低扫描速率或高电解质浓度的情况下,电流响应滞后现象弱化后,EC的双电层充放电曲线呈“棒槌”形。在较负的电位区间内双电层电容明显大于电位较正区域。因此,EC用作超级电容器电极材料时,作为负极材料其电容性能更优。

图6 450 °C-4.5 V-EC 在不同扫描速率(电解液:10 mmol·L-1 Na2SO4) (a)和扫描速率 50 mV·s-1、100 mmol·L-1 Na2SO4电解液中(b)的CV曲线Fig.6 Cyclic voltammograms of 450 °C-4.5 V-EC at different scan rate in 10 mmol·L-1 Na2SO4 aqueous solution (a) and at the scan rate of 50 mV·s-1 in 100 mmol·L-1 Na2SO4 aqueous solution (b).

图7 EC在不同极化状态下离子吸脱附示意图Fig.7 The schematic diagram of different ion distribution state on EC surface.
实验进一步研究了电解液中阴阳离子种类对该类碳材料 CV特性的影响,发现阴阳离子的变化都不改变其表观特征,但临界电位会受到阳离子半径大小的影响。图8a为 450 °C-4.5 V-EC在10 mmol·L-1(NH4)2SO4电解液中的CV测试曲线,可以看出,电流为零对应的临界电位负移到了-0.32 V。与Na+相比,半径较大28,EC对其的吸附作用力较弱,在极化反向时离子脱出较快致使临界电位出现明显负移。当改变电解液中阴离子组成时,如图8b,EC的电化学特性基本不受影响,且正向扫描临界电位不变。由此说明,静电作用下阳离子在 EC的孔道内存在特性吸附造成测试过程中阴阳离子交替缓慢,且这一过程与阳离子的种类有关。
综上,EC的电化学特性与其表面存在大量含氧官能团所引起的特殊界面性质有密切的联系,而不同的制备条件直接影响了 EC的形貌及氧含量。因此我们对不同制备条件下得到的EC的电化学特性进行了进一步探讨。
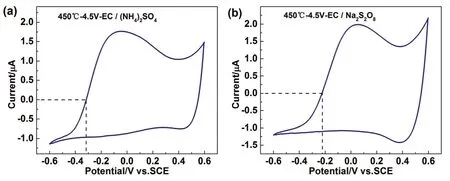
图8 450 °C-4.5 V-EC 在 10 mmol·L-1 (NH4)2SO4 电解液(a)和 10 mmol·L-1 Na2S2O8 电解液(b)中的 CV 曲线Fig.8 Cyclic voltammogram of 450 °C-4.5 V-EC in 10 mmol·L-1 (NH4)2SO4 (a) and 10 mmol·L-1 Na2S2O8 aqueous solution (b).
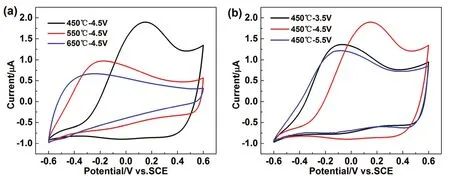
图9 不同熔盐温度下制备的EC的CV曲线(a);450 °C不同槽压下制备的EC的CV曲线(b)Fig.9 Cyclic voltammograms of EC synthesized at different electrolysis temperature (a) and different cell voltages (b).
3.3 电解制备条件对EC电化学特性的影响
3.3.1 熔盐温度对EC电化学特性的影响
在电解槽压为4.5 V的条件下,对在450、550和650 °C熔盐温度下制备的三种EC的电化学特性进行了探讨。由图9a可以看出,在450 °C下制备的碳材料的阳离子脱附峰电流最大。而随着电解温度的升高,制备的碳材料的充放电滞后现象减弱。这与制得的碳材料的比表面积及含氧量有关,结合表1数据和形貌研究结果4,当熔盐温度升高时,碳材料的主要形貌由颗粒状转为尺寸较大的片状,比表面积下降,同时在制备过程中熔盐温度的升高在一定程度上可实现含氧官能团的去除,使得所制备碳材料含氧量下降。综合两方面影响,熔盐温度升高,碳材料对阳离子特性吸附能力减弱,CV曲线所表现出的充放电滞后现象减弱。
3.3.2 电解槽压对EC电化学特性的影响
在相同的电解温度下,对不同电解槽压(3.5、4.5、5.5 V)制备的EC进行CV测试(图9b),由图可知不同槽压下制备的碳材料均表现出类似的电化学特性。在3.5 V槽压下制备的碳材料虽然氧含量高达17.5%,但其比表面积小于4.5 V制备的碳材料,因此特性吸附能力略小。而当电解槽压过高时(5.5 V),熔盐分解产生的碱金属会沉积到碳粉表面,在碳自下而上的生长过程中会使碳粉的结构细微化,使其比表面积增大(868.3 cm2·g-1),但同时其含氧量降低,仅为 14.0%,所以在测试过程中,正向扫描充电电流迟滞现象有所减弱,进一步说明了 EC所具有的独特电化学性质与碳材料本身的比表面积及氧含量的综合效应有关。
4 结论
本文采用粉末微电极循环伏安测试揭示了熔盐电化学还原CO2制备碳材料与其他碳材料所不同的电化学特性,探讨了不同熔盐温度及电解槽压下制备的碳材料存在的电化学特性规律。研究表明,EC表现出的双电层充放电响应迟滞现象是其本征存在的特殊界面性质,与材料的比表面积和较高的含氧量及其对阳离子的特性吸附有关。不同条件制备的电解碳中,较大的比表面积和较高的含氧量均有利于EC对阳离子的特性吸附,表现出更明显的充放电迟滞现象,EC在电位较负区域双电层电容较高。对EC这一独特电化学性质的认识对其后续在储能或电吸附等领域的应用具有一定的指导意义。

