袖状胃切除术治疗BMI≥100 kg/m2肥胖症患者1例报告
山东大学齐鲁医院 刘少壮,刘 腾,王 超,齐 峰,陈宁远,陈晓梅,翟永华,胡三元
肥胖症是由多种原因引起的体内脂肪堆积过多或分布异常导致体重增加,其危害主要在于并发的糖尿病、高血压、睡眠呼吸暂停综合征、多囊卵巢综合征、骨关节炎等。肥胖症早于1948年即被世界卫生组织列入疾病分类名单,是世界卫生组织确定的十大慢性疾病之一。肥胖症主要通过体重指数(body mass index,BMI)诊断,目前我国约有9 000万肥胖症患者,是世界第一肥胖症大国。减重代谢手术是目前唯一可有效减轻体重并长期维持减重效果的减重方式。目前全球每年开展减重代谢手术近70万例,其中袖状胃切除术(sleeve gastrectomy,SG)、Roux-en-Y式胃旁路术(Roux-en-Y gastric bypass,RYGB)是开展最广泛的两种术式[1]。BMI≥100 kg/m2的肥胖症患者极为少见,行减重代谢手术治疗的经验鲜有详细报道。山东大学齐鲁医院于2006年12月开展了首例腹腔镜SG[2],至今积累了丰富的治疗经验。近日,我院收治了一例体重334 kg,BMI高达102.07 kg/m2的超级肥胖症患者,顺利施行了腹腔镜SG。根据文献检索及媒体报道查阅,此患者是目前我国体重、BMI均最大的肥胖症患者,现将其诊疗经过报道如下。患者男,19岁,因“进行性体重增加19年”于2018年5月22日就诊于山东大学齐鲁医院。患者出生体重4 kg,体重进行性增加,4岁时体重40 kg,8岁时145 kg(身高不详),饮食均衡,饭量为同龄人的2~4倍。曾于体校进行“柔道”、“摔跤”等专业训练6年,运动强度大,饮食较均衡,但体重仍进行性增加。2年前体重增至210 kg并停止训练,后生活不规律,饮食不规律,运动量少,睡眠昼夜倒置,体重迅速达300 kg以上(具体不详)。曾尝试口服代餐减重,体重短暂下降后反弹。平时多汗、怕热,活动后出现气促、憋喘,运动能力降低。睡眠时打鼾,鼾声大,白天嗜睡,否认晨起头痛、记忆力下降等。吸烟史2年,10支/d。否认饮酒等不良嗜好。父亲BMI 30 kg/m2,合并高血压。家庭经济情况较差。查体:心率99次/min,血压150/87 mmHg,体重334.4 kg,身高181 cm,BMI 102.07 kg/m2,上臂围62 cm,大腿围105 cm,胸围205 cm,腰围212 cm,臀围223 cm,颈围64 cm,腰/臀1.05。颈粗短,颈背部、腋窝、乳下、下腹部、腹股沟、会阴部、手指背部等位置可见黑色色素沉积,部分角化过度。腋窝及会阴处体毛较少,外生殖器不可见。足底皴裂,少量出血。匹兹堡睡眠质量评分:6分;Epworth嗜睡程度量表评分:4分;SCL-90症状自评量表:总分131,阳性项目:26,阳性症状平均分2.17;康奈尔医学指数量表总分41,M-R值:17。患者于2018年5月28日入院后完善各项辅助检查,明确诊断。辅助检查结果:(1)睡眠呼吸监测:AHI 55.4/h,最低SpO247%,符合重度阻塞性睡眠呼吸暂停低通气综合征;(2)动脉血气分析:pH 7.36,pCO251 mmHg,pO262 mmHg,sO292.08%;(3)心脏彩超:左心室射血分数0.67,左室肥厚,左房扩大;(4)肺功能:中度混合性通气功能障碍;(5)血液学检查:甘油三酯2.10 mmol/L,尿酸450 μmol/L,维生素B147.86 nmol/L,维生素C 32.13 μmol/L,泌乳素25.79 ng/mL,雌二醇79.79 pg/mL,睾酮0.59 ng/mL,糖化血红蛋白5.9%,空腹胰岛素42.98 μIU/mL,空腹C肽4.45 ng/mL。诊断:(1)病态肥胖症;(2)2型呼吸衰竭;(3)重度睡眠呼吸暂停低通气综合征;(4)混合性通气功能障碍;(5)代谢综合征;(6)性激素紊乱;(7)心肌病变(心肌肥厚、房室扩大);(8)高尿酸血症;(9)维生素缺乏(B1);(10)黑棘皮病;(11)腰痛;(12)足底皴裂。多学科会诊明确诊断并确定先行术前减重、改善心肺功能。术前治疗方案包括:(1)术前减重,包括饮食调整、利尿;(2)戒烟,配合雾化、化痰药物治疗;(3)夜间佩戴睡眠呼吸机治疗;(4)加强手术宣教、心理疏导。经积极术前治疗,患者1个月后体重下降24 kg,于2018年7月6日再次入院。肺通气功能检查示:轻度阻塞性通气功能障碍,动脉血气分析:pH 7.38,pCO250 mmHg,pO259 mmHg,sO291.80%,无显著改善。经多科学会诊评估,意见为:符合减重手术指征,但手术风险大。经与患者、家属充分沟通,在律师见证下签署手术知情同意书,决定行腹腔镜SG。于2018年7月11日施术,器械准备:MAQUET手术台,承重450 kg;准备普通腔镜器械(33 cm)、加长器械(43 cm)、超长器械(50 cm),普通Trocar(9.8 cm)、加长Trocar(15 cm)、超长Trocar(20 cm),普通气腹针(12 cm)、加长气腹针(20 cm)(图1);加长超声刀,切割闭合器。患者入室后开通静脉通路,接心电监护。头、肩、背部垫高,保持胸骨上凹与外耳道于同一水平。应用丁卡因进行表面麻醉,尝试清醒插管失败后选择诱导麻醉。依次应用咪达唑仑、依托咪酯、丙泊酚、罗库溴铵、舒芬太尼,常规快速诱导喉镜监视下气管插管(ID7.5)成功,接麻醉机机械通气。超声引导下右颈部深静脉置管输液,右桡动脉穿刺行动脉压检测。双侧肋腹部加做神经肌肉阻滞。术中根据呼气末二氧化碳值、气道压力等调整麻醉机参数,并持续微量泵注射罗库溴铵,保证肌松效果,根据情况调整泵入速度。麻醉成功后,患者取水平仰卧、大字位。四肢固定、足底置挡板、双侧腰部置腰桥,防止患者体位调整时滑落。脐内侧做2 mm切口,穿刺特制25 cm Veress针,充入CO2建立气腹,压力维持在16 mmHg。脐上缘内侧做10 mm切口,穿刺20 cm超长10 mm Trocar,置入腹腔镜,在腹腔镜监视下于右锁骨中线脐水平上5 cm处穿刺13.5 mm Trocar为主操作孔,右腋前线肋缘下2 cm、左锁骨中线脐水平线上5 cm、右腋前线肋缘下2 cm穿刺25 cm超长5 mm Trocar作为辅助操作孔,置入特制加长腹腔镜操作器械。探查后见腹腔内脂肪堆积,腹腔内空间狭小,脏器显露不佳。遂决定使用悬吊装置提升腹壁,增加腹腔内空间。于剑突下5 cm水平穿刺直径2 mm克氏针,连接腹壁悬吊装置提拉腹壁,固定于悬吊架(图2)。悬吊腹壁后,腹腔内空间显著增加(图3)。首先显露幽门,距幽门约4 cm处于胃大弯血管弓内侧游离,打开大网膜至胃后间隙。沿血管弓内侧游离胃大弯,上至His角,显露左侧膈肌脚,将胃大弯侧及胃底完全游离。游离完毕后经口置入36F引导管,引导管头通过幽门至十二指肠。在引导管标记下使用直线型切割吻合器距幽门4 cm处开始切除胃大弯侧胃窦、胃体、胃底,共计使用11枚钉仓。切缘全层连续缝合加固(图4)。检查腹腔内无活动性出血,于脾窝、胃后放置22号引流管一根,将切除胃组织自主操作孔取出。撤器械及气腹,逐一缝合关闭各切口,结束手术。手术极其困难,手术时间6小时50分钟。术毕患者转入ICU,持续咪达唑仑、丙泊酚、舒芬太尼镇静、镇痛,口插管接呼吸机辅助通气,由IPPV模式改为CPAP模式,持续左侧桡动脉有创血压监测平稳。术后6 h患者苏醒,术后第1天晨8点查血气分析结果可,9点充分吸痰后脱机,半小时后复查血气可,于10点拔除气管插管,予以经鼻高流量吸氧、无创呼吸机、抑酸、补液、抗凝等治疗。术后第4天转回外科病房,拔除胃管、腹腔引流管,白天低流量吸氧,增加活动量,夜间无创呼吸机辅助通气。术后第9天心率、氧饱和度、动脉血气等各项指标恢复至术前水平,流质饮食总量超过3 000 mL,无不适,准予出院。出院后继续应用呼吸机治疗,加强饮食、运动指导。体重、BMI等变化见表1。辅助检查结果如下:(1)腹部超声:胆囊泥沙样结石;(2)肺功能:轻度阻塞性通气功能障碍;(3)血液学检查:甘油三酯1.98 mmol/L,尿酸598 μmol/L,维生素B147.86 nmol/L,维生素D 28.98 μmol/L,泌乳素18.04 ng/mL,雌二醇59.26 pg/mL,睾酮0.77 ng/mL,糖化血红蛋白5.2%,空腹胰岛素32.60 uIU/mL,空腹C肽3.81 ng/mL。
表1 患者手术前后体重等指标的变化
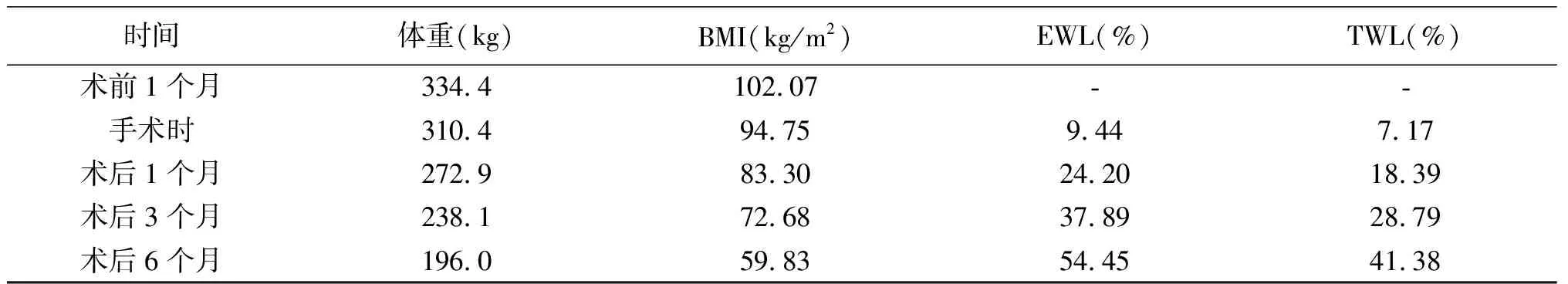
时间体重(kg)BMI(kg/m2)EWL(%)TWL(%)术前1个月334.4102.07--手术时310.494.759.447.17术后1个月272.983.3024.2018.39术后3个月238.172.6837.8928.79术后6个月196.059.8354.4541.38
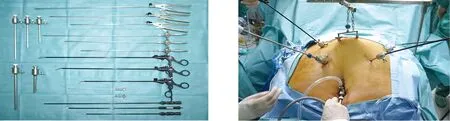
图1 所用器械 图2 Trocar位置及腹壁悬吊

图3 腹壁悬吊前(A)较腹壁悬吊后(B)空间小
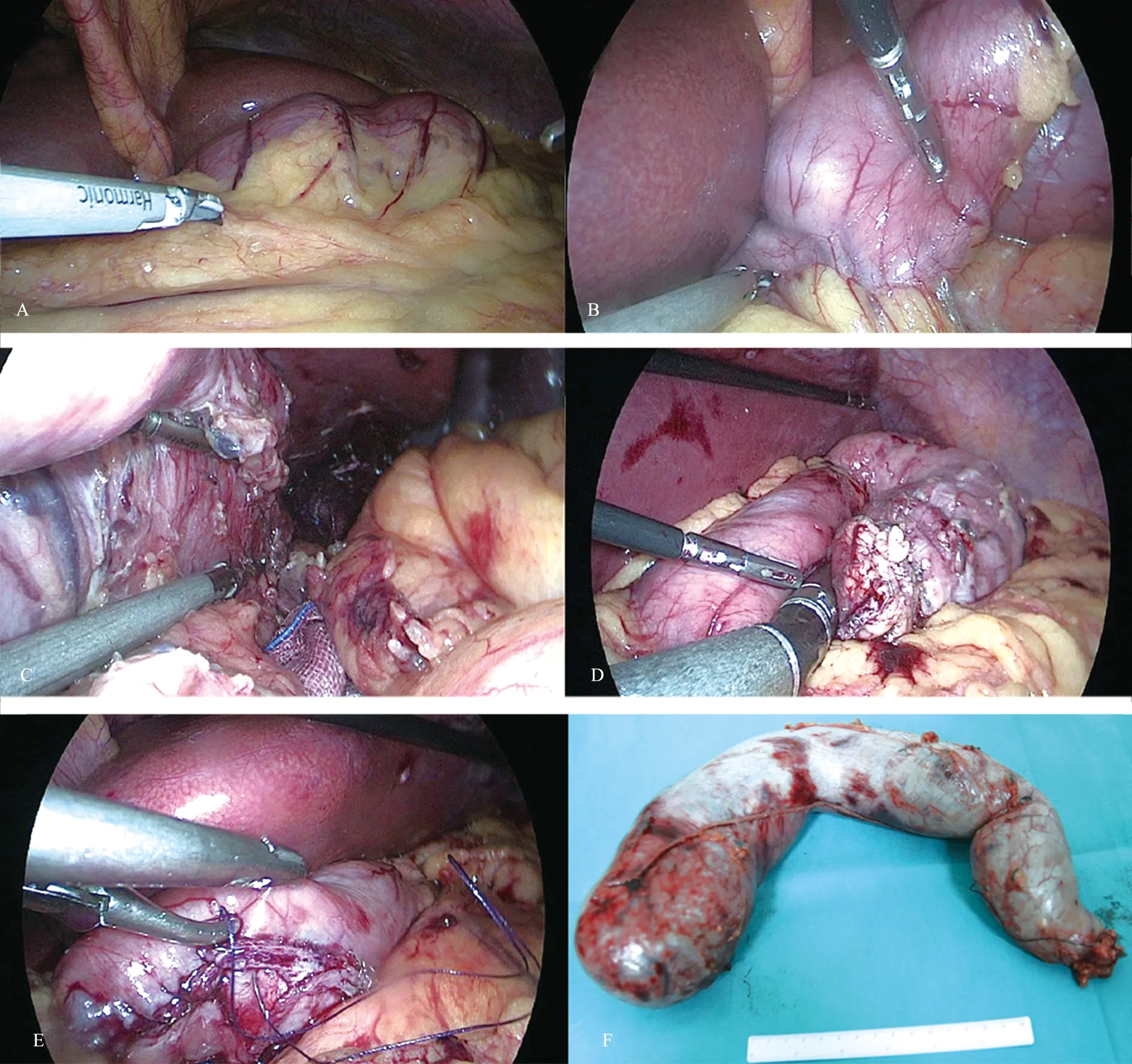
图4 手术步骤(A:探查;B:游离至幽门上2 cm;C:游离胃底,显露膈肌角;D:切割闭合;E:可吸收线连续全层加缝;F:切除的胃标本)
讨 论 目前,BMI仍是肥胖症诊断与分级的主要参考指标。根据现有诊断标准,BMI≥40 kg/m2确定为3度肥胖。根据文献报道,通常将BMI≥50 kg/m2称为超级肥胖,文献将BMI≥60 kg/m2称为超超级肥胖,甚至将BMI≥70 kg/m2称为三超肥胖[3]。目前尚无BMI≥100 kg/m2患者行减重代谢手术的详细报道。本文报道的病例BMI为102.6 kg/m2,是目前国内报道的行代谢手术BMI最大的肥胖症患者。文献报道BMI最大为107.8 kg/m2[4],新闻报道中也有500 kg患者接受减重代谢手术的案例,但均未见详细的病例报道。因此,本文是国际上首例BMI≥100 kg/m2的肥胖症患者接受减重代谢手术的详细报道,对极端肥胖患者的围手术期、手术处理具有重要的借鉴意义。
肥胖症患者术前评估的常规检查包括胸部CT或正侧位X线、腹部MRI或超声、垂体MRI、肺通气功能、心脏彩超、体脂分析等。但目前多数医疗仪器设备研发、设计、参数设置并未将超级肥胖患者考虑在内。因此,在超级肥胖患者的术前评估过程中,经常遇到检查床无法承重、X线无法穿透、超声探及不清等尴尬情况,似乎回到了上世纪七、八十年代。在本例患者的术前评估过程中,曾一度出现X线机器过载的情况。CT、MRI均无法检查,心脏彩超、腹部彩超仅能以清晰度有限的影像进行粗略评估,肺功能检查结果只能以最高设置体重参数(250 kg)进行评估。经粗略评估,本例患者存在重度睡眠呼吸暂停低通气综合征、2型呼吸衰竭与心脏结构变化(心肌肥厚、房室扩大)等严重并发症。由于缺乏准确的术前评估,客观上增加了此例患者的治疗风险。经过第一次多学科讨论,考虑患者年轻、心肺功能尚可满足日常活动,虽然风险极大,但可在积极术前准备后进行手术。
关于术前减重对减重代谢手术患者益处的研究较多,但结论并不统一。低卡路里饮食(1 000~1 200 kcal/d)或极低卡路里饮食(800 kcal/d)是许多减重代谢手术中心常用的术前减重方案,此方案已被证实可减少5%~20%的肝脏体积[5],并被认为可降低手术操作难度[6]。但在不同的系统回顾研究中,术前减重对缩短手术时间、减少围手术期并发症、增强减重效果的结果不统一[5]。术前减重效果好的患者,倾向于获得更佳的长期减重效果,这可能与术后随访率较高有关[7]。结合临床工作经验,笔者认为,术前减重的主要目的是改善患者的心肺功能,降低全身炎症、水肿状态。因此,对于BMI<50 kg/m2、无严重并发症(心肺功能衰竭、重度睡眠呼吸暂停低通气综合征等)的肥胖症患者,术前减重并非必须的步骤。而对于超级肥胖患者,尤其合并严重并发症时,术前减重有助于改善患者的心肺功能,从而降低围手术期心肺并发症。本例患者合并2型呼衰、重度阻塞性睡眠呼吸暂停低通气综合征、下腹部与双下肢严重水肿,因此,术前减重是必要的。术前予以高蛋白高纤维素低热量饮食、多饮水、利尿、无创呼吸机等治疗。需要重点说明的是,无创呼吸机治疗(CPAP或Bi-PAP)是改善睡眠呼吸暂停低通气综合征的重要措施,不但可改善患者肺部通气换气功能,纠正全身组织缺氧状态,还具有一定的减重作用。经过一个月,患者减重24 kg,水肿症状显著减轻,睡眠质量改善,肺功能由术前的重度变为中度通气功能障碍。
由于减重代谢外科在我国的发展仍比较缓慢,目前我国开展减重代谢手术的医院少有配备专门用于减重代谢手术的手术床。对于超级肥胖患者,手术床的承重、患者的固定、体位调整等均是对手术室硬件的巨大考验。本例患者使用的是Maquet手术床,承重450 kg,可自动调整体位。为保证手术安全,术前请患者到手术室进行了手术转运、固定、术中体位调整等演练,不但成功确定了术中转运、固定等方案,还减轻了患者因手术室陌生环境、手术等产生的焦虑,为手术成功、术后顺利恢复提供了有力保证。
超级肥胖患者的麻醉与气道管理是对麻醉医生的重大挑战,应在麻醉诱导前做好准备与处理预案。气管内插管是肥胖症患者的麻醉标准,采用特定的直接喉镜可降低肥胖症患者气管插管的难度。本例患者尝试清醒插管失败后,采用快速诱导喉镜监视下气管插管。超级肥胖患者容易发生困难面罩通气与困难气管插管,因此清醒气管插管是常用的选择之一。由于本例患者难以配合,麻醉团队遂改行快速诱导气管内插管。为保证紧急气道出现、插管不成功情况下患者的安全,麻醉团队准备了新型肌肉松弛药拮抗剂(舒更葡糖钠注射液)。此外,神经肌肉阻滞可在不增加气腹压力的情况下改善手术条件,建议常规应用于超级肥胖症患者。因麻醉用药量较大、脂肪内蓄积多、代谢时间慢,超级肥胖患者术后多需转运至ICU进行复苏。建议患者完全苏醒后、自主呼吸状态持续血气分析中PaCO2、PaO2达到术前水平时拔除气管插管,拔管序贯Bi-PAP治疗。建议超级肥胖患者接受减重代谢手术后夜间继续无创呼吸机治疗1~3个月,促进CO2排出、提高氧饱和度是气管插管拔除后治疗的关键。本例患者术后第1天上午顺利拔除气管插管,我们予以及早下床活动、睡眠时无创呼吸机、清醒时低流量吸氧(2 L/min)等措施促进CO2的排出,提高氧饱和度,患者术后恢复顺利,第4天转回普通病房。
SG与RYGB是目前开展最广泛的减重代谢手术。SG最早用于超级肥胖患者的一期手术,后作为独立的减重代谢手术在全球范围内广泛应用。本手术团队于2006年12月开展了国内首例腹腔镜SG,我们也为本例患者成功施行SG。对SG治疗病态肥胖、超级肥胖、超超级肥胖的比较结果显示,虽然体重越大,手术减重效果越差,但手术治疗肥胖合并症的效果并无差异[8]。此外,对于超级肥胖患者,SG与RYGB的减重效果无显著差别[9]。对本例患者的持续随访发现,患者减重效果良好,术后6个月EWL%为53.08,显著高于文献报道[9]。
由于本例患者体重巨大、腹壁厚重,术中使用14~16 mmHg气腹难以将腹壁鼓起,加之患者肝脏体积与重量巨大、腹腔内脂肪堆积、水肿严重,患者腹腔空间显露极差,无法进行手术操作。随后手术团队采用了腹壁悬吊的方法,显著增加了腹腔空间、改善了手术野。经检索,这是在国际范围内腹壁悬吊加气腹用于SG的首次报道。笔者在后来超级肥胖患者的减重手术中多次应用此方法,证实是安全、可行的。
综上所述,SG治疗BMI>100 kg/m2极端肥胖患者是安全、有效的。术前心肺功能改善、手术方案设计与实施、麻醉与术后复苏、术后持续宣教及随访是保证治疗安全、取得良好减重效果的关键,对于此类患者的治疗,国内外均缺乏相应的临床经验,本例患者的治疗经验也需要进一步的临床验证。

