基于风险管理设计临床生物化学酶类检测项目质量控制策略*
孔丽蕊,王华丽,吴 风
(成都市郫都区中医医院检验科,成都 611730)
目前,实验室质量控制(quality control,QC)仅仅是把重点放在分析仪器上,就好像把检测系统作为实验室的病人一样,已不再令人满意。自从发表了ISO15189[1]和CLSI EP23[2]等风险管理指南后,实验室现今设计的QC策略将更加关注患者。本研究基于风险管理,应用Sigma-SQC诺曼图,设计日立7180生化分析仪临床生物化学酶类检测项目的质量控制策略,最大程度地降低患者风险。
1 材料与方法
1.1 材料 生物化学酶类检测项目丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、谷氨酰转肽酶(GGT)、碱性磷酸酶(ALP)、肌酸激酶(CK)、淀粉酶(AMY)和乳酸脱氢酶(LDH)检测仪器为日立7180全自动生化分析仪,试剂和校准品由四川迈克公式提供,室内质控为伯乐公司(BIO-RAD) 提供的干粉生化多项质控品,2个水平( 批号分别为45772,45773)。
1.2 方法
1.2.1 确定分析质量要求:本研究中的酶类检测项目临床允许分析总误差(allowable total error,TEa)参照WS/T 403-2012临床生物化学检验常规项目分析质量要求[3]。
1.2.2 确定分析方法性能:不精密度源于成都市郫都区中医医院检验科2017年1~12月累计的标准差(s)和变异系数(CV)。偏倚(Bias)源于2017年四川省临床检验中心室间质量评价结果,共10份测定样本,计算项目偏倚绝对值的平均值。
1.2.3 计算Sigma度量值:Sigma=(TEa%-Bias%)/CV%。
1.2.4 Sigma-SQC诺曼图:见图1。定义候选质量控制策略。
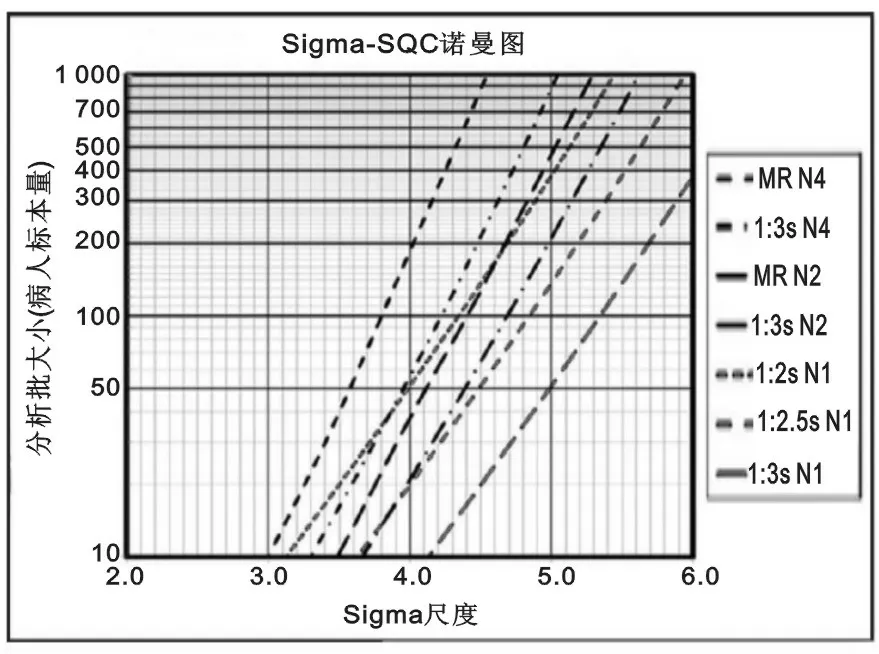
注:X轴代表Sigma度量值,虚线代表不同的SQC程序;Sigma度量值作垂直线与SQC程序线交叉点确定质控规则和质控测定的个数;交叉点对应Y轴上的值即样本分析批长度或质控频率。
图1 Sigma-SQC诺曼图
1.2.5 Sigma-SQC诺曼图的规则:①MR N4:13s/22s/R4s/41s多规则,每次测定质控4次,误差检出概率(Ped)为1.00,假失控概率(Pfr)为0.03;②13sN4:13s单规则,每次测定质控4次,Ped 为0.98,Pfr为0.01;③MR N2:13s/22s/R4s多规则,每次测定质控2次,Ped为0.94,Pfr为0.01;④13sN2:13s单规则,每次测定质控2次,Ped为0.85,Pfr为0.00;⑤12sN1:12s单规则,每次测定质控1次,Ped为0.90,Pfr为0.05;⑥12.5s N1:12.5s单规则,每次测定质控1次,Ped为0.82,Pfr为0.01;⑦13sN1:13s单规则,每次测定质控1次,Ped为0.66,Pfr为0.00。
2 结果
2.1 临床生物化学酶类检测项目的Sigma度量值 见表1。
表1临床生物化学酶类检测项目的Sigma度量值
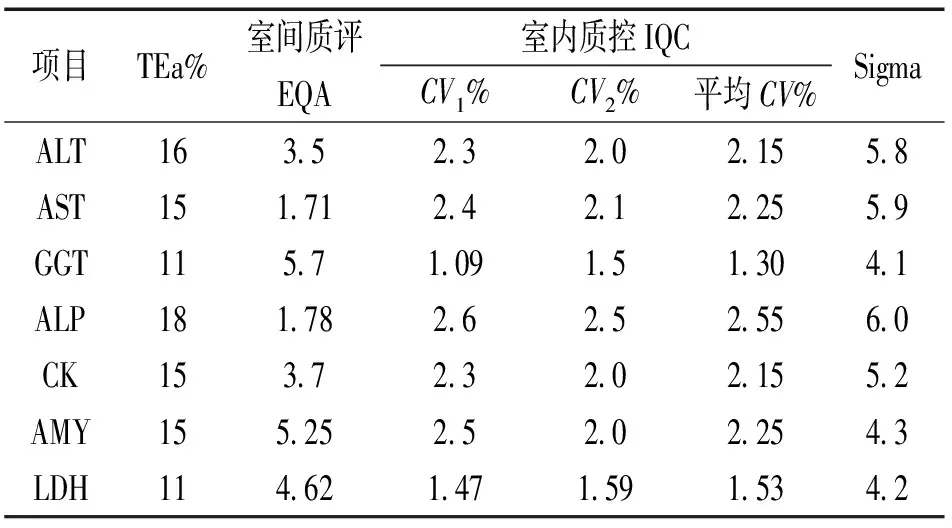
项目TEa%室间质评EQA室内质控IQCCV1%CV2%平均CV%SigmaALTASTGGTALPCKAMYLDH161511181515113.51.715.71.783.75.254.622.32.41.092.62.32.51.472.02.11.52.52.02.01.592.152.251.302.552.152.251.535.85.94.16.05.24.34.2
2.2 临床生物化学酶类检测项目SQC策略 见表2。根据标本工作量,以起始质控误差检出率最大,过程监测质控假失控率最低为原则,设计酶类检测项目起始SQC程序和过程监测SQC程序。
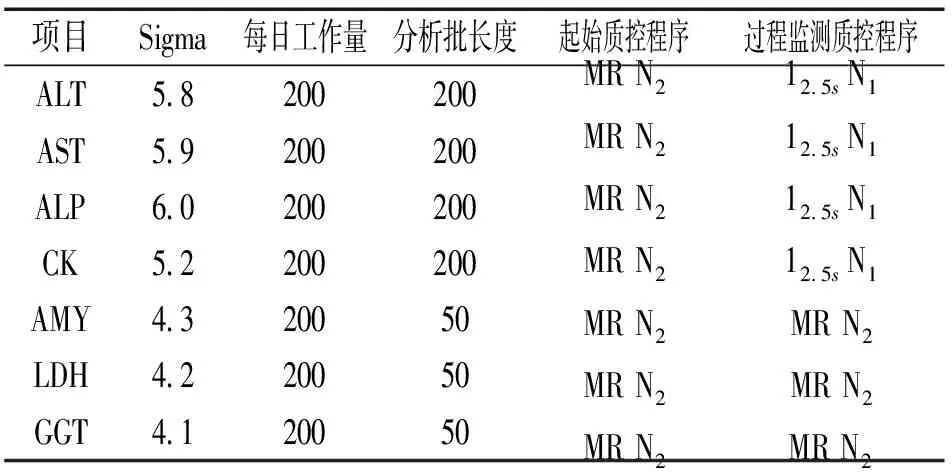
表2 临床生物化学酶类检测项目SQC策略
2.3 临床生物化学酶类检测项目SQC工作计划 见表3。
表3临床生物化学酶类检测项目SQC工作计划
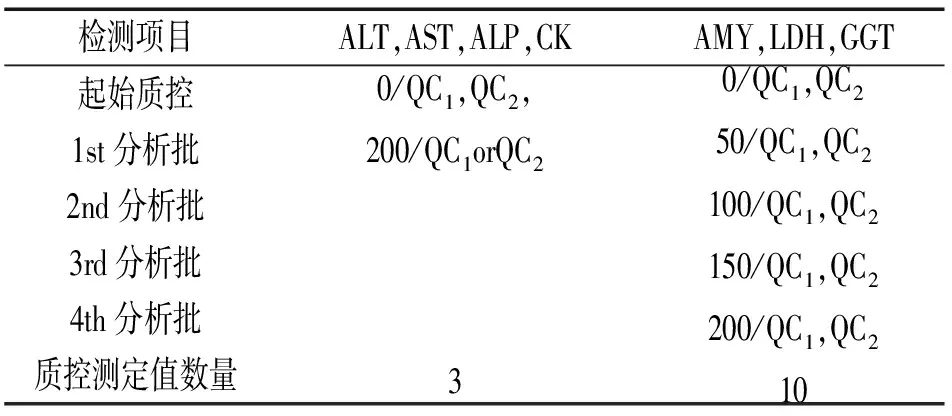
检测项目ALT,AST,ALP,CKAMY,LDH,GGT起始质控1st分析批2nd分析批3rd分析批4th分析批质控测定值数量0/QC1,QC2,200/QC1orQC2 30/QC1,QC250/QC1,QC2100/QC1,QC2150/QC1,QC2200/QC1,QC210
3 讨论
传统统计质量控制(statistical quality control,SQC),以误差检出率(Ped)或Sigma度量值评价检测系统分析的性能,设计QC规则和QC个数,但尚未涉及QC频率。Parvin等[4,5]提出了一个替代指标患者风险参数MaxE(NUF),即在最坏情况下,检测到失控状态前产生和报告不可靠患者结果的预期数量。该指标由质量目标、QC规则、QC频率、失控类型和大小决定。患者结果超过质量目标即为错误的(不正确的、不可靠的或不可接受的)结果,导致不适当的临床决策和行为给患者带来风险;QC规则决定了Ped ,即决定了实验室分析项目检测性能,能识别出误差的潜在能力;QC频率越高,越容易检测出分析过程中的误差,降低不可靠结果所导致的患者风险。CLSI C24-Ed4[6]提出了MaxE(NUF)用于9 Sigma和4 Sigma的测定程序的QC频率,为实验室设计质量控制策略提供了新的质量管理误差模型及方案,但没有具体的工具来帮助实验室验证这些结果或实际应用于实验室。
Yago等[7-8]将经典的Westgard的Sigma质量控制方法与Parvin的MaxE(NUF)风险管理方法结合起来改进SQC,解决Sigma度量值、Ped与MaxE(NUF)之间的函数关系,具有高Ped的检测系统同时伴有低的MaxE(NUF)。Westgard等[9]绘制Sigma-SQC诺曼图图形工具为实验室提供了简单、容易操作的具体设计质量控制计划(quality detection and quality control plan,QCP)的方法,依据Sigma度量值评价检测系统分析性能,Sigma功效函数图得到不同QC规则、QC个数和Ped,按照Sigma-SQC诺曼图得到MaxE(NUF),利用公式100/MaxE(NUF)计算出分析批大小(QC频率)。
MaxE(NUF)是在失控状态下所能接受的最大期望报告错误结果的数量,MaxE(NUF)≤1可以最大程度地降低患者风险,按照起始质控误差检出率大于0.9,过程监测质控假失控率小于0.05,保证质量、节约成本为原则,每组以最小Sigma度量值决定分析批长度候选质控策略。分析方法的性能Sigma度量值大小决定了分析批长度或控制频率,减少质量控制频率就要提高分析方法的性能,高Sigma度量值方法仅需少量的质量控制且支持较长的分析批长度,低Sigma度量方法要求大量的质量控制且短的分析批长度。但是,基于患者风险设计SQC质控程序策略,患者的结果必须在检测的开始和结束时应用SQC程序,质控频率与目前多数实验室质控做法相比,增加了实验室QC的成本,并且患者结果必须在QC结果评估可接受后才能发放报告,QC失控就必须采取纠正措施重复患者样本的检测。
风险管理已成为医学实验室质量控制计划的基础,实验室设计良好的SQC质控策略确保其质量控制实践的重点是降低患者风险和降低成本,切实可行的风险管理策略有利于实验室的风险规避和质量的持续改进。

