改性香蕉皮粉末和香蕉皮活性炭吸附水中甲氰菊酯的对比研究
孟 琪,吴 彦,李 灵,罗冉嘉,程绪红,樊一桥,平 巍
(重庆三峡学院 三峡水库水环境演变与污染防治重点实验室,重庆 404100)
由于农药、化肥的大量使用,农业面源污染导致的水体污染问题已引起广泛的重视[1]。甲氰菊脂是一种被广泛应用于现代农业生产的拟除虫菊酯类高效杀虫剂[2]。甲氰菊酯能通过多种途径进入水体,对人体和水生生物有较高的毒性[3-5]。人体少量接触会引起皮肤刺痛感;若大量接触会出现头晕、恶心呕吐等症状,严重者会抽搐昏迷甚至休克[6]。目前水中甲氰菊酯的去除主要有混凝法[7]、生物降解法和化学氧化法[8],而吸附法作为一种廉价、易操作的水处理方法,用以去除水中的甲氰菊酯鲜有系统深入的研究。赵华等[9]在其研究中指出,土壤对甲氰菊酯有较好的吸附特性,但是其作为一种天然矿物,成分和性质多样,难以在工程化的水处理系统中大规模应用。所以新型吸附材料的开发和应用对利用吸附法处理甲氰菊脂废水的研究具有重大的实践价值。
香蕉是一种热带水果,产量在水果中位居第二,一半以上产自亚洲[10],在我国南方产量较高[11]。香蕉皮的主要成分为纤维素[12]。纤维素为多孔结构,并且分子结构中有大量羟基,引入特定官能团会大大提高吸附性能[13-14]。在国外已有很多改性纤维素作吸附剂的应用[15-16]。而利用农业固体废物制备活性炭去除水中的污染物在国内外也有大量研究报道[17-18]。为比较利用农业固体废物制备吸附材料方法的应用,笔者以香蕉皮粉末为原料,分别制备化学改性吸附剂和活性炭,对比考察两种材料对水中甲氰菊酯的吸附特性。采用BET介孔分析对比两种材料的表面孔道结构特征,采用静态吸附实验对比了两种材料对水中甲氰菊酯的吸附速率和去除性能,并进一步通过等温拟合分析和吸附动力学分析分别对比讨论了两种材料对水中甲氰菊酯的吸附机制。
1 实验材料与方法
1.1 实验材料
市售香蕉去除果肉取皮,用去离子水冲洗干净,于105℃烘至恒重,研磨成80~100目的粉末,保存于干燥器中备用。甲氰菊酯水溶液配制:取甲氰菊酯标样(浓度100 μg/mL)1 mL定容至100 mL,即配置成1 000 μg/L的甲氰菊酯储备液。实验所用的甲氰菊酯废水均用甲氰菊酯储备液稀释。
仪器:SHA-C水浴恒温振荡器购自上海亨钛科学仪器有限公司,高温燃烧管式炉购自北京市永光明仪器厂,NOVA2000e比表面及孔径分析仪购自美国康塔仪器公司,JSM-7800F扫描电子显微镜购自日本电子株式会社,PHS-3CpH计购自上海仪电科学仪器股份有限公司,安捷伦7820A气相色谱仪购自美国安捷伦科技有限公司。
1.2 改性香蕉皮粉末及活性炭的制备方法
改性香蕉皮粉末(MBP)的制备方法:精确称取1.0 g干香蕉皮粉末,加入100 mL 0.2 mol/L NaOH溶液中,置于磁力搅拌器上,均匀搅拌25 min,取出后用去离子水反复冲洗抽滤,直到滤液pH为7且呈无色状态,于105℃烘干,即制得MBP。
香蕉皮活性炭(BAC)的制备方法:将香蕉皮粉末放于管式电炉中(氩气保护)于450℃碳化3.5 h,冷却至室温后,加入KOH固体(炭碱质量比1∶4)研磨、混合,于管式炉中(950°C)活化3 h(氩气保护)。冷却至室温后取出,用去离子水反复冲洗抽滤,烘干后即制得BAC。
1.3 吸附实验
称取MBP和BAC吸附材料各0.1 g,投入100 mL锥形瓶中,再加入50 mL甲氰菊酯溶液,放于恒温摇床,在25℃下振荡2 h,然后用0.25 μm滤膜进行过滤,用气相色谱法测定滤液中甲氰菊酯的剩余浓度[5]。吸附速率实验时间梯度10 min。材料对甲氰菊酯的吸附容量采用公式(1)进行计算,对比试验采用相同条件下不加吸附剂的甲氰菊酯水溶液进行,空白试验添加去离子水。

式中:qe为吸附平衡时吸附剂的吸附量,单位为μg/g;C0为吸附前甲氰菊酯浓度的初始浓度,单位为μg/L;Ce为吸附达到平衡时滤液中甲氰菊酯剩余浓度,单位为μg/L;V为水样体积,单位为L;m为吸附剂用量,单位为g。
2 结果与讨论
2.1 样品表征
2.1.1 表面形态结构对比分析

图1 MBP和BAC的SEM表征图片Fig.1 SEM images of MBP and BAC
图1是MBP和BAC吸附甲氰菊酯前后的扫描电镜(SEM)图片。对比图1(a)和(b),发现MBP表面存在较多的线状褶皱,材料表面密实,孔隙率不高。这是因为MBP虽然经过了NaOH浸泡,部分组织被浸出,但其仍然是一种天然的生物材料,主要成分仍然是纤维素和多糖物质;而BAC则具备明显的层状结构,表面孔隙结构明显较MBP发达。从吸附的过程分析,BAC更有利于吸附质通过孔道进入材料内部而发生吸附。而通过对比吸附前后的SEM图片,可以看出,两种材料在吸附甲氰菊酯后,材料表面均变得相对光滑,这是因为材料表面的褶皱和孔道被附着的甲氰菊酯覆盖和填充,这也说明,甲氰菊酯确实被材料吸附。
2.1.2 BET比表面积及孔径分布对比
MBP和BAC的比表面积和孔分析数据如表1所示。结果显示,BAC的BET比表面积和空隙总容积远大于MBP,而孔径分布方面,MBP的平均孔径大于BAC,BAC的空隙以微孔为主(比孔容大于56%),而MBP的空隙以介孔为主(比孔容大于90%)。这是因为MBP本质上还是属于生物有机体,其成分主要是纤维素、半纤维素和多糖物质[19]。虽然在材料改性过程中内部的部分物质被NaOH溶液浸出[20],但比表面积依然有限。而香蕉皮经过高温碳化及KOH活化之后,其主要组织结构在材料表面留下发达的空隙结构,但BAC的比表面积数值仍远小于超高比表面积活性炭(最高可超过 2 000 m2/g)[21]。

表1 比表面积及孔径分布对比Tab.1 Comparison on BET surface area and pore size distribution
2.1.3 表面官能团结构对比分析
MBP和BAC的傅里叶红外光谱图(FTIR)如图2所示。MBP在3 140/cm,1 727/cm,1 450/cm,1 020/cm和669/cm处有吸收峰,BAC在3 140/cm,1 727/cm,1 020/cm,669/cm处未显示有明显吸收峰。3 140/cm,1 450/cm,699/cm处的吸收峰分别是C—H的伸缩振动、弯曲振动和面外弯曲振动引起的,这与BAC在1 420/cm,876/cm处的吸收峰所指示的官能团一致;1 727/cm处的吸收峰是伸缩振动[22]引起的;1 020/cm处的吸收峰是由C—O的伸缩振动引起的,说明在MBP中含有C和C—O官能团,而在BAC的图谱中并未出现。另外,MBP在3 630/cm的吸收峰强度明显强于BAC,3 630/cm处的吸收峰由O—H的伸缩振动引起,表明MBP的O—H较BAC更为丰富。MBP相较BAC含有更丰富的官能团结构,可能发生多种类型的化学吸附。

图2 MBP和BAC的FTIR图谱对比Fig.2 Comparison on FTIR spectra between MBP and BAC
2.2 改性香蕉皮粉末及蕉皮活性炭对甲氰菊酯吸附研究
2.2.1 不同pH条件下吸附量的对比
吸附剂投加量为0.1 g,甲氰菊酯溶液体积50 mL,浓度100 μg/L,吸附时间2 h,对不同pH条件下的甲氰菊酯溶液进行吸附实验,结果如图3所示。pH对于两种材料的吸附效果均有影响。当pH=7时,两种吸附剂对于甲氰菊酯的吸附量都达到最大值,这是因为在酸性或碱性条件下,大量的游离H+或OH-与吸附材料中的有机官能团发生了结合,占据了吸附点位,同时改变了吸附材料表面基团的性质,使得材料对水中甲氰菊酯的吸附能力下降。同时,在中性条件下,溶液中的甲氰菊酯为分子形态,更有利于吸附材料的吸附[22]。此外,在实验pH范围内,BAC对甲氰菊酯的吸附能力均强于MBP。

图3 不同pH条件下吸附量的对比Fig.3 Comparison on adsorbance under various pH conditions
2.2.2 不同初始浓度吸附量的对比
配制不同初始浓度甲氰菊酯溶液各50 mL,分别加入0.1 g MBP和BAC两种材料作为吸附剂,吸附时间2 h,比较其对水中甲氰菊酯的吸附量,结果如图4所示。MBP在甲氰菊酯初始浓度0~280 μg/L范围内,吸附量随甲氰菊酯初始浓度的升高而升高,当初始浓度为280 μg/L时,MBP对甲氰菊酯的吸附量达到58.215 μg/g。BAC在甲氰菊酯初始浓度0~400 μg/L范围内,吸附量随甲氰菊酯初始浓度的升高显著升高,当初始浓度增加至400 μg/L时,BAC对甲氰菊酯的吸附倾向饱和,此时吸附量达到91.005 μg/g。在所有初始浓度条件下,BAC对甲氰菊酯的吸附量均高于MBP,这是因为BAC具有较大的比表面积,且能适应更大的浓度范围。BAC的比表面积远大于MBP,但无论是在同一浓度条件下的吸附量还是饱和吸附量,两者的相差程度远小于其比表面积的相差程度。因此,初步判断吸附过程不仅由材料的比表面积主导,而且MBP对甲氰菊酯可能存在化学吸附。

图4 不同初始浓度条件下的吸附量对比Fig.4 Comparison on adsorbance under various initial concentration
2.3 吸附等温线模型对比分析
用Langmuir吸附方程和Freundlich吸附方程对不同浓度甲氰菊酯的吸附实验结果拟合,线性拟合方程分别如式(2)和式(3)所示,拟合结果如图5和表2所示。

式中,qe为平衡吸附量,单位为μg/g;KL为Langmuir常数,单位为L/μg;q0饱和吸附量,单位为μg/g;KF为Freundlich常数,单位为μg/g·(μg/L)-1/n;1/n为无量纲的与吸附强度有关的系数;ce为平衡浓度,单位为μg/L。
由表2可知,对于MBP,两种等温模型拟合相关性均大于0.9,表明MBP对甲氰菊酯的吸附既存在单层吸附,也存在多层吸附。而BAC对甲氰菊酯的吸附则明显更倾向于单层吸附。Langmuir拟合结果显示,MBP和BAC对甲氰菊酯的饱和吸附量分别为 64.392 μg/g,95.057 μg/g,分析认为,BAC由于具有相对较大的比表面积,能够提供较多的吸附结合点位,所以具有较大的吸附容量[23];MBP作为一种粗加工的生物材料,其未经过碳化过程,虽然其比表面积远小于BAC,但材料内部大量的官能团得以保留,能够高效地吸附甲氰菊酯,所以其对甲氰菊酯的吸附容量依然比较可观,这与之前的推断是一致的。Freundlich拟合结果表明,两种材料1/n值均小于1,说明两种材料对甲氰菊酯的吸附属于“优惠型”的吸附。相比较,BAC具有更小的1/n值,所以,BAC对甲氰菊酯的吸附更容易发生,推测其仍然和其较大的比表面积相关。
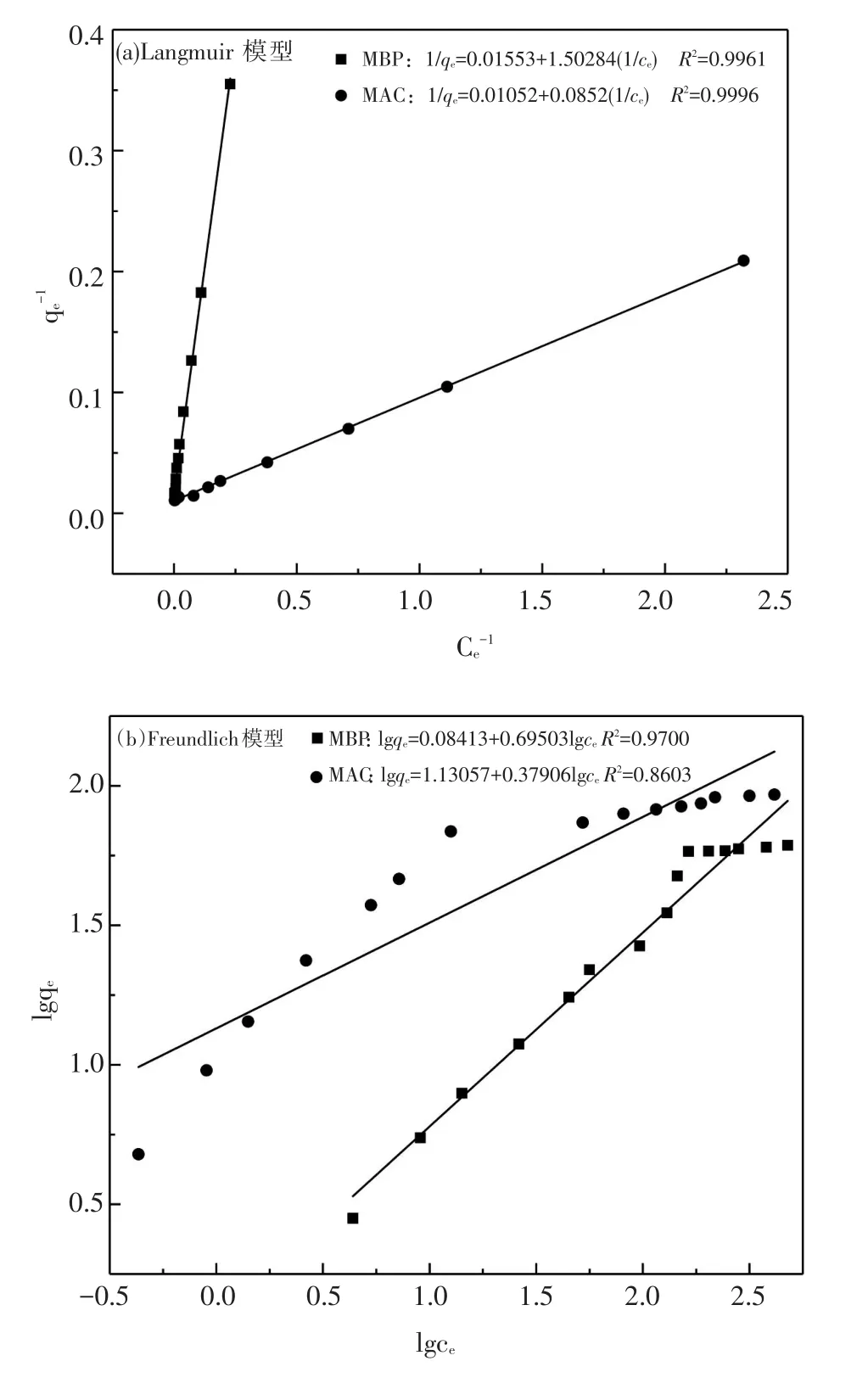
图5 等温拟合结果对比Fig.5 Comparison on results of adsorption isothermal fitting

表2 等温拟合参数对比Tab.2 Comparison on parameters of isothermal fitting
2.4 吸附速率对比及动力学分析
吸附剂投加量为0.1 g,甲氰菊酯初始浓度为100 μg/L,体积50 mL,不同吸附时间的吸附量如图6所示。在0~50 min,MBP对甲氰菊酯的吸附量随着吸附时间的延长而迅速增加;在50 min时,吸附量为20.530 μg/g,继续延长吸附时间,则吸附量变化不明显,表明MBP对甲氰菊酯的吸附平衡时间为50 min。而BAC对甲氰菊酯的吸附在60 min时趋于平衡,此时对应的吸附量为45.460 μg/g。同时,在实验时间范围内,BAC的吸附量均大于MBP,表明在研究时间范围内,BAC对甲氰菊酯的吸附速率均大于MBP。这是因为BAC具有较大的比表面积,孔道结构更为发达,水中的甲氰菊酯离子更容易通过扩散进入材料内部而被吸附。同时,对比两种材料在同一时间的吸附量相差程度,远小于其比表面积的相差程度,这也预示了MBP对甲氰菊酯的吸附存在化学吸附的可能性。

图6 吸附速率对比Fig.6 Comparison on the adsoption rate
分别用准一阶动力学模型(4)、准二阶动力学模型(5)和粒子吸附模型(6)对实验数据拟合,方程分别如下。

式中,Qm为平衡吸附量,单位为μg/g;qt为t时刻的吸附量,单位为μg/g;K1为一阶吸附速率常数,单位为min-1;t为吸附时间,单位为min;K2为二阶吸附速率常数,单位为g/(μg·min);Kp为颗粒内扩散速率常数,单位为μg/(g·min0.5),C为边界层常数。
根据表3的吸附动力拟合结果,MBP和BAC的准二阶动力学模型相关系数均大于准一阶动力学模型,因此准二阶吸附动力模型更能解释香蕉皮改性吸附剂对甲氰菊酯的吸附过程。这表明两种材料对甲氰菊酯的吸附过程倾向于物理化学吸附,即先通过物理扩散迅速富集在材料表面,后期发生化学吸附。这与等温拟合的结论一致。

表3 吸附动力学拟合参数对比Tab.3 Comparison on parameters of adsorption kinetics
另一方面,从粒子吸附模型拟合曲线(图7)可以看出,无论是MBP还是BAC,拟合曲线不是直线的形式,且不通过坐标原点,这说明两种材料对水中甲氰菊酯的吸附都是分两个阶段完成的,即吸附前期由表面扩散迅速吸附,后期甲氰菊酯粒子通过孔内扩散进入材料内部,发生更深的吸附。对比两个阶段的吸附参数,粒子吸附阶段的相关性系数和扩散常数均远小于表面吸附阶段,因此可以推断,粒子扩散阶段不是主要的控制吸附速率的因素,也就是说,两种材料吸附甲氰菊酯主要是表面吸附作用,倾向于单层吸附。
应当指出,MBP由于未经过碳化,仍然是一种生物材料,其表面存在多种化学基团,这些基团可能都会对吸附过程造成影响。考虑到其吸附甲氰菊酯的动力学模型相关性系数值均不高,且比较接近,暗示其对甲氰菊酯的吸附可能存在多种作用。

图7 吸附动力学拟合结果对比Fig.7 Comparison on results of adsorption kinetics
3 结论
(1)BAC对水中甲氰菊酯的吸附能力强于MBP,吸附速率更快。
(2)BAC作为一种相对稳定的材料,能有效去除水中的甲氰菊酯。而改性吸附剂吸附性能低于活性炭,但作为一种低成本一次性吸附材料仍能够用于处理低浓度的甲氰菊酯废水。
(3)MBP和BAC对水中甲氰菊酯的吸附过程符合Langmuir等温模型,其动力学拟合结果倾向于准二阶动力学模型。表明两种材料对水中甲氰菊酯的吸附均以化学吸附为主导。

