pH值和EGCG对β-胡萝卜素乳液化学稳定性的影响
刘 蕾 陈历水,2 马 莺 高彦祥 李 慧,5 杨海莺,2
(1.中粮营养健康研究院有限公司品牌食品研发中心, 北京 102209; 2.老年营养食品研究北京市工程实验室, 北京 102209; 3.哈尔滨工业大学化工与化学学院, 哈尔滨 150090; 4.中国农业大学食品科学与营养工程学院, 北京 100083; 5.营养健康与食品安全北京市重点实验室, 北京 102209)
0 引言
β-胡萝卜素是一种脂溶性类胡萝卜素,是合成维生素A的前体物质,具有猝灭单线态氧和使自由基失活等多种生物学功能。在食品工业中,由于β-胡萝卜素在水中的溶解度低、熔点高、在光和热的环境中容易发生化学降解等性质,限制了其广泛应用。近年来,有学者利用水包油的乳液进行了β-胡萝卜素传递系统的制备,此体系成本较低,可有效提高β-胡萝卜素的水溶性、稳定性及生物利用率[1-2]。
茶叶富含多酚类物质,其富含的茶多酚因对人体无害并具有较高的抗氧化活性越来越受到关注,其中表没食子儿茶素没食子酸酯(EGCG)是茶多酚中含量最高同时抗氧化活性最强的物质。EGCG在乳液中有双重作用,既可以发挥抗氧化作用也可以发挥促氧化作用。ZHOU 等[3]研究了在水包亚麻籽油的乳液中,EGCG添加量和乳液pH值对EGCG抗氧化和促氧化活性的影响。结果表明,在pH值为2~4,EGCG添加量为5~100 μmol/L时,EGCG对亚麻籽油在乳液中的氧化起促进作用;但在较高的pH值条件下(5~7),EGCG添加量在25~500 μmol/L时,EGCG可以抑制亚麻籽油的氧化。因此,乳液pH值和EGCG添加量同时影响EGCG的抗氧化作用。
目前,利用抗氧化剂抑制β-胡萝卜素在乳液中降解的报道较少。QIAN等[4]报道了将油溶性抗氧化剂(辅酶Q10)和水溶性抗氧化剂(EDTA(乙二胺四乙酸)和维生素C)加入以吐温20和β-乳球蛋白为乳化剂的β-胡萝卜素乳液中,结果表明EDTA和辅酶Q10比维生素C对β-胡萝卜素的保护效果好。
本文在不同pH值的β-胡萝卜素乳液中,添加不同含量的EGCG,测定贮藏期间EGCG对乳液中β-胡萝卜素含量和贮藏前后色差的影响。研究EGCG影响乳液化学稳定性的机理,测定界面EGCG含量,以期为将EGCG作为抗氧化剂添加到β-胡萝卜素乳液中提供理论依据。
1 材料与方法
1.1 材料与试剂
α-LA 购于美国 Davisco 公司,纯度为95%以上;EGCG购于北京北实纵横科技发展有限公司,纯度为99.5%以上;中链三酸甘油酯(Medium chain triacylglycerol, MCT)购于奎斯特国际有限公司;30% β-胡萝卜素-MCT 悬浮液购于浙江医药有限公司新昌制药厂;柠檬酸、磷酸氢二钠、正己烷、碳酸钠、磷酸、无水乙醇均购自北京化工厂,纯度为99.5%以上;福林-酚试剂、叠氮化钠购于美国Sigma 公司。
1.2 仪器与设备
M-110型高压微射流均质机,美国Microfluidizer公司;HD-1型高速乳化均质机,北京华远航实验设备厂;UV-1800型紫外-可见分光光度计,日本岛津公司;RC2-S型超高速离心机,美国Sorvall 仪器公司;HSP-150型恒温恒湿培养箱,江苏友联仪器研究所;S22-2型恒温磁力搅拌器,上海司乐仪器有限公司;WSC-S型色差计。
1.3 方法
1.3.1β-胡萝卜素乳液制备
将质量分数1.5%α-LA溶解于0.1 mol/L pH值2.0或pH值7.0的柠檬酸-磷酸氢二钠缓冲溶液中,在室温(20℃)下搅拌4 h至α-LA全部溶解,待用。将30% β-胡萝卜素-MCT悬浮液加热溶解于MCT中至其完全溶解待用,溶解方法参照XU等[5]的方法,并做一定调整。
在高速剪切仪的搅拌下将溶解有β-胡萝卜素的MCT缓慢加入α-LA溶液中,12 000 r/min剪切10 min,形成粗乳液。将制备的粗乳液进一步通过微射流(82.7 MPa)均质,循环3次[6]。由此制备的β-胡萝卜素乳液(10%油相(含有0.5% β-胡萝卜素),1.5% α-LA)用于后续实验。取制备好的β-胡萝卜素乳液与不同浓度的EGCG缓冲溶液等质量混合。乳液中各组分的最终质量分数为:MCT 5%(其中含有0.5% β-胡萝卜素),α-LA 0.75%。pH值2.0乳液中EGCG添加量:0.002 5%、0.005 0%、0.010 0%、0.020 0%、0.050 0%、0.100 0%、0.200 0%、0.400 0%、0.500 0%;pH值7.0乳液中EGCG添加量:0.002 5%、0.005 0%、0.010 0%、0.020 0%、0.050 0%、0.100 0%。
1.3.2β-胡萝卜素含量测定

1.3.3β-胡萝卜素乳液色差测定
利用WSC-S型色差计测定β-胡萝卜素乳液贮藏前后色差。仪器采用标准白板进行校正,每个乳液样品重复测定3次,取平均值。色差参数包括L值、a值、b值。其中L值表示黑白或亮暗,正值表示偏白,负值表示偏暗;a值表示红绿,正值表示偏红,负值表示偏绿;b值表示黄蓝,正值表示偏黄,负值表示偏蓝[8]。
颜色由亮度和色度共同表示,其中色度是不包括亮度在内的颜色性质。色调是由物体反射的光线中以哪种波长占优势来决定的,不同波长产生不同颜色感觉,色调是颜色的重要特征。色度Cab和色调Hab计算公式为
(1)
(2)
1.3.4乳液界面EGCG含量测定
为测定界面EGCG含量,通过超高速离心法将乳液中游离相EGCG与界面上EGCG分离。参照FARAJI等[9]的方法,将乳液置于10 mL的超高速离心管中,在超高速离心机中离心50 min,离心力为36 000g。为避免β-胡萝卜素在离心过程中发生氧化,将离心机温度设定在10℃。离心结束后,利用带有长针头的注射器小心分离下层清液和上层乳析层。
取一定体积的下清液通过孔径0.1 μm的聚偏二氟乙烯(Polyvinylidene Fluoride,PVDF)膜进行过滤,去掉较大液滴乳析层颗粒[10]。取0.5 mL过滤后的下清液,加入2.5 mL 0.2 mol/L 福林-酚试剂,振荡20 s后反应5 min,再加入2.0 mL 0.075 g/mL碳酸钠溶液,振荡20 s后避光反应2 h。反应后溶液在760 nm处测定吸光度。空白对照以去离子水代替样品进行反应[11]。
1.4 数据分析
在所有实验中,每个样品设置3个平行样品,并根据实验结果计算平均值和标准差。实验中使用GraphPad prism 5(美国GraphPad Software 公司)软件,利用ANOVA方差分析和Turkey检验进行结果的显著性分析。
2 结果与分析
2.1 β-胡萝卜素降解
茶多酚在水包油的乳液体系中可以起到双重作用,因其本身较强的提供氢原子和接受自由基的作用使其具有较强的抗氧化作用[12-13],但在一定条件下,由于茶多酚可以提高金属离子的促氧化作用,使得由金属离子催化的氧化反应高于由自由基反应引起的氧化反应,因此在乳液中表现出促氧化作用[2,14-15]。影响茶多酚发挥抗氧化作用和促氧化作用的因素有乳液的pH值和乳液中茶多酚的添加量[16]。为了确定茶多酚在水包油的乳液中对β-胡萝卜素的降解作用,研究了不同pH值(2.0和7.0)和EGCG添加量(0.002 5%~0.500 0%)对乳液中β-胡萝卜素降解的影响,结果如图1和图2所示。
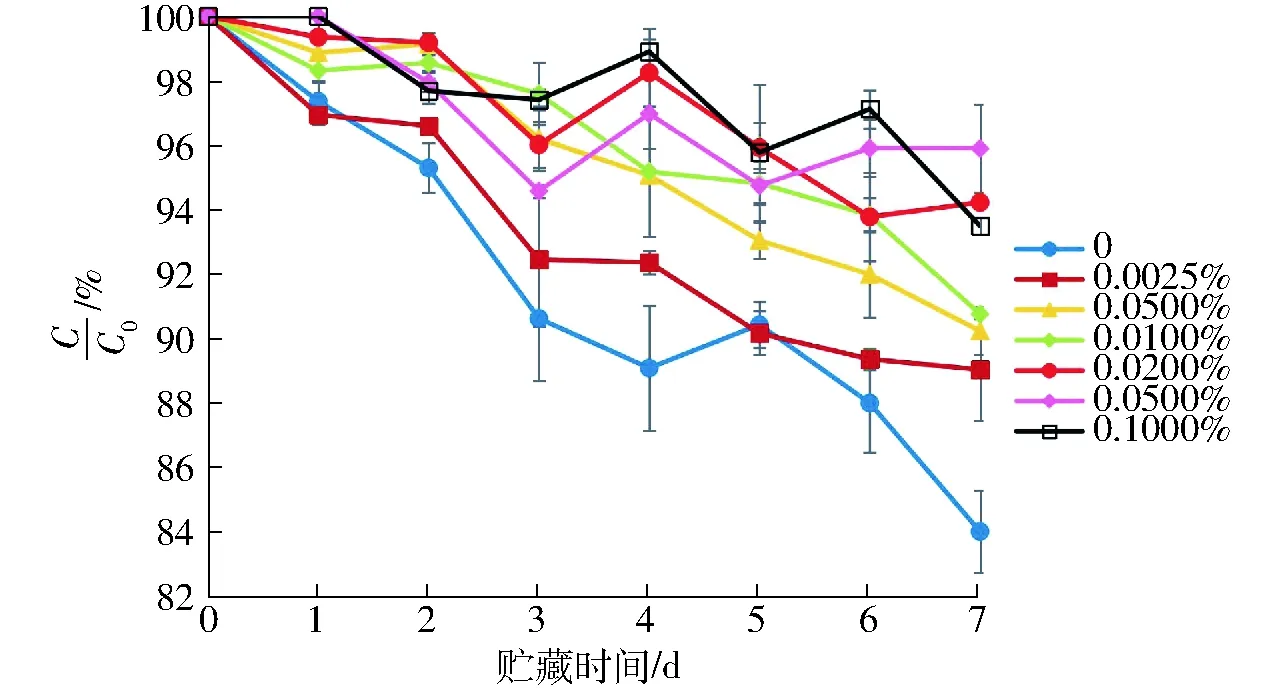
图2 EGCG添加量对pH值7.0乳液中β-胡萝卜素降解的影响Fig.2 Influence of EGCG on degradation of β-carotene in emulsions at pH value of 7.0
由图1可以得出,pH值2.0的β-胡萝卜素乳液随着贮藏时间的延长,β-胡萝卜素含量呈下降趋势。其中未添加EGCG的乳液中β-胡萝卜素的保留率在贮藏过程中低于添加了EGCG的乳液。贮藏7 d后,未添加EGCG的乳液中,β-胡萝卜素的保留率是50.45%,而添加了EGCG的乳液中β-胡萝卜素的保留率不低于51.69%。由此,在pH值2.0的β-胡萝卜素乳液中,添加0.002 5%~0.500 0%的EGCG可以作为抗氧化剂对β-胡萝卜素起保护作用。EGCG添加量为0.002 5%~0.100 0%时,随着EGCG添加量的增多,贮藏期间保留在乳液中的β-胡萝卜素含量呈增高趋势(P<0.05)。当EGCG添加量为0.002 5%时,乳液贮藏7 d后,β-胡萝卜素的保留率为51.69%;当EGCG添加量为0.100 0%时,贮藏7 d后,β-胡萝卜素的保留率为86.57%。当EGCG添加量大于0.100 0%时,继续加大EGCG添加量对β-胡萝卜素的保留率没有显著影响(P>0.05),当EGCG添加量为0.500 0%时,β-胡萝卜素的保留率为89.37%。由以上实验结果可以得出,在pH值2.0的β-胡萝卜素乳液中,EGCG添加量在一定范围时(0.002 5%~0.100 0%),可以对β-胡萝卜素的降解起显著的抑制作用;当EGCG添加量大于0.100 0%时,过量的EGCG不能对β-胡萝卜素起到更好的保护作用。结合当EGCG添加量大于0.200 0%时,EGCG的添加会显著降低乳液的物理稳定性,在pH值2.0的乳液中,添加0.200 0%的EGCG作为抗氧化剂可以既不破坏乳液物理稳定性,同时最大程度地提高β-胡萝卜素的保留率。
EGCG对pH值7.0的乳液中β-胡萝卜素降解的影响如图2所示。在pH值7.0的β-胡萝卜素乳液中,添加了EGCG的乳液中β-胡萝卜素的保留率显著大于未添加EGCG乳液中β-胡萝卜素的保留率,因此EGCG在pH值7.0的乳液中也可以作为抗氧化剂抑制β-胡萝卜素的降解。随着EGCG添加量的增加,保留在乳液中β-胡萝卜素的含量逐渐增大(P<0.05)。当EGCG添加量为0.002 5%和0.100 0%时,乳液贮藏7 d后,β-胡萝卜素的保留率分别为89.00%和93.48%。
比较不同pH值乳液中β-胡萝卜素的降解速率可以得出,在相同贮藏时间内,EGCG添加量相同的乳液中,pH值2.0的乳液中β-胡萝卜素的保留率低于pH值7.0的乳液中的保留率。其中比较未添加EGCG的乳液时,pH值7.0的乳液在贮藏7 d后,β-胡萝卜素的保留率为83.97%,而pH值2.0的乳液中,β-胡萝卜素的保留率为50.45%。此结果与QIAN等[17]的报道相同。这是由于β-胡萝卜素在酸性环境中时,与酸形成的离子对会解离形成类胡萝卜素阳离子,类胡萝卜素阳离子比类胡萝卜素分子更容易发生降解反应[18-19]。另外,pH值2.0和pH值7.0的β-胡萝卜素乳液在55℃下避光贮藏7 d。由于β-胡萝卜素乳液避光保存,β-胡萝卜素的光降解途径在本研究中不存在。因此,在pH值7.0的乳液中,β-胡萝卜素的主要降解途径是由自由基和金属离子催化的降解;但β-胡萝卜素在pH值2.0的乳液中除了由自由基和金属离子催化的降解反应之外,还存在酸降解途径。
由以上实验结果可以得出,在pH值2.0和7.0的β-胡萝卜素乳液中,EGCG均可抑制β-胡萝卜素降解,其中由于β-胡萝卜素在酸性环境中容易发生酸降解,因此与pH值7.0的β-胡萝卜素乳液相比,在pH值2.0的乳液中β-胡萝卜素的降解速率较快。
2.2 β-胡萝卜素乳液色差
β-胡萝卜素是在食品行业中应用最广泛的色素,作为着色剂其可以应用于很多食品中,我国食品添加剂使用标准(GB 2760—2014)中规定了其可以应用的食品类别以及添加量。色差参数是评价着色剂颜色的重要指标。在食品加工及流通过程中,贮藏是一个必不可少的环节。其中贮藏环境的温度、光照以及贮藏时间会显著影响食品中β-胡萝卜素的感官性质,即色差。为了研究在55℃避光贮藏7 d后β-胡萝卜素乳液的色差改变,在贮藏前后对乳液的色差进行了测量。pH值2.0的β-胡萝卜素乳液在贮藏前后的色差参数如表1、2所示。

表1 pH值2.0 β-胡萝卜素乳液贮藏前色差参数Tab.1 Color parameters of β-carotene emulsions at pH value of 2.0 before storage
注:同列不同字母表示差异显著(P<0.05)。下同。

表2 pH值2.0 β-胡萝卜素乳液贮藏后色差参数Tab.2 Color parameters of β-carotene emulsions at pH value of 2.0 after storage
由表1可以得出,pH值2.0的β-胡萝卜素乳液在贮藏前,表征乳液亮度的L值、红色的a值、黄色的b值均为正值。这表明β-胡萝卜素乳液在色差测量上是亮的、具有红色和黄色的混合样品,这与图3中β-胡萝卜素乳液的感官性质相符。在pH值2.0的乳液中,EGCG添加量对贮藏前β-胡萝卜素乳液的色差参数L值、a值和b值没有显著影响(P>0.05)。Cab和Hab在不同EGCG添加量的乳液中也没有显著差异(P>0.05)。在图3中,贮藏前未添加EGCG的β-胡萝卜素乳液与EGCG添加量为0.5%的β-胡萝卜素乳液相比,两者之间没有肉眼可见的颜色差异,与色差参数相符。

图3 在55℃贮藏前后pH值2.0的β-胡萝卜素乳液Fig.3 Photos of β-carotene emulsions at pH value of 2.0 before and after storage at 55℃
pH值2.0的β-胡萝卜素乳液贮藏7 d后的色差参数如表2所示。比较表1、2中乳液的色差参数可以得出,与贮藏前的色差参数相比,贮藏后乳液的L值、a值和b值均降低。这说明贮藏后乳液的亮度下降、红色值和黄色值都降低。同时贮藏前后色度Cab值也有明显差异。从图3可以看出,对比贮藏前后β-胡萝卜素乳液的颜色,在视觉上存在显著性差异,贮藏后乳液的亮度降低,颜色的饱和度降低。这与贮藏前后色差参数值的变化相符。由在贮藏期间测定β-胡萝卜素的含量可知,随着贮藏时间的延长,β-胡萝卜素的含量逐渐降低。因此,在pH值2.0的乳液中,色差的变化可能是由β-胡萝卜素含量的变化所致。
为了研究色差变化与β-胡萝卜素含量之间的关系,比较了不同EGCG添加量的β-胡萝卜素乳液的色差参数的差异。由表2可得,随着EGCG添加量的增加,乳液的L值、a值、b值呈增高的趋势。由贮藏期间测定的β-胡萝卜素含量可知,随着EGCG添加量的增加,β-胡萝卜素的保留率逐渐增大。由图3中贮藏后乳液的颜色可以看出,添加0.5% EGCG的乳液与不添加EGCG的乳液贮藏后相比,添加了0.5%EGCG的乳液亮度较大,颜色饱和度较大,与测定的色差参数相一致。综上所述,pH值2.0的乳液在贮藏期间的色差变化是由乳液中β-胡萝卜素含量不同引起的。
从表3可以得出,pH值7.0的β-胡萝卜素乳液在55℃贮藏之前,表征乳液亮度的L值、红色的a值、黄色的b值、色度的Cab值和色调的Hab值随着EGCG添加量的不同,没有显著性差异(P>0.05)。pH值7.0的β-胡萝卜素乳液贮藏7 d后的色差参数如表4所示。比较表3、4中乳液的色差参数可以得出,未添加EGCG的乳液在贮藏前后色差参数没有显著差异。但在贮藏期间,未添加EGCG乳液中β-胡萝卜素含量下降了16%,这可能是因为在pH值7.0的乳液中,β-胡萝卜素含量的减少不是引起色差改变的主要原因。
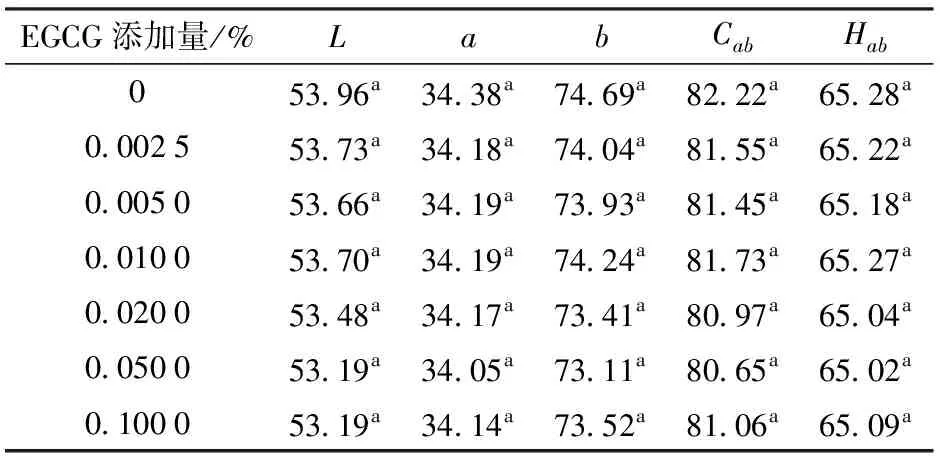
表3 pH值7.0 β-胡萝卜素乳液贮藏前色差参数Tab.3 Color parameters of β-carotene emulsions at pH value of 7.0 before storage

表4 pH值7.0 β-胡萝卜素乳液贮藏后色差参数Tab.4 Color parameters of β-carotene emulsions at pH value of 7.0 after storage
在添加了EGCG的β-胡萝卜素乳液中,随着EGCG添加量的增多,贮藏前后的色差参数差异逐渐增大。其中添加了0.100 0%EGCG的乳液中,贮藏7 d后,L值由53.19下降到44.86,a值由34.14下降到29.72,b值由73.52下降到60.37。由于贮藏后乳液a值和b值的下降,使得表征色度的Cab值差异达13.77,在色度表上有明显的改变。在此乳液中,贮藏7 d后只有7%的β-胡萝卜素发生了氧化。结合未添加EGCG的乳液结果,其中14%的β-胡萝卜素降解后,乳液色差未发生显著变化。因此,在pH值7.0的乳液中,β-胡萝卜素含量的改变不是引起色差参数变化的主要原因。随着EGCG添加量的增加,贮藏前后色差参数的差异逐渐增大,EGCG添加量可能是引起色差参数变化的原因。
从表4可以得出,随着EGCG添加量的增加,表征乳液亮度的L值、红色的a值、黄色的b值均呈减小趋势,说明β-胡萝卜素乳液的亮度降低,红色值减小同时黄色值减小。由于a值和b值的减小,色度发生了显著改变。图4中显示了贮藏7 d后,不同EGCG添加量的β-胡萝卜素乳液的感官差异(左边第1个是未贮藏的乳液,从左边第2个乳液开始EGCG添加量依次为0、0.002 5%、0.005 0%、0.010 0%、0.020 0%、0.050 0%、0.100 0%)与表4中色差参数的变化相符。

图4 55℃贮藏后不同EGCG添加量的pH值7.0 β-胡萝卜素乳液Fig.4 Photos of β-carotene emulsions with different concentrations of EGCG at pH value of 7.0 after storage at 55℃
由以上结果可以得出,在pH值2.0的乳液中,贮藏前后色差参数的变化主要是由β-胡萝卜素含量的变化引起;在pH值7.0的β-胡萝卜素乳液中,贮藏前后色差的变化与β-胡萝卜素含量的变化没有相关性,与EGCG 的添加量有关,这可能是因为EGCG在pH值7.0条件下,容易发生氧化反应,生成颜色较深的聚合物。因此,在pH值7.0条件下,将EGCG添加到β-胡萝卜素乳液中会影响乳液的色差。
2.3 界面EGCG含量
抗氧化剂的抗氧化效率一部分来源于其化学结构,另外其在体系中的作用位置也是影响其发挥作用的重要因素[13]。在油相体系中水溶性抗氧化剂的效果比油溶性抗氧化剂的效果好,这是因为水溶性抗氧化剂可以吸附在空气和水相的界面上,由于界面是发生氧化反应的主要位置,因此在界面上的抗氧化剂可以发挥更大的抗氧化作用;同理在水包油的乳液中,油溶性抗氧化剂的抗氧化效果比水溶性抗氧化剂的效果好[20-21]。因此,测定EGCG在界面上的含量对理解其抗氧化效率非常重要。
利用超高速离心法将水相中EGCG和油滴上EGCG进行分离,测定了吸附在油滴上的EGCG含量,结果如图5所示。从图中可以得出,pH值7.0 β-胡萝卜素乳液中界面EGCG含量高于pH值2.0乳液中的界面EGCG含量。图中不同小写字母表示pH值7.0的乳液中界面EGCG含量差异显著(P<0.05),不同大写字母表示pH值2.0的乳液中界面EGCG含量差异显著(P<0.05)。EGCG在pH值7.0的溶液中与蛋白的结合效率高于在酸性环境的溶液[22]。因此,在pH值2.0的β-胡萝卜素乳液中,结合到乳液界面上的EGCG较少。
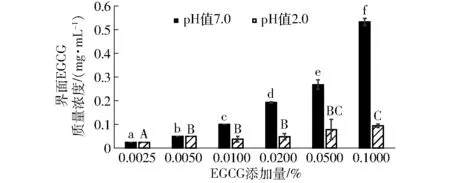
图5 胡萝卜素乳液中EGCG添加量对界面EGCG含量的影响Fig.5 Influence of EGCG on interfacial EGCG concentration of β-carotene emulsions
在pH值7.0的β-胡萝卜素乳液中,随着EGCG添加量的增加,界面EGCG含量逐渐增加。当EGCG添加量为0.002 5%~0.010 0%时,添加到乳液中的EGCG全部结合到界面上;当EGCG添加量为0.020 0%~0.100 0%时,结合到界面上的EGCG占总的EGCG添加量的百分比从96.8%降到53.3%。由此可得,当EGCG添加量为0.010 0%时,EGCG完全吸附到界面蛋白上,但随着EGCG添加量的继续增加,并不是所有的EGCG都吸附到界面上,还有游离在水相中的EGCG。
将界面EGCG的含量与乳液在贮藏过程中β-胡萝卜素的含量相结合可以得出,在pH值7.0的乳液中,界面EGCG含量高,在贮藏过程中β-胡萝卜素的保留率较高。而pH值2.0的β-胡萝卜素乳液中,结合在界面上的EGCG含量较少,β-胡萝卜素在贮藏过程中的保留率较低。这可能是因为结合在界面上的EGCG可以在β-胡萝卜素与水相之间形成一层屏障,因此,可以保护β-胡萝卜素不受来自水相中自由基及金属离子的催化,从而抑制β-胡萝卜素的降解。另外,在乳液中水油界面是发生氧化反应的主要位置,EGCG结合在界面上,使得其抗氧化效率提高,从而可以更加有效地保护β-胡萝卜素[13]。
将界面EGCG含量与色差变化联系可以得出,EGCG添加量对pH值7.0的乳液色差影响较大,这可能是因为在pH值7.0的乳液中,界面EGCG的含量较多,在贮藏过程中,界面EGCG发生氧化反应,使其颜色加深,进而影响作为芯材的β-胡萝卜素的显色,使其在贮藏前后的色差变化较大。而pH值2.0的β-胡萝卜素乳液中,界面EGCG含量较少,对β-胡萝卜素的显色影响不显著。
3 结论
(1)在pH值2.0和pH值7.0的β-胡萝卜素乳液中,EGCG均可作为抗氧化剂抑制β-胡萝卜素的降解。在贮藏过程中,随着EGCG添加量的增加,β-胡萝卜素保留率逐渐增大。在pH值2.0的乳液中β-胡萝卜素的降解速率比在pH值7.0的乳液中的降解速率快,这主要是因为在pH值2.0的乳液中,除了由自由基和金属离子催化的β-胡萝卜素降解反应以外,还有由酸引起的酸降解反应。同时pH值7.0的乳液中,界面EGCG含量高于pH值2.0的乳液,其发挥抗氧化的效率较高。
(2)在pH值2.0和pH值7.0的β-胡萝卜素乳液中,EGCG的添加对贮藏前β-胡萝卜素乳液的色差没有显著影响。贮藏7 d后,在pH值2.0的乳液中由于β-胡萝卜素含量在乳液中的保留率不同,使不同EGCG添加量的乳液色差产生较大差异;pH值7.0的乳液在贮藏7 d后,色差参数的差异不随β-胡萝卜素的保留率变化而变化,而与EGCG的添加量有关。
(3)界面EGCG含量直接影响β-胡萝卜素在乳液中的降解,并可能对乳液的色差产生影响。

