盐酸吗啡注射液安全性实验评价*
魏文芝,孙继超,朱从会,张敏娟,王天学
(1.青海省药品检验检测院,西宁 810016;2.青海省中藏药现代化研究重点实验室,西宁 810016;3.中国检验检疫科学研究院综合检测中心,北京 100123;4.青海省食品检验检测院,西宁 810000)
盐酸吗啡属于阿片类强效镇痛药,适用于其他镇痛药无效的急性锐痛,如严重创伤、战伤、烧伤及晚期癌症患者的三阶梯止痛等,是术后手术刺激痛、癌痛等中、重度疼痛镇痛药首选[1],盐酸吗啡注射液广泛应用于临床[2-5],其安全性研究笔者未见报道。盐酸吗啡有轻微的阿托品样作用,可引起心搏增快,逾量中毒时可出现呼吸减慢、浅表而不规则,发绀和嗜睡现象[6]。笔者参照《化学药物刺激性、过敏性和溶血性研究技术指导原则》《化学药物急性毒性实验技术指导原则》及相关文献[7-11],对盐酸吗啡注射液局部刺激性、全身过敏性、体外溶血性进行研究,报道如下。
1 材料与方法
1.1实验动物 健康、雄性、成年家兔,体质量2.0~2.5 kg;健康、雄性、成年豚鼠,体质量300~400 g;实验动物均购买自北京金牧阳实验动物养殖有限公司,实验动物生产许可证号:SCXK(京)2015-0005)。实验动物饲养环境温度为18~25 ℃,相对湿度为40%~70%,实验动物使用许可证号:SYXK(京)2011-0016。
1.2试药 盐酸吗啡注射液(东北制药集团沈阳第一制药有限公司,批号:150302-1,150701-1,150609-2,规格1 mL:10 mg),卵白蛋白(Sigma公司,批号:SLBL7392V),0.9%氯化钠溶液(晨欣药业股份有限公司,批号:1509191703),10%甲醛溶液(北京益利精细化学品有限公司)。
1.3仪器 电子称(广东香山衡器集团股份有限公司),赛多利斯BT25S电子天平(德国Sartorius公司,感量:0.1 mg),HH-1数显恒温水浴锅(金坛市华龙实验仪器厂),TDC-40B台式离心机(上海安亭科学仪器厂),奥林巴斯CX31生物显微镜(日本)。
1.4血管刺激性实验 参照文献[12-13]。取家兔4只,每只家兔耳缘静脉给药,采用同体左右侧自身对比法,左侧给药,右侧作为对照。设置受试物单一剂量组和阴性对照组,单次给药剂量为2.8 mg·kg-1,阴性对照组予溶媒(0.9%氯化钠溶液),给药频次为每天1次,连续给药3 d。给药后1,5 h,肉眼观察并记录给药血管局部变化,之后每天继续观察动物耳给药部位局部及周围血管情况,末次给药48 h后将家兔处死,取组织做病理检查,离注射点向心端1.0~2.5 cm取材(所取标本应包含有耳缘静脉),阴性对照组应取相应部位,用10%甲醛固定,制备石蜡切片并进行局部组织病理学检查。
1.5肌肉刺激性实验 参照文献[12-13]。取家兔4只,采用同体左右侧自身对比法。剪去两侧股四头肌部位的兔毛,用碘酊和乙醇消毒后分别在右侧股四头肌注入盐酸吗啡注射液,左侧股四头肌注入等量0.9%氯化钠注射液,作为对照,单次给药剂量为2.8 mg·kg-1,给药频次为每天1次,连续给药3 d,给药后5 h肉眼观察给药部位局部反应,如充血、红肿等。末次给药后48 h处死家兔,观察注射部位肌肉组织反应情况,量取充血范围,评价并计算反应级数。解剖并取出股四头肌,沿肌纤维平行方向切开肌肉,暴露注药部位,制备石蜡切片并进行局部组织病理学检查。
1.6全身过敏性实验 参照文献[12-13]。取豚鼠18只,随机分为3组,每组6只,设置盐酸吗啡注射液组、0.9%氯化钠注射液组、卵白蛋白组。盐酸吗啡注射液组给予盐酸吗啡注射液,单次给药剂量为2.8 mg·kg-1,卵白蛋白组给予卵白蛋白,单次给药剂量为50 mg·kg-1。采用隔日腹腔注射给药致敏,共给药3次,分别于末次给药后第14天,第21天采用一次性快速静脉注射盐酸吗啡注射液进行攻击。致敏期间每日观察动物症状,首次给药、末次致敏、激发前动物称定质量。激发后即刻观察动物反应至30 min,包括症状出现及消失时间,至少观察3 h,进行评价分级。
1.7溶血性实验 参照文献[12-13]。健康成年家兔,心脏穿刺兔血15 mL,放入含玻璃珠的三角烧瓶中振摇10 min,用玻璃棒搅动血液,除去纤维蛋白原。加入10倍量0.9%氯化钠溶液,摇匀,1500 r·min-1离心15 min,除去上清液,沉淀的红细胞再用0.9%氯化钠溶液按上述方法洗涤 2或3次,至上清液不显红色为止。将所得红细胞用0.9%氯化钠溶液配成2%混悬液,供实验用。取洁净试管7只,进行编号,1~5号管为供试品管,6号管为阴性对照管,7号管为阳性对照管。按要求加入2%红细胞悬液、0.9%氯化钠溶液或纯化水,配制各组反应体系,混匀后,立即置(37.0±0.5)℃恒温箱中进行温育,开始每隔15 min观察1次,之后间隔1 h观察1次,观察至3 h,并于24 h后观察溶血与红细胞凝聚现象。
2 结果
2.1血管刺激性实验 家兔单次耳缘给予供试品盐酸吗啡注射液后1,5 h时观察,均发现动物活动量明显减少,反应灵敏性降低;肉眼观察药物注射部位及远离注射处血管及组织,均未见出血、淤血、水肿等异常改变,与注射0.9%氯化钠注射液的对照侧耳部血管相比无明显差异,但受试组与阴性对照组均见静脉注射部位血管轻微充血,疑与受试物药效活性有关。末次给药后48 h,处死家兔,取两耳注射部位的血管及周围组织进行病理学检查,受试组与阴性对照组家兔耳缘静脉注射部位近端、中端、远端处血管内均未见血栓,血管内皮细胞未见肿胀、增生、血管外周围组织均未见出血。见图1。
2.2肌肉刺激性实验 给药后5,24,48 h,肉眼观察家兔肌肉注射给药部位局部反应,均未见充血、红肿等异常反应。末次给药后48 h处死家兔,解剖并取出股四头肌,沿肌纤维平行方向切开肌肉,暴露注药部位,制备石蜡切片并进行局部组织病理学检查,受试动物未见充血、变性、混合性炎症细胞浸润。1只动物(2号)0.9%氯化钠注射液对照左后肢股四头肌局灶性混合性炎性细胞浸润,其他3只动物左肢肌肉未见类似改变。见图2。
2.3全身过敏性实验 豚鼠全身过敏性实验结果显示,致敏期间各组动物饮食、活动等状态均无异常,未发现明显毒性体征,各组动物体质量差异无统计学意义。分别给予各组实验动物3次致敏后第14天激发,30 min内观察动物反应症状,0.9%氯化钠注射液组未见动物出现躁动、竖毛、搔鼻、流泪、痉挛等变态反应;盐酸吗啡注射液组发现1只动物出现躁动症状(反应级数为1),10 min后恢复正常,其他均未见任何过敏反应症状;卵白蛋白组激发后5 min内出现明显的呼吸困难、痉挛、直至死亡,剂量减半后仍然出现上述症状,并在10 min内死亡。上述结果表明盐酸吗啡注射液不会引起豚鼠全身过敏性反应。
2.4溶血性实验 本实验条件下,盐酸吗啡注射液未引起明显溶血或凝血现象,见表1。
3 讨论
在本次肌肉刺激性实验中,0.9%氯化钠注射液组1只动物右肢股四头肌发生的改变,因其发生率低,且见于对照股四头肌,分析与注射操作不当有关,与盐酸吗啡注射液本身特性无关。

A.近端;B.中端;C.远端
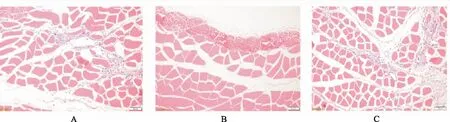
A.0.9%氯化钠注射液组左后肢(4号鼠);B.盐酸吗啡右后肢(4号鼠);C.0.9%氯化钠注射液组左后肢(2号鼠)

表1 盐酸吗啡注射液溶血性实验结果
“+”为溶血,“-”为无溶血,“±+”表示有轻微溶血现象
“+” hemolysis ;“-” no hemolysis; “±+” mild hemolysis
实验结果表明,盐酸吗啡注射液对家兔血管和肌肉无明显的刺激性,豚鼠全身过敏性实验未见变态反应,对家兔红细胞未见溶血或凝血作用,符合注射液安全用药要求,为临床安全用药提供理论依据,因其属于国家特殊管理的麻醉药品,同时具有治疗作用和依赖性,规范使用方可有效减少不良反应的发生,达到治疗目的。

