头孢妥仑匹酯有关物质的合成及其结构确证
朱希 高浩凌 范钢 盛力 沈大冬,*
(1 浙江省绍兴市食品药品检验研究院,绍兴 312071;2 浙江医药股份有限公司研究院,绍兴 312500)
头孢妥仑匹酯(cefditoren pivoxil)是日本明治制果株式会社研制的第四代头孢菌素类抗生素,具有广泛的抗菌作用,尤其对葡萄球菌属、肺炎链球菌等革兰阳性菌、大肠埃希菌、卡他布兰汉球菌、克雷伯菌属、变形菌属、流感嗜血菌等革兰阴性菌以及消化链球菌属、痤疮丙酸杆菌、拟杆菌属等厌氧菌有很强的抗菌力,其作用机制为抑制细菌细胞壁合成与各种细菌青霉素结合蛋白(PBP)的亲和性高,发挥杀菌作用[1-2]。药品中有关物质的种类和含量直接决定药品的安全性,为确保安全性,就要求对药品有关物质进行分析[3]。目前尚无文献报道头孢妥仑匹杂质的合成及其结构确证,仅有文献[4-5]通过LC-MS对其杂质的分析,本研究在课题研究的基础上[6-7],根据美国药典公布的头孢妥仑匹酯的杂质谱[8],通过化学法合成3个杂质(图1),并运用HMR、HRMS等分析方法对其结构进行详解,为质量研究和控制提供参考依据。
1 实验部分
1.1 仪器与试剂
仪器:Agilent1260高效液相色谱(美国Agilent公司)、AgilentTechnologies 6520液质联用仪(美国Agilent公司)、Bruker AvanceDMX400超导核磁共振仪(德国Bruker公司)、熔点仪(YRT-3,天大天发科技有限公司)。
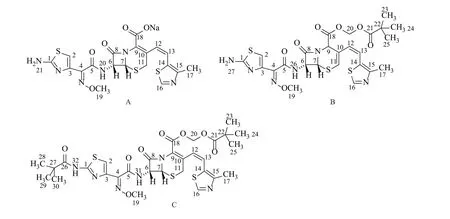
图1 杂质A、B、C的化学结构Fig.1 Chemical structure of the impurities A, B and C
试剂:7-氨基-3-(4-甲基噻唑基)-3-头孢环-4-羧酸(自制)、头孢妥仑匹酯(自制)、AE活性酯(百灵威科技有限公司),其他试剂均为AR。
1.2 HPLC方法
色谱柱:YMC-Pack ODS-AM(150mm×4.6mm,5μm);流动相为23mmol/L磷酸二氢钠水溶液(磷酸调pH至3.0):甲醇:乙腈=2:1:1(V/V/V);流速1.0mL/min;检测波长为254nm;柱温为30℃。
1.3 合成方法与结果
1.3.1 杂质A(头孢妥仑酸钠)的合成
反应瓶内加入THF(80mL)、7-氨基-3-(4-甲基噻唑基)-3-头孢环-4-羧酸(5.00g, 14.5mmol),室温滴加5%NaHCO3(50mL)溶液,搅拌至溶解澄清,加入AE活性酯(5.58g, 15.9mmol),室温反应5h,滴加丙酮(110mL),析出固体,过滤,用丙酮(50mL)洗滤饼,干燥得浅黄色固体A(6.40g,83.6%),mp. 197~200℃(文献[9]钠盐:195~200℃),纯度93.87%,HRMS,m/z:507.0578[M+H]+。
1.3.2 杂质B(Δ-3异构体)的合成
反应瓶中加入THF(50mL)、头孢妥仑匹酯(5.00g, 8.1mmol),搅拌溶解澄清后,加入浓氨水(2.0mL),45℃油浴反应12h,硅胶柱层析纯化(VDCM:VMeOH=20:1)得到2.4g粗品。粗品再由制备色谱柱分离提纯,得到白色固体B(2.12g, 42.4%),纯度90.63%,HRMS,m/z:621.1254[M+H]+。
1.3.3 杂质C(特戊酰胺取代物)的合成
反应瓶中加入THF(50mL)、头孢妥仑匹酯(5.00g, 8.1mmol),室温搅拌至溶解澄清,加入NaHCO3(2.30g),N2置换保护,转移至-10℃下,缓慢滴加特戊酰氯(2mL),搅拌30min,室温反应24h。加入纯化水(200mL),用乙酸乙酯(40mL×4)萃取,有机层用饱和食盐水(20mL×2)洗涤,无水Na2SO4干燥,硅胶柱层析纯化(VDCM:VMeOH=1:0~70:1)得到C(4.84g,84.7%),纯度95.38%,HRMS,m/z:705.1827[M+H]+。
2 结构确证
2.1 杂质A
外观为浅黄色固体,HRMS显示[M+H]+离子峰为507.0578,其熔点为197~200℃(文献[9]钠盐:195~200℃),推测分子式为C19H17N6O5S3Na。样品的1H NMR显示有17个氢[δ3.071(2H, dd)、δ1.193(2H, t)为杂质峰],其中有3个氢[δ9.670(1H, d,J=8.0Hz)、δ7.242(2H, s)]经D2O交换消失,为活泼氢。13C NMR和DEPT135°显示有19个碳[δ45.91、δ8.94为杂质峰],其中9个伯碳或叔碳、1个仲碳、9个季碳(表1~2)。
COSY谱中,仲氨质子氢δ9.670(1H, d,J=8.0Hz)与δ5.844(1H, dd,J=3.6, 4.8Hz)相关,δ5.844(1H, dd,J=3.6, 4.8Hz)与δ5.247(1H, d,J=5.2Hz)相关,结合HSQC谱,因此可将δ5.844(1H, dd,J=3.6, 4.8Hz)、δ5.247(1H, d,J=5.2Hz)分别归属为H-6、H-7,δ59.24、δ58.06分别归属为C-6、C-7;HMBC谱中,仲氨质子氢与δ163.27相关,H-6和H-7与δ164.05相关,可将δ163.27、δ164.05分别归属为C-5、C-8。
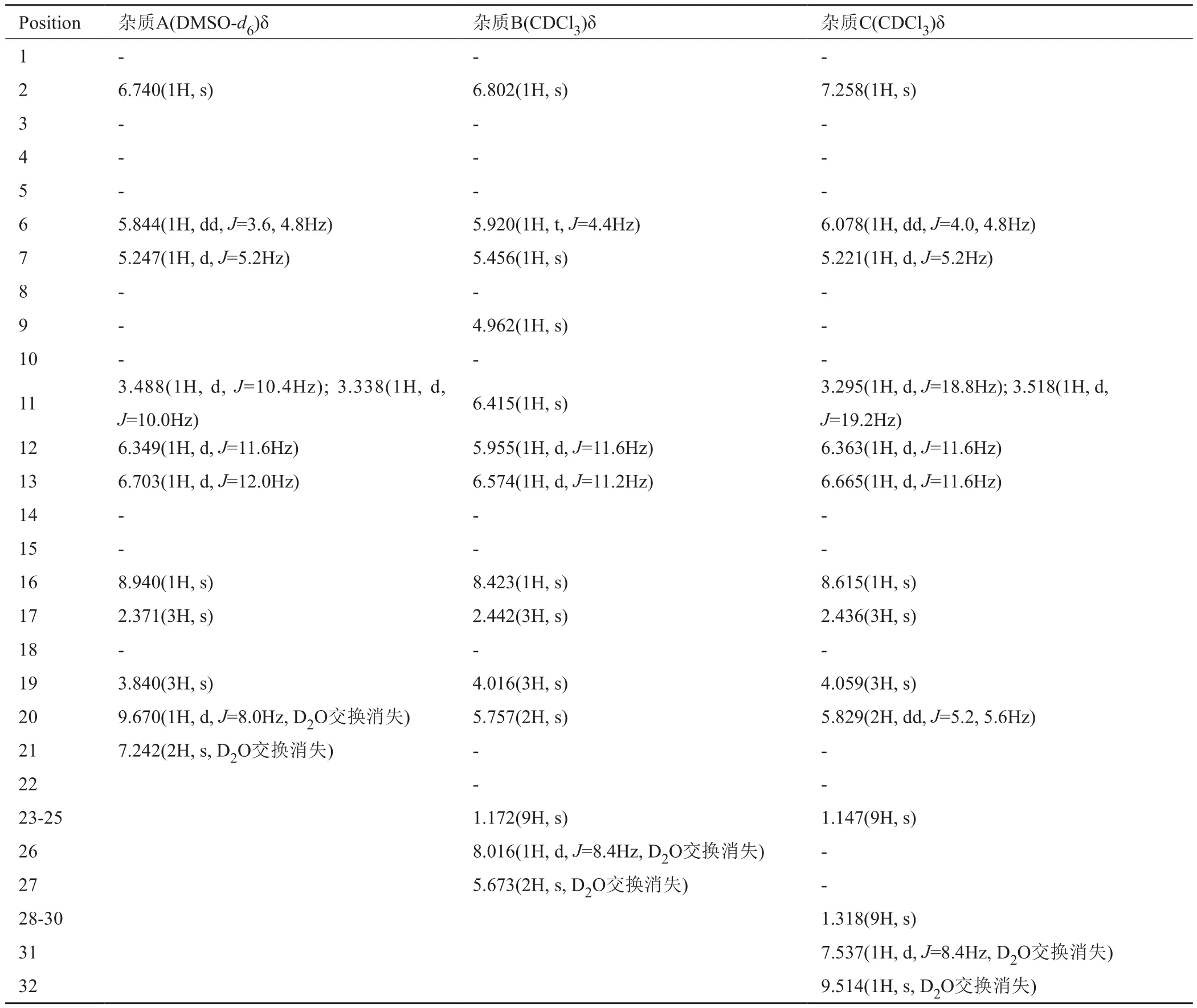
表1 杂质A、B、C氢谱数据Tab. 1 1H NMR data of the impurities A, B and C
HMBC谱中,甲基氢δ2.371(3H, s)、δ8.940(1H,s)分别与δ126.54、δ152.55都相关,另一甲基氢δ3.840(3H, s)没有相关的碳信号,可将δ2.371(3H,s)、δ8.940(1H, s)、δ3.840(3H, s)分别归属为H-17、H-16、H-19,结合HSQC谱可将δ15.74、δ153.49、δ62.38、δ126.54、δ152.55分别归属为C-17、C-16、C-19、C-14、C-15。
结合HSQC谱和COSY谱,仲碳(δ27.48)上的氢分裂为δ3.488(1H, d,J=10.4Hz)、δ3.338(1H, d,J=10.0Hz),可归属为H-11,δ27.48归属为C-11。COSY谱中,δ6.349(1H, d,J=11.6Hz)和δ6.703(1H, d,J=12.0Hz)相关,HMBC谱中,δ6.703(1H, d,J=12.0Hz)与C-14、C-15,可将δ6.349(1H, d,J=11.6Hz)、δ6.703(1H, d,J=12.0Hz)分别归属为H-12、H-13,结合HSQC谱,δ128.17、δ121.54分别归属为C-12、C-13;H-11、H-12、H-13与δ126.28、δ126.67都相关,可将δ126.28、δ126.67分别归属为C-9、C-10。
剩余氢δ6.740(1H, s)可归属为H-2,结合HSQC谱,δ109.40归属为C-2;HMBC谱中,H-2与δ168.87、δ149.44、δ143.00相关,由于H-2与δ149.44相关信号较弱,C-1位连接氨基,可将δ168.87、δ149.44、δ143.00分别归属为C-1、C-4、C-3。
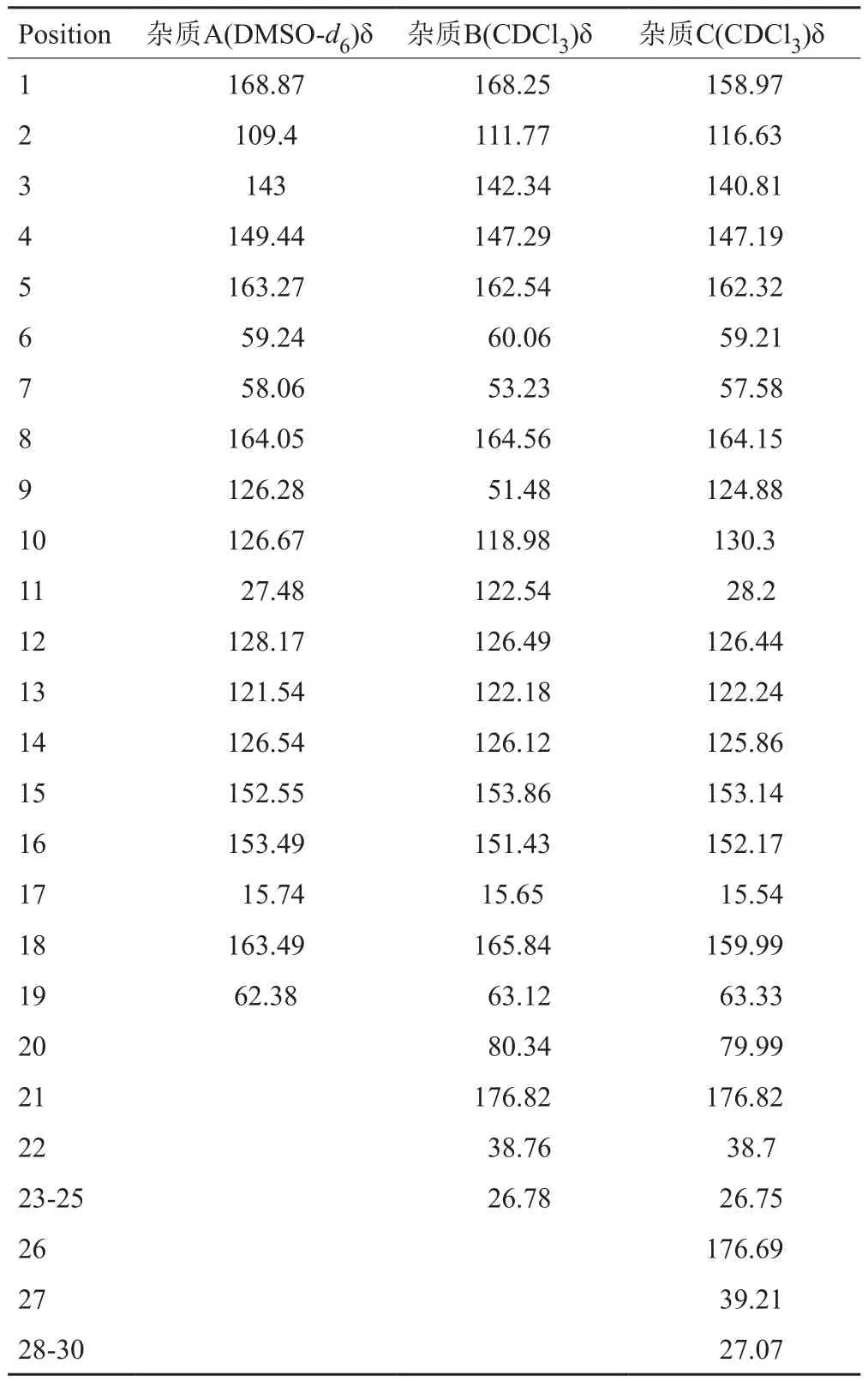
表2 杂质A、B、C碳谱数据Tab. 2 13C NMR data of the impurities A, B and C
2.2 杂质B
外观为白色固体,HRMS显示[M+H]+离子峰为621.1254,推测分子式为C25H28N6O7S3。样品的1H NMR显示有28个氢,其中有3个氢[δ8.016(1H, d,J=8.4Hz)、δ5.673(2H, s)]经D2O交换消失,为活泼氢。13C NMR和DEPT135°显示有23个碳,其中11个伯碳或叔碳、1个仲碳、11个季碳,HSQC谱显示δ1.172(9H, s)为单峰与δ26.78相关,可判断叔丁基碳信号叠加,因此该分子共有25个碳(表1~2)。
由HSQC谱可将δ1.172(9H, s)归属为H-23、H-24、H-25,δ26.78归属为C-23、C-24、C-25;HMBC谱图中,δ1.172(9H, s)与δ38.76、δ176.82相关,因羰基碳位于低场,可将δ38.76归属为C-22,δ176.82归属为C-21。仲碳δ80.34归属为C-20,δ5.757(2H, s)归属为C-20,再结合HSQC谱,δ5.757(2H, s)归属为H-20。
COSY谱中,仲氨质子氢δ8.016(1H, d,J=8.4Hz)与δ5.920(1H, t,J=4.4Hz)相关,δ5.920(1H, t,J=4.4Hz)与δ5.456(1H, s)相关,结合HSQC谱,因此可将δ5.920(1H, t,J=4.4Hz)、δ5.456(1H, s)分别归属为H-6、H-7,δ60.06、δ53.23分别归属为C-6、C-7;HMBC谱中,仲氨质子氢与δ162.54相关,H-6 和H-7与δ164.56相关,可将δ162.54、δ164.56分别归属为C-5、C-8。
HMBC谱中,δ2.442(3H, s)、δ8.423(1H, s)分别与δ126.12、δ153.86都相关,可将δ2.442(3H, s)、δ8.423(1H, s)分别归属为H-17、H-16,δ126.12、δ153.86分别归属为C-14、C-15;结合HSQC谱,可将δ15.65、δ151.43分别归属为C-17、C-16。
COSY谱中,δ5.955(1H, d,J=11.6Hz)与δ6.574(1H, d,J=11.2Hz)相关,结合HMBC谱,δ6.574(1H, d,J=11.2Hz)与C-14、C-15相关,可将δ5.955(1H, d,J=11.6Hz)、δ6.574(1H, d,J=11.2Hz)分别归属为H-12、H-13,结合HSQC谱,δ126.149、δ122.18分别归属为C-12、C-13。
HMBC谱中,C-12与δ4.962(1H, s)、δ6.415(1H,s)相关,δ4.962(1H, s)与低场碳δ165.84相关,可将δ4.962(1H, s)、δ6.415(1H, s)分别归属为H-9、H-11,δ165.84归属为C-18,结合HSQC谱,可将δ51.48、δ122.54分别归属为C-9、C-11。结合H-9和HMBC谱,可将δ118.98归属为C-10。
剩余的甲基氢δ4.016(3H, s)和δ6.802(1H, s)可分别归属为H-19、H-2,结合HSQC谱,可将δ63.12、δ111.77分别归属为C-19、C-2。HMBC谱中,C-2与δ168.25、δ142.34、δ147.29相关,C-1上连接氨基,可将低场碳δ168.25归属为C-1,由于C-2与δ142.34相关信号较强,因此可将δ142.34、δ147.29分别归属为C-3、C-4。
2.3 杂质C
外观为白色固体,HRMS显示[M+H]+离子峰为705.1827,推测分子式为C30H36N6O8S3。样品的1H NMR显示有36个氢,其中有2个氢[δ7.537(1H, d,J=8.4Hz)、δ9.514(1H, s)]经D2O交换消失,为活泼氢。13C NMR和DEPT135°显示有26个碳,其中12个伯碳或叔碳、2个仲碳、12个季碳,HSQC谱显示δ1.318(9H, s)、δ1.147(9H, s)为单峰分别与δ27.07、δ26.75相关,可判断叔丁基碳信号叠加,因此该分子共有30个碳(表1~2)。
HMBC谱中,δ1.318(9H, s)与δ176.69、δ39.21相关,δ1.147(9H, s)与δ176.82、δ39.21相关,仲碳δ5.829(2H, dd,J=5.2, 5.6Hz)与δ176.82、δ159.99相关,可将δ1.318(9H, s)归属为H-28、H-29、H-30,δ1.147(9H, s)归属为H-23、H-24、 H-25,δ176.82、δ176.69、δ159.99、δ39.21、δ39.21分别归属为C-21、C-26、C-18、C-27、C-21;结合HSQC谱,δ26.75归属为C-23、C-24、 C-25,δ27.07归属为C-28、C-29、 C-30。
COSY谱中,仲氨质子氢δ7.573(1H, d,J=8.4Hz)与δ6.078(1H, dd,J=4.0, 4.8Hz)相关,δ6.078(1H, dd,J=4.0, 4.8Hz)与δ5.221(1H, d,J=5.2Hz)相关,结合HSQC谱,因此可将δ6.078(1H, dd,J=4.0, 4.8Hz)、δ5.221(1H, d,J=5.2Hz)分别归属为H-6、H-7,δ59.21、δ57.58分别归属为C-6、C-7;HMBC谱中,仲氨质子氢δ7.573(1H, d,J=8.4Hz)与δ162.32相关,H-6 和H-7与δ164.15相关,可将δ162.32、δ164.15分别归属为C-5、C-8。
HMBC谱中,甲基氢δ2.442(3H, s)、δ6.665(1H, d,J=11.6Hz)、δ8.615(1H, s)分别与δ125.86、δ153.14都相关,COSY谱中,δ6.363(1H, d,J=11.6Hz)与δ6.665(1H,d,J=11.6Hz)相关,因此可将δ2.442(3H, s)、δ6.363(1H,d,J=11.6Hz)、δ6.665(1H, d,J=11.6Hz)、δ8.615(1H,s)分别归属为H-17、H-12、H-13、H-16,δ125.86、δ153.14分别归属为C-14、C-15;结合HSQC谱,可将δ15.54、δ126.44、δ122.24、δ152.17分别归属为C-17、C-12、C-13、C-16。
结合HSQC谱和COSY谱,仲碳(δ28.20)上的氢分裂为δ3.295(1H, d,J=18.8Hz)、δ3.518(1H, d,J=19.2Hz),可归属为H-11,δ27.48归属为C-11。HMBC谱中,H-11与δ124.88、δ130.30相关,H-12与δ124.88相关,H-13与δ130.30相关,可将δ124.88、δ130.30分别归属为C-9、C-10。
剩余氢δ7.258(1H, s)可归属为H-2,结合HSQC谱,δ116.63归属为C-2;HMBC谱中,H-2与δ158.97、δ147.19、δ140.81相关,由于H-2与δ147.19相关信号较弱,C-1位连接酰胺基,可将δ158.97、δ147.19、δ140.81分别归属为C-1、C-4、C-3。
3 讨论
头孢妥仑匹酯是临床上应用较广的抗生素,其有关物质非常复杂,仅美国药典公布的杂质谱就超过10个,目前除少数几种工艺杂质外,大多数杂质尚未对其进行结构确证,因此制备各种有关物质并进行确证对提高头孢妥仑匹酯的质量及其控制至关重要。本研究利用化学法合成得到3个杂质:头孢妥仑酸钠、Δ-3异构体、特戊酰胺取代物,并运用一维和二维核磁共振、质谱等检测方法对其碳氢信号进行了详细的解析和归属,为头孢妥仑匹酯的杂质研究和质量控制提供了参考。

