碱化插层二维过渡金属碳化物的制备及其对铀酰离子的电化学检测
樊懋, 王琳, 裴承新, 石伟群
碱化插层二维过渡金属碳化物的制备及其对铀酰离子的电化学检测
樊懋1, 王琳2, 裴承新1, 石伟群2
(1. 国民核生化灾害防护国家重点实验室, 北京 102205; 2. 中国科学院 高能物理研究所, 北京 100049)
二维过渡金属碳化物(MXenes)具有良好的电化学性能与辐照稳定性, 其在放射性核素电化学检测领域有潜在应用价值。本研究通过碱活化的方式处理碳化钛型MXene(Ti3C2T), 随后将钾插层的Ti3C2T(K-Ti3C2T)负载到玻碳电极(GCE)上得到K-Ti3C2T/GCE修饰电极。采用XRD、SEM、XPS等手段分别对Ti3C2T和K-Ti3C2T进行分析表征, 并进一步研究了K-Ti3C2T/GCE对痕量铀酰离子(UO22+)的电化学检测性能。循环伏安(CV)实验结果表明, 相比于GCE电极, K-Ti3C2T/GCE修饰电极对UO22+的电化学响应显著增强。进一步使用差分脉冲伏安法(DPV)扫描, 发现pH=4.0时, K-Ti3C2T/GCE修饰电极对UO22+在铀浓度0.5~10 mg/L范围内呈现良好的线性检测关系, 本方法的检测限为0.083 mg/L(S/N=3), 稳定性和重复性好。
铀酰离子; 碱化Ti3C2T; 电化学检测
铀是一种具有长寿命放射性与高化学毒性的锕系元素[1-2]。根据所处环境不同, 铀可以呈现出二价、三价、四价、五价、六价等多种氧化态, 而U(VI)是其在自然界中最常见的存在形式[3]。铀对于生态圈与人类健康造成的危害主要源自于U(VI)在环境中的扩散, 这是由于U(VI)相比于其他铀的低氧化种态水溶性和迁移能力显著增强。近年来随着我国核能和平利用的不断发展, 产生的大量含U(VI)放射性废水[4]进一步增加了铀在水体中扩散风险。而过多的铀进入人体会使肾脏结构受损, 可能导致急性肾功能衰竭, 此外还会增加患骨癌、肝癌和血液病的风险[5-7]。因此, 监测水系统中的痕量铀是非常必要, 对公众安全具有重要意义。
传统的铀含量检测方法主要有:激光诱导荧光法(LIF)[8]、X射线荧光光谱法(XRF)[9]、电感耦合等离子体质谱法(ICP-MS)[10]、原子光谱法(ETAAS)[11]、激光拉曼光谱法[12]以及电感耦合等离子体光发射光谱(ICP-OES)[5]。这些方法往往需要昂贵的仪器和复杂的操作, 不利于在小型实验室和现场中检测铀酰。电化学检测具有便携性好、灵敏度高、检测仪器简单和维护成本低等优点[13], 为在现场环境构建原位监测铀酰离子的便携式设备提供了可能性。
二维材料因其优异的电、热、力学和光学性能而受到广泛关注[14-15]。2011年, Naguib等[16]使用氢氟酸刻蚀法首次合成了一类新型二维过渡金属碳化物, 因其具有类似于石墨烯的层状结构而被称作MXene。MXene材料具有良好的导电性、亲水性和高比表面积[16-18], 被广泛用于锂离子电池[19]、超级电容器[20-21]等能源领域的应用研究。近期已有报道将MXene用于重金属离子和H2O2等的电化学检测[22-23]。同时, 由于MXene材料具有良好的耐辐照性和热稳定性, 在放射性核素的吸附去除领域展现了卓越的性能[3,24]。基于MXene材料的以上优点, 本工作开展了碱化处理的Ti3C2T对铀酰离子(UO22+)的电化学检测研究, 取得了初步成果。
1 实验方法
1.1 Ti3C2Tx的制备
将0.5 g Ti3AlC2粉体(纯度98wt%, 北京福斯曼科技有限公司, 实验前对原料进行了15mm过筛处理)缓慢加入20 mL 15wt% HF(稀释自40wt% HF), 混合物在40℃搅拌反应48 h。将产物5000 r/min离心并水洗6次, 抽滤后转移至真空干燥箱, 50℃真空干燥12 h, 得到多层Ti3C2T。
1.2 碱化K-Ti3C2Tx的制备
将50 mg Ti3C2T分散在20 mL 1 mol/L的KOH溶液中, 室温下磁力搅拌24 h。得到的悬浊液经离心、水洗、抽滤后转移至真空干燥箱, 50℃真空干燥12 h, 得到K-Ti3C2Tx。
1.3 K-Ti3C2Tx/GCE修饰电极的制备
每次实验前, 用1和0.05 μm的氧化铝抛光粉依次对玻碳电极(GCE, 3 mm)进行打磨, 使GCE表面呈现镜面。分别使用HNO3(1 : 1,/)、乙醇和水对抛光后的GCE超声5 min, 清洗掉电极表面的残留杂质。取4 mg制备的碱化K-Ti3C2T固体分散在4 mL乙醇中, 加入80 μL Nafion溶液(5wt%), 超声分散均匀。取4 μL的K-Ti3C2T滴涂在GCE上, 自然晾干后得到修饰电极K-Ti3C2T/GCE。
1.4 表征与测试
使用Hitachi S-4800场发射扫描电镜(SEM)观测MXene材料碱处理前后的表面形貌。通过Bruker D8 Advance 粉末X射线衍射(XRD)仪对MXene样品的特征衍射峰和晶面间距进行表征。测试条件:CuKα靶,= 0.15406 nm, 步长为0.02°。利用Thermo Scientific ESCALAB 250Xi 型X射线光电子能谱(XPS)仪对碱化处理前后MXene的表面化学组分进行测定。使用Autolab PGSTAT 302N (Metrohm, Inc)型电化学工作站对铀酰离子的电还原信号进行采集。
实验采用常规三电极体系进行电化学测量, 其中K-Ti3C2T/GCE修饰电极为工作电极, 铂电极为对电极, 自制银/氯化银电极(Ag/AgCl)作为参比电极。电位设置通过NOVA 1.10软件控制。实验在20 mL的石英杯中进行, 以0.01 mol/L NaCl作为支持电解质, 根据需要加入适当浓度的铀酰离子溶液, 每次测试前预调pH, 随后使用氩气通气5 min, 去除溶液中的氧。测试过程中保持液面上方的氩气氛围, 通过电化学工作站的循环伏安模块(CV)和差分脉冲模块(DPV)对溶液中的UO22+进行电化学检测。
2 结果与讨论
2.1 XRD表征
如图1所示, 经过HF刻蚀之后, 母体材料Ti3AlC2在39.01°处的特征峰消失, 这证明了HF成功将Ti3AlC2刻蚀完全[16]。刻蚀后Ti3C2T的(002)峰由9.56°左移至8.85°, 对应的片层材料轴晶格常数(-LP)由1.849 nm增加到1.997 nm。经过KOH处理后的K-Ti3C2T(002)峰左移至6.92°,-LP增大至2.595 nm, 这证明碱活化处理后K离子进入到MXene的层间, K离子的插层作用进一步扩大了Ti3C2T的层间距。
2.2 SEM形貌分析
使用SEM观测了Ti3AlC2以及K离子插层前后Ti3C2T的形貌(图2)。原始的Ti3AlC2颗粒表现出了紧密排列的层状结构(图2(a))。Ti3AlC2在经过48 h HF蚀刻后, 出现了明显的分层, 得到的Ti3C2T呈现出手风琴状的层状结构(图2(b)和(c))。从图2(d)中可以看到, 经过KOH插层活化后的K-Ti3C2T宏观多层堆叠结构保持不变, 但其微观表面被绒毛状纳米颗粒所覆盖, 这表明在KOH的插层过程中, Ti3C2T高活性表面可能发生了部分氧化。
2.3 XPS分析
使用XPS对K+插层前后Ti3C2T表面的化学成分进行分析, 全谱扫描(图3(a))表明Ti3C2T样品中含有Ti、O、C和F元素, 碱活化处理后在293和377 eV处出现了K2p与K2s的特征峰, 证明了K离子的成功插层。对Ti2p的高分辨XPS谱进行分峰拟合, 如图3(b)所示, 发现454.89、455.78、456.9和458.6 eV分别对应于Ti–C、Ti2+、Ti3+、Ti(IV)–O的Ti2p3/2特征峰, 460 eV以后则为相应的Ti2p1/2特征峰[23]。可以看出原始Ti3C2T样品中的Ti以低价种态为主, 而Ti(IV)–O的含量很少。经KOH处理后K-Ti3C2T中低价Ti种态减少, Ti(IV)–O特征峰所占比例显著增加, 并且其峰位与TiO2的Ti–O键结合能数值非常接近[24]。而O1s高分辨XPS图谱(图3(c)也表明碱活化后样品中的氧含量有所增加。以上结果确认了KOH处理使得Ti3C2T样品表面部分氧化, 结合之前的SEM结果, 可推知K-Ti3C2T表面形成了少量TiO2纳米颗粒[25]。

图1 Ti3AlC2、Ti3C2Tx、K–Ti3C2Tx三种材料的XRD图谱

图2 三种材料的SEM照片
(a) Ti3AlC2; (b) Ti3C2T; (c) Enlarged view of Ti3C2T; (d) K-Ti3C2T
2.4 UO22+在修饰电极上的循环伏安行为
2.4.1 电化学响应增益
分别使用GCE、Ti3C2T修饰的玻碳电极(Ti3C2T/GCE)以及K-Ti3C2T/GCE在pH=4, –0.6~–0.1 V的电位范围内, 对50 mg/L的U(VI)进行循环伏安扫描, 扫速为100 mV/s, 每组进行10次平行扫描(图4所示)。玻碳电极上UO22+在–0.35 V的电位出现微弱的还原峰信号(图4(A)中(b)所示), 经确认为U(VI)向U(V)转化的还原特征峰[26]。使用硝酸钠代替硝酸铀酰进行空白实验, 在循环伏安扫描范围内未检出氧化还原峰, 表明阴离子对于铀酰离子的检测无显著影响。Ti3C2T/GCE修饰电极由于多层Ti3C2T的电容效应[20], 遮盖了电极对UO22+的还原峰信号(图4(B)所示)。而K-Ti3C2T/GCE修饰电极相较于纯玻碳电极, 出现了更强的还原峰(图4(A)中(c)所示)。K-Ti3C2T/GCE对U(VI)具有更高的电化学响应主要原因如下: (1)相比于GCE, K-Ti3C2T自身的多层结构使其具有更大的比表面积以及更多的吸附位点; (2)K-Ti3C2Tx表面带有负电荷[27],有利于UO22+阳离子的预吸附富集; (3)K离子的插层提高了Ti3C2T的层间稳定性[28], 从而有效抑制循环伏安扫描时电解质进出MXene层间产生的电容效应; (4)已有研究表明Ti-O键对重金属离子以及锕系离子具有较强的配位作用[27,29], 碱活化处理使MXene表面的Ti-O和Ti-OH端基含量增加(图3(c)), 并且形成了部分的纳米TiO2[25], 提供了更多的UO22+活性配位位点, 从而提高了电化学响应的选择性。
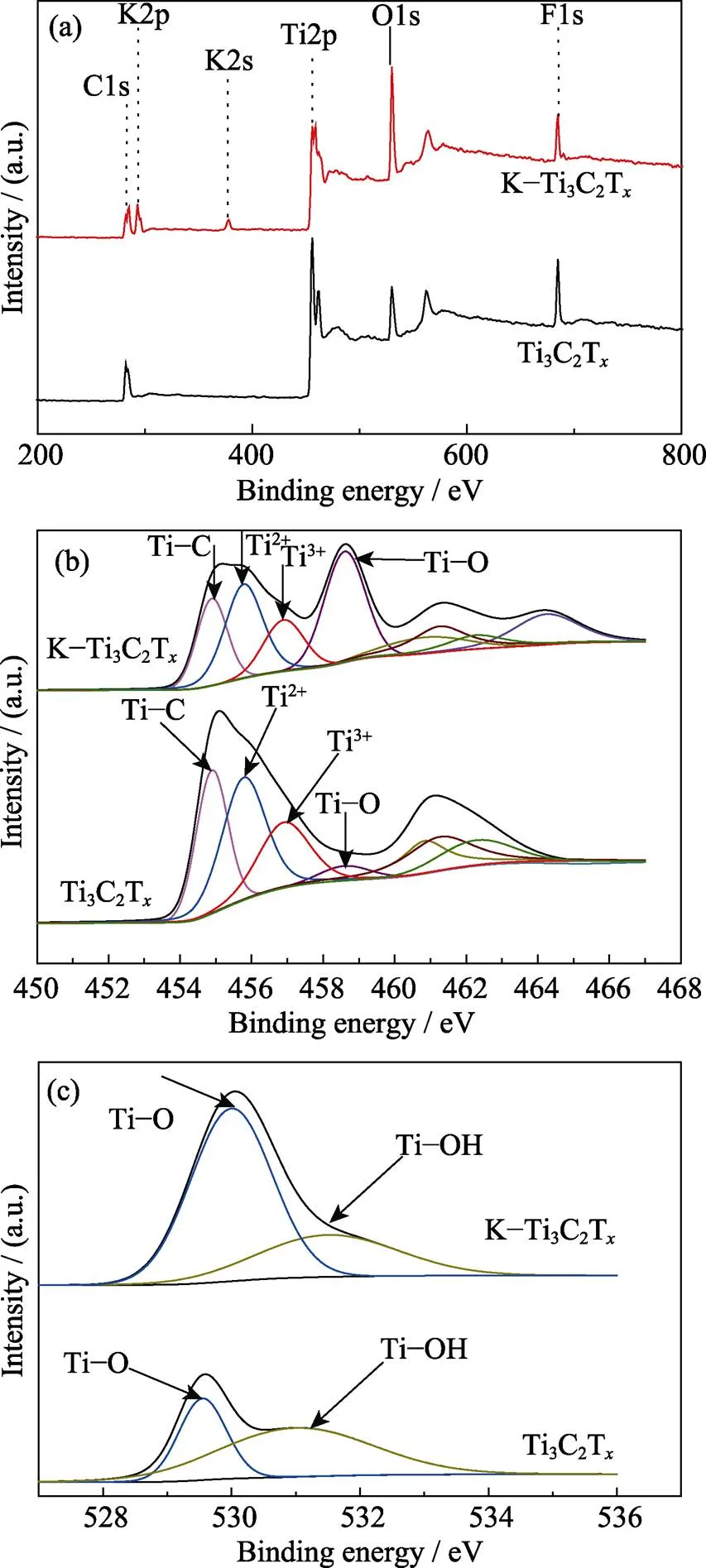
图3 (a) Ti3C2Tx和K-Ti3C2Tx的XPS光谱图, (b)Ti3C2Tx和K-Ti3C2Tx的Ti2p高分辨图, (c)Ti3C2Tx和K-Ti3C2Tx的O1s高分辨图
2.4.2 pH的影响
将修饰电极在0.01 mol/L的NaCl溶液中, 用50 mV/s的扫速, 分别在pH为3、4和5的条件下, 对50 mg/L的U(VI), 在–0.6~0.2V电位区间内进行循环伏安(CV)扫描。如图5结果显示, 在pH为4的条件下, 修饰电极K-Ti3C2T/GCE对UO22+具有较好的响应, 峰电流大, 还原峰明显。当pH升高到5时, 还原峰电流降低, 这可能与高pH下溶液中部分铀酰离子以(UO2)2(OH)22+、(UO2)3(OH)5+等多核种态的形式存在, 不利于U(VI)的电化学还原有关。当pH降低到3时, 背景电流增大使得还原峰的峰型变得不再尖锐, 不利于U(VI)还原峰的检测。由于H+的离子半径很小, 更易在MXene层间扩散迁移, 低pH下溶液中H+浓度显著增加, 从而导致循环伏安扫描所引起的电容效应背景电流增大。因此, 选择pH=4作为UO22+检测的最佳pH。

图4 UO22+在不同电极上的循环伏安(CV)响应
(A) (a) K- Ti3C2T/GCE, [U]=0 mg/L, (b) GCE, [U]= 50 mg/L, (c) K Ti3C2T/GCE, [U]=50 mg/L; (B) Ti3C2T/GCE, [U]= 50 mg/L
2.4.3 不同扫速下循环伏安图
修饰电极在0.01 mol/LNaCl, pH=4.0, 在–0.6~ 0.2 V电位区间, 以不同扫速对50 mg/L的U(VI)进行循环伏安扫描。如图6(a)所示, 在0.01~0.1 V/s的范围内, 氧化峰和还原峰的大小均与扫速的平方根成正比, 如图6(b)所示, 其相关系数分别为0.997和0.999, 说明此时的电极过程主要受扩散控制, 电极表面发生氧化还原反应。
2.5 差分脉冲伏安(DPV)对U(VI)的测定
2.5.1 U(VI)标准曲线
基于以上的测试结果, 本课题组在pH为4, 电解质为0.01 mol/L的NaCl中, 在–0.6~–0.1 V的电位范围, 使用差分脉冲伏安法(DPV)对UO22+的还原峰进行电化学检测。结果显示, 在–0.35 V左右的电位时, 出现UO22+的还原峰, 这与循环伏安(CV)的结果相吻合。进一步研究发现, 在0.5~10 mg/L铀浓度范围内, 修饰电极对U(VI)呈现良好的线性关系, 标准曲线为(μA)=0.4356(mg/L)+3.7375, 相关系数2=0.997(图7所示)。对同一空白对照溶液平行测量10次, 计算空白溶液的标准偏差, 并以3倍空白溶液的标准偏差作为检出限, 计算方法的检测限为0.089 mg/L(S/N = 3)。

图5 pH对K- Ti3C2Tx /GCE检测UO22+的影响

图6 K-Ti3C2Tx GCE于0.01 mol/L pH=4.0的NaCl中对UO22+的循环伏安扫描结果, 扫描速度为10~100 mV/s, [U]=50 mg/L
(a) CV curves; (b) Plots of peak currentsscan speed

图7 K-Ti3C2Tx/GCE对UO22+的DPV扫描结果, pH=4.0, [U]=0.5~10 mg/L
Fig 7 Differential pulse voltammetry (DPV) results of UO22+/ (K-Ti3C2T/GCE), pH =4.0, [U]=0.5-10 mg/L
(a) DPV curves; (b) Plots of peak currentsconcentration of uranium
2.5.2 实际样品测试
选取实验室中的自来水作为空白水体, 加0.01 mol/L氯化钠作为支持电解液, 加入5 mg/L的U(VI), 进行实际测试。用上述测试方法中的差分脉冲伏安法(DPV)进行测试分析, 记录还原峰电流, 通过标准曲线得到测量的水体中铀的浓度。对样品平行测试3次, 自来水中样品的测试结果如下表1。自来水中铀浓度的测试结果为5.30 mg/L, 相对标准方差为1.32%, 表明测试方法的准确性和稳定性好, 可以应用于实际水体中痕量铀的定量检测。
2.5.3 回收率、稳定性和重现性
以1 mg/L的U(VI)溶液作为底液, 按上述样品分析步骤进行回收率测试, 测试结果列于表2。四次加标回收率在93%~103%之间, 同时每个浓度三个平行测试得到的RSD小于2%, 表明K-Ti3C2T电极对U(VI)的检测结果具有良好的可靠性。用修饰电极对5 mg/L的U(VI)溶液进行连续10次的差分脉冲伏安法扫描, 十次测定的还原峰的电流的相对标准偏差为1.9%, 说明测试过程的电流响应重现性良好。将同一批次的K-Ti3C2T材料在4℃下保存, 放置一个月后, 制备的修饰电极K-Ti3C2T/GCE对5 mg/L的U(VI)使用差分脉冲伏安法DPV进行扫描, 结果显示UO22+的还原峰电流保持在95%以上, 说明材料具有很好的稳定性。

表1 自来水中样品的分析结果

表2 K-Ti3C2Tx/GCE电极对U(VI)的回收率结果
3 结论
使用HF刻蚀法和碱化插层后处理的方法, 分别得到了Ti3C2T和钾离子插层的K-Ti3C2T两种二维层状MXene材料。循环伏安扫描结果显示, K-Ti3C2T对玻碳电极的修饰可以显著提高对UO22+的电化学响应, 这是由于Ti3C2T本身具有良好的导电性、较大的比表面积以及负的表面电荷。同时碱化过程使得Ti3C2T表面Ti-O/Ti-OH端基含量增加, 并且生成了部分TiO2纳米颗粒, 从而进一步增加U(VI)活性配位位点。此外, K离子在Ti3C2T层间的插层消除了Ti3C2T自身电容效应的干扰。DPV结果显示, K-Ti3C2T/GCE修饰电极在铀含量0.5 mg/L至10 mg/L范围内, 对UO22+的还原峰和峰电流呈现良好的线性关系, 为(A)=0.4356(mg/L)+3.7375, 相关系数2=0.997, 检测限为0.083 mg/L (S/N = 3), 可靠性、稳定性和重复性好, 有望应用于水体中痕量铀的定量检测。
[1] LI J, WANG X, ZHAO G,. Metal–organic framework-based materials: superior adsorbents for the capture of toxic and radioactive metal ions., 2018, 47(7): 2322–2356.
[2] HONGWEI P, XIANGXUE W, WEN Y,Removal of radionuclides by metal oxide materials and mechanism research., 2017, 48(1): 58–73.
[3] SANTOS J S, TEIXEIRA L S G, DOS SANTOS W N L,Uranium determination using atomic spectrometric techniques: an overview., 2010, 674(2): 143–156.
[4] WANG L, YUAN L, CHEN K,Loading actinides in multilayered structures for nuclear waste treatment: the first case study of uranium capture with vanadium carbide MXene., 2016, 8(25): 16396–16403.
[5] JAMALI M R, ASSADI Y, SHEMIRANI F,. Synthesis of salicylaldehyde-modified mesoporous silica and its application as a new sorbent for separation, preconcentration and determination of uranium by inductively coupled plasma atomic emission spectrometry.,2006, 579(1): 68–73.
[6] Mehra R, Singh S, Singh K. Uranium studies in water samples belonging to Malwa region of Punjab, using track etching technique., 2007, 42(3): 441–445.
[7] Zikovsky L. Determination of uranium in food in Quebec by neutron activation analysis., 2006, 267(3): 695–697.
[8] Kumar S A, Shenoy N S, Pandey S,. Direct determination of uranium in seawater by laser fluorimetry., 2008, 77(1): 422–426.
[9] Misra N L, Dhara S, Mudher K D S. Uranium determination in seawater by total reflection X-ray fluorescence spectrometry., 2006, 61(10/11): 1166–1169.
[10] Avivar J, Ferrer L, Casas M,Fully automated lab-on-valve-multisyringe flow injection analysis-ICP-MS system: an effective tool for fast, sensitive and selective determination of thorium and uranium at environmental levels exploiting solid phase extraction., 2012, 27(2): 327–334.
[11] Kumar M, Rathore D P S, Singh A K. Pyrogallol immobilized Amberlite XAD-2: a newly designed collector for enrichment of metal ions prior to their determination by flame atomic absorption spectrometry., 2001, 137(3/4): 127–134.
[12] Cho H R, Jung E C, Cha W,Quantitative analysis of uranium in aqueous solutions using a semiconductor laser-based spectroscopic method., 2013, 85(9): 4279–4283.
[13] Zhang L, WanG C Z, Tang H B,Rapid determination of uranium in water samples by adsorptive cathodic stripping voltammetry using a tin-bismuth alloy electrode., 2015, 174: 925–932.
[14] Ahmed S, Yi J. Two-dimensional transition metal dichalcogenides and their charge carrier mobilities in field-effect transistors., 2017, 9(4): 50-1-23.
[15] Xiao J, Zhang Y, Chen H,Enhanced performance of a monolayer MoS2/WSe2heterojunction as a photoelectrochemical cathode., 2018, 10(4): 60-1-9.
[16] Naguib M, Kurtoglu M, Presser V,Two-dimensional nanocrystals produced by exfoliation of Ti3AlC2., 2011, 23(37): 4248–4253.
[17] Lukatskaya M R, Mashtalir O, Ren C E,Cation intercalation and high volumetric capacitance of two-dimensional titanium carbide., 2013, 341(6153): 1502–1505.
[18] Mashtalir O, Naguib M, Mochalin V N,. Intercalation and delamination of layered carbides and carbonitrides., 2013, 4: 1716-1-7.
[19] Zhou J, Zha X, Zhou X,Synthesis and electrochemical properties of two-dimensional hafnium carbide., 2017, 11(4): 3841–3850.
[20] Li H, Hou Y, Wang F,. Flexible all-solid-state supercapacitors with high volumetric capacitances boosted by solution processable MXene and electrochemically exfoliated graphene., 2017, 7(4): 1601847–1–6.
[21] Luo J, Zhang W, Yuan H,Pillared structure design of MXene with ultralarge interlayer spacing for high-performance lithium-ion capacitors., 2017, 11(3): 2459–2469.
[22] Lorencová L, Bertok T, Dosekova E,Electrochemical performance of Ti3C2TMXene in aqueous media: towards ultrasensitive H2O2sensing., 2017, 235: 471–479.
[23] Zhu X, Liu B, Hou H,. Alkaline intercalation of Ti3C2MXene for simultaneous electrochemical detection of Cd (II), Pb (II), Cu (II) and Hg (II)., 2017, 248: 46–57.
[24] Bonato M, Allen G C, Scott T B. Reduction of U(VI) to U(IV) on the surface of TiO2anatase nanotubes., 2008, 3(2): 57–61.
[25] Liu Y, Du H, Zhang X,. Superior catalytic activity derived from a two-dimensional Ti3C2precursor towards the hydrogen storage reaction of magnesium hydride., 2016, 52(4): 705–708.
[26] Kaneto K, Bidan G. Electrochemical recognition and immobilization of uranyl ions by polypyrrole film doped with calix [6] arene., 1998, 331(1/2): 272–278.
[27] Wang L, Tao W, Yuan L,Rational control of the interlayer space inside two-dimensional titanium carbides for highly efficient uranium removal and imprisonment., 2017, 53(89): 12084–12087.
[28] Osti N C, Naguib M, Ostadhossein A,Effect of metal ion intercalation on the structure of MXene and water dynamics on its internal surfaces., 2016, 8(14): 8859–8863.
[29] Peng Q, Guo J, Zhang Q,. Unique lead adsorption behavior of activated hydroxyl group in two-dimensional titanium carbide., 2014, 136(11): 4113–4116.
Alkalization Intercalation of MXene for Electrochemical Detection of Uranyl Ion
FAN Mao1, WANG Lin2, PEI Cheng-Xin1, SHI Wei-Qun2
(1. State Key Laboratory of NBC Protection for Civilian, Beijing 102205, China; 2. Institute of High Energy Physics, Chinese Academy of Sciences, Beijing 100049, China)
Given the good electrochemical performance and excellent irradiation stability of two dimensional transition metal carbides (MXenes), the development of MXene-based electrode materials for radionuclide detection is very promising. In this work, Ti3C2TMXene was activatedan alkalization strategy to form K+intercalated Ti3C2T(K-Ti3C2T). Then the modified electrode of K-Ti3C2T/GCE was prepared on glassy carbon electrode (GCE). Ti3C2Tand K-Ti3C2Twere characterized by XRD, SEM and XPS techniques, and the electrochemical detection performance of K-Ti3C2T/GCE for trace uranyl ion (UO22+) was further investigated. Cyclic voltammetry (CV) experiments showed that the electrochemical response of K-Ti3C2T/GCE modified electrode to UO22+increased significantly. Under the differential pulse voltammetry (DPV) scanning at pH 4.0, the K-Ti3C2T/GCE modified electrode presented a good linear detection relationship for UO22+in the uranium concentration range of 0.5-10mg/L. The detection limit of this method is 0.083 mg/L (S/N = 3), with decent stability and repeatability.
uranyl ion; alkalization of Ti3C2T; electrochemical detection
1000-324X(2019)01-0085-06
10.15541/jim20180232
TQ174
A
2018-05-17;
2018-07-19
国家自然科学基金(21577144, 11675192, 21790373) National Natural Science Foundation of China (21577144, 11675192, 21790373)
樊懋(1994–), 男, 硕士研究生. E-mail: fanmao@ihep.ac.cn
石伟群, 研究员. E-mail: shiwq@ihep.ac.cn

