硝普钠对生姜根茎抗氧化酶和苯丙烷途径的影响
李 雪,葛永红,2,*,李灿婴,2,段 斌,魏美林,唐 琦,陈延儒
(1.渤海大学食品科学与工程学院,辽宁锦州 121013;2.生鲜农产品贮藏加工及安全控制技术国家地方联合工程研究中心,辽宁锦州 121013)
姜(ZingiberofficinaleRosc.),别名生姜、白姜,是一种多年生草本植物,有芳香及辛辣味,是全世界许多国家所喜爱的香辛植物原料之一,主要以鲜食为主[1-2]。生姜具有抗菌、抗氧化等作用[3]。鲜姜对低温敏感、不易保存,贮藏温度一般控制在20 ℃左右[3],贮藏过程中极易发生冷害和腐烂变质,也极易失去水分而品质劣变[1]。因此研究安全、有效、广谱的新型保鲜方法迫在眉睫。
研究表明,NO能明显延缓梨和荔枝果实失重、果皮颜色变化、病原菌侵染等[4-5],且对抗氧化保护系统的酶活性具有调节作用[6]。苯丙氨酸解氨酶(PAL)和4-香豆酸/辅酶A连接酶(4CL)是苯丙烷代谢途径的关键酶[7]。通过此途径积累的酚类化合物,黄酮类和木质素等可以增强细胞壁,从而增强果实的抗病性。NO能够延缓蘑菇和芒果果实的成熟衰老[8-9],可诱导提高草莓果实苯丙烷代谢关键酶的活性[10],能明显诱导甜瓜果实O2-的产生速率和H2O2的快速积累,明显提高贮藏期间甜瓜果实超氧化物歧化酶(SOD)和过氧化物酶(POD)的活性[11],且提高了高温胁迫下姜叶活性氧代谢[12]。硝普钠(SNP)常被用作NO供体,用SNP溶液浸泡能够摆脱果实进行NO处理所需无氧条件的束缚,且浸泡处理更有效[13]。已有研究表明,SNP处理提高了西兰花中过氧化氢酶(CAT),抗坏血酸过氧化物酶(APX),谷胱甘肽还原酶(GR)和POD的活性,延长了保质期[14];采前SNP处理通过抑制桃果实的乙烯产量,维持硬度和抗坏血酸含量以及增强抗氧化酶活性来增加耐寒性进而延长货架期[15];SNP处理可有效降低香蕉皮的黄腐病和鲜重,降低可滴定酸和抗坏血酸含量,抑制可溶性蛋白质和可溶性固形物含量的增加,达到保鲜目的[16]。但SNP对生姜根茎采后贮藏保鲜效果的作用尚不明确。
本研究以生姜根茎为试材,采后用不同浓度SNP常温(20±2 ℃)浸泡处理,研究其对呼吸强度和失重率的影响,以此筛选最佳浓度,同时探讨最佳浓度SNP处理对H2O2积累及主要清除酶活性、苯丙烷代谢关键酶活性和产物积累的影响,以期为SNP在生姜根茎保鲜中的应用提供理论依据。
1 材料与方法
1.1 材料与仪器
生姜(ZingiberofficinaleRosc)根茎 辽宁省锦州市北镇市,选取质地优良姜体肥大、色泽土黄、无病虫害、表皮完整、无擦划伤口的生姜,纸箱包装当天运回实验室处理;硝普钠(SNP) 由天津市科密欧化学试剂开发中心提供(分析纯);Tris(纯度99.9%)、辅酶A(≥99%)、氮蓝四唑、ATP 北京索莱宝科技有限公司。
H2050R型高速冷冻离心机 湘仪离心机仪器有限公司;UV-1081紫外/可见分光光度计 北京瑞利分析仪器有限公司;JA5003电子天平 上海舜宇恒平学科学仪器有限公司;A 11 basic 研磨机 德国IKA集团;HH-4 单列四孔水浴锅 常州国宇仪器制造有限公司;Forma 702型-80 ℃超低温冰箱 美国Thermo公司。
1.2 实验方法
1.2.1 SNP处理及贮藏 选择无机械损伤和病虫害的生姜,先用1%次氯酸钠消毒1 min,然后分别用0.25、0.5、1.0 mmol/L SNP溶液(含0.01% Tween 20)浸泡处理10 min,以清水处理为对照。自然晾干后20 ℃,RH 55%~60%,避光贮藏待用。
1.2.2 呼吸强度测定 在生姜根茎贮藏第0、3、6、9、12、15、18 d后取不同浓度SNP处理和对照生姜5块,分别称重后装入自封袋中,密封保存1 h后用便携式CO2分析仪测定CO2浓度。呼吸强度以单位时间内单位重量的生姜根茎消耗产生CO2的量表示mL/(h·kg)。
1.2.3 失重率测定 生姜根茎贮藏第0、3、6、9、12、15、18 d称重。不同浓度SNP处理和对照每次称重用生姜5块,重复3次。质量损失率(%)=(每次称重量-原始重量)×100/原始重量。
1.2.4 取样 分别于SNP和清水处理后第0、3、6、9、12、15、18 d用不锈钢刀取皮下3~5 mm组织3.0 g,锡箔纸包装液氮冷冻后,放入-80 ℃冰箱保存待用。
1.2.5 过氧化氢(H2O2)含量测定 参照曹建康等[17]方法。取生姜根茎组织3.0 g,用3.0 mL冷丙酮在冰浴下研成匀浆,匀浆液于离心管内置于暗处4 ℃下放置20 min,然后在4 ℃、12000×g条件下离心30 min。反应体系包括2.0 mL上清液,40 μL 20%的四氯化钛溶液和50 μL浓氨水,混匀反应5 min之后在12000×g低温离心10 min,取沉淀部分再用冷丙酮洗涤3次,最后将沉淀溶于3.0 mL 1.0 mol/L H2SO4溶液中,反应完成后测定410 nm吸光度值。按同样方法制作H2O2标准曲线,H2O2含量以μmoL/g FW(鲜重)表示。
1.2.6 超氧化物歧化酶(SOD)活性测定 参照Wang等[18]方法。取生姜根茎组织3.0 g,用3.0 mL 100 mmol/L、pH7.5的磷酸缓冲液在冰浴下研成匀浆。SOD活性以每毫克蛋白抑制氮蓝四唑(NBT)光化还原的50%为一个酶活性单位(U)表示,SOD活性表示为U/mg protein。
1.2.7 过氧化物酶(POD)活性的测定 参考Chen等[19]方法并修改。取生姜根茎组织3.0 g,用5.0 mL 0.05 mol/L磷酸缓冲液在冰浴下研成匀浆,匀浆液于离心管内置于暗处4 ℃下放置20 min,然后在4 ℃、12000×g条件下离心15 min。反应体系包括2.5 mL 0.025 mol/L愈创木酚、0.2 mL 0.25 mol/L H2O2和0.2 mL上清液,加酶液后1 min开始记录反应体系在470 nm处每分钟OD值变化,连续测定3 min,以每分钟吸光度值变化0.01为1个活力单位,POD活性表示为U/mg protein。
1.2.8 抗坏血酸过氧化物酶(APX)活性的测定 参照Rahnama等[20]方法并修改。取生姜根茎组织3.0 g,用5.0 mL 100 mmol/L磷酸缓冲液在冰浴下研成匀浆,匀浆液于离心管内置于暗处4 ℃下放置20 min,然后在4 ℃、12000×g条件下离心20 min。反应体系包括2.0 mL 100 mmol/L磷酸缓冲液(pH7.5)、0.8 mL 3.0 mmol/L 抗坏血酸、200 μL上清液和0.5 mL 0.5 mmol/L H2O2,然后测定反应混合液在290 nm处的OD值,连续测定2 min,以每分钟吸光度值变化0.01为1个活力单位,APX活性表示为U/mg protein。
1.2.9 谷胱甘肽还原酶(GR)活性的测定 参照Rahnama等[20]方法。取生姜根茎组织3.0 g,用5.0 mL预冷的100 mmol/L磷酸缓冲液在冰浴下研成匀浆,匀浆液于离心管内置于暗处4 ℃下放置20 min,然后在4 ℃、12000×g条件下离心30 min。反应体系包括3.0 mL 100 mmol/L磷酸缓冲液(pH7.5)、0.1 mL 5.0 mmol/L GSSG、0.2 mL上清液和30 μL 3.0 mmol/L NADPH,反应15 s后开始测其在340 nm处的OD值变化,连续测定2 min,以每分钟吸光度值变化0.01为1个活力单位,GR活性表示为U/mg protein。
1.2.10 苯丙氨酸解氨酶(PAL)活性的测定 参照闫媛媛等[21]方法。取生姜根茎组织3.0 g,用3.0 mL pH8.8,0.1 mol/L的硼酸缓冲液在冰浴下研成匀浆,匀浆液于离心管内置于暗处4 ℃下放置20 min,然后在4 ℃、12000×g条件下离心15 min。反应体系包括0.5 mL上清液,0.5 mL 0.02 mol/L苯丙氨酸和3.0 mL蒸馏水。反应完成后立即测定290 nm吸光度值。而后再于30 ℃水浴下反应30 min,再次测定吸光度值。以每小时内吸光度变化0.01为1个活性单位(U),PAL活性表示为U/mg protein。
1.2.11 4-香豆酰CoA连接酶(4CL)活性的测定 参照王焕宇等[22]方法。取生姜根茎组织3.0 g,用3.0 mL预冷的0.2 mol/L Tris-HCl缓冲液在冰浴下研成匀浆,匀浆液于离心管内置于暗处4 ℃下放置20 min,然后在4 ℃、12000×g条件下离心15 min。反应体系包括0.15 mL 1.0 μmol/mL 辅酶A(CoA),0.45 mL 75.0 mmol/L MgCl2,0.15 mL 2.0 mmol/mL p-香豆酸,0.15 mL 0.8 mmol/mL ATP和0.5 mL上清液,反应完成测定333 nm吸光度值。以每分钟吸光度值变化0.001为1个酶活力单位(U),4CL酶活性表示为U/mg protein。
1.2.12 总酚和类黄酮含量测定 参照Hu等[23]方法。取生姜根茎组织3.0 g,用5.0 mL预冷的1% HCl-甲醇在冰浴下研成匀浆,匀浆液于离心管内置于暗处4 ℃下放置20 min,然后在4 ℃、12000×g条件下离心15 min,上清液在280 nm和325 nm下测定吸光值。总酚、类黄酮含量分别以OD280/g FW和OD325/g FW表示。
1.2.13 木质素含量测定 参照曹建康等[17]方法。反应体系包括0.5 mL上清液,用冰醋酸定容至9.0 mL,反应完成后测定280 nm吸光度值。木质素含量以OD280/g FW表示。
1.2.14 蛋白含量 参照曹建康等[17]方法,考马斯亮蓝染色法测定蛋白质含量。
1.3 数据处理
上述实验均进行3次平行重复,用Excel计算数据标准偏差和均值,用SPSS数据软件进行显著性分析(p<0.05)。
2 结果与分析
2.1 SNP处理对生姜根茎呼吸强度和失重率的影响
采后生姜根茎由于自身的呼吸和蒸腾作用而发生萎缩,从而影响其外观和品质。随着贮藏时间的延长,各浓度 SNP处理和对照生姜根茎的呼吸强度整体呈下降趋势,贮藏后期维持在一个较低的水平(图1A)。0.25 mmol/L SNP处理生姜根茎的呼吸强度始终低于对照和其他浓度SNP处理。在整个贮藏期间,SNP处理和对照生姜根茎的失重率逐渐增加,其中0.25 mmol/L SNP处理生姜根茎的失重率增加最缓慢(图1B)。由此说明,采后SNP处理能够抑制生姜根茎的呼吸强度的变化和失重率的增加,其中以0.25 mmol/L SNP处理效果较佳。因此,后续实验以0.25 mmol/L SNP处理生姜根茎。

图1 不同浓度SNP处理对生姜根茎呼吸强度(A)和失重率(B)的影响Fig.1 Effect of different concentrations of SNP treatment on the respiratory intensity(A)and weight loss(B)in ginger rhizomes
2.2 SNP对生姜根茎H2O2含量的影响
H2O2能够作为植物防御反应的信号分子和直接参与者,在植物抗病反应和抵御病原菌的侵入过程中起到重要作用,前期H2O2的升高有利于启动寄主的防卫反应如强化细胞壁结构、苯丙烷代谢、病程相关蛋白积累等,后期大量产生的H2O2被体内抗氧化酶所清除,从而减少对寄主细胞的伤害[24]。随着贮藏时间的延长,SNP处理生姜H2O2含量呈先升高后降低趋势,对照生姜H2O2含量整个贮藏期间变化比较平缓,没有明显的峰值(图2),处理组生姜H2O2含量在贮藏第3 d出现高峰且显著高于对照,是对照H2O2含量的2倍。激发子处理能够诱导很多果实产生H2O2,如硅酸钠处理的杏果实和ASM浸泡甜瓜果实等,都诱导了前期H2O2含量的积累,提高果实的抗病性[25-26]。

图2 采后硝普钠处理对生姜根茎H2O2含量的影响Fig.2 Effect of postharvest SNP treatment on the content of hydrogen peroxide in ginger rhizomes
2.3 SNP对生姜根茎SOD活性的影响

图3 采后硝普钠处理对生姜根茎SOD活性的影响Fig.3 Effect of postharvest SNP treatment on the activity of SOD in ginger rhizomes
2.4 SNP对生姜根茎POD活性的影响
随着贮藏时间的延长,对照和SNP处理后生姜POD活性呈先升高后降低的趋势,SNP处理在贮藏第6~18 d显著(p<0.05)提高了生姜POD的活性,SNP处理的POD活性高峰出现在贮藏第6 d,而对照POD活性高峰出现在贮藏第9 d(图4)。POD能够清除植物体内的H2O2,能使H2O2还原为H2O和O2[29]。本实验中SNP处理后生姜根茎POD活性升高且高于对照,促进了这种还原过程能及时清除过量产生的H2O2,维持活性氧代谢平衡。前人研究表明,采后外源NO处理茄子[30]和新疆伽师瓜果实[31],都提高了POD活性,从而增加果实的抗氧化能力。
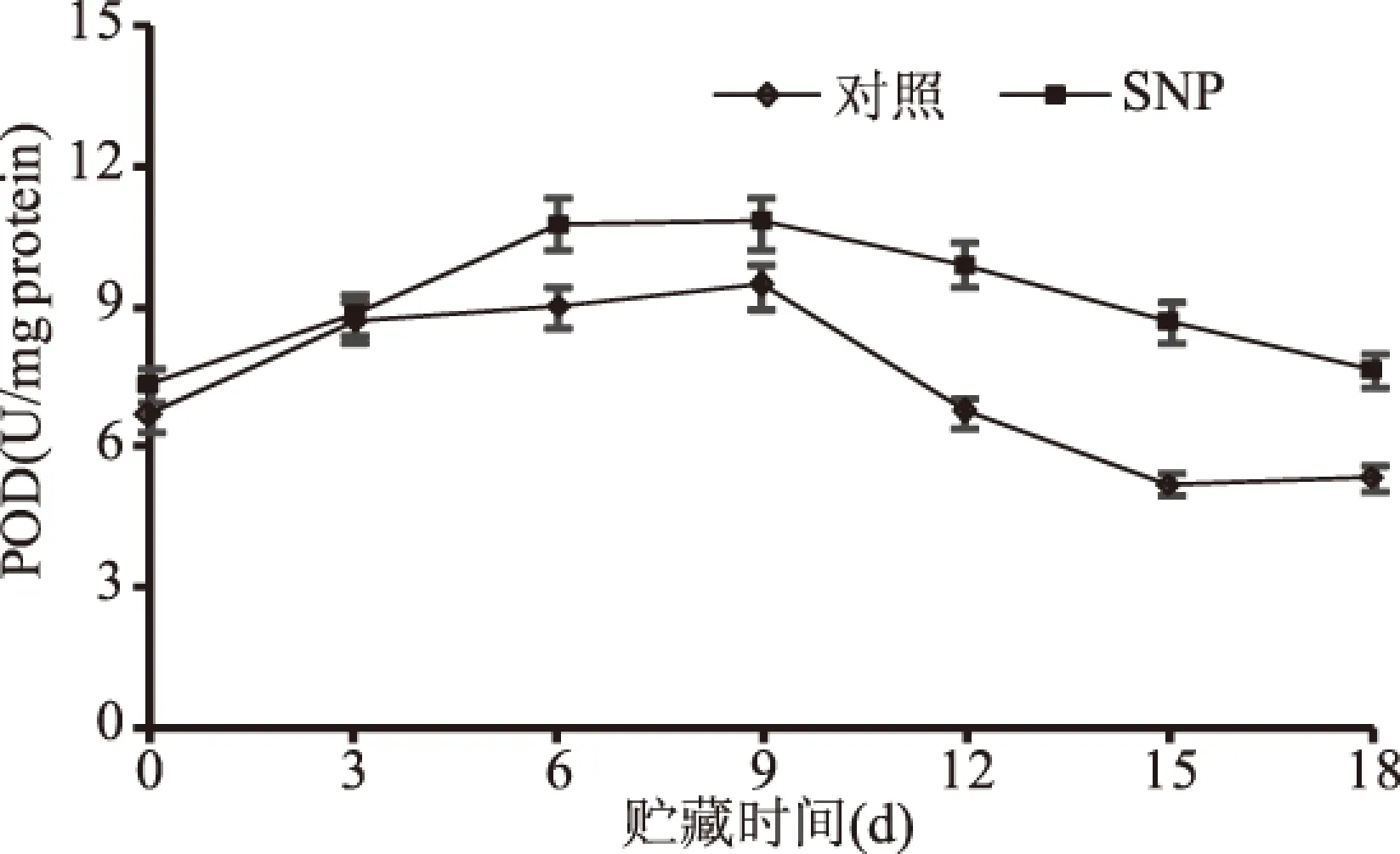
图4 采后硝普钠处理对生姜根茎POD活性的影响Fig.4 Effect of postharvest SNP treatment on the activity of POD in ginger rhizomes
2.5 SNP对生姜根茎APX和GR活性的影响
随着贮藏时间的延长,SNP处理生姜APX活性呈双峰变化趋势,分别在第6 d和12 d出现APX活性高峰,对照生姜APX整体变化比较平缓,没有明显的活性高峰,但SNP处理在贮藏第3~18 d显著(p<0.05)提高了生姜APX活性(图5A)。在贮藏第6 d和12 d时SNP处理生姜APX活性对照的1.91倍和2.36倍。SNP处理生姜GR活性呈先升高后降低趋势,在第9 d出现GR活性高峰,对照生姜GR活性整个贮藏期间无明显变化(图5B)。在贮藏第9 d时SNP处理生姜GR活性是对照的1.37倍。APX和GR是分别以抗坏血酸和氧化型谷胱甘肽为底物清除过量H2O2以保护细胞免受氧化损伤的抗氧化酶,使细胞免受活性氧毒害,在防御系统中发挥重要的作用[32]。本实验结果表明,SNP处理提高了生姜根茎APX和GR活性,及时清除了过量的H2O2,维持了生姜根茎较高的抗氧化能力,进而使细胞免受氧化损伤。在SNP处理西兰花的研究中也得到了同样的结果[14]。

图5 采后硝普钠处理对生姜根茎APX(A)和GR(B)活性的影响Fig.5 Effect of postharvest SNP treatment on the activity of APX(A)and GR(B)in ginger rhizomes
2.6 SNP对生姜根茎PAL和4CL活性的影响
在植物苯丙烷代谢中PAL和4CL是关键酶,具有防御功能[7]。PAL是苯丙烷代谢途径的一个限速酶,其活性高低与酚类、黄酮类和木质素的积累密切相关能够提高果蔬的抗病性和维持果蔬的形态[33-35]。随着贮藏时间的延长,对照和SNP处理PAL和4CL的活性均呈先升高后降低的趋势。SNP处理在贮藏第12~18 d显著提高了生姜根茎PAL活性,并且在贮藏第9~15 d显著(p<0.05)提高了生姜4CL的活性,且均在贮藏第12 d时出现高峰,分别是对照的1.7倍和1.27倍(图6)。PAL和4CL活性的提高,也促进了总酚,类黄酮和木质素的积累。研究表明,NO处理增加了芒果果实PAL和4CL活性,增强了果实抗病能力[9]。
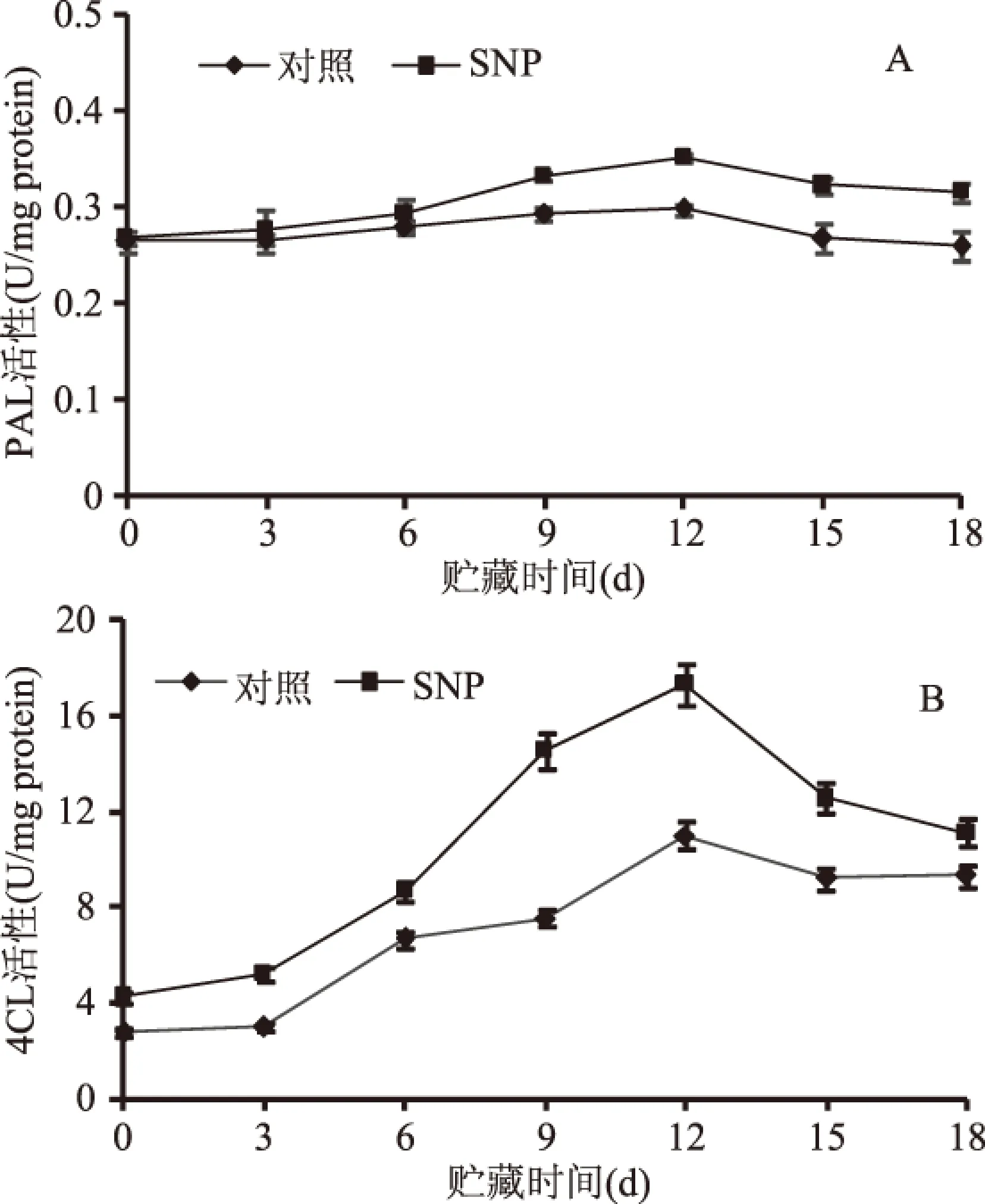
图6 采后硝普钠处理对生姜根茎PAL(A)和4CL(B)活性的影响Fig.6 Effect of postharvest SNP treatment on the activity of PAL(A)and 4CL(B)in ginger rhizomes
2.7 SNP对生姜根茎总酚、类黄酮和木质素含量的影响
由图7可知,随着贮藏时间的延长,对照和SNP处理生姜总酚、类黄酮和木质素含量呈先升高后降低趋势,SNP处理生姜总酚和木质素含量高峰出现在贮藏第12 d,类黄酮含量高峰出现在贮藏第15 d。在贮藏第12 d时SNP处理生姜总酚和木质素含量分别是对照的1.25和1.23倍,在贮藏第15 d时SNP处理生姜类黄酮含量是对照的1.18倍。酚类物质可以抵御病原物,类黄酮有抑菌作用,木质素的积累有利于增强细胞壁厚度,从而提高对病原物的抵抗力。研究表明,NO处理促进了芒果果实中木质素的积累,促进苯丙烷代谢途径火龙果中总酚、木质素和类黄酮含量的积累,增强了果实的抗病性[9,36]。

图7 采后硝普钠处理对生姜根茎总酚(A),类黄酮(B)和木质素(C)含量的影响Fig.7 Effect of sodium nitrate treatment on the total phenololic compounds(A),flavonoids(B) and lignin(C)content in ginger rhizomes
3 结论
采后0.25 mmol/L SNP处理有效降低了生姜根茎呼吸强度,并且抑制了失重率的增加。SNP处理还提高了生姜根茎H2O2含量,同时提高了活性氧清除酶的活性,H2O2的积累可能作为信号分子启动果实的防卫反应,而活性氧清除酶活性的提高有利于降低过量产生的活性氧对细胞的伤害。此外,SNP处理还提高了苯丙烷类代谢关键酶活性和产物的积累。然而,SNP处理调控生姜根茎衰老过程中活性氧代谢和苯丙烷代谢的分子机制尚需进一步研究。

