UHPLC 法同时测定参麦注射液中8 种人参皂苷
杨 林, 徐晓珍, 陈劲柏, 吴友苹, 陈娇婷, 辛艳飞
(1. 浙江省医学科学院安全性评价研究中心, 浙江 杭州310013; 2. 浙江工业大学长三角绿色制药协同创新中心, 浙江 杭州310013; 3. 绍兴市中医院, 浙江 绍兴312499; 4. 浙江大学医学院附属儿童医院,浙江 杭州310006)
参麦注射液是由古方参麦饮衍变而来, 由红参、 麦冬提炼精制而成, 为临床常用中药注射液之一[1-2], 在益气固脱、 养阴生津的传统药效基础上, 它还具有抗心肌缺血、 去除氧自由基等药理作用, 临床上广泛应用于治疗心血管疾病、 免疫功能低下、 各种慢性疾病[3-5]。
研究表明, 人参皂苷是参麦注射液中最主要的有效成分, 但现行检测标准仅采用HPLC 法对人参皂苷Rg1、 Re、 Rb1 含有量进行测定, 难以全面控制制剂质量[6]; 目前也有采用HPLC 法同时测定其中多种人参皂苷含有量的报道[7-8], 但受限于方法分离度和灵敏度问题, 分析时间较长, 分离效果也不理想。 本实验采用超高效液相色谱(UHPLC)法同时测定参麦注射液中人参皂苷Rg1、 Re、 Rf、Rb1、 Rc、 Rb2、 Rd、 Rg3 的含有量, 以期为全面评价该制剂质量提供参考。
1 材料
1.1 仪器 Agilent 1290 infinity 超高效液相色谱仪(美国Agilent 公司); MS105DU 型电子天平[梅特勒-托利多仪器(上海) 有限公司]。
1.2 试药 人参皂苷Rg1(批号Z26S7X21730, 含有量98%)、 人参皂苷Re (批号B10M8S35243,含有量98%)、 人参皂苷Rf (批号P09M8F31017,含有量98%)、 人参皂苷Rb1(批号Z06M8L30693,含有量98%)、 人参皂苷Rc (批号P24F8F30057,含 有 量 98%)、 人 参 皂 苷 Rb2 ( 批 号P09M8F35575, 含有量98%)、 人参皂苷Rd (批号Z27F8X30060, 含有量98%)、 人参皂苷Rg3 (批号Z01D7X25885, 含有量98%) 对照品购于上海源叶生物科技有限公司。 参麦注射液由杭州正大青春宝有限公司提供(批号1706271、 1611071、1611081、 1611082, 10 mL/支)。 乙腈为色谱纯(德国Merck 公司); 其他试剂为分析纯; 水为超纯水。
2 方法与结果
2.1 色谱条件和系统适应性考察 Agilent Eclipse Plus C18色谱柱(2.1 mm×50 mm, 1.8 μm); 流动相乙腈 (A) -水 (B), 梯度洗脱 (0 ~10 min,19%A; 10 ~18 min, 19% ~23% A; 18 ~21 min;23%A; 21 ~31 min, 23% ~40% A; 31 ~40 min,40% ~45%A); 体积流量0.3 mL/min; 柱温30 ℃;检测波长203 nm; 进样量1 μL, 理论塔板数按人参皂苷Rg1 计, 应不低于5 000。 8 种成分与其他组分均能达到基线分离, 色谱图见图1。

图1 各成分UHPLC 色谱图Fig.1 UHPLC chromatograms of various constituents
2.2 对照品溶液制备 精密称取人参皂苷Rg1(5.081 mg)、 人参皂苷Re (3.579 mg)、 人参皂苷Rf (1.062 mg)、 人参皂苷Rb1 (10.061 mg)、 人参皂苷Rc (5.023 mg)、 人参皂苷Rb2 (5.033 mg)、人参 皂 苷 Rd (10.011 mg)、 人 参 皂 苷 Rg3(0.901 mg) 对照品, 置于1 mL 量瓶中, 20%乙腈溶解并稀释至刻度, 制成贮备液, 精密吸取适量至10 mL 量瓶中, 加初始比例流动相至刻度, 制成分别含人参皂苷Rg1、 Re、 Rf、 Rb1、 Rc、 Rb2、 Rd、Rg3 0.390、 0.170、 0.072、 0.790、 0.308、0.220、 0.139、 0.019 mg/mL 的溶液, 即得。
2.3 供试品溶液制备 将注射液过0.22 μm 微孔滤膜, 弃初滤液3 滴后收集续滤液, 即得。
2.4 线性关系考察 精密吸取“2.2” 项下对照品溶液适量, 制成5 个质量浓度 (表1), 在“2.1” 项色谱条件下进样1 μL 测定。 以对照品质量浓度为横坐标(X), 峰面积为纵坐标(Y) 进行回归, 结果见表2, 可知各成分在各自范围内线性关系良好。

表1 各成分线性浓度范围(mg/mL)Tab.1 Linear concentration ranges of various constituents (mg/mL)
2.5 精密度试验 取同一供试品溶液 (批号1706271), 在“2.1” 项色谱条件下进样测定6次, 测得人参皂苷Rg1、 Re、 Rf、 Rb1、 Rc、 Rb2、Rd、 Rg3 峰 面 积RSD 分 别 为0.53%、 1.29%、2.21%、 0.55%、 0.64%、 0.43%、 0.66%、 2.71%,表明仪器精密度良好。

表2 各成分线性关系Tab.2 Linear relationships of various constituents
2.6 重复性试验 取同一注射液 (批号1706271), 按“2.3” 项下方法平行制备6 份供试品溶液, 在“2.1” 项色谱条件下进样测定6 次,测得人参皂苷Rg1、 Re、 Rf、 Rb1、 Rc、 Rb2、 Rd、Rg3 含有量RSD 分别为1.39%、 2.32%、 1.73%、0.54%、 0.41%、 2.57%、 0.39%、 1.05%, 表 明该方法重复性良好。
2.7 加样回收率实验 精密吸取含有量已知的供试品溶液 (批号1706271) 0.5 mL, 精密加入“2.4” 项下对照品溶液0.5 mL, 充分混匀, 平行6 份, 过0.22 μm 微孔滤膜, 在“2.1” 项色谱条件下进样测定, 计算回收率。结果, 人参皂苷Rg1、 Re、 Rf、 Rb1、 Rc、 Rb2、 Rd、 Rg3 平均加样回收率 (RSD) 分别为98.64% (1.39%)、98.00% ( 2.19%)、 97.43% ( 1.05%)、 97.95%(0.37%)、 104.24%(5.34%)、 100.43 (1.00%)、99.68% (2.62%)、 100.91% (0.91%)。
2.8 样品含有量测定 取4 批注射液, 过0.22 μm微孔滤膜, 在“2.1” 项色谱条件下进样测定, 计算含有量, 结果见表3。
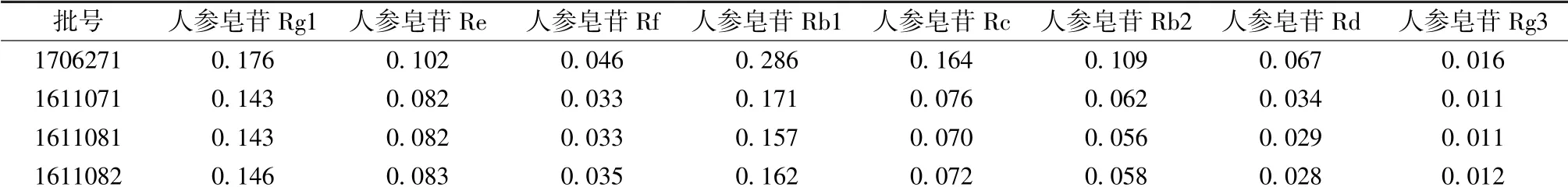
表3 各成分含有量测定结果(mg/mL, n=6)Tab.3 Results of content determination of various constituents (mg/mL, n=6)
3 讨论
前期查阅文献发现, 不同类型人参皂苷的结构十分相似, 分离难度较大, 故在文献报道基础上采用梯度洗脱方式[9-10]。 本实验考察了不同流动相系统对分离效果的影响, 如乙腈-水、 0.05% KH2PO4缓冲盐-乙腈等, 最终确定乙腈-水作为流动相进行梯度洗脱; 考察了柱温(20、 25、 30、 35、 40 ℃)和体积流量(0.1、 0.2、 0.3、 0.4、 0.5 mL/min)对分离度的影响, 发现30 ℃、 0.3 mL/min 下各色谱峰分离度最优, 并且能保持柱压在合理范围内;考察了进样量对分离度的影响, 发现1 μL 时色谱峰峰形最佳, 而大于1 μL 时峰形较差, 小于1 μL时峰面积太小。
根据Van Deemter 理论, 色谱柱粒径越小, 塔板数高度越低, 柱效越高, 本实验采用1.8 μm 小颗粒填料色谱柱, 35 min 内即可实现参麦注射液中8 种人参皂苷的有效分离, 可大大提高分析效率。与常规HPLC 法相比, 在所测皂苷类成分含有量基本一致的情况下[11]UHPLC 法可节省近60 min, 故本实验采用该方法测定时可为快速全面评价参麦注射液质量提供参考。

