压力控制反比通气对腹腔镜手术患者死腔及炎症反应的影响
杨 俏,金立民,范 雪,许丽妍,宋雪松
(吉林大学第一医院 麻醉科,吉林 长春130021)
腹腔镜手术具有疼痛轻、恢复快、住院时间短等优势,但与此同时手术时建立的人工气腹会对机体产生很多负面的影响,同时改变呼吸机制。在气腹建立后的头低脚高位使气道峰压和平台压力增加至少50%,同时也减少了50%的肺顺应性[1]。在这种情况下,即使在CO2气腹终止后肺顺应性的降低也无法完全恢复。通过适当的调节呼吸参数,短时间内完成的腹腔镜手术通常可以避免上述不良影响的产生。然而较长时间和较复杂的腹腔镜手术越来越多,比如腹腔镜下胃癌根治术相比之下就需要更长的时间。因此选择最佳的通气策略十分重要。国内外目前有关研究中有结论指出,采用反比通气的模式可以改善患者的呼吸参数[2],但尚未有人对反比通气的最适比值选择做出研究,因此本项研究在观察腹腔镜下胃癌根治术中根据呼气流速时间波来个体化调整反比通气吸呼比(1∶1,1.5∶1和2∶1),探讨对患者死腔分数以及术后炎症反应的影响,为腹腔镜手术患者选择最佳通气策略提供参考。
1 资料与方法
1.1一般资料本研究已获本院伦理委员会批准,并与患者本人及家属签署知情同意书。选取2017年2月-6月吉林大学第一医院拟行腹腔镜下胃癌根治术患者60例,年龄在55-75岁,ASAⅠ或Ⅱ级。排除标准:慢性阻塞性肺疾病(COPD),哮喘,气胸病史,肺部手术史;大量吸烟;肥胖(BMI≥30 kg/m2);ASA分级在Ⅲ级以上的患者以及术前发现低氧饱和度者(SpO2<95%)。
1.2分组方法将纳入研究的患者随机分为3组:容量控制通气组(VCV),压力控制参考通气组(PCV),压力控制反比通气组(PC-IRV)。
1.3麻醉方法麻醉诱导:患者入手术室后常规给予心电图、血压、脉搏血氧饱和度监测(监护仪Philips IntelliVue MP50),建立有创动脉血压监测,并用麻醉深度检测仪(Narcotrend-Compact)监测麻醉深度。麻醉诱导应用丙泊酚1.5-2 mg/kg或依托咪酯0.2-0.3 mg/kg、芬太尼3-5 μg/kg、顺式阿曲库铵0.15 mg/kg。麻醉维持:麻醉维持应用丙泊酚4-6 mg/kg/h,瑞芬太尼0.1-0.3 μg/kg/min,间断给予肌松药。麻醉深度维持在40-60之间,术毕所有患者均拔管后送入苏醒室。
1.4机械通气所有患者在麻醉诱导后均采用容量控制通气模式,潮气量6-8 ml/kg(理想体重),呼吸频率10-12次/分,吸呼比设为1∶2,FIO2设置为0.4-0.6,PEEP设置为4 cmH2O。术中保持组间手术床倾斜角度基本相同(30-45度)。气腹建立并且头低脚高位后根据实验分组调整通气模式。PC-IRV组根据麻醉机的流速时间波调整吸呼比为2∶1,1.5∶1和1∶1,即下一个吸气开始位于前次呼气波转折点与预计到达基线点的中点。术中其他通气参数不变,根据ETCO2调整其呼吸频率,使其在35-45 mmHg的范围。术中人工CO2气腹压11-14 mmHg。术中VCV模式的气道峰压(PIP)和PCV、PC-IRV模式的气道平台压(Pplat)大于30 cmH2O或者SpO2低于95%的患者排除研究。术中患者血压及心率在基础值±20% 之间,若超出此范围,给予血管活性药来维持血流动力学的稳定,并且该患者被排除。
1.5观察指标在手术开始后调整相应通气模式,血流动力学稳定后30 min记录呼吸力学、血流动力学指标,采集动脉血,并根据测量值计算死腔分数,氧合指数(PaO2/FiO2),肺动态顺应性(CL =VT/(Pmax-PEEP))[3]。死腔分数根据2010年 Frankenfield DC等研究提出的校正公式进行计算:VD/VT=0.320+0.0106(PaCO2-ETCO2)+0.003 (呼吸频率,RR) +0.0015 (年龄,Age),充分考虑年龄、呼吸、肌松药等因素,偏倚更小[4]。观察术后72 h胸片有无浸润性改变、肺不张、二次插管发生率等肺部并发症发生的情况,以及术后1 d、3 d、5 d白细胞计数、降钙素原(PCT)和超敏C反应蛋白(hs-CRP)等炎性指标。

2 结果
2.1三组患者之间年龄,性别,BMI,手术时间等一般情况比较差异无统计学意义(P>0.05),见表1。
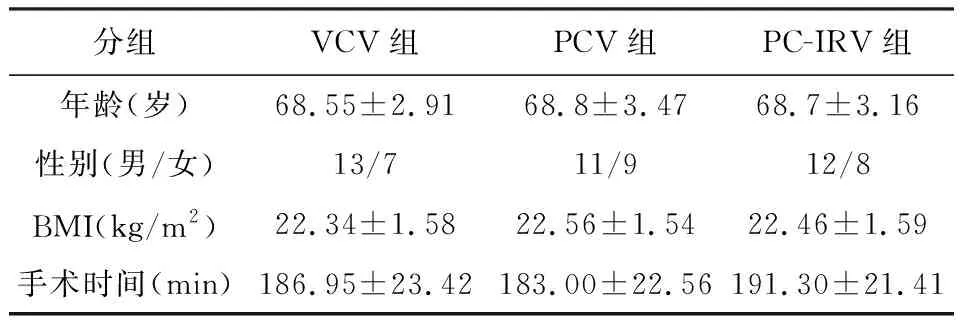
表1 三组患者一般情况比较
2.2三组之间机械通气参数设置潮气量,呼吸频率,吸呼比及PEEP,见表2。其中PC-IRV组吸呼比1∶1的有7例,1.5∶1的8例,2∶1组5例。吸气平台阶段VCV组为0 s,PCV组为1.7-2 s,PC-IRV组为2.5-4 s。
2.3在三组死腔分数、氧合指数与肺动态顺应性性结果及比较,见表3。

表2 三组患者术中呼吸力学及血流动力学比较
*为与VCV组相比,P<0.05,差异有统计学意义;#为与PCV组相比,P<0.05,差异有统计学意义

表3 三组患者死腔分数及氧合指数肺动态顺应性比较
*为与VCV组相比,P<0.05,差异有统计学意义;#为与PCV组相比,P<0.05,差异有统计学意义
2.4三组术后并发症相比较60例患者全部治愈,VCV组出现1例术后肺不张,其余患者均未出现术后并发症。三组术后各时间的白细胞计数,PCT和CRP比较,见表4。

表4 三组患者术后炎症因子比较
*为与VCV组相比,P<0.05,差异有统计学意义;#为与PCV组相比,P<0.05,差异有统计学意义
3 讨论
在进行本项研究后,得出的主要结论是:在进行腹腔镜手术时,采用压力控制反比通气并根据呼气流速波对患者个体化调整吸呼比,可以降低死分数,改善氧合指数、肺动态顺应性,减轻术后炎症反应,不引起肺部恶性扩张,不影响血流动力学稳定。
根据上述结果,分析PC-IRV模式降低死腔分数的原因主要有:(1)PC-IRV通气模式与其他两种通气模式相比,气道死腔减少[5],在三种机械通气的模式中,吸气相的时长是不同的,吸气高流速和延长吸气时间有利于气体在气道内的扩散,减少了气道死腔。(2)PC-IRV模式改善了分流死腔,明显的减少了动脉血二氧化碳分压和肺泡内二氧化碳分压的差值。PC-IRV通气模式的高流速吸气和长吸气相为二氧化碳提供了足够时间去从肺毛细血管弥散到肺泡当中[6]。(3)还有一种可能的机制是PC-IRV模式减少了血液分流,PC-IRV模式下肺泡缓慢的持续扩张,增强有效的侧枝通气。此外,很可能是因为PC-IRV通气模式的呼气时间相对缩短,这种情况下产生了内源性PEEP,防止了肺泡萎陷[7]。
目前PC-IRV通气模式多用于ARDS的治疗[8],通常吸呼比设置为2∶1到4∶1之间,并未对患者进行个体化的调整,通常造成呼气时间过短[9]。在肺部健康的患者中,这些通气设置有可能由于呼气时间过短而产生很高的内源性PEEP以至于肺泡的过度膨胀[10]。有研究显示,气道内疾病,特别是慢性阻塞性肺疾病、炎症、肌松药、体位和气腹都会影响呼气流速[11]。目前对压力控制反比通气策略的研究中常采用2∶1-4∶1的吸呼比,并没有相关研究根据患者情况进行个体化的调整,因此常造成肺过度充气和循环抑制[12]。在本研究中,吸呼比根据呼气流速曲线进行了个体化调整,避免了发生动态的肺过度充气。
在本研究中,患者在术中均应用了肌松药且肺部健康,因此呼气峰流速要比ARDS患者要慢。在严重的ARDS患者治疗中要求内源性PEEP来防止肺泡的萎陷,因此在本研究中不需要更高的PEEP[13]。因此,在PC-IRV通气模式中个体化调整吸呼比造成动态肺恶性扩张的风险较低。
对比PCV和VCV通气模式,PC-IRV模式减少了死腔并且减少了动脉血二氧化碳分压。已有研究表明常规PCV通气模式可以显著降低吸气压力峰值[14]。而PC-IRV通气模式最重要的优势通过相对较低的潮气量达到目标动脉血氧分压和二氧化碳分压。在很多时候由于患者肥胖、长时间的气腹和头低脚高位都可能造成高碳酸血症。在这种情况发生时,PC-IRV模式是一种可行的替代方式以较小的潮气量来达到正常的动脉氧合和二氧化碳分压,同时与VCV组和PCV组相比有较低的气道峰压和平台压。
炎症因子可以反应患者的应激反应,是机体急性应激反应后比较敏感的指标,在本研究中测量了白细胞,降钙素原(PCT),超敏C反应蛋白(CRP)三种指标,提高了敏感性[15],从结果中可以得出:与传统吸呼比通气模式相比,PC-IRV通气模式可以减轻肺泡的机械性损伤,从而减少了炎症因子的释放,减轻了术后炎症反应,减低了术后肺部并发症发生的风险。但独立的各项指标特异性较差,无法专一性的反应机体炎症产生部位,因此只能宏观反应机体整体炎症水平的变化,而机体全身炎症水平与手术时长、手术操作、患者自身体条件等均有关[16],并且在本实验中,由于实际情况,只观察了术后72 h胸片有无浸润性改变、肺不张、二次插管发生率等肺部并发症发生的情况,在该时刻只观测到了VCV组有1例术后肺不张的发生,后续几天无辅助检查证据,因此可能有患者存在术后并发症但未被记录,因此导致3组术后肺部并发症几乎无差别,但炎症因子计数相差较大的结果,这也是本项研究的不足之处,在接下来的研究中,还应细化观察的指标,为研究提供更加明确的理论支持。
除此之外,在本实验中仍有不足之处,我们调整吸呼比是从2∶1,1.5∶1,1∶1,这三种比率中选择,通过观察呼气流速时间波,使吸气开始点位于呼气返回线折点与与预测返回零点之间的中点上。通过人为目测观察来调整,有一定的误差,最好是用麻醉机可以通过对呼气流量波监测并进行自动分析,对呼气的起始点进行优化,并对吸呼比进行优化。但是目前没有麻醉机带有这个功能,因此需要进一步的研究来开发一种方法,以确定每个病人最适宜的吸呼比,并将此方法应用于临床麻醉的实践中。

