心脏死亡器官捐献供体情况对受体肝脏移植术后终末期肝病模型评分影响研究
方大正,胡伟*,张波
肝脏移植已被公认为是挽救终末期肝功能衰竭患者生命的最佳办法,但肝脏供体短缺已成为当前我国肝脏移植事业发展的障碍[1],因为我国肝脏疾病的基础数量较大导致我国较世界其他国家面临着更严峻的肝脏供体短缺问题[2]。捐献供体主要有脑死亡器官捐献(donation after brain death,DBD)供体与心脏死亡器官捐献(donation after cardiac death,DCD)供体两种,目前国际社会的器官捐献以DBD为主要来源。但是在我国因没有相关法律支持,DBD供体仍需等待其呼吸循环完全停止以后才能进行器官获取[3]。在我国现阶段,开展DBD的条件尚不成熟,但实行DCD已经具备伦理、法律、技术等方面要求,所以近年来我国DCD肝脏移植呈快速增长趋势。2002年美国器官资源共享网络(UNOS)将终末期肝病模型(model for end-stage liver disease,MELD)评分作为美国新的器官分配评分系统,用于预测和评定终末期肝病的严重程度和肝脏疾病患者等待肝脏移植期间的死亡危险度,以决定器官分配的优先顺序[4]。但目前国内并未设立很好的DCD供体准入指标,故本研究针对华中科技大学同济医学院附属同济医院器官移植研究所DCD肝脏移植供体和受体情况进行总结,探讨供体术前情况对受体肝脏移植术后MELD评分变化的影响,现报道如下。
1 资料与方法
1.1 一般资料 回顾性选取2013年9月—2015年9月华中科技大学同济医学院附属同济医院器官移植研究所DCD肝脏移植供体25例,均符合国际标准M-Ⅲ[5]和中国标准C-Ⅲ[6],在器官切取前均为程序性停止呼吸循环支持,术前均有较完善的病例资料和血清学检测,器官移植前完成病理学检查。其中男19例,平均年龄(38±5)岁,重症监护室(ICU)治疗时间(4.0±0.5)d;女6例,平均年龄(36±6)岁,ICU治疗时间(6.0±0.5)d。25例受体均为非恶性肿瘤性肝病,原发病:乙型肝炎后肝硬化9例,胆汁性肝硬化6例,酒精性肝硬化4例,肝功能衰竭3例,肝豆状核变性2例,肝糖原异常沉积症1例。
1.2 器官切取前情况 25例供体为在本院或外院ICU患者,死亡原因:脑创伤16例,脑血管意外8例,其他1例;合并糖尿病8例,高血压6例,慢性乙型肝炎3例,同时合并高血压和糖尿病3例。
1.3 器官切取方法 捐献者均先停用呼吸机和循环支持,转移到医院手术室,监测、判断并临床死亡。而后大十字切口进腹,经腹主动脉插管,使用保存液灌注,整体切取肝脏和肾脏。
1.4 器官移植前病理学检查 器官切取后肉眼均未见明显肿瘤性病变,组织未见明显肿胀、充血、大颗粒脂肪浸润表现。移植前均对移植物行快速石蜡切片检查,17例未见脂肪浸润、6例轻度脂肪浸润、1例中度脂肪浸润、1例重度脂肪浸润,病理学检查均未见明显肿瘤细胞浸润。
1.5 器官移植手术和术后治疗 受体手术方式为经典原位肝移植术和背驮式肝移植术,胆管重建方式均为胆管端端吻合,未放置胆管T管引流。受体肝脏移植术后均采用他克莫司(Tac)或环孢素A(CsA)+吗替麦考酚酯(MMF)+泼尼松三联免疫抑制方案,术后半年内Tac血药浓度维持在6~8 μg/L,CsA血药浓度峰值维持在0.8~1.2 mg/L,并逐渐减少泼尼松用量至停用,半年后Tac血药浓度维持在6~7 μg/L,CsA血药浓度峰值维持在0.6~1.0 μg/L。术后患者半年生存率为100%。记录器官移植术前及术后30 d内患者血清生化指标,包括肝肾功能、凝血功能、血常规等,术后前5 d每天抽血检测,5 d后每5 d一次。
1.6 MELD评分 器官移植术前及术后第1、2、3、4、5、10、15、20、25、30天分别对受体进行MELD评分,MELD评分计算公式:R=9.6×ln〔肌酐(mg/dl)〕+3.8×ln〔胆红素(mg/dl)〕+11.2×ln〔国际标准化比值(INR)〕+6.4×病因(胆汁淤积性和酒精性肝硬化为0,病毒等其他原因肝硬化为1)。MELD评分越高,其风险越大,生存率越低[4]。MELD评分下降速度以术后第20天MELD评分与术前MELD评分比值来表示。
1.7 统计学方法 采用SPSS 13.0统计软件进行统计学分析。计量资料符合正态分布以(±s)表示,两组间比较采用成组t检验,多组间比较采用单因素方差分析;计数资料比较采用χ2检验;相关性分析采用Pearson直线相关分析及线性回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 受体肝脏移植术后30 d内MELD评分 受体肝脏移植术前MELD评分20.6~35.4分,受体肝脏移植术后第1天MELD评分19.8~36.5分,术后第2天MELD评分 22.3~37.4分,术后第 3天 MELD 评分 20.6~37.8分,术后第4天MELD评分18.7~37.7分,术后第5天MELD评分18.3~40.5分,术后第10天MELD评分12.3~35.6分,术后第15天MELD评分10.6~36.4分,术后第20天MELD评分9.9~33.7分,术后第25天MELD评分8.7~32.6分,术后第30天MELD评分6.8~30.5分(见表1)。
2.2 供体性别、年龄及ICU治疗时间与受体肝脏移植术后MELD评分下降速度关系 男性供体19例,女性供体6例,受体肝脏移植术后MELD评分下降速度分别为(2.80±1.32)%和(1.40±0.66)%,差异有统计学意义(t=2.476,P=0.021);供体年龄<45岁15例,≥45岁10例,受体肝脏移植术后MELD评分下降速度分别为(2.73±1.26)%和(2.07±1.40)%,差异无统计学意义(t=-1.210,P=0.242);供体ICU治疗时间<5 d 3例,5~10 d 14例,>10 d 8例,受体肝脏移植术后MELD评分下降速度分别为(2.30±1.38)%、(2.85±0.85)%、(2.94±1.76)%,差异无统计学意义(F=0.957,P=0.516)。
2.3 相关性及回归分析 供体丙氨酸氨基转移酶(ALT)13~667 U/L,平均(218±15)U/L;天冬氨酸氨基转移酶(AST)11~765 U/L,平均(362±24)U/L;直接胆红素(DBiL)5.1~72.5 μmol/L,平均(34.2±5.7)μmol/L;总胆红素(TBiL)8.6~117.6 μmol/L,平均(62.5±11.2)μmol/L;白细胞计数(WBC)(2.5~17.4)×109/L,平均(13.8±1.8)×109/L;血红蛋白(Hb)75~601 g/L,平均(147±31)g/L。供体年龄、ICU治疗时间、术前AST、DBiL、WBC、Hb水平、受体肝脏移植术前MELD评分与受体肝脏移植术后MELD评分下降速度均无直线相关关系(r=-0.344,P=0.093;r=-0.294,P=0.154;r=-0.271,P=0.090;r=-0.181,P=0.386;r=-0.310,P=0.096;r=-0.205,P=0.325;r=-0.219,P=0.294)。供体术前 ALT、TBiL水平与受体肝脏移植术后MELD评分下降速度均呈负相关(r=-0.301,P=0.044;r=-0.372,P=0.012)。线性回归分析显示,供体术前ALT、AST、TBiL水平与受体肝脏移植术后MELD评分下降速度相关(P<0.05,见表2)。
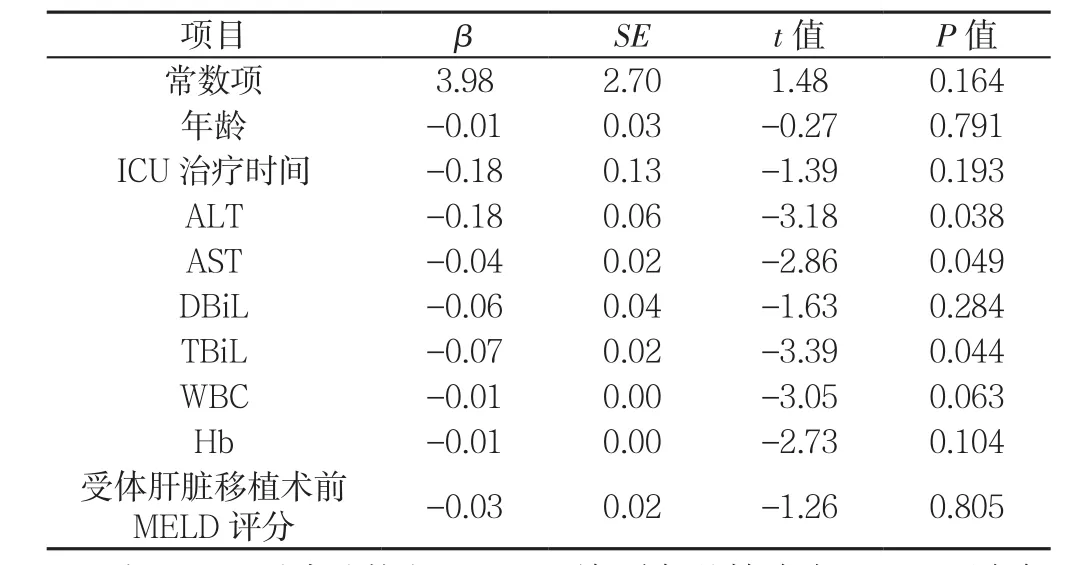
表2 受体MELD评分下降速度相关因素分析Table 2 Analysis of the factors related to the decrease in recipient MELD scores
3 讨论
肝脏移植已成为目前终末期肝脏疾病治疗的一种主要手段,但严重供体器官短缺越来越成为阻碍肝脏移植发展的关键性因素[7]。近年来,随着器官移植技术的不断发展,肝脏移植手术技术的日趋成熟,供体短缺问题愈发严重,使得DCD需求量呈逐年上升趋势,DCD已成为国际上被公认的供者三大来源之一,从客观上缓解了移植器官短缺的紧迫现状[8-9]。但是,鉴于DCD肝脏移植后缺血性胆管损伤等胆管并发症、原发性移植物无功能等并发症发生率较高[10],于是探索如何进行有效评估供体器官可用性和体外修复来提高供体器官的利用率,提高器官移植术后存活率及患者生存质量成为目前研究的热点。
MELD评分系统最初作为评价经颈内静脉门体静脉分流术(TIPS)肝硬化患者预后的指标[11-12],后来发现其在判断终末期肝脏疾病患者待肝期内短期死亡危险度方面优于Child-Turcotte-Pugh(CTP)评分,克服了其临床指标主观性等不足,现被用来对终末期肝脏疾病患者肝功能的评估及对受体筛选、供肝分配的指导,和对患者器官移植前后生存率、存活质量等的预测和评估[13]。本研究采用MELD评分系统研究DCD供体因素对肝脏移植术后患者预后的影响,从而对临床选择手术时机、降低术后死亡率以及肝脏合理分配提供一定的理论依据。
本研究通过术前供体临床资料的比较及各指标与受体肝脏移植术后MELD评分下降速度进行线性回归分析,发现供体年龄及ICU治疗时间与受体肝脏移植术后MELD评分下降速度无直线相关关系,与文献报道一致[14],但术前ALT、AST、TBiL水平与受体肝脏移植术后MELD评分下降速度相关,即ALT、AST和TBiT水平越高,受体肝脏移植术后MELD评分下降速度越低,患者恢复越慢。ICU治疗时间虽与受体肝脏移植术后MELD评分下降速度呈负相关,但无统计学意义,只具备一定的参考意义,如ICU治疗时间越长,受体肝脏移植术后MELD评分下降速度越低,患者术后恢复越慢,这与实际吻合,但影响程度不大,在临床上可作为手术参考。
综上所述,DCD供体术前血清学指标(ALT、AST、TBiL)与受体肝脏移植术后MELD评分有密切的关系,通过纠正术前血清学指标,尤其是纠正ALT、AST和TBiL水平及改善患者一般情况,来降低受体肝脏移植术后MELD评分,为合理选择手术时机和分配肝源提供一定理论依据,有利于降低肝脏移植术后并发症发生率和围术期病死率,提高患者的生存质量。本研究病例数较少存在一定局限性,此外MELD评分除了受TBiL影响外,还受肌酐水平及凝血功能的影响,并且DCD供体供肝质量影响较大的因素如术前升压药物的使用、用量及时间、低血压时间、是否有心肺复苏病史等因素均对受体肝脏移植术后的恢复有较大影响,本研究并未将其纳入研究。因此,还有诸多问题有待于今后进一步探讨和研究。
作者贡献:方大正、张波进行文章的构思与设计,研究的实施与可行性分析,数据收集与整理;方大正、胡伟进行统计学处理,结果的分析与解释,撰写论文,论文的修订,负责文章的质量控制及审校,对文章整体负责,监督管理。
本文无利益冲突。
编后语:
本研究通过对25例心脏死亡器官捐献(DCD)供体术前情况对受体肝脏移植术后终末期肝病模型(MELD)评分的影响进行了研究,发现年龄及重症监护室(ICU)治疗时间与受体肝脏移植术后MELD评分下降速度无相关性;供体术前丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、总胆红素(TBiL)水平越高,受体肝脏移植术后MELD评分下降速度越低,患者恢复越慢。供体术前ALT、AST、TBiL水平是肝脏移植术后并发症发生的主要高危因素。由于目前我国肝脏移植供体器官短缺现象显著,DCD肝脏移植是近年来新出现的概念,本研究选题新颖,有一定临床应用价值,但是MELD评分除了受TBiL影响外,还受肌酐水平及凝血功能的影响,纳入预测肝脏移植术后的因素时应该考虑到肌酐水平及凝血因素;此外,对DCD供肝质量影响较大的因素如术前升压药物的使用、用量及时间,低血压时间,是否有心肺复苏病史等因素均对术后受体的恢复有较大影响,建议今后研究考虑这些因素。

