CoMoS x/γ-Al2O3催化剂在还原脱硫中的吸附性能和催化活性
刘哲男 耿云峰 石 泉 黎汉生*, 史大昕吴 芹 赵 芸 冯彩虹 矫庆泽,3
(1北京理工大学化学与化工学院,北京 100081)
(2北京北大先锋科技有限公司,北京 100080)
(3北京理工大学珠海学院化工与材料学院,珠海 519085)
0 引 言
随着工业化不断推进,大量工业废气严重污染了空气质量,其中SO2是空气主要污染物之一。中国是SO2排放的第一大国,大气中90%的SO2来自于煤炭的直接燃烧。因此,开发高效清洁的脱硫方法成为研究者广泛关注的领域。利用CO选择性还原SO2制单质硫过程,自提出以来受到了研究者们普遍青睐。该方法不仅可以克服目前湿法脱硫过程所带来的二次污染,而且可以回收烟气中的硫资源,因此一直是环境催化领域的研究热点之一。
根据相关文献报道[1-4],CoMoSx/γ-Al2O3在还原脱硫过程中呈现出优异的催化活性和单质硫选择性。这种催化剂的优势在于反应温度较低,催化活性和选择性高,然而在反应过程中会出现副产物COS[5-9],致使催化剂表面硫元素的流失。因此有必要从CoMoSx/γ-Al2O3入手,开展催化机理研究,探索其结构与性能之间的构效关系。
本研究采用等体积浸渍法与原位还原硫化法相结合制备了CoMoSx/γ-Al2O3催化剂,利用XRD、SEM/EDS、XPS和TPR/TPD/TPSR-MS等表征技术对其结构和表面特性进行了表征,考察了CoMoSx/γ-Al2O3的结构、在催化还原过程中SO2和CO的吸附-脱附特性,为高活性、高单质硫选择性、高稳定性的CO选择性还原SO2合成单质硫催化剂开发提供基础数据。
1 实验部分
1.1 催化剂的制备
称取 1.950 8 g (NH4)6Mo7O24·4H2O(国药集团化学试剂有限公司,分析纯)溶于5.75 mL蒸馏水中,10 gγ-Al2O3(山东瑞鼎科技有限公司)浸渍在该钼酸铵溶液中 12 h,经过110℃干燥 12 h,520℃煅烧 12 h (2 ℃·min-1)后得到 MoO3/γ-Al2O3;之后称取1.708 8 g Co(NO3)2·6H2O(国药集团化学试剂有限公司,分析纯)溶于5.75 mL蒸馏水中,将所制备的MoO3/γ-Al2O3在该 Co(NO3)2溶液再浸渍 12 h;随后在110℃下干燥12 h,520℃下煅烧12 h(2℃·min-1升温速率),即得到CoMoO4/γ-Al2O3。 催化剂中负载量基于金属氧化物计算,负载量为16%(wMoO3/wγ-Al2O3)MoO3/γ-Al2O3和 4%(wCoO/wγ-Al2O3)CoO-16%(wMoO3/wγ-Al2O3)MoO3/γ-Al2O3,分别记为 MoO3/γ-Al2O3和 CoMoO4/γ-Al2O3。最后,在500℃,Ar为保护气的条件下,将CoMoO4/γ-Al2O3在 10%(V/V)H2S/H2的混合气中预硫化 1 h,制得 CoMoSx/γ-Al2O3。
1.2 催化剂的表征
XRD测试采用日本理学电机株式会社DMAX-βBX 射线仪。 Cu Kα 辐射(λ=0.154 nm),石墨单色器,管电压 40 kV,管电流 100 mA,扫描速度 10°·min-1,扫描范围 2θ=5°~80°。 采用日立 Hitachi-4800扫描电镜进行SEM/EDS表征,其测试电压为10 kV,工作距离为 8 mm 左右。对 Al、O、Co、Mo和 S 元素进行了检测。XPS测试在PHI 5000 Versaprobe进行,Al Kα 射线(hν=1 486.60 eV),扫描面积 0.8 mm2,功率250 W,样品室真空度为1.60×10-6Pa。各元素的结合能以284.6 eV的C1s电子结合能作为校正标准,对 Co、Mo、S、Al、O 元素进行全谱测试。
1.3 催化剂的吸附-脱附和表面反应性能测试
程序升温脱附/程序升温还原/程序升温表面反应-质谱联用(TPD/TPR/TPSR-MS)在天津先权公司化学动态吸附仪TP-5076上进行,以北京英格海德公司HPR-20质谱仪为检测器。选择质量数为28、44、60 和 64 分别检测 CO、CO2、COS 和 SO2。 样品装填量为0.1 g,在Ar保护下300℃预处理1 h。
TPD:以 5%(V/V)SO2/Ar、5%(V/V)CO/Ar和 5%(V/V)COS/Ar为原料气,样品吸附饱和后通入Ar气吹扫反应器,最后,在Ar气氛下以10℃·min-1的速率升至700℃,记录程序升温下CO、CO2、COS和SO2的脱附情况。
TPR: 于 5%(V/V)CO/Ar气氛下以 10℃·min-1的速率升至700℃,记录程序升温下CO、CO2、COS和SO2随着温度的变化。
(SO2+CO)-TPSR:通入 5%(V/V)SO2/Ar至样品吸附饱和,之后通入Ar气吹扫;最后,在5%(V/V)CO/Ar气氛下以10℃·min-1的恒定速率升至700℃,记录CO、CO2、COS和SO2的含量随着温度的变化。
(CO+SO2)-TPSR:通入 5%(V/V)CO/Ar至样品吸附饱和,之后通入Ar气吹扫,最后,在5%(V/V)SO2/Ar气氛下以10℃·min-1的恒定速率升至700℃,记录CO、CO2、COS和SO2的含量随着温度的变化。
1.4 微型反应性能评价
在微型反应器中装入0.4 g CoMoSx/γ-Al2O3催化剂,之后通入浓度为(0.5%(V/V)SO2+1%(V/V)CO)/Ar的气体,在200~400℃下进行活性测试。选择质量数为 28,44,60 和 64 分别检测 CO、CO2、COS 和SO2。根据检测结果计算得到SO2的转化率、COS的选择性、硫单质的选择性和硫单质的产率。代表的进口浓度代表SO2的出口浓度,代表COS的出口浓度。计算方法如下:

2 结果与讨论
2.1 CoMoS x/γ-Al2O3的表征
图1 为 γ-Al2O3、CoMoO4/γ-Al2O3和 CoMoSx/γ-Al2O3的 XRD 图。 由图可知,CoMoO4/γ-Al2O3存在明显的 γ-Al2O3的(2θ=37°,46°,67°)衍射峰[10],并未出现CoO、MoO3的晶相,可见CoO、MoO3在硫化前样品中分散均匀。CoMoO4/γ-Al2O3经硫化后 CoMoSx/γ-Al2O3中γ-Al2O3晶相并未发生明显变化,也没有出现 CoO、MoO3、Co9S8和 CoS2的衍射峰, 只有在 2θ=34°时有明显的MoS2峰。这说明催化剂在硫化过程中并没有形成有序的晶型。
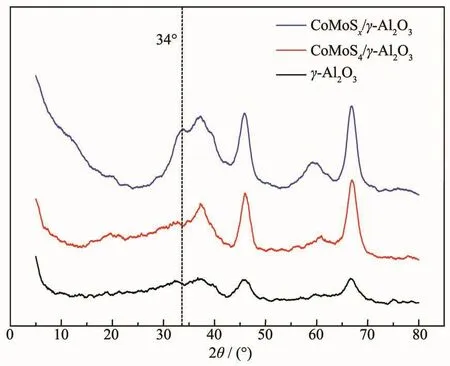
图1 γ-Al2O3、CoMoO4/γ-Al2O3和 CoMoS x/γ-Al2O3的XRD图Fig.1 XRD patterns ofγ-Al2O3,CoMoO4/γ-Al2O3 and CoMoS x/γ-Al2O3

图2 CoMoS x/γ-Al2O3的 SEM/EDS 图Fig.2 SEM/EDSimages of CoMoS x/γ-Al2O3
图2 是预硫化后 CoMoSx/γ-Al2O3的 SEM/EDS图。从SEM可以看出,催化剂并没有出现规则的形貌。EDS谱图表明元素分布较为均匀。尽管硫化温度较高,表面的Co和Mo也没有发生团聚,硫元素也均匀地分散在表面。以上表明采用等体积浸渍法可以获得高分散的CoMoSx/γ-Al2O3催化剂。
图3(a)为催化剂 CoMoSx/γ-Al2O3上 Mo 物种的XPS图谱。由图3(a)和表1可以看出,催化剂中Mo物种的电子结合能228.98和232.40 eV处的谱峰分别归属于Mo4+3d5/2和Mo4+3d3/2,主要对应MoS2和CoMoS,所占百分比为37.91%和20.02%;231.30和234.27 eV处的谱峰归属于Mo5+3d5/2和Mo5+3d3/2,对应Mo2O5和MoOxSy,所占百分比为0.15%和0.95%;231.87和235.02 eV处的谱峰分别归属于Mo6+3d5/2和Mo6+3d3/2,对应未被硫化的MoO3,所占百分比为40.97%,这说明催化剂中Mo的硫化物占总Mo含量的57.93%,其他的Mo并未硫化。电子结合能225.80 eV处的峰谱则归属于S2s的特征结合能,在图中出现是因为S2s的峰位置与Mo4+3d5/2邻近[12]。
催化剂Co2p3/2的XPS表征结果如图3(b)所示。对谱图进行分峰拟合,电子结合能778.92 eV处的谱峰归属于CoMoS活性相,781.79和786.29 eV处的谱峰归属于氧化态的Co。由图3(b)可见,催化剂中并没有出现 Co9S8(778.0 eV)[11]的归属峰,在硫化过程中也并没有形成其他的Co的硫化相,而Co氧化物的出现可能是因为样品的转移导致Co被空气中的氧气氧化[13-14]。

表1 CoMoS x/γ-Al2O3中Mo3d的XPS能谱分析结果Table 1 XPSspectra analysis results of Mo3d in CoMoS x/γ-Al2O3
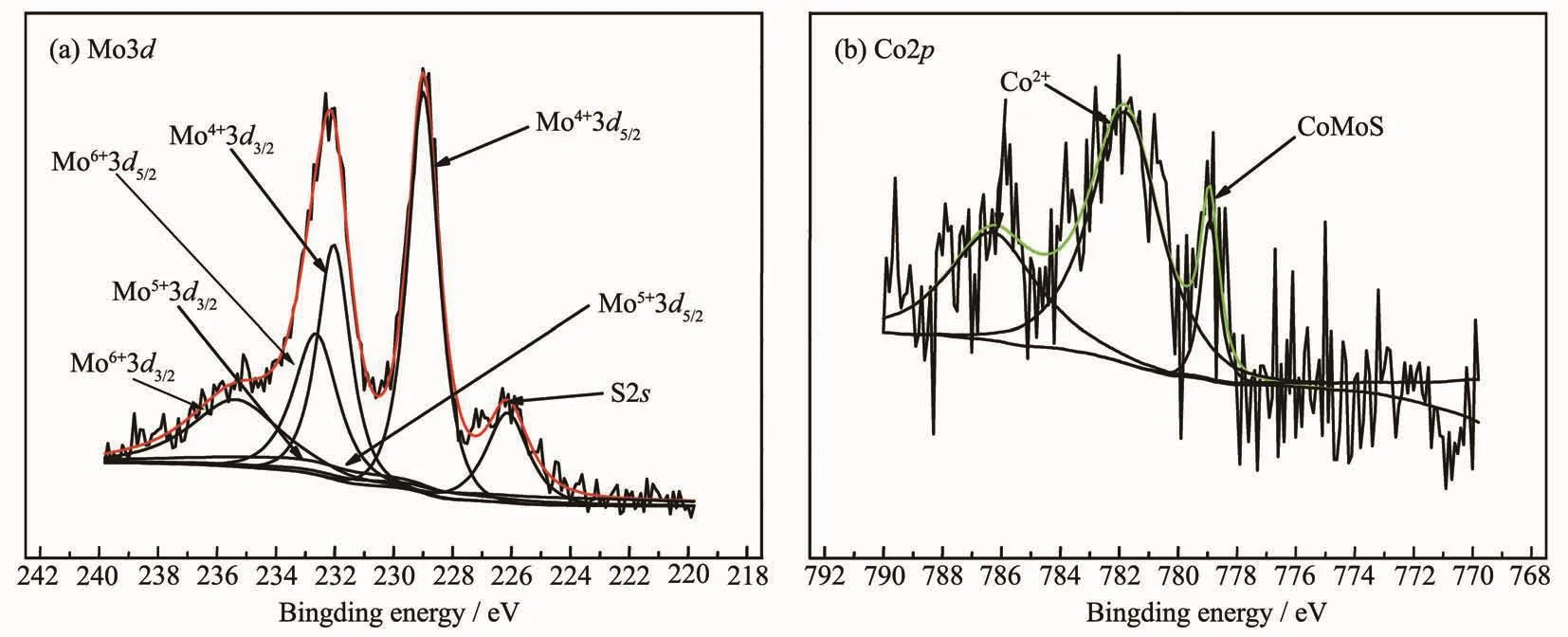
图3 催化剂 CoMoS x/γ-Al2O3的 XPS图谱Fig.3 XPSspectra of CoMoS x/γ-Al2O3
2.2 CoMoS x/γ-Al2O3的 TPD/TPR/TPSR-MS 分析
图4 为 γ-Al2O3、CoMoSx/γ-Al2O3的 SO2-TPD 和CoMoSx/γ-Al2O3的热分解图,同时显示了 CoMoSx/γ-Al2O3高温分解曲线。由图4可知,SO2会吸附在γ-Al2O3和 CoMoSx/γ-Al2O3上。 从 30 ℃开始升温,SO2会随着温度的升高逐渐脱附。在γ-Al2O3(黑色曲线)有1个脱附峰,峰面积较大,说明SO2的吸附量较多,这主要是因为γ-Al2O3表面的L酸位吸附SO2。在CoMoSx/γ-Al2O3催化剂(蓝色曲线)上有2个脱附峰,分别位于50和420℃左右。50℃左右的脱附峰为吸附在γ-Al2O3上的SO2的脱附所致,属于弱吸附作用,与γ-Al2O3相比其脱附量明显减小。这说明CoMoSx覆盖了大部分γ-Al2O3的L酸位。420℃左右的脱附峰是CoMoSx上吸附的SO2脱附(属于强吸附作用)或分解产生的SO2所致。为了验证该峰的归属,考察了未吸附SO2的CoMoSx/γ-Al2O3在Ar气氛下的分解情况(绿色曲线)。可以发现CoMoSx/γ-Al2O3并没有完全被硫化,温度高于400℃时,CoMoSx会迅速分解,与表面的氧形成SO2,然而该脱附峰面积明显低于吸附SO2的CoMoSx/γ-Al2O3脱附量。综上,在 CoMoSx/γ-Al2O3催化剂上,γ-Al2O3对 SO2有弱吸附作用,CoMoSx有强吸附作用,温度高于400℃时,表面S容易以SO2的形式流失。
图5 为 γ-Al2O3和 CoMoSx/γ-Al2O3的 CO-TPD图。由图5可知,随着温度的升高,γ-Al2O3始终没有出现CO的脱附,证明CO几乎不会吸附在γ-Al2O3上。而在CoMoSx/γ-Al2O3上,从400℃左右CO会开始脱附,这说明CoMoSx会吸附CO,且属于强吸附作用。在脱附的过程中,并不会有COS出现,说明CO的脱附属于可逆脱附过程。
图6 是 γ-Al2O3、CoMoSx/γ-Al2O3的 COS-TPD 图。如图6所示,COS会吸附在γ-Al2O3上,但根据信号强度判断,COS的吸附量较少。从30℃开始升温,COS会随着温度的升高逐渐脱附,在200℃左右COS几乎脱附完全,这说明COS在γ-Al2O3上为弱吸附作用。CoMoSx/γ-Al2O3催化剂对COS会有微量的吸附,因为CoMoSx覆盖了大部分的酸位,所以导致COS吸附量很少。
图7是 CoMoSx/γ-Al2O3的 CO-TPR图。 从图 7中可以看出CO2的含量会在180℃时开始发生明显地变化,含量随着温度的升高而逐渐升高,这进一步证明CoMoSx/γ-Al2O3并没有被完全硫化。在程序升温的过程中,COS会出现2个脱附峰,COS的第1个脱附峰较大,第2个脱附峰较小。在40℃时COS开始出现,在200℃时脱附量达到最大,390℃时信号值接近噪音。随着温度的继续升高,COS的信号值又开始加强,560℃到达最大值,随后开始下降。出现2个脱附峰说明大部分的硫在催化剂表面,而另一部分硫进入到晶格当中。
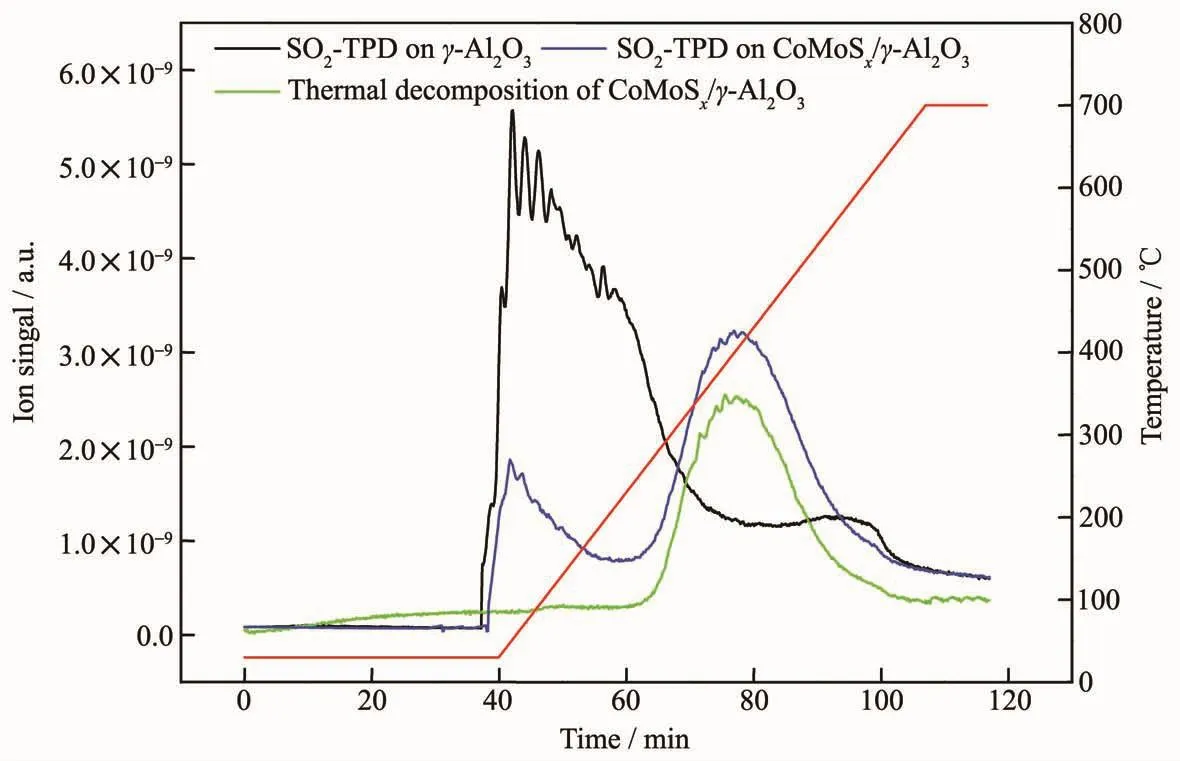
图4 γ-Al2O3、CoMoS x/γ-Al2O3的 SO2-TPD 和 CoMoS x/γ-Al2O3的热分解图Fig.4 SO2-TPD ofγ-Al2O3,CoMoS x/γ-Al2O3 and thermal decomposition of CoMoS x/γ-Al2O3
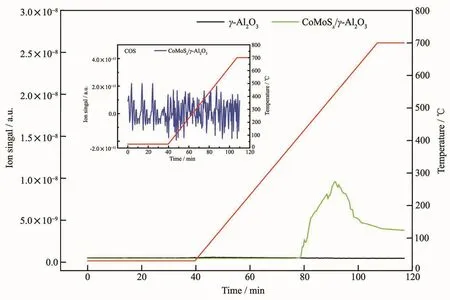
图5 γ-Al2O3和 CoMoS x/γ-Al2O3的 CO-TPD 图Fig.5 CO-TPD ofγ-Al2O3 and CoMoS x/γ-Al2O3
图8 是 CoMoSx/γ-Al2O3的(SO2+CO)-TPSR 图。 如图8所示,CO的曲线在125℃时逐渐下降,在380℃以后达到平稳,说明CO在125℃以后开始消耗。通过与图 3对比后发现,SO2在CoMoSx/γ-Al2O3催化剂的第1个脱附峰依然会出现,而第2个脱附峰接近消失,这说明CO不会在较低温度时与吸附在γ-Al2O3上的SO2反应,而是与吸附在 CoMoSx/γ-Al2O3上的SO2发生反应。由此也可以推断,SO2与CO的最佳反应温度在350~430℃之间;通过对比CO-TPR和 (SO2+CO)-TPSR的CO2信号强度可知,CO2的生成量增加,证明 CO 转化为 CO2。 (SO2+CO)-TPSR中COS的变化趋势与CO-TPR中COS的变化趋势相同。
图9 是 CoMoSx/γ-Al2O3的 (CO+SO2)-TPSR 图。如图9所示,CO和COS的曲线不随温度的升高而发生变化,信号值接近噪音,说明CO和COS几乎不存在,而CO2会在350℃开始上升,在700℃之后开始下降,这说明CO并没有脱附,而是生成了CO2,这与(SO2+CO)-TPSR 的结论相同,进一步证明CO参与了SO2的还原反应,反应温度在350℃以上。

图6 γ-Al2O3和 CoMoS x/γ-Al2O3的 COS-TPD 图Fig.6 COS-TPD ofγ-Al2O3 and CoMoS x/γ-Al2O3

图7 CoMoS x/γ-Al2O3的 CO-TPR 图Fig.7 CO-TPR of CoMoS x/γ-Al2O3

图8 CoMoS x/γ-Al2O3的(SO2+CO)-TPSR 图Fig.8 (SO2+CO)-TPSR of CoMoS x/γ-Al2O3
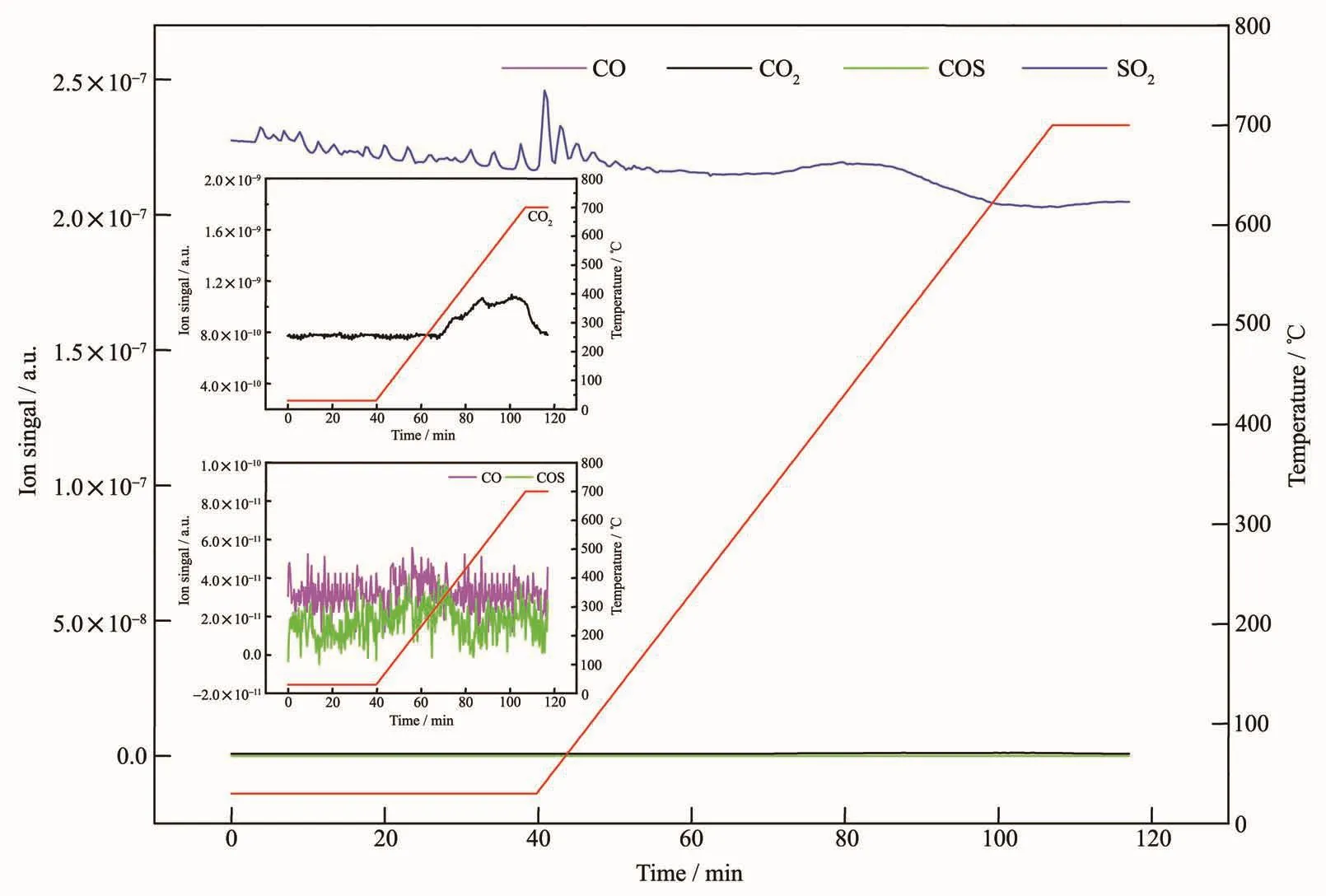
图9 CoMoS x/γ-Al2O3 的(CO+SO2)-TPSR 图Fig.9 (CO+SO2)-TPSR of CoMoS x/γ-Al2O3
2.3 CoMoS x/γ-Al2O3的催化活性和选择性
图10 是CoMoSx/γ-Al2O3的催化活性曲线。如图10(a)所示,SO2的转化率会随着温度的升高而逐渐升高。当温度在300℃以下时,SO2的转化率较低;当温度为300和350℃时,SO2的转化率分别为73.82%和94.71%;而温度为400℃时,SO2的转化率为100%。
根据图 10(b,c)可知,COS 是反应的中间产物,随着温度逐渐升高,COS的选择性在300℃之前逐渐升高,SO2生成硫单质的选择性逐渐降低,而温度高于300℃时,COS的选择性逐渐降低,硫单质的选择性逐渐升高。在350℃时,COS的选择性为5.90%,硫单质的选择性为94.10%,在400℃时,COS的选择性接近0,硫单质的选择性接近100%。由COS的选择性随温度的变化趋势、CO-TPR和(SO2+CO)-TPSR 可 以 判 断 ,CO 首 先 与 CoMoSx/γ-Al2O3催化剂表面的硫反应,生成COS,之后COS与吸附在CoMoSx表面的SO2反应生成硫单质和CO2。当温度低于300℃时,COS和SO2的反应速率较慢;而温度在350℃以上时,COS和SO2的反应很快,在400℃时反应完全。催化剂表面硫和晶格硫都会参与反应,COS的选择性接近0时是晶格硫参与反应。
图10(d)为硫单质的产率随温度的变化趋势图。在300℃之前,因为COS的选择性较低,所以硫单质的产率较低,低于20%;当温度为350和400℃时,以硫单质的产率分别为88.46%和100%。所以在400℃时反应活性最高。其反应机理如下:

□为晶格硫缺位,S*为晶格硫。
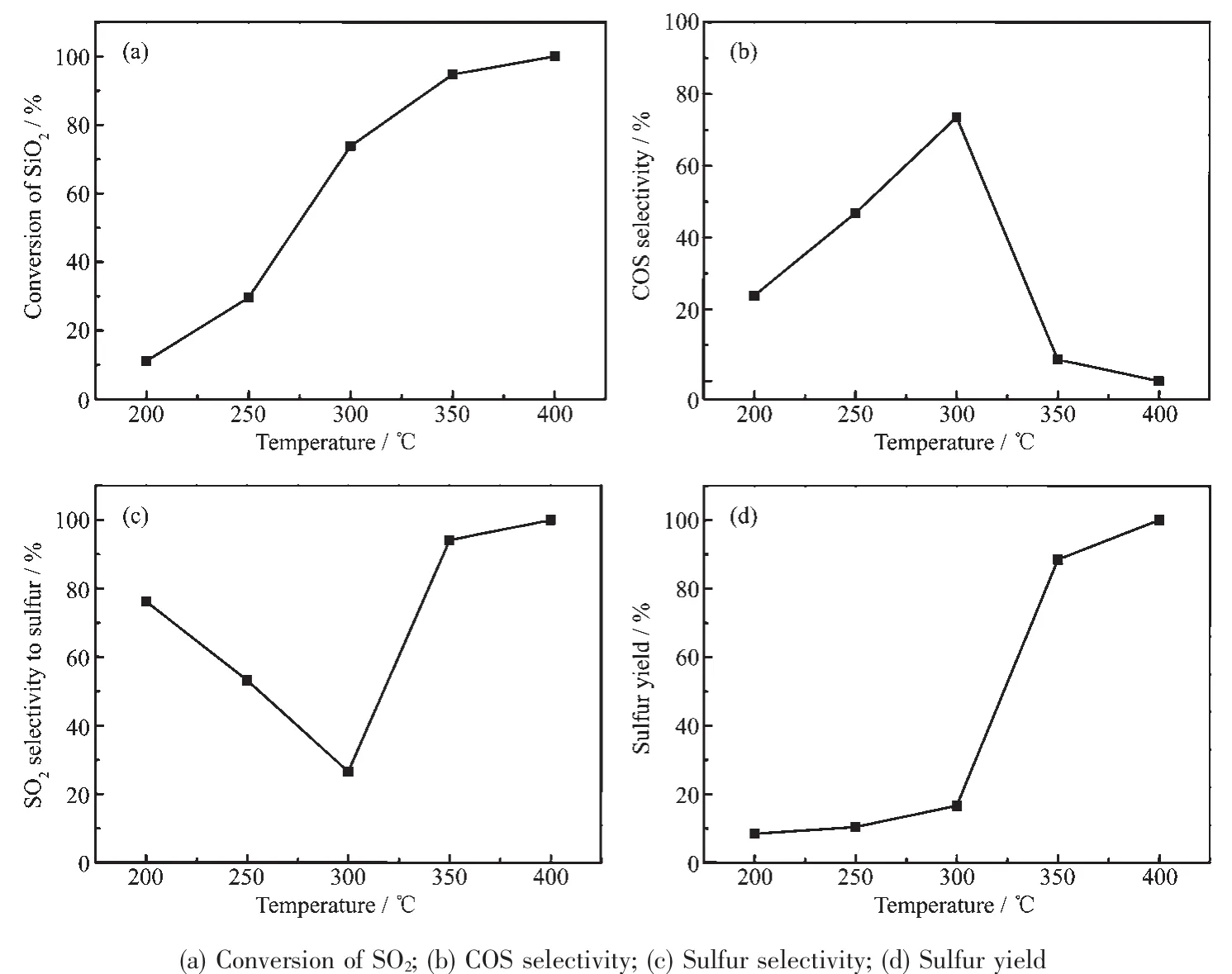
图10 CoMoS x/γ-Al2O3的催化活性和选择性Fig.10 Catalytic activity of CoMoS x/γ-Al2O3
3 结 论
以上结果表明:(1)CoMoSx/γ-Al2O3催化剂由 γ-Al2O3和Co-Mo-S组成,且硫化并不完全,硫化后不会出现 CoS2和 Co9S8等硫化物;(2)CO吸附在CoMoSx上,会生成中间物COS;吸附在γ-Al2O3和CoMoSx上的 SO2都会与 COS 反应;(3)CoMoSx/γ-Al2O3催化剂的硫流失主要是因为COS在低温下不会与 SO2充分反应;(4)CoMoSx/γ-Al2O3催化剂在CO催化还原SO2制硫单质的反应中具备优异的催化活性和选择性,在400℃时,SO2的转化率、硫单质的选择性和硫单质的产率都接近100%。

