紫草色素抗瘢痕的疗效观察
陈曦
(徐州开放大学,江苏徐州 221006)
瘢痕是各种创伤后所引起的皮肤组织外观形态和组织病理学的改变的统称,它是人体创伤(即使是轻微的损伤)后,在伤口或创面自然愈合过程中的一种正常的生理反应,也是创伤愈合过程的必然结果。瘢痕的本质是一种不完全具备正常皮肤组织结构及生理功能的,有的甚至可能失去正常组织活力。中医药治疗瘢痕具有疗效好、费用低、副作用小、兼顾性好的优点,必将发挥其巨大的潜力。但现有治疗瘢痕的方药多为零散的单方、验方,尚未研制出有效的中成药或研究确切的药物单体,用药途径单一,这些都有待于进一步研究。
紫草(Lithospermum erythrorhizon),为紫草科(Boraginaceae)多年生草本植物,其主要品种有软紫草(俗称新疆紫草)、硬紫草、内蒙紫草[1]。紫草具有凉血活血、解毒和透疹的功能,主治血热毒盛,斑疹紫黑,麻疹不透,湿疹,水火烫伤等。紫草色素是从紫草根部提取的多种萘醌(naphthoquinone)类色素,为紫红色萘醌类天然色素,通称总色素,是紫草发挥治疗作用的主要有效成分。紫草色素的主要成分是紫草醌及其衔生物,包括紫草素(Shikonin)、乙酰紫草素(acetyl shikonin)、P,p'-二甲基丙烯酰紫草素(p,p'-dimethylacryl Shikonin)、p羟基异戊酰紫草素(p-hydaro-xyisovaleryl shikonin )、异戊酰紫草素(isovaleryl shikonin)、去氧紫草素 (deoxy shikonim) 等。紫草色素主要是由母体萘茜与侧链相连而成的化合物,主要有2种异构形式:一种为S-型(命名为阿卡宁类,alknnin)[2],另一种为R-型(命名为紫草素类,shikonin),结构如图1所示,它们的旋光性正好相反。
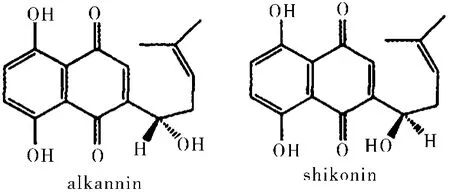
图1 紫草色素两种异构形式
本实验在前期紫草研究基础上,进一步从紫草中提取紫草色素(紫红色萘醌类混合物),来观察其对抗瘢痕形成的作用,报告如下。
1 材料与方法
1.1 材料、试剂与仪器
1.1.1 实验动物
昆明小鼠30只(雌雄各半),健康,由同济医学院实验动物部提供。
1.1.2 实验动物实验材料及试剂
动物笼子、饮水瓶、标准饲料,由同济医学院实验动物部提供;紫草,来源于天成大药房;硫化钠晶体(天津市化学试剂三厂),苦味酸晶体(天津市恒兴化学试剂有限公司),医用酒精(湖北省武汉市惠昌物资贸易公司分装),95%乙醇(上海振兴化工一厂),戊巴比妥纳粉末(国药集团化学试剂有限公司),生理盐水(武汉滨湖双鹤药业有限责任公司),甲醛(上海溶剂厂)。
1.1.3 主要仪器
基本手术器械(手术刀、止血钳、剪刀、注射器、镊子),显微观察仪,旋转蒸发仪。
1.2 试验方法
1.2.1 紫草色素的提取
用800 mL 95%乙醇浸泡250 g紫草[3],24 h后先用纱布过滤除去片状药材,再用布氏漏斗抽滤掉滤渣,将滤液转移至旋转蒸发仪减压蒸发至液体浓稠,取出备用。用回收的乙醇继续浸泡紫草滤渣,24 h后以上重复操作,合并提取液,反复5次,其间适量补充乙醇。最后合并的浓稠状提取液于58 ℃恒温下,烘干成紫黑色的紫草色素固块,称重为9.1 g。紫草中的萘醌类色素成分具有对热不稳定性,加热60℃以上颜色将由红色变成紫黑色,随温度升高变化速度加快,薄层色谱法检查斑点消失,表示紫草色素被破坏,所以此试验烘干过程中保持温度在60 ℃以下。称取5 g制得的紫草色素固体,逐渐加入20 mL无水乙醇中不断搅拌,直到紫草色素固体无法溶解为止,过滤,称取剩余紫草色素固体共为0.9 g,制得高浓度(饱和)紫草色素乙醇溶液,浓度为0.205 g/mL;用同样方法制备饱和紫草色素乙醇溶液,稀释至4倍体积,得试验所需低浓度(1/4饱和)紫草色素乙醇溶液,浓度为0.05 g/mL。
1.2.2 小鼠全层皮损模型的建立
配制0.01 g/L的戊巴比妥溶液,按照10 mL/kg剂量对小鼠进行腹腔注射,约10 min后小鼠进入完全麻醉状态。将小鼠固定在手术台上,用新鲜配制的8%硫化钠溶液作为去毛剂,将小鼠上背部去毛,并用记号笔描绘出d=1 cm的圆形标记,用酒精擦拭消毒,然后用手术剪刀切除小鼠上背部标记的皮肤,建立小鼠上背部皮肤全切伤口模型(图2)。造模后,小鼠随机分为模型对照组、高浓度给药组(紫草色素0.205 g/mL)、低浓度给药组(紫草色素0.05 g/mL)3组。每组10只,雌雄各半。将每只小鼠放于一个小鼠笼饲养,每天伤口涂药1次。给予标准饲料、自来水,自然光照,并定期换垫料、清洁,室温保持在18~23 ℃饲养。
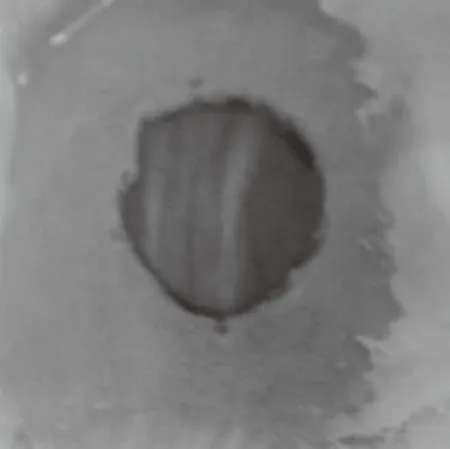
图2 小鼠上背部全层皮损模型
1.2.3 瘢痕组织制备病理切片
伤后60天处死小鼠,切取瘢痕皮肤,经生理盐水清洗,用4%甲醛固定,石蜡包埋,HE染色观察。
2 结果与分析
2.1 各组小鼠一般情况及体重
模型组与对照组小鼠的活动情况并无差异,手术麻醉效果结束后均呈现虚弱状态,于6~18 h后恢复正常生活状态,皆与健康小鼠无异。
2.2 伤口愈合期间各组小鼠创伤情况各项指标
2.2.1 伤后5天
三组小鼠上背部伤口均呈现愈合状态,共同表现为术后1~5天均有不同程度炎性渗出液,皮肤自伤口外缘向内逐渐产生收缩趋势,肉芽组织产生并由外向内逐渐扩散,逐渐在皮肤损伤处由外向内结起一层圆形的痂,整体痂大小为皮肤损伤原大小d=1 cm左右,与手术时伤口大小差异较小。
其不同处在于:模型对照组炎性渗出液较多,第5天依然有半数小鼠伤口处的中心部分呈现炎性渗出液浸润状态,即痂未完全长成,肉芽组织由外向内生长速度较慢,炎性反应持续时间较长,且损伤处结痂较薄(图3);高浓度组炎性渗出液较少,3天后不再产生,第5天为止全组小鼠皮肤损伤处结起一层完整的圆形的痂且痂表面干燥,并持续逐渐增厚(图3);低浓度组炎性渗出液较少,3天后不再产生,第5天为止全组小鼠皮肤损伤处结起一层完整的圆形的痂且痂表面干燥,并持续逐渐增厚。在此期间与高浓度组差别不大(图3)。注:模型组结痂为桔红色为自然皮肤损伤结痂的眼色,而给药组呈现紫红色,为紫草色素乙醇溶液固有颜色,高浓度组色深,低浓度组色浅。
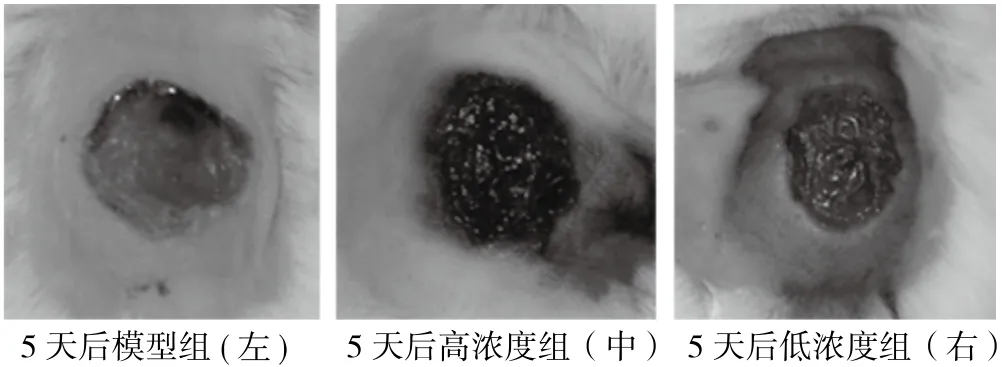
图3
2.2.2 伤后10天
三组小鼠上背部伤口处继续呈现愈合状态,肉芽组织迅生长填充创伤处,结起一层痂,损伤处皮肤边缘持续呈现由外向内收缩状态。其不同处在于:模型对照组炎性渗出液较1~5天内明显变少,但伤口处痂表面依然不呈现干燥状态,抚之质硬,但略有粘滞感;痂薄,增厚速度慢,10天后痂成型,痂面积较手术时伤口面积小,d=0.8±0.1 cm(图4);高浓度组无炎性渗出液,痂已呈现完全干燥状态,抚之质硬且厚,整个痂面积与手术时创伤面积差异不明显d=0.9±0.1 cm(图4);低浓度组无炎性渗出液,痂呈现完全干燥状态,抚之质硬且厚,但比高浓度组略薄,整个痂面积与手术时创伤面积差异不明显d=0.9±0.1 cm(图4)。
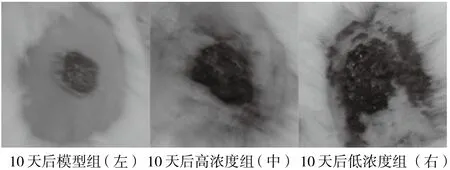
图4
2.2.3 伤后20天
三组小鼠上背部伤口处继续稳定愈合。模型对照组:痂较10天前逐渐变硬,但厚度无明显差异,抚之干燥。20天后,d为(0.6±0.1)cm(图5)。给药组:痂在15~20天内逐渐脱落,高低浓度给药两组在痂脱时间上无明显差别。痂脱前面积大小并无差异,只是痂周围皮肤较之前干净整洁(图5)。痂脱落后,原创伤处中心只剩有一个明显小于之前痂面积的伤口(图5),也明显小于同期的对照组伤口。伤口呈规则圆形,微有渗出液浸润,这和痂脱落与小鼠主动撕扯有关。继续给药后2天,炎性渗出液消失,新结起一层薄痂覆盖在创伤处,除了颜色为紫红色以外面积较小以外,形态与模型对照组无异。20天后,高浓度组d为(0.3±0.1)cm,低浓度组d为(0.4±0.1)cm。
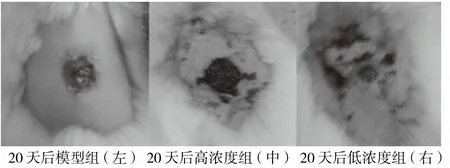
图5
2.2.4 伤后35天
三组小鼠上背部伤口继续稳定愈合,痂逐渐层状脱落,21~25天内小鼠新毛逐渐长出,对照组(图6)与给药组(图6)长毛时间与形态并无明显差异,对照组伤口d=(0.2±0.1),给药组伤口d=(0.2±0.1) 。30天后,3组小鼠痂已完全脱落,有嫩红颜色的瘢痕组织出现,瘢痕面积与结痂大小无明显差别。35天后,拨开三组小鼠上背部原创伤处新生的毛已可看到比正常皮肤颜色红的瘢痕,对照组(图7)所见瘢痕比给药组(图7)明显,但此时不易脱毛观察,因为硫化钠去毛剂有一定刺激性,会损伤原创伤处新生皮肤造成新的伤口。所以暂不做脱毛观察。

图6 25天模型组长毛(左)25天给药组长毛 (右)
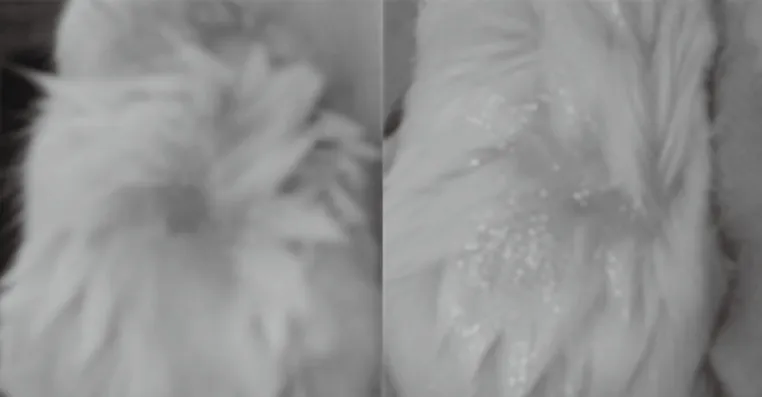
图7 35天模型组(左)35天给药组 (右)
2.2.5 伤后60天
用8%硫化钠做去毛剂,给3组小鼠手术部位去毛,观察瘢痕形成情况。绘制图表。
模型组、高浓度组、低浓度组(图8)

图8

表2 瘢痕面积

表3 瘢痕颜色:粉红、紫红、暗红
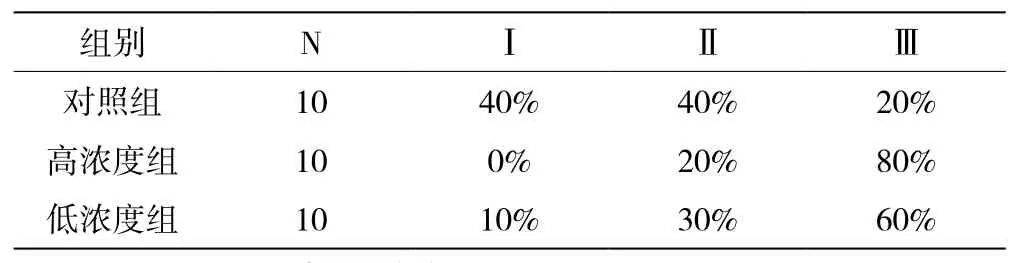
表4 瘢痕与正常皮肤界限:Ⅰ明显、Ⅱ模糊、Ⅲ不明显
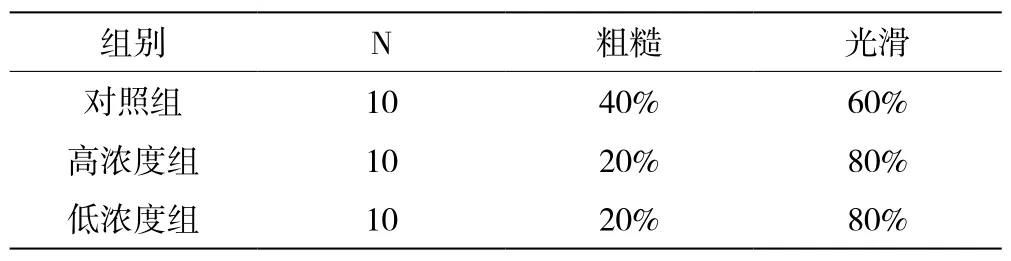
表5 瘢痕光滑度:粗糙、光滑
2.3 各组小鼠瘢痕组织制片染色病理学结果
组织切片用HE染色,其中正常皮肤真皮组织血管数较少,毛囊数多,脂肪细胞多,纤维组织少,真皮厚度约为230μm ,表皮厚度约为15μm(图9,13);模型组小鼠血管很少,毛囊少,脂肪多,纤维组织很多且稠密,真皮厚度约为280μm,表皮厚度约为38μm(图10,14);高浓度组小鼠血管少见,毛囊较多,脂肪细胞较少, 纤维组织层比模型组明显变薄,真皮厚度约为200μm,表皮厚度约为25μm(图11,15);低浓度组小鼠血管少见,毛囊较多,脂肪细胞较多, 纤维组织层比模型组明显变薄,真皮厚度约为200μm,表皮厚度约为7.5μm(图12,16)
3 结论
通过60天后对各小组小鼠瘢痕形成情况的对比易可见:用药组小鼠的皮肤恢复情况明显较对照组更接近于小鼠正常皮肤,形成的瘢痕面积较小,颜色粉嫩,与正常皮肤界限不明显,瘢痕形成较为光滑。通过瘢痕组织制片显微观察可得:用药组的瘢痕纤维组织层比对照组明显变薄,真皮厚度接近正常皮肤,而对照组生成了较厚的瘢痕组织。抗炎作用是紫草的传统药效,即消炎,收敛和解热。自古以来,人们就利用紫草根处理伤口,直到1976年,紫草的这一药用性才得到实验证实。临床研究表明,用紫草制成的药剂具有很好的愈合伤口和抗炎的作用,紫草的乙醇、水、乙醚提取物均有一定的抗炎作用。紫草抗炎的主要有效成分是紫草素(Shikonin)和乙酰紫草素(acetyl shikonin),它们对炎症急性渗出期的血管通透性亢进,渗出和水肿有明显的拮抗作用[4]。
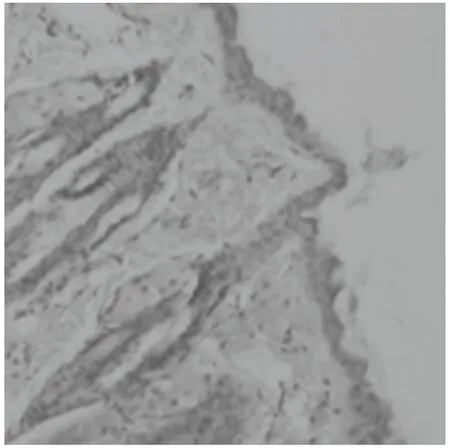
图9 正常组HE×100
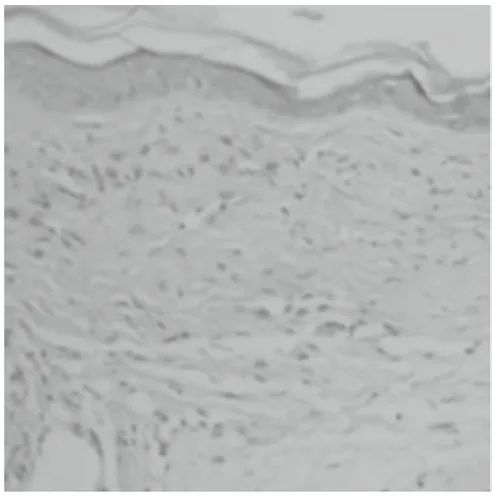
图10 模型组HE×100
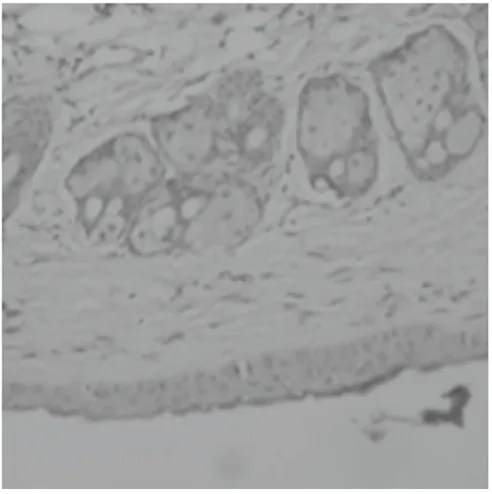
图11 高浓度组HE×100
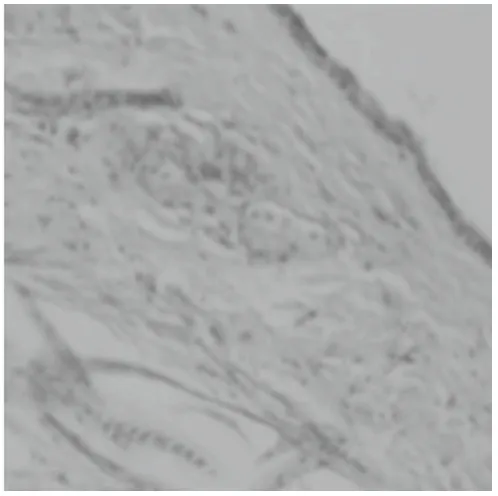
图12 低浓度组HE×100
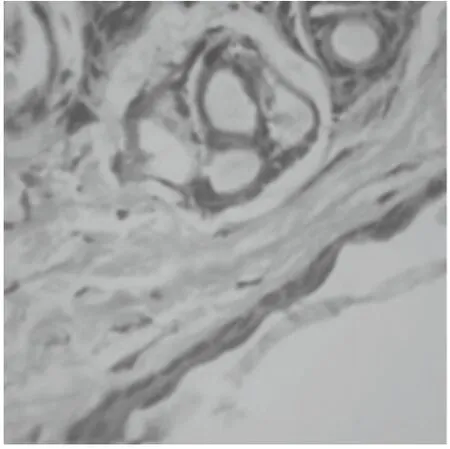
图13 正常组HE×400
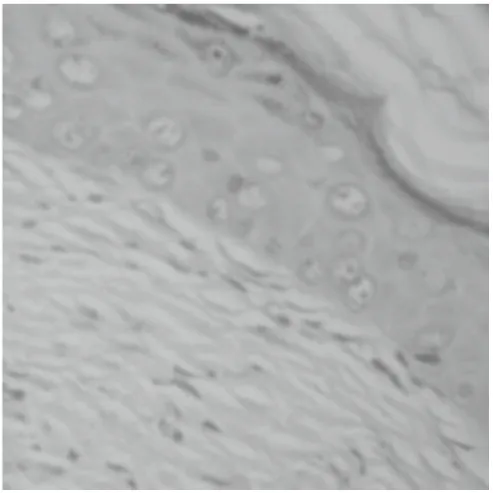
图14 模型组HE×400

图15 25高浓度组HE×400
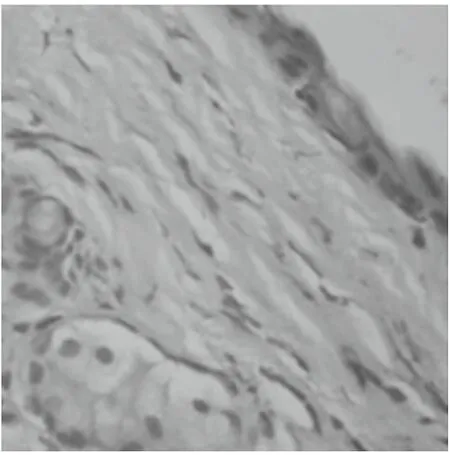
图16 26低浓度组HE×400
乙酰紫草素(acetyl shikonin)、β、β-二甲基丙烯酰紫草素(β、β-dinethylacryl shikonin)均能显著抑制组织胺引起的局部血管通透性亢进(前者5mg/kg,腹腔注射,抑制率34.5%;后者10mg/kg,腹腔注射,抑制率38%)。
20世纪90年代的一项研究表明,紫草素具有抑制白三烯B4(leukotriene B4)和5-羟基二十碳四烯酸(5-hydroxyeicosateranoic acid)生物合成的作用[5]。LTB4和5-HETE是AA的代谢产物,前者是白细胞的强趋化剂,后者为白细胞的激活剂,在炎症过程中起重要作用。
瘢痕的主要成分是胶原纤维。正常情况下,伤口内的胶原合成与分解呈动态平衡,多种因素可破坏这种平衡,导致成纤维、肌纤维母细胞合成胶原增多,阻碍胶原增多,阻碍胶原酶活性,造成瘢痕过度增生,体内合成胶原增速;胶原酶的活性也升高,表示胶原的分解较正常皮肤增加;但因胶原合成速度远大于胶原分解,最终导致了胶原沉积。
以下从几种角度说明此次试验中可能影响小鼠伤口处胶原代谢失衡的原因:
(1)小鼠伤口创面感染和血肿。伤口创面感染后易发生瘢痕,因为创面感染后发生炎性反应,创面炎性细胞浸润,细菌毒素能抑制上皮细胞的移行和增殖,组织蛋白和真皮的多糖被消耗,肌成纤维细胞和成纤维细胞迅速增多。肉芽组织增生过度,易于形成瘢痕组织。一般情况下,感染越久,则形成瘢痕的程度越严重。感染的伤口如不充分将炎性渗出液引流或清除坏死组织,伤口将难以愈合,即使能愈合,愈后也会较容易形成瘢痕。同时,创面血肿为感染创造了条件,对伤口愈合也产生不良影响,将有利于瘢痕的形成。由上述紫草抗炎作用可得知,紫草色素给药组小鼠的创伤部位发生炎性反应的时间比模型对照组的时间短,并且炎性反应较轻,所以模型对照组小鼠伤口处形成的瘢痕较给药组明显。同时,紫草色素另有止血的作用,对于小鼠伤口处的停止出血时间起到一定的帮助。
(2)小鼠伤口创面异物。若小鼠上背部伤口创面落有灰尘、木屑、毛发、棉花纤维等异物,可刺激瘢痕组织增生,较容易诱发更多的瘢痕形成。由本次试验中的伤口愈合过程可知,紫草色素给药组的小鼠创面上结痂的速度较模型对照组快,且痂不断增厚,在结痂的时间内对痂下的皮肤创面愈合起到了隔绝外界的保护作用,所以痂下皮肤愈合速度变快,愈合后伤口形状更规则。
(3)慢性刺激。小鼠伤口创面处的瘢痕与摩擦,搔抓等慢性刺激有关,这些刺激都有利于瘢痕的形成,同时,小鼠的活动也会带动创面边缘皮肤的拉扯,使伤口创面处在不稳定的环境中,延长了伤口的愈合时间。所以可得,紫草色素给药组的小鼠创面上结成的痂较厚,对创面皮肤起到了一定的固定作用。
(4)小鼠创面修复的时间。创面愈合时间越早,瘢痕的发生率越低,否则瘢痕的发生率就增高。
如上所述,紫草色素有加速伤口愈合的药理作用,并一定程度减轻了瘢痕的发生率。

