超高效液相-三重四级杆质谱法测定健脾丸中展青霉素的含量
刘东升 刘婷婷 苏蕊 徐继军 姚世霞 朱旭江
[摘要]目的 建立超高效液相-三重四级杆质谱法(UPLC-MS/MS)测定健脾丸中展青霉素的含量。方法 样品经果胶酶酶解后,用乙酸乙酯提取展青霉素,提取液经HLB固相萃取小柱净化后,采用UPLC-MS/MS进行测定。结果 展青霉素在0.020~2.010 μg/ml内线性关系良好,回归方程为Y=666 825X+27 524(r=0.9970),检出限(LOD)为0.0101 μg/ml,定量限(LOQ)为0.0201 μg/ml。结论 本法灵敏、快速、准确、专属性强,可用于健脾丸中展青霉素的测定。
[关键词]健脾丸;展青霉素;超高效液相-三重四级杆质谱法
[中图分类号] R917 [文献标识码] A [文章编号] 1674-4721(2019)11(c)-0031-04
Determination of patulin in Jianpi Pills by ultra high performance liquid chromatography-tandem triple quadruple mass spectrometry
LIU Dong-sheng LIU Ting-ting SU Rui XU Ji-jun YAO Shi-xia ZHU Xu-jiang
Gansu Institute for Drug Control, Lanzhou 730070, China
[Abstract] Objective To establish an ultra high performance liquid chromatography-tandem triple quadruple mass spectrometry (UPLC-MS/MS) method for the content determination of patulin in Jianpi Pills. Methods After being enzyme-hydrolyzed by pectinase, extracted by water, and purified by HLB solid-phase extraction column, patulin were analyzed by UPLC-MS/MS. Results The calibration curves of the patulin showed good linearities in the range of 0.020-2.010 μg/ml with the regression equation Y=666 825X+27 524 (r=0.9970). The limit of detection (LOD) was 0.101 μg/ml, and the limit of quantification (LOQ) was 0.0201 μg/ml. Conclusion The method is sensitive, rapid, accurate and specific enough to determine patulin in Jianpi Pills.
[Key words] Jianpi Pills; Patulin; Ultra high performance liquid chromatography-tandem triple quadruple mass spectrometry
展青霉素(patulin),屬多聚乙酰内酯,可以造成人体神经系统、呼吸系统和泌尿系统的严重损害,并具有一定的致癌性[1-3]。正是由于展青霉素对人体的严重危害性,许多国家都对食品中的展青霉素的含量进行限定。WHO规定苹果汁中展青霉素的量最高为50 μg/kg[4];我国也对苹果及其山楂为原料制成品中展青霉素的量进行了同样的限定。研究相关文献发现对于展青霉素在山楂等酸性果实及其食品制成品中检验检测方法的报道最为常见[5-13]。但是含酸性果实类中药以及中成药中展青霉素的检验检测方法的报道较少,且多为中药材[14-18]。由于健脾丸为原粉入药,所以笔者对处方中的山楂可能存在展青霉素污染的风险进行研究。并且针对中成药基质干扰以及样品特点,结合前人的研究,建立了超高效液相-三重四级杆质谱法(ultra high performance liquid chromatography-tandem triple quadruple mass spectrometry,UPLC-MS/MS)测定健脾丸中的展青霉素的含量。并采用Oasis HLB固相萃取柱对样品进行净化处理,旨在为研究含山楂类的中成药中展青霉素提供一定的参考依据。
1仪器与试药
1.1仪器设备
LCMS-8045 UPLC-MS/MS联用仪(岛津);METTLER TOLEDO ME204和MS205DU型分析天平(梅特勒-托利多公司);KQ-500DE数控超声波清洗器(昆山市超声仪器有限公司);XK80-A快速混匀器(江苏新康医疗器械有限公司);SHY-2A多功能水浴恒温振荡器(金坛市大地自动化仪器厂);5430R离心机(艾本德);微孔滤膜(希波士);HGC-24A氮气吹干仪(天津市很高科技发展有限公司)。10 μl Eppendorf加样枪和100 μl Eppendorf加样枪(艾本德)。
1.2试药
展青霉素标准品(TRC公司,批号:4-YMK-42-4)、果胶酶(麦克林公司,批号:C100083945);Oasis HLB柱(美国Waters公司,3 ml/60 mg);甲醇、乙腈、乙酸乙酯、冰乙酸均为色谱纯;水为纯净水;其他试剂为分析纯。
1.3样品
健脾丸(2018年国抽),批号详见下文表3。
2方法与结果
2.1液相色谱条件
色谱柱:CAPCELL CORE C18(2.1×150 mm,2.7 μm);流速0.3 ml/min;流动相A为乙腈,B为水;柱温:35℃;进样量:5 μl;洗脱方式:梯度洗脱,A相初始浓度为5%;时间程序:0~6 min,5%~10%;6~8 min,10%~90%;8~10 min,90%~5%(10 min时流动相A回到初始浓度5%)。
2.2质谱条件
采用质谱检测器,离子源:电喷雾离子源(electronic spray ionization,ESI),负离子扫描,采用多反应监测模式(MRM);干燥气温度350℃;干燥气流速10 L/min;雾化气压力30 psi;源电压4000 V;保留时间:4.25 min,母离子152.8 m/z,子离子108.4 m/z,裂解电压20.0 eV;子离子81.1 m/z,裂解电压20.0 eV。
2.3溶液的制备
2.3.1对照溶液制备 取展青霉素对照品适量,精密称定(10.05 mg)于10 ml的棕色量瓶中,加乙酸乙酯溶解并定容至刻度(含展青霉素1 mg/ml),即得,将上述储备液避光保存在-20℃冰柜中。使用前精密移取适量的上述标准储备溶液于棕色量瓶中,在溶剂充分挥干后换用0.2%乙酸制成含50 μg/ml展青霉素中间溶液,同样避光并保存于4℃冰柜中。使用时,以实验中的空白基质溶液作为溶剂将中间溶液稀释成为相应的对照品溶液(对照溶液应临用新制)。
2.3.2供试品溶液制备 取本品9丸(约45 g)精确称定,剪碎,置于250 ml锥形瓶中,加入80 ml水,振摇,离心,取上清液,低温减压浓缩至20 ml,加入果胶酶溶液200 μl,于40℃恒温水浴箱中避光2 h进行酶解。在酶解后的溶液中加入乙酸乙酯20 ml,涡旋20 min后,离心3 min(6000 r/min),分层。将下层液用乙酸乙酯分两次提取,每次20 ml,最后收集两次的乙酸乙酯提取液,40℃挥发干溶剂后,用1%乙酸溶液溶解,转移至5 ml棕色容量瓶中并定容,然后将上述样品溶液全部转移于活化过的HLB柱内(Oasis HLB柱用6 ml色谱甲醇和6 ml水活化使之以3 ml/min的速度流过HLB柱),然后用乙酸乙酯进行洗脱,将洗脱液收集并回收溶剂,最后用0.2%乙酸溶液溶解残渣于2 ml的棕色量瓶中并定容至刻线。
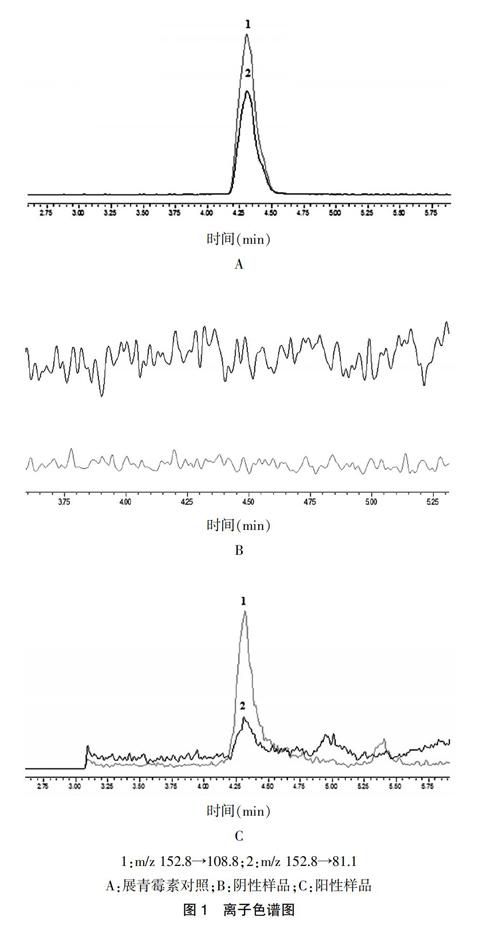
2.3.3阴性样品溶液制备 取健脾丸阴性样品(按处方及工艺,制备不含山楂的健脾丸阴性样品)9丸(约45 g)精确称定,按供试品溶液的制备方法制备,离子色谱图见图1。
2.4方法学考察
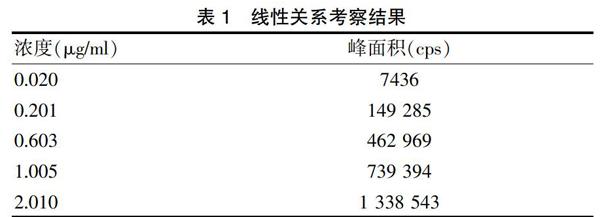
2.4.1线性关系 取上述储备溶液加空白基质溶液分别制的含0.020、0.201、0.603、1.005、2.010 μg/ml展青霉素的系列对照品溶液,按2.1和2.2项下条件,注入液相色谱仪,测得峰面积。测定峰面积积分值,以展青霉素对照品溶液的浓度(μg/ml)为纵坐标(X),峰面积积分值为横坐标(Y)绘制标准曲线,得到近过原点的一条直线。计算回归方程:Y=666 825X+27 524(r=0.9970)。结果表明,展青霉素对照品在0.020~2.010 μg/ml浓度内有良好的线性关系,具体见表1。
2.4.2检出限(LOD)和定量限(LOQ) 取2.4.1项下不同浓度的展青霉素对照品溶液,精密吸取5 μl注入液质联用仪,记录色谱图。计算信噪比为3∶1时,该浓度为仪器LOD为0.0101 μg/ml;计算信噪比为10∶1时,该浓度为仪器LOQ为0.0201 μg/ml。
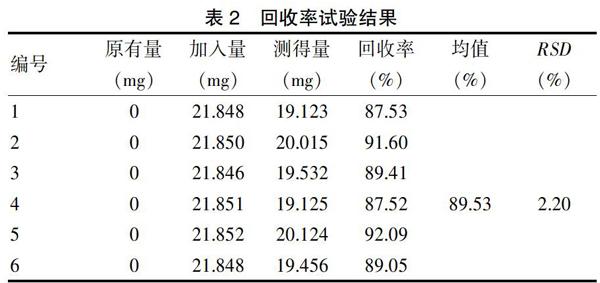
2.4.3精密度和准确度 精密量取完全不含展青霉素的供试品溶液(H厂,批号:20180301)各6份,每份约23.0 g,精密称定,分别精密加入展青霉素对照品溶液(50.23 μg/ml)10 ml,按供试品溶液的制备方法处理,在上述色谱条件下测定。结果显示,回收率在87.52%~92.09%,相对标准偏差(RSD)<3.0%(n=6),满足实验要求,具体见表2。
2.5含量测定
按本方法对所有样品进行测定,结果详见表3。
3讨论
本研究在样品溶液净化处理的基础上采用UPLC-MS/MS法对健脾丸中展青霉素进行测定,与传统的液相色谱法比较消除了5-羟甲基糠对测定结果的干扰以及中成药中多药味对检测影响[12]。结合文献报道对不同提取液、淋洗液和洗脱液进行分析比较和优化[7]。由于展青霉素易溶于水,在酸性条件下稳定,故选用1%乙酸溶液对乙酸乙酯提取后的残渣进行溶解,转移并定容至5 ml的量瓶,后转移于活化过的HLB固相萃取柱(Oasis HLB)內,分别用甲醇和水各6 ml淋洗。并使之以一定的速度流过固相萃取柱,后用乙酸乙酯进行洗脱,将洗脱液收集并回收溶剂至干,最后用0.2%乙酸溶液溶解残渣。对净化处理后的样品通过建立的UPLC-MS/MS测定其展青霉素的含量。并且对质谱和高效液相测定方法结合文献进行优化,使之符合实验要求[14-18]。本研究结果显示,12个厂家的27批健脾丸样品中,有8个厂家11批样品检出展青霉素,检出率为40.7%。但其含量均低于LOQ。
综上所述,该方法具有灵敏度高、快速、准确、专属性强的特点,可应用于健脾丸中展青霉素的测定并且该方法的建立为含山楂类中成药中展青霉素的检测方法的建立提供了实验参考依据。
[参考文献]
[1]周玉春,杨美华,许军.展青霉素的研究进展[J].贵州农业科学,2010,38(2):112-116.
[2]杨倩,刘艳琴,赵男,等.食品中展青霉素的研究进展[J].食品研究与开发,2017,38(8):211-216.
[3]张琼,谈晓君,李红洲,等.展青霉素的检测方法研究进展[J].大众科技,2017,19(9):36-38.
[4]吕伟超,申书昌,王超.固相萃取-超高效液相色谱联用测定水果及果酱中的展青霉素[J].色谱,2017,35(11):1160-1164.
[5]张欣怡,王威浩,邓丽莉,等.水果及其制品中展青霉素的研究进展[J].食品工业科技,2017,38(11):379-384.
[6]王立亚,刘嘉飞,李星星,等.超高效液相色谱-三重四极杆质谱法测定固体山楂制品中的展青霉素[J].食品安全质量检测学报,2018,9(12):2975-2979.
[7]赵红磊,杨丽蓉,赵红艳.超高效液相色谱-质谱联用法(UFLC-MS/MS)测定山楂片中展青霉素含量的研究[J].生物技术世界,2016,(2):16-18.
[8]张嘉坤,张少军,钱训,等.梨果实及其制品中真菌毒素的污染、检测及控制方法研究进展[J].食品安全质量检测学报,2018,9(25):5816-5822.
[9]许欣欣,毛丽莎,陈慧玲,等.高效液相色谱-串联质谱联用法测定果汁中的展青霉素、乐果和多菌灵[J].实用预防医学,2015,22(6):749-751.
[10]曾丽花.高效液相色谱-质谱联用仪器检测果酒中的展青霉素[J].现代食品,2017,(15):105-107.
[11]芦智远,王妍,彭辉,等.SPE-UPLC-MS/MS测定苹果汁中展青霉素的含量[J].中国食品添加剂,2017,(4):189-192.
[12]吴仲,张勋.HPLC法同時测定山楂中展青霉素和5-羟甲基糠醛的含量[J].山西农业科学,2018,46(11):28-31,34.
[13]Wei DM,Xu J,Dong FS,et al.Penicillium and patulin distribution in pears contaminated with Penicillium expansum.Determination of patulin in pears by UHPLC-MS/MS[J].J Integr Agric,2017,16(7):1645-1651.
[14]黄柳霞.超高效液相色谱法食品中展青霉素的方法研究[J].食品与发酵科技,2018,54(2):116-119.
[15]梁晟,邱婧,李瑞莲,等.UPLC-MS/MS法检测苍耳子中的展青霉素[J].华西药学杂志,2018,33(4):393-395.
[16]邓鸣,宾春燕,朱斌,等.高效液相色谱-串联质谱法同时测定中成药中5种真菌毒素[J].中国卫生检验杂志,2014, 24(18):2654-2656.
[17]Beltrán E,Ibánez M,Sancho JV,et al.Determination of patulin in apple and derived products by UHPLC-MS/MS.Study of matrix effects with atmospheric pressure ionisation sources[J].Food Chem,2014,142:400-407.
[18]王少敏,郑荣,俞灵,等.HPLC-MS/MS法测定中药材枳壳中展青霉素[J].中国卫生检验杂志,2011,21(7):1593-1594.
(收稿日期:2019-05-14 本文编辑:任秀兰)

